頭部熱塑膜固定于乳腺托架聯合標記線提高乳腺癌調強放療擺位的準確性
蔣 清, 竺 銘, 許 赪, 王舒蓓, 曹 璐, 蔡 嶸, 陳佳藝, 蔡 鋼
(上海交通大學醫學院附屬瑞金醫院放射治療科,上海 200025)
乳腺/胸壁聯合區域淋巴結預防性照射是乳腺癌術后腋窩淋巴結陽性病人的重要治療方案之一[1-2]。擺位誤差的大小直接影響從臨床靶區向計劃靶區(planning target volume,PTV)外擴的邊界,后者又影響正常組織的體積劑量。乳腺托架是目前乳腺癌調強放療 (intensity-modulated radiotherapy,IMRT)技術下基本的固定裝置,但常用的乳腺托架在頭頸部位的固定相對薄弱。如何提高高危病人區域淋巴結復發風險最高的頸部至鎖骨下部分,即鎖骨上、下區域擺位的穩定性,是目前亟需改善的問題。本研究借鑒熱塑膜對頸部和鎖骨上、下區的良好固定,結合乳腺托架對乳腺/胸壁及上臂固定的穩定性,將頭部熱塑膜通過自制的連接裝置固定于常用的乳腺托架板上,與傳統體位固定方式作射野中心、鎖骨區棘突和鎖骨位移分布方面的比較。
資料和方法
一、一般資料
2016年8月至2017年3月我院放療科收治的10例女性乳腺癌術后病人進入本研究。中位年齡48(40~69)歲。所有病人接受乳房手術和腋窩淋巴結清掃。左乳癌5例,右乳癌5例。保乳術2例,單側浸潤性乳腺癌改良根治術8例。經腋窩淋巴結清掃或前哨淋巴結活檢證實腋窩淋巴結轉移。東部腫瘤協作組(Eastern Cooperative Oncology Group,ECOG)評分<2,患側上肢活動度好。行胸壁/乳腺聯合鎖骨上、下區放療,經一體化調強計劃,達到靶區和累及器官體積-劑量標準。
二、設備
飛利浦85 cm孔徑40排螺旋CT模擬機(Philips,荷蘭)。X線模擬機 (Simulix-HQ,荷蘭)。PINNACLE 9.1治療計劃系統(Philips,荷蘭)。Precise直線加速器(醫科達,瑞典)。MED-TEC 350乳腺托架(CIVCO,美國)。 頭部熱塑膜(CIVCO,美國)。
三、方法
(一)體位固定
病人仰臥位,頭偏健側。上身裸露平躺于MEDTEC 350乳腺托架上,雙上臂外展上舉≥90°。調整托架高度至水平,并調整頭枕、雙側上臂、腕部、臀部等部位至自然舒適。頭部熱塑膜固定于乳腺托架板上(見圖 1)。

圖1 乳腺托架聯合頭部熱塑膜和標記線固定
(二)CT定位及治療計劃
由同一位醫師在病人體表放置標記點,標記靶區的邊界及激光擺位標志。沿患側胸鎖乳突肌至胸部方向的體表標記線,同時標記在熱塑膜上,以保證病人頭頸部偏轉方向的一致性。在自由呼吸下行CT檢查模擬定位。層厚為5 mm,掃描范圍自乳突至對側或同側乳腺皺褶下5 cm。CT檢查圖像傳輸至PINNACLE 9.1治療計劃系統。參考美國放射腫瘤協作組 (Radiation Therapy Oncology Group,RTOG)標準勾畫患側胸壁或全乳、鎖骨上/下區、心臟、兩側肺、患側肱骨頭、脊髓等關鍵器官,制定治療計劃。采用以乳腺/胸壁切線野為主的4~6個照射野,以及針對鎖骨上、下區的1~2個前野、1個后外側野,以區域淋巴結和乳腺/胸壁作為整體靶區進行一體化優化的逆向IMRT。所有病人乳腺/胸壁和區域淋巴結靶區處方劑量為50 Gy/(25次·5周)。要求≥90%的PTV達到100%的處方劑量。保乳病人序貫瘤床加量10 Gy/5次。數據采集至治療結束時。
(三)治療及驗證
每例病人在首次治療前接受錐形束CT檢查驗證,要求擺位誤差不超過3 mm后,開始治療。
(四)數據收集
為比較不同的擺位嚴格性對誤差的影響,在X線模擬機下對同一病人,仰臥位平躺于乳腺托架,雙手上舉,序貫模擬三項不同的限制條件,行解剖參數和射野中心比對。A組(無標記線和熱塑膜):病人頭部自然偏向健側,核對激光中心,不核對頸胸部標記線,不用頭部熱塑膜。B組(有標記線):病人頭部偏向健側,核對頸胸部標記線,不用頭部熱塑膜。C組(有標記線和熱塑膜):病人頭部偏向健側,頭部熱塑膜固定,并核對頸胸部和熱塑膜上的標記線。復位X線片、數字重建圖像(digital reconstructed radiograph,DRR)及照射野中心點、鎖骨區棘突不同位置、鎖骨測量點數據采集方法見圖2。
四、統計方法
應用SPSS 17.0軟件處理數據。3組位移對比采用單因素方差分析。P<0.05,再進行配對t檢驗。
結 果
一、復位時X線片
10例病人在X線模擬機下根據3組擺位要求,每周1次復位并留存復位X線攝片圖像。每例病人分別放置3個位置(3組),每個位置有5套數據,共150組。有9組數據因圖像質量等原因無法測量,實際獲得每個擺位47組配對定位片和數據,3個擺位共141組數據。所有病人乳腺/胸壁和區域淋巴結靶區處方劑量為50 Gy/(25次·5周),要求90%及以上的PTV達到100%的處方劑量。保乳病人序貫瘤床加量10 Gy/5次。
二、各組照射野中心點的位移比較
在上述3個擺位條件下獲得的照射野中心點左右、頭足、前后方向的位移絕對值分布詳見表1,擺位誤差的絕對值見表2。
3組照射野中心點在左右、頭足、前后方向的位移絕對值方面,≤3 mm的比例分別為89.4%、93.6%、100%,74.5%、80.9%、93.6%,87.2%、97.9%、97.9%(見表1)。其中,C組較A組、C組較B組在左右、頭足、前后3個方向的誤差均小,且差異有統計學意義(P<0.05)(見表2)。在前后方向的位移絕對值方面,B組較A組誤差小,且差異有統計學意義(P=0.003)。
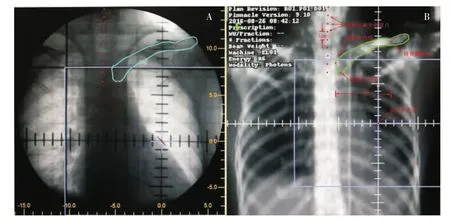
圖2 復位X線片、DRR及照射野中心點、鎖骨區棘突不同位置、鎖骨測量點數據采集方法
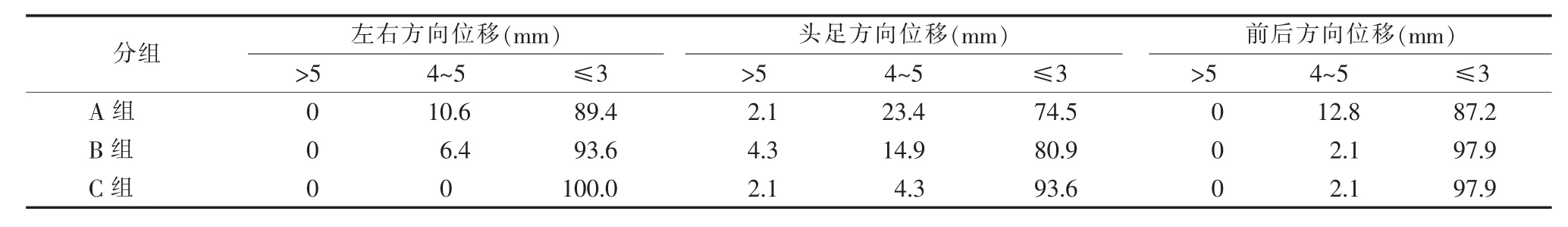
表1 3組照射野中心點的位移分布(%)
三、鎖骨區棘突的左右位移分布及分析
根據鎖骨上、下區域淋巴結的勾畫指南[3],考慮到鎖骨上、下淋巴結部位所對應的頭足方向層面,在3組擺位條件下,對鎖骨區棘突頭足方向,分別采集鎖骨頭下緣,鎖骨頭上緣,鎖骨頭上 1、2、3、4、5和6 cm左右方向的位移絕對值。其分布見表3,擺位誤差的絕對值見表2。
在鎖骨區棘突的左右位移方面,距離鎖骨頭下緣越往上,擺位誤差越大。A組、B組、C組在棘突鎖骨頭上6 cm處的左右位移>5 mm的病人分別占12.8%、6.4%和2.1%(見表3)。
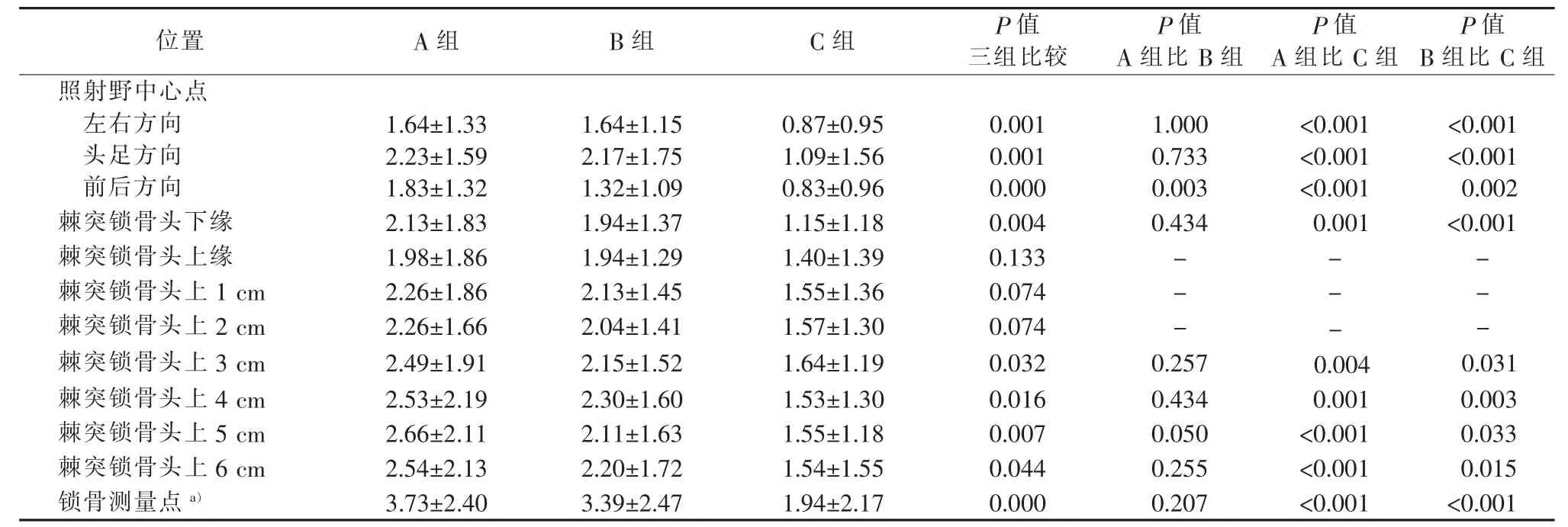
表2 3組照射野中心點不同方向、不同位置棘突左右方向、鎖骨測量點頭足方向的擺位誤差絕對值比較(mm)
C組較另外兩組擺位都顯著降低鎖骨上下、區域不同層面,以棘突為參照標準的左右位移絕對值差異,C組較A組、C組較B組誤差小(見表2)。且除棘突鎖骨頭上緣、棘突鎖骨頭上1、2 cm處外,其他不同測量點處,C組的擺位誤差均顯著優于A、B組(P<0.05)(見表 2)。
四、鎖骨的頭足方向位移分布及分析
由于棘突左右的誤差測量無法準確判斷鎖骨的頭足方向誤差,因此另外采集鎖骨的測量點,定義為距鎖骨頭內緣往外7 cm處,頭足方向取鎖骨的中間點(見圖2)。在3組擺位條件下,鎖骨測量點的頭足方向位移絕對值分布見表3,擺位誤差的絕對值見表2。發現C組較另外兩組擺位都顯著降低鎖骨測量點在頭足方向位移絕對值差異。C組較A組、C組較B組誤差小,且差異均有統計學意義(P<0.001)(見表 2)。
討 論
在乳腺癌各個淋巴引流區域中,鎖骨上、下區復發占區域淋巴結復發的首位,且鎖骨上、下區毗鄰脊髓、臂叢神經和氣管等關鍵限量器官,所以鎖骨上、下淋巴結區域照射的劑量穩定性對高危病人保證術后放療最大獲益至關重要。在二維放療時代,鎖骨上區的照射既往采用的是單前野混合射線照射。隨著國際指南對包括區域淋巴結在內的靶區均優先推薦CT定位,RTOG、歐洲放射治療和腫瘤學會 (European SocieTy for Radiotherapy and Oncology,ESTRO)等學會也都完善乳腺及區域淋巴結靶區勾畫指南,乳腺/胸壁聯合鎖骨上、下區一體化調強技術在臨床上應用逐漸成熟[3-4]。
現代精確放療實施中,良好的體位固定裝置可保障分次放療期間體位的重復性和準確性。二維時代,鎖骨上野采用單前野混合射線照射,鎖骨上野的擺位是按病人皮膚表面標記線源到皮膚距離擺位,鎖骨上野和乳腺/胸壁擺位的射野中心不同。同時,由于照射野局限在二維的骨性標志,射野范圍相對較大,缺乏嚴格的靶區體積劑量評估概念,對擺位誤差的要求較寬松。隨著NCCN等國內、外指南[3]一致推薦,乳腺癌的放射治療首選基于CT定位,采用靶區和正常組織體積劑量評估的治療技術,且越來越強的循證醫學證據支持,在N1和高危N0病人區域淋巴結照射的獲益不僅得到局部區域控制,而且轉換成降低遠處轉移的獲益,甚至在一定程度上提高乳腺癌特異生存率[5-6]。區域淋巴結照射的重要性逐漸凸顯。聯合乳房/胸壁和區域淋巴結的三維技術,成為乳腺癌術后放療的主流。乳腺癌區域淋巴結靶區勾畫技術的推薦漸趨成熟,而且鎖骨上、下區是區域淋巴結復發的高危區域[7]。經過多年的技術探索,目前乳腺癌一體化多野IMRT的技術穩定,正常組織體積劑量安全性高,已獲得更大接受度[4]。
局部和區域的一體化IMRT計劃可實現一個射野中心、一次擺位完成的優勢。精確的治療計劃需精確擺位。臨床上常用的單一乳腺托架固定裝置,在鎖骨上、下區域至頸部的固定相對薄弱。對于部分區域淋巴結復發的病人,需將照射野延伸超過常規鎖骨上區,固定尤其不穩定。為此,有采用水固化頭枕聯合乳腺托架、熱塑膜聯合多功能體板等提高鎖骨上野擺位的準確性[8-9],目的是強調鎖骨上、下區固定的穩定性。本研究發現,增加頸胸部標記線有一定改善,其中在射野中心處,可分別將左右、頭足和前后方向平均位移4~5 mm的比例從10.6%、23.4%和12.8%降低至6.4%、14.9%和2.1%。本研究還在成熟乳腺托架基礎上,將頭部熱塑膜通過自制的固定裝置,固定于常用的乳腺托架板上,并配合標記線擺位。既保證原有乳腺托架對胸部固定的穩定性,又不增加額外成本,解決了臨床常見的技術問題,可在臨床推廣。
本研究顯示,3組照射野中心點擺位的重復性和準確性均可。3組分別僅有2.1%、4.3%和2.1%病人的頭足方向位移>5 mm,其余均≤5 mm。在左右、頭足和前后方向方面,C組的位移優于A、B組,且差異有統計學意義。這與筆者既往的研究[10]和相關文獻報道[11]相類似,說明乳腺托架的固定對于照射野中心點的擺位可滿足臨床需求。就位移的平均絕對值而言,C組優于A、B組。其主要原因可能是,無標記線的情況下,鎖骨上、下區域完全靠射野中心點3處激光定位標記固定,而激光定位標記一般位于鎖骨頭下2~3 cm處,縱軸方向難以保證頭部及偏轉方向的穩定性。B組可將擺位參照點延伸至鎖骨上區域,但仍不足以解決頸部未固定的薄弱問題。乳腺托架左、右無刻度標記,每次擺位時射野中心和乳腺托架縱軸刻度可保持一致。但在左右方向與乳腺托架會有少量偏差。由于熱塑膜和乳腺托架的相對扣合位置固定,因此當頭部熱塑膜上的標記線和病人頸胸部的標記線重合時,就很好解決這一問題。也有學者提出,增加乳腺托架頭足兩端的刻度標記來減少左右方向的誤差,可使其≤2.6 mm[12],或通過讀取頸/胸壁標記線的激光刻度來減少誤差。總之,在乳腺托架基礎上增加病人頭部,尤其是左右方向位置和托架的相對固定位置,可改善鎖骨上、下區的固定薄弱處。
對鎖骨上、下區位移的評價,筆者采用X線模擬機下每周復位時拍X線片,直觀地測量鎖骨區棘突和鎖骨的位移。雖有不少同時采用頭頸部和胸部固定裝置的研究[8-9],然而這些研究大多僅得到照射野中心點的擺位誤差,或根據錐形束CT(cone-beam CT,CBCT)得到的整體誤差[13-14],并未直觀針對鎖骨區擺位誤差進行研究。本研究顯示,在鎖骨區棘突的左右位移方面,距離鎖骨頭下緣越往上,擺位誤差越大,A組棘突鎖骨頭上6 cm處左右位移>5 mm的病人達12.8%,而C組僅占2.1%。C組的位移優于A、B組,距離鎖骨頭上3 cm以上差異有統計學意義,而A組與B組之間的差異無統計學意義。同樣,在鎖骨頭內緣外7 cm處,C組鎖骨的頭足位移也優于A、B組。在頭頸部腫瘤的體位固定時,熱塑膜已成為標準固定裝置。乳腺/胸壁部位放療,病人需上抬手臂,常規的乳腺托架上未配備熱塑膜的底座。從A、B組結果可看到,鎖骨上、下區固定并不理想,無法滿足一體化IMRT的技術要求,從而使靶區照射不準確,并增加不良反應。吳傳鋒等[15]對單用乳腺托架固定的下頸部擺位誤差研究發現,鎖骨上靶區放療擺位誤差較大,臨床靶區外在左右、上下、前后方向應≥8.08、8.13、6.30 mm,需進一步改良固定方法。C組約90%的結果位移<3 mm。其優勢的主要原因是:一方面,熱塑膜帶來的鎖骨區良好固定;另一方面,擺位時對齊熱塑膜和頸胸部體表上的標記線,相當于在乳腺托架頭足兩端做刻度標記,滿足乳腺/胸壁聯合鎖骨上野一體化IMRT的精確要求。
CBCT已在當前放療的擺位誤差得到廣泛應用[16]。然而,與位于射野中心的乳腺/胸壁不同,由于鎖骨上、下區皮膚肌肉組織外形變化較大,固定相對不理想、存在鎖骨上、下區配準標準的問題。如自動配準還是需結合手動配準?手動配準的主觀性等。尤其是CBCT掃描范圍不足以完全涵蓋鎖骨上、下區的影響。CBCT可反映整體擺位誤差,但仍不足以精細化分析鎖骨上、下區域不同固定條件下,各個方向的誤差特點。所以,本研究利用在X線模擬機下顯像清晰、直觀的優勢。但由于該分析是離線的,所以對擺位實時差異性的反映為間接性。在線影像引導可實時反映擺位誤差,后續將優化多種在線影像驗證方式的組合,以達到在線實時和聯合多層面精細化分析,為提高鎖骨上、下區擺位誤差精確性提出更完善的方案。
綜上,在乳腺托架聯合頭部熱塑膜和標記線固定下,照射野中心點、鎖骨和鎖骨區棘突擺位誤差更小,能很好地同時滿足乳腺/胸壁和鎖骨上、下區一體化IMRT技術擺位的準確性要求,且簡單方便,值得臨床應用推廣。

