鋰空氣電池正極催化劑研究進展
肖 昂
(青島科技大學 高分子科學與工程學院,山東 青島 266000)
21世紀,能源問題是人類社會面臨的最大挑戰之一[1]。隨著人口的增長和工業化的發展,世界對能源的需求將不可逆地增長[2]。因此,開發具有高能量密度的新型儲能系統是迫切且必要的。若不考慮參與反應的氧氣的質量,鋰空氣電池的能量密度可達11430 W·h·kg-1,與汽油相當[3]。基于此,2009年。IBM公司推出“電池500”項目,其目標就是利用鋰空氣電池實現汽車的行駛里程達到500 km。從此鋰空氣電池受到全世界眾多科研工作者的關注[4]。
1 鋰空氣電池概述
Littauer和Tsai[5]在1974年首次提出鋰空氣電池的概念,當時的設計是采用堿性水溶液作為電池的電解液。該電池具有2.9到3.0 V的開路電壓,在大約200 mA·cm-2的電流密度下具有2.0 V的工作電壓,不過它只能是一次電池或者機械式充電系統,無法作為二次電池使用。1996年,Abraham和Jang報道了一種非水電解液鋰空氣電池[6]。該電池由金屬鋰負極、凝膠聚合物電解質和負載催化劑的碳空氣電極組成。這種電池在室溫下的開路電壓約為3.0 V,可以多次充放電,并且碳正極負載的酞菁鈷催化劑使其具有較高的庫倫效率。2006年,Bruce及其合作者[7]通過采用負載有MnO2催化劑的Super P正極改善了鋰空氣電池的循環性能,該電池在70 mA·g-1的電流密度下循環50次后比容量仍能保持在600 mA·h·g-1。

圖1 四種類型鋰空氣電池示意圖[3]
Fig 1 Schematics of four types of Li-O2cells[3]
鋰空氣電池結構和鋰離子電池類似,主要由以下幾個部分組成:金屬鋰負極、隔膜、電解液、空氣電極。根據電解質的不同,鋰空氣電池主要分為四種類型,包括非質子鋰空氣電池,水系鋰空氣電池,全固態鋰空氣電池和混合鋰空氣電池,其中,非質子鋰空氣電池由于其良好的可再充電性和相對簡單的結構而成為研究相對較多的電池。非質子鋰空氣電池的主要化學反應為:
總反應:
2Li+O2?Li2O2(Eocv=2.96 V),
陽極和陰極的單獨放電/充電反應用下式:
(i)在鋰電極上,Li?Li++e-(Ea= -3.05 V vs.標準氫電極(SHE),Li氧化和還原);
(ii)在氧電極:O2+2Li++ 2e-?Li2O2(Ec= -0.09 V vs 標準氫電極(SHE),O2氧化還原和析出反應)。
其中Ea和Ec分別是陽極和陰極的熱力學開路電壓。有限的電子轉移和質量傳輸效率以及放電/充電過程中不可預測的副反應是導致電極上電化學反應緩慢和不可持續的的主要原因。進而導致鋰空氣電池實際容量低,庫倫效率差,倍率能力有限和循環性能差等缺點。
開發新型高效的正極催化劑是解決上述問題的關鍵。目前空氣電極主要存在三大挑戰:1)對放電反應(ORR)和充電反應(OER)的催化活性差,導致放電和充電過程容量低;2)氧氣環境下碳的副反應,包括電解液在充電過程中的分解反應;3)在放電過程中發生孔堵塞,阻礙氧氣、中間體和產物的輸送,從而限制了放電容量。因此開發更加實用、高效的催化劑對解決能源問題具有至關重要的意義。
2 鋰空氣電池催化劑概述
作為放電產物Li2O2形成和分解的主要場所,空氣電極是鋰空氣電池中研究最多的部分。根據Li2O2產生的放電機理,空氣電極有以下四個主要功能:1)催化Li2O2在表面活性位點的形成和分解;2)將多孔通道中的鋰離子和氧氣輸送到活性位點;3)作為放電產物Li2O2的儲存空間;4)誘導Li2O2在電極表面的生長和形態演變。目前,常見的空氣電極催化劑主要為:碳材料、貴金屬以及非貴金屬化合物等。
2.1 碳材料
由于高的導電性、低密度、低成本和易于構造多孔結構等優勢,碳材料被廣泛應用于鋰空氣電池中。碳材料的低質量密度和高導電性有利于鋰空氣電池獲得較大的重量比容量。碳電極的孔結構可以用現有技術輕松調節,從而提高鋰離子和氧氣的傳輸效率。此外,碳材料的電子結構可以通過摻雜雜原子進行調整,摻雜雜原子可以形成催化Li2O2形成和分解的有效活性位點。基于以上優點,碳材料既可以作為催化劑單獨使用,也可以作為其他催化劑的載體使用。Liao等人[8]開發了一種可再生的木材衍生陰極,具有良好對齊的細長微通道,用于高性能鋰空氣電池。他們將白楊木碳化、活化之后負載上RuO2納米顆粒(4.15%),將其應用于鋰空氣電池正極催化劑(RuO2/WD-C)。RuO2/WD-C正極可以通過簡單的水洗,從深度放電-充電循環或100個容量循環中完全再生。再生RuO2/WD-C正極的面積容量與初始正極的性能相當。在200次循環后,截止電壓高于2.6 V。即使再次進行再生,RuO2/WD-C正極仍然表現出與初始正極幾乎相同的高性能,表明其較高的穩定性和出色的可再生性。
Lin等人[9]介紹了一種高質量負載(高達10 mg·cm-2)石墨烯基空氣電極的制造及對其電化學性能和機械性能的研究。由于石墨烯片上的孔結構賦予了石墨烯材料干壓縮性,因此通過壓縮多孔石墨烯材料,可以在無溶劑和無粘合劑的條件下輕易地制備出這種空氣電極,將其應用于鋰空氣電池正極,電池表現出優異的重量容量以及超高的面積容量(高達~40 mA·h·cm-2)。

圖2 a)在LiClO4/DMSO電解質中,應用MCC和CB催化劑的鋰空氣電池首圈充放電曲線(2.0~4.6 V的電壓范圍,200mA·g-1電流密度);具有b)MCC和c)CB催化劑的鋰空氣電池在LiClO4/DMSO電解質中在不同電流密度下的放電曲線;d)鋰空氣電池在不同電流密度下的容量保持能力[11]
Fig 2 a) The charge/discharge profiles of Li-O2cells with MCC and CB catalysts in the first cycle at 200 mA·g-1in the voltage range of 2.0~4.6 V in a LiClO4/DMSO electrolyte,Discharge curves of Li-O2cells with b) MCC and c) CB catalysts at different current densities in a LiClO4/DMSO electrolyte,d) Capacity retention capability of Li-O2cells at different current densities[11]
Yang等人[10]報道了一種獨特分級的碳結構(HOM-AMUW)的合成,其由高度有序的大孔(250 nm)組成,在其超薄壁(4~5 nm)上具有豐富的中孔。這種碳結構在500 mA·g-1和2000 mA·g-1的電流密度下分別具有超高的放電容量37523 mA·h·g-1和12686 mA·h·g-1。使用低結晶Ru納米團簇進一步官能化之后應用于鋰空氣電池正極,電池呈現出較低的充電極化電壓和出色的循環穩定性。顯著的性能增強主要歸因于其獨特的分級多孔結構,其中有序大孔和超薄中孔壁顯著增強了氧氣和鋰離子的擴散能力,并且大孔有利于容納更多的放電產物,從而實現更大的容量。此外,分級多孔結構將放電產物的形態調制為具有高電荷傳輸能力的三維多孔結構,這也有助于電化學反應的進行。
Sun等人[11]報道了一種新型的中孔碳納米立方體的制備方法。由中孔碳納米立方體制成的氧電極包含多個分級的中孔和大孔,其可促進整個電極中的氧擴散和電解質浸漬,并提供足夠的空間容納不溶的放電產物。將其用作正極催化劑,在200 mA·g-1電流密度下鋰空氣電池放電容量可達26100 mA·h·g-1,遠高于商業炭黑催化劑。此外,中孔納米立方體結構還可以用作其他高效催化劑的導電主體結構。例如,Ru官能化的中孔碳納米立方體對氧析出反應顯示出優異的催化活性。具有Ru官能化中孔碳納米立方體催化劑的鋰空氣電池,在截止電壓循環模式下,充電/放電效率高達86.2%(電流密度為200 mA·g-1),并且在400 mA·g-1的電流密度、截止容量為1000 mA·h·g-1的條件下,可以穩定循環120圈。
2.2 貴金屬
貴金屬和貴金屬化合物,如Au,Pt,Pd,Ru,RuO2和IrO2等,可以極大促進鋰空氣電池的電化學反應,已被廣泛研究作為鋰空氣電池中的正極催化劑。
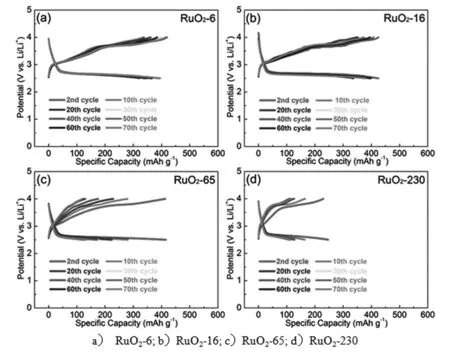
圖3 不同孔徑參數的RuO2陰極的2-70次循環曲線[12]
Fig.3 Typical discharge and charge curves from the 2nd cycle to 70th cycle of porous RuO2samples at 100 mA·g·-1[12]
Zhou等人[12]以二氧化硅微球為模板制備出不同孔結構參數的有序多孔RuO2材料,用作鋰空氣電池的無碳陰極,系統研究了多孔RuO2孔結構參數對電化學性能的影響。結果表明,比表面積和孔徑決定了鋰空氣電池的比容量和庫倫效率,孔太小會導致孔堵塞并阻礙鋰離子和氧氣的擴散,從而導致較小的比容量和較高的過電勢;孔太大會削弱多孔RuO2的機械性能,從而導致電化學反應過程中容量的迅速下降。
Yin等人[13]報道了一種由氮摻雜的碳納米管(CNT)、Co2P和Ru納米顆粒構成的高催化活性空氣陰極。均勻分散的Co2P和Ru催化劑可以有效地調節Li2O2在放電/充電過程中的形成和分解行為,改善Li2O2的電絕緣性能,并構建均勻低阻抗的Li2O2/催化劑界面。由于Co2P和Ru的協同效應,大大改善了ORR/OER動力學,Co2P/Ru/CNT電極提供更高的氧還原觸發起始電位和更高的ORR和OER電流。基于Ru/Co2P/CNT電極的鋰空氣電池顯示出改善的ORR/OER過電位為0.75 V,在1 A·g-1下具有12800 mA·h·g-1的優異倍率性能,并且在電流密度為100 mA·g-1、截止容量為1000 mA·h·g-1時,可以穩定循環185圈以上,顯示出優異的循環性能。
Shen等人[14]研究設計并制備了一種氮摻雜空心碳球,并用Ir納米粒子進一步修飾,作為鋰空氣電池中的正極催化劑。通過對含胺基有機前體的高溫碳化處理,不僅實現了原位氮摻雜,而且確保了摻雜的均勻性,并因此改善了該催化劑的電化學活性。中孔(約60 nm)與超薄中孔殼結合,顯著改善了傳質能力。空心碳球的大空腔(直徑約250 nm)為放電產物Li2O2提供了足夠的容納空間,并且約550.6 m2·g-1的大比表面積提供了大量的活性位點,從而可以提高電化學反應速率,進而增強鋰空氣電池的倍率性能。此外,均勻分布的Ir納米顆粒可以顯著降低充電過電位并改善了鋰空氣電池的循環穩定性。
2.3 非貴金屬化合物
盡管貴金屬基材料對Li2O2形成/分解表現出優異的催化活性,但是它們的高成本和稀缺性,以及它們與有機電解質的副反應,目前都難以克服。因此,開發價格低、儲量大、制備簡單的非貴金屬催化劑便成為解決這些問題的可能策略。此外,通過調整非貴金屬催化劑的形貌結構可以得到更多的傳輸通道和更大的儲存放電產物的空間,這些優勢都是傳統貴金屬基材料所不具備的。
2.3.1 金屬氧化物

圖4 海膽狀NiO-NiCo2O4的場發射掃描電鏡照片[15]
Zhao等人[15]通過簡單水熱法成功合成出海膽形狀的NiO-NiCo2O4微球,以100 mA·g-1的電流密度進行充放電時,容量可達到9231/8349 mA·h·g-1,以500 mA·g-1的電流密度進行充放電時,容量可達3711/2254 mA·h·g-1,表現出較好的倍率性能,在電流密度為100 mA·g-1且截止容量為600 mA·h·g-1時,可穩定工作80個循環。這種優異的電催化性能源于NiO-NiCo2O4的獨特海膽狀結構。它可以促進循環過程中氧氣傳輸和電荷傳輸,并為Li2O2的沉積和分解提供足夠的反應位點和場所。
Zhang等人[16]將CoO-Co3O4納米顆粒錨定在氮摻雜碳球上,并將其作為鋰空氣電池的陰極材料。結果顯示出該電池具有較高的催化性能,在電流密度為300 mA·g-1時可獲得24265 mA·h·g-1的超高放電容量,在1000 mA·g-1的電流密度下的比容量可達3622 mA·h·g-1。截止容量為500 mA·h·g-1,應用N-HC@CoO-Co3O4電極的電池可以達到112次以上的循環。這是由于氮摻雜的空心碳球不僅確保了用于容納Li2O2放電產物的超高比表面積,而且還提供了更多的反應活性位點。負載在氮摻雜空心碳球表面的CoO-Co3O4納米粒子可以有效地催化蠕蟲狀Li2O2的形成和分解。
Qiao等人[17]通過犧牲模板法制備出具有多孔壁的新型3D空心α-MnO2骨架(3D α-MnO2),并將其應用于鋰空氣電池陰極材料,結果顯示在100 mA·g-1的電流密度下實現了8583 mA·h·g-1的高比容量,在300 mA·g-1下具有6311 mA·h·g-1的優異比容量,并且在200 mA·g-1的電流密度下具有170個循環的良好循環穩定性。這是由于獨特的3D空心骨架結構為鋰空氣電池提供了一些特有的性能,包括α-MnO2的固有高催化活性,三維α-MnO2納米線在3D骨架上的催化活性位點,以及連續空心網絡和豐富的孔隙度,這些特性都有利于放電產物的儲存聚集和氧擴散。
2.3.2 金屬硫化物
Long等人[18]以硝酸銅、硝酸鈷等為原料,采用一步水熱法,直接在泡沫鎳上生長出CuCo2S4,將其應用于鋰空氣電池正極,在電流密度為100 mA·g-1,時,電池比容量可達9673 mA·h·g-1,并且在電流密度為200 mA·g-1且截止容量為500 mA·h·g-1時,電池可穩定工作164個循環而沒有嚴重極化,表明該電池具有優異的循環性能。進一步研究發現,性能提升主要來自于以下幾個方面:1)CuCo2S4納米片的獨特陣列結構可以促進氣體擴散并同時保持足夠的氧濃度和電解質浸入;2)CuCo2S4@Ni的大表面積可為ORR和OER反應提供豐富的催化位點,并為容納放電產物提供充足的空間;3)CuCo2S4納米片的均勻分布可以有效地減輕電池充放電期間的體積變化。
Yin等人[19]報道了在導電碳紙上包覆NiCo2S4@NiO核-殼陣列3D分層異質結構作為鋰空氣電池的自支撐陰極,表現出較低的過電位0.88 V,以及優異的倍率性能和循環性能。獨特的分層陣列結構可以構建用于氧擴散和電解質浸漬的多維通道。NiCo2S4和NiO之間的內置界面電位可以顯著增強界面電荷轉移動力學。根據密度泛函理論計算,NiCo2S4和NiO固有的Li2O2親和特性對促進大顆粒Li2O2的形成具有重要的協同作用,有利于構建低阻抗Li2O2/陰極接觸界面。
Kim等人[20]通過原位液相氧化還原嵌入和剝離的方法,將1T-MoS2與功能化的碳納米管(CNT)雜化,作為不含粘結劑的自支撐空氣電極。結果表明其具有優異的電化學性能,在200 mA·g-1的電流密度、500 mA·h·g-1的截止容量條件下可以穩定循環100圈。
2.3.3 金屬碳化物
Gao等人[21]通過對WO3@g-C3N4的原位裂解還原,制備出超薄N摻雜的缺陷碳層包封的W2C雜化物(W2C@NC),并將其應用于鋰空氣電池的正極催化劑。結果顯示這種催化劑不僅對ORR和OER有高活性,而且對不需要的副產物Li2CO3的分解也顯示出高活性。應用W2C@NC的鋰空氣電池顯示出更高的初始容量,更低的過電位和更長的循環壽命,這很大程度上歸因于超細W2C納米粒子和幾乎單層N摻雜碳的的協同效應。
Liu等人[22]開發了一種基于TiC的碳基陰極,獨立的TiC納米線陣列陰極原位生長在碳織物上,覆蓋其暴露的表面。與沒有Ru改性的TiC納米線陣列相比,通過與Ru納米顆粒的沉積,TiC納米線陣列顯示出增強的氧還原/進化活性和可循環性。
2.3.4 金屬氮化物
Liao等人[23]報告了一種新型的TiN納米棒陣列陰極,其制備方法是首先通過在碳紙(CP)上生長TiN納米棒陣列,然后在TiN納米棒上沉積MnO2超薄片或Ir納米粒子以形成良好的有序、三維(3D)和獨立的結構陰極:TiN@MnO2/CP和TiN@Ir/CP。兩種陰極都表現出良好的比容量和優異的循環穩定性。它們的放電比容量分別高達2637和2530 mA·h·g-1。在100 mA·g-1的電流密度下可以穩定循環200個圈。
Choi等人[24]報道了以嵌段共聚物為模板,制備出具有2D六方結構的介孔氮化鈦(m-TiN),并將其作為鋰空氣電池的陰極催化劑。由于TiN具有良好排列的孔結構和良好的導電性,使電池擁有較好的可逆性,可以穩定循環100圈以上。

圖5 鋰空氣電池正極材料充放電前后的TEM圖像[23]
Fig.5 TEM images of Li-O2batteries[23]
Yang等人[25]通過原位化學氣相沉積(CVD)制備活化的鈷-氮摻雜的碳納米管/碳納米纖維復合物(Co-N-CNT/CNF),并將其作為鋰空氣電池正極。該電極的獨特結構有助于氧氣擴散和電解質滲透。同時,氮摻雜的碳納米管/碳納米纖維(N-CNT/CNF)和Co/CoNx用作促進放電產物的形成/分解的反應位點。Co-N-CNT/CNF陰極的鋰空氣電池在放電平臺(2.81 V)和低電荷過電位(0.61 V)方面表現出優異的電化學性能。此外,鋰空氣電池還具有較高放電容量(在100 mA·g-1下為11512.4 mA·h·g-1),以及較長的循環壽命(130個循環)。同時,Co-N-CNT/CNF正極還具有優異的柔韌性,因此具有Co-N-CNT/CNF的組裝柔性電池可以在各種彎曲條件下正常工作并保持良好的容量保持率。
2.3.5 MOF

圖6. (a)常規Ru-C催化劑和(b)MOF衍生的Ru-MOF-C催化劑在鋰空氣電池中長期循環后的示意圖[26]
Shao等[26]報道了一種新型Ru-金屬-有機骨架(MOF)衍生的碳復合材料,其特征在于在碳基質內實現Ru納米顆粒立體的分布,應用于鋰空氣電池的催化劑,500 mA·g-1的電流密度下具有高達800圈(~107天)的穩定充電-放電循環,以及較低的放電/電荷過電勢(~0.2/0.7 V vs Li)。
Wang等人[27]通過3D打印技術,制備出含Co的自支撐多孔碳骨架結構的新型陰極材料。該新型材料具有良好的導電性和機械穩定性,此外,多孔骨架由在Co-MOF衍生的碳薄片和薄片內形成的中孔和微孔之間形成的豐富的微米尺寸的孔組成,這些孔有利于Li2O2顆粒的有效沉積和分解,從而可以顯著提高鋰空氣電池的充放電容量和循環性能。
3 結語
鋰空氣電池因其超高的比容量而被廣泛研究,但是諸如電解液易分解、循環性能較差、倍率性能較差、庫倫效率較低等問題依然沒有從根本上解決。雖然目前已有大量材料被應用于正極催化劑,但是其性能都不盡人意,例如,碳材料在電化學反應過程中本身不穩定,容易發生各種各樣的副反應;貴金屬催化劑催化性能強,但是價格昂貴且容易導致電解液的分解;金屬氧化物價格低、獲取簡單,但是導電性較差。這些問題都制約了鋰空氣電池正極催化劑的商業化發展,因此還需要在未來投入大量的研發工作。正因如此,尋找高效穩定的正極催化劑成為了提高鋰空氣電池性能的關鍵。目前正極催化劑的研究主要從以下兩點出發:(1)構建納米多孔結構提高反應位點的數量,進而提升鋰空氣電池的倍率性能,進一步增加放電產物的存儲空間,大幅提升鋰空氣電池的比容量;(2)多種催化劑進行復合,發揮其協同效應。相信在不久的將來,鋰空氣電池必將因其各種優異性能,得到更為廣泛的應用,改善人類的生活。

