改性甘蔗葉炭對水中氨氮的吸附研究
柳富杰,周永升,陳賢廷,吳國勇
(廣西科技師范學院 食品與生化工程學院,廣西 來賓 546119)
隨著社會的迅速發展,工業農業的大規模發展,產生的工業和生活廢水對環境也造成了巨大的壓力。化肥、石油化工等行業產生的工業廢水中富含大量營養元素,工業廢水進入水體中造成水體富營養化[1]。其中氨氮的過度排放是造成水體富營養化的重要原因之一[2]。廢水中的氮常以氨態氮(NH4+)形式存在的[3]。目前,氨氮引起的水體富營養化已經成為一個嚴重的環境問題。排污水體的富營養化會使水中溶解氧下降,引起魚類大量死亡,還會導致毒素在水生生物上的積累,甚至直接威脅著人類的生命健康[4]。水體中含氮、磷等有害物質已成為我國水體環境災害的主要污染物,且已成為制約社會和經濟的可持續發展的重要因素[5]。因此,必須要從現狀出發,進一步對含氨氮廢水處理技術和手段進行研究,確保能夠更有效的治理污水,降低其對各方面帶來的不良影響[6]。其中,吸附法由于其工藝簡單有效、運行成本低、經濟實用,被認為是一種十分有前景的處理氨氮廢水技術[7]。近年來用于去除廢水中氨氮的吸附材料主要有: 沸石、石灰石、粉煤灰、海泡石、竹炭、木炭及活性炭等。其中生物質炭由于其價鉻便宜和制備工藝簡單等優點成為研究熱點[8]。生物質炭是在限氧或者無氧的條件下對富含碳的生物質(如樹葉、肥料和農業殘留物)進行熱分解進行熱裂解,產生的富碳固體物質[9]。研究[9-10]發現,生物炭可以通過吸附作用有效去除水中的有機和無機污染物。在土壤中加入生物炭可以減少氮浸出和固定NH4+的作用,從而起到保持土壤中的養分的作用[11]。但是近年來,研究發現生物質炭吸附水體中的氨氮能力較其它吸附劑低,導致其工業化應用受限[12]。
采用甘蔗葉作為原料,將其經限氧高溫裂解成生物質炭,經改性后作為水中氨氮的吸附劑目前在國內未見報道。甘蔗作為我國的主要糖料,每年榨季都會產生大量的甘蔗葉[13],甘蔗葉作為一種含碳豐富的生物質材料,經過處理后可以將其制成生物質炭。有研究表明MgCl2改性生物質炭可以提高其對氨氮的吸附性[14]。本研究考察MgCl2改性甘蔗葉炭吸附廢水中氨氮吸附效果,在單因素試驗基礎上進行響應面優化實驗,尋找不同因素對改性甘蔗葉炭吸附水中氨氮的影響次序,找出最佳吸附工藝條件;并通過等溫吸附和吸附動力學對吸附過程機理展開探索。
1 材料與方法
1.1 材料與儀器
1.1.1 材料
甘蔗葉 廣西來賓市興賓區周邊蔗地;酒石酸鉀鈉、氯化鎂、納氏試劑、氯化銨 廣州化學試劑廠,以上試劑均為分析純。
改性甘蔗葉炭的制備:甘蔗葉采集回來后于烘箱中烘干粉碎過60目篩,取甘蔗葉于坩堝中加蓋壓實密封在箱式電阻爐重保持450℃限氧裂解5 h。冷卻后研磨過100目篩,得到甘蔗葉生物質炭。取一定量的生物質炭浸泡于1.0 mol/L的氯化鎂溶液中12 h(每克初始蔗葉生物質炭加入20 mL的氯化鎂溶液),用去離子水沖洗過濾至浸出液的pH值恒定(pH值在7左右),置于電熱鼓風干燥箱中,將溫度調至105℃,恒溫烘干24 h,即得到用氯化鎂改性的甘蔗葉生物質炭。
1.1.2 儀器
電熱恒溫鼓風干燥箱 上海躍進醫療器械有限公司;SX2-5-12箱式電阻爐 上海躍進醫療器械有限公司;TS-100B臺式恒溫振蕩箱 常州光啟實驗儀器有限公司;pHS-3E pH計 上海儀電科學儀器股份有限公司;UV-2600紫外光分光光度計 日本島津。
1.2 試驗方法
1.2.1 溶液中氨氮的測定和計算
氨氮的測定方法根據國標使用納氏試劑分光光度計法,計算方法如下:
溶液中氨氮濃度使用納氏試劑分光光度法在425 nm波長下測定,通過吸附前后溶液中氨氮濃度的變化,計算出改性前后甘蔗葉生物質炭對氨氮的吸附率和吸附容量。
吸附率、吸附容量計算公式如下:
η=[(C0-Ce)/C0]×100%
(1)
Qe=[(C0-Ce)V]/m
(2)
式中,η為氨氮的去除率,%;C0、Ce分別為氨氮的初始、平衡的質量濃度,mg/L;Qe為氨氮平衡時的吸附容量,mg/g;V為氨氮廢水體積,L;m為吸附劑質量,g。
1.2.2 響應面試驗
前期單因素實驗結果發現,溶液pH值=6,吸附時間為8 h,氨氮初始濃度為25 mg/L時改性炭對水中氨氮吸附容量達到2.60 mg/g以上。
根據Box-Behnken中心組合實驗設計原理,在單因素試驗基礎上,以pH(X1)、吸附初始濃度(X2)、吸附時間(X3)為因素,吸附容量為響應值,設計響應面試驗,因素與水平編碼見表1。

表1 Box-Behnken實驗設計因素與水平
1.2.3 等溫吸附線試驗
取改性前后甘蔗葉炭各0.3 g放到離心管內,加入50 mL濃度為5、10、15、20、25、30、35 mg/L的氨氮溶液,將pH值調節為6后置于恒溫振蕩器內震蕩吸附12 h后,取出過濾,測定濾液氨氮含量。
1.2.4 吸附動力學試驗
分別稱取0.3 g改性甘蔗葉炭加入6支離心管,加入50 mL初始濃度為25 mg/L的氨氮溶液,將pH值調節到6后放入恒溫振蕩器分別吸附2、4、6、8、10和12 h,取出過濾,測定濾液氨氮含量。
2 實驗結果與分析
2.1 響應面方案結果分析
根據表1因素水平編碼表選擇初始濃度、pH值、吸附時間為自變量,分別記為X1、X2和X3,以吸附容量為響應值Y,設計響應面實驗,實驗方案及結果如表2所示。實驗方案經過Design Expert8.06軟件處理,得到響應面二次回歸方程:
Y=-6.66750+0.27500X1+1.04875X2+0.49625X3+7.50000×10-4X1X2-1.25000×10-3X1X3+0.020625X2X3-5.05000×10-3X12-0.094063X22-0.032812X32。

各因素的P值大小表示各因素對響應值的影響顯著性大小。由表3可知,這三個因素對吸附容量影響均顯著,顯著性由大到小排序為pH值>吸附時間>吸附濃度。響應面模型預測最優條件為:初始濃度為26.60 mg/L,pH值6.68,時間為9.16 h,響應面模型預測的吸附容量為2.77 mg/g。根據實驗室的實際情況及實施方案的可操作性將最優方案工藝參數更正為初始濃度26.60 mg/g,pH值6.7,吸附時間為9 h。根據該參數進行三次平行試驗,測得改性生物質炭吸附氨氮容量為2.75 mg/g,相比響面模型預測值誤差0.02 mg/g,說明通過響應面優后得到的工藝參數準確可靠。

表2 Box-Behnken試驗設計及結果

表3 回歸模型方差分析表

表3(續)
2.2 響應面圖形分析
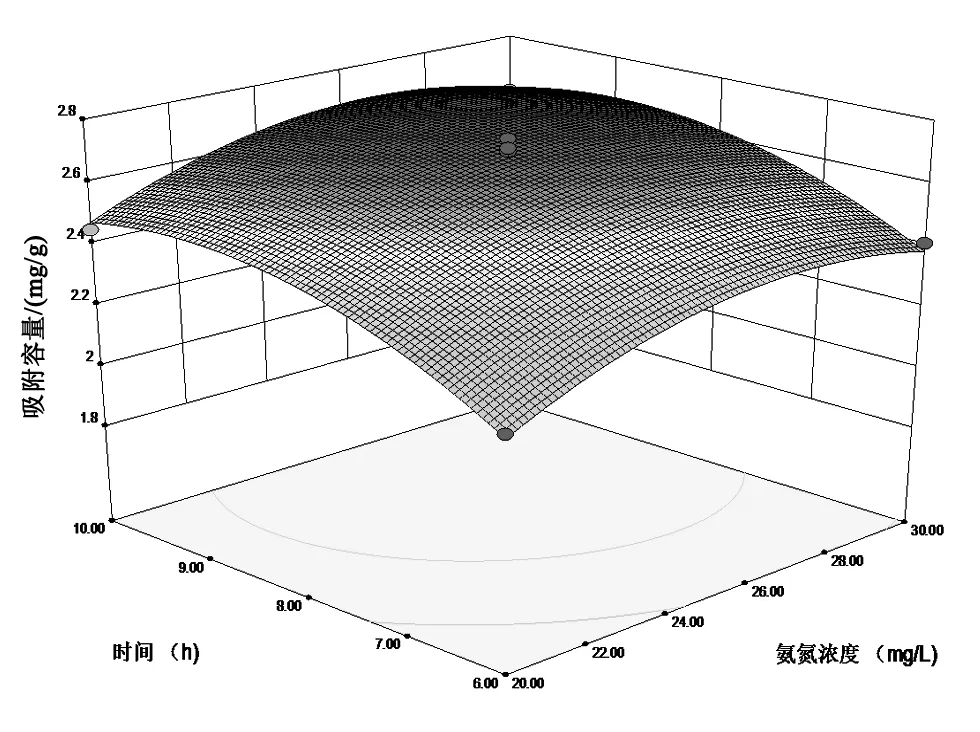
圖1 氨氮初始濃度和吸附時間對改性甘蔗葉炭氨氮吸附容量的響應曲面圖

圖2 氨氮初始濃度和pH值對改性甘蔗葉炭氨氮吸附容量的響應曲面圖
Fig.2 Response surface diagram of ammonia nitrogen initial concentration and pH on ammonia nitrogen adsorption capacity of modified sugarcane leaves

圖3 pH值和吸附時間對改性甘蔗葉炭氨氮吸附容量的響應曲面圖
改性甘蔗葉炭吸附氨氮的響應曲面見圖1~3。圖1~3非常直觀的反映出各個因素對響應值的影響的顯著性。在圖1中,響應曲面近似圓形說明氨氮初始濃度和吸附時間交互作用對氨氮吸附影響不顯著,隨著吸附時間和濃度的增加,響應曲面逐漸趨向平面;圖2顯示在氨氮初始濃度和pH值的交互作用對氨氮吸附容量的影響顯著;圖3響應曲面表明,在pH值的交互作用對改性甘蔗葉炭的氨氮吸附容量的影響顯著。
3 等溫吸附線和吸附動力學研究
3.1 等溫吸附線研究
圖4為等溫吸附試驗結果。MgCl2改性甘蔗葉炭和甘蔗葉生物質炭對氨氮的吸附作用機理可以用Langmuir和Freundlich吸附等溫方程進行描述。對著兩種等溫方程進行數據擬合,擬合結果見表4。
由表4可知,Langmuir和Freundlich等溫吸附方程都能描述常溫下改性前后的甘蔗葉生物質炭對氨氮吸附表面吸附機理,但Langmuir方程的相關系數更高,R2均大于0.95,由此可知改性前后的甘蔗葉炭對氨氮的吸附時均一的單分子層吸附[5]。改性后最大吸附量Qm、b和K均增大,說明改性有利于吸附的發生,這和試驗結果吻合[15]。

圖4 改性前后生物質炭對氨氮的吸附等溫吸附線

表4 Langmuir和Freundlich等溫方程參數
3.2 吸附動力學研究

圖5 吸附動力學試驗結果
圖5為吸附動力學試驗結果。對吸附過程進行吸附動力學的研究可以進一步解析改性甘蔗葉炭吸附吸附氨氮的機理。根據等溫吸附實驗結果,對吸附過程進行Lagergren準一級、Lagergren準二級和顆粒內部擴散模型進行擬合,數據擬合結果見表5。
由表5可知,Lagergren準二級動力學擬合氯化鎂改性甘蔗葉生物質炭吸附氨氮所得擬合方程相對于其他兩種動力學模型擬合度更好,相關系數達到0.994,說明使用Lagergren準二級動力學描述氯化鎂改性甘蔗葉生物質炭吸附氨氮動力學特性更準確。影響準二級動力學方程吸附作用的主要因素是化學鍵,說明改性炭吸附氨氮的過程主要以化學吸附為主[16]。

表5 吸附動力學模型方程及參數
4 結論
(1)由響應面試驗可知在改性甘蔗葉炭吸附氨氮過程中,吸附濃度、pH值和吸附時間對氨氮吸附容量的影響顯著性順序為:pH值>吸附時間>吸附濃度,最佳吸附條件為氨氮初始濃度26.60 mg/g,pH值6.7,吸附時間為9 h,在此吸附條件下氨氮吸附容量達到2.75 mg/g。
(2)等溫吸附線研究表明Langmuir等溫吸附方程可以描述常溫下改性前后的甘蔗葉生物質炭對氨氮吸附表面吸附機理,改性前后的甘蔗葉炭對氨氮的吸附時均為均一的單分子層吸附。
(3)吸附動力學研究表明氯化鎂改性甘蔗葉生物質炭吸附氨氮動力學特性可以使用Lagergren準二級動力學進行描述,說明改性炭吸附氨氮的過程主要以化學吸附為主。

