一氧化碳納米管束低壓相的第一性原理研究*
周紅才 黃樹來 李桂霞 于桂鳳 王娟 步紅霞
1) (青島農業大學理學與信息科學學院,青島 266109)
2) (齊魯師范學院物理與電子工程學院,濟南 250200)
對低壓下一氧化碳(CO)晶體結構的研究已有半個多世紀,研究其晶體內部結構的方法有很多,實驗人員通過紅外設備進行紅外分析,或者通過更先進的激光設備進行拉曼分析,以求得到精準的CO晶體的內部結構.通過基于不同原理的計算分析手段,科學家可以預言或者驗證碳原子和氧原子如何排序來形成CO固體結構.基于密度泛函理論,本文設計了一種類似于碳納米管束狀結構的CO晶體結構.通過分析計算,該CO納米管束狀晶體是寬帶隙半導體,與目前已經研究報道的最穩定的CO分子晶體和鏈狀晶體相比,具有能量的更穩定性.截然不同的電子結構性質以及能量上的高度穩定性,使得該結構不僅豐富了低壓下CO晶體結構的多樣性,還為探究低壓下CO晶體的內部結構提供了新的思路與方向.
1 引 言
在自然界的氣體中,像氧氣(O2)、氮氣(N2)、氫氣(H2)、一氧化碳(CO)、二氧化碳(CO2)等,分子內部存在很強的相互作用力.例如O2中的氧?氧雙鍵,N2中的氮?氮三鍵和CO2中的碳?氧雙鍵等都具有很強的相互作用力,或者說是共價鍵.但分子間的相互作用力,如常見的范德瓦耳斯力(石墨層與層之間的作用力),或者是氫鍵(水分子之間的氫鍵)比較弱,其鍵能比共價鍵小1-2個數量級,通過加壓或者降溫等物理方式,自然界中的氣體可以轉化為液體、聚合物、共價鍵晶體甚至離子晶體等.在最近一二十年間,有大量的新型材料是在極端條件下被設計和預測的[1?6].擁有全新的力學、光學和電學等物理特性的聚合物不斷地被發現和報道[1,6?13],其中CO分子晶體就是被廣泛研究的一種[14,15].原因在于CO氣體比N2和CO2氣體更容易形成分子晶體,研究發現CO2和N2只有在高壓下才能形成分子晶體,N2需56 GPa[11]左右,CO2要相對容易一些,也需20 GPa[12].而對于CO氣體,在10 GPa以下即可得到分子晶體[16?18].N2分子需要110-130 GPa的超高壓才能形成高聚物[3,9,19],CO2分子也需要40-80 GPa的壓強才能合成聚合物[2,4,20?24],而CO分子在4 GPa左右即能形成聚合物[25].此外,最新研究發現聚合物狀態的CO比CO分子晶體能量更低.CO固體狀態的多樣性吸引著科研工作者一直致力于此方面的研究.
早在20世紀70年代,CO的固態相變過程已經開始被人們研究.例如低溫低壓下(4 GPa,50 K左右),氣體就可以轉化為ε相聚合物,形成菱方晶格的CO固體,此時如果溫度升高到100 K時,ε相轉化為δ相,形成立方晶格的CO固體[25].當壓強升到5 GPa,共價鍵就會發生化學變化,由CO轉化為二氧化三碳(C3O2)和三氧化二碳(C2O3),接著C3O2也會分離,僅剩余二聚體-C2O3[26,27].但在1998年,有實驗組經過更加精確的紅外分析法和拉曼分析法得出了相悖的結論-沒有任何證據證明C3O2分子的存在,同時也就不能推斷出C2O3二聚體的存在[14].同年,有研究表明CO在低壓下更易形成五環狀的CO高聚物[15].隨著科技的進步,CO晶體材料的研究得到了廣泛的發展,不斷有新的發現被報道,從0 GPa到80 GPa,壓強不斷升高的過程中,CO氣體發生了一系列變化,由氣體到高聚物、到分子晶體、到原子晶體,Sun等[16]給出了系統詳細的分析.研究顯示,CO分子晶體結構要比CO高聚物更穩定,鏈狀的CO晶體結構要比分子晶體穩定.當壓強為0 GPa時,Pnma和P21/m空間群CO晶體結構要比α相的CO分子晶體在能量上低0.18 eV/CO,而α相的CO分子晶體是由液態CO在低溫大氣壓下結晶形成的[18],在低壓下,Pnma和P21/m空間群的CO晶體結構是目前研究中最穩定的結構狀態.
在低壓下,Sun等[16]認為,通過共價鍵和范德瓦耳斯力形成的鏈狀晶體結構是CO的最穩定結構.納米管束結構內部是共價鍵,管與管之間是范德瓦耳斯力,Pnma和P21/m空間群的CO晶體結構也類似,分子鏈內為共價鍵,分子鏈之間為范德瓦耳斯力.既然CO能夠形成鏈狀晶體,那么CO能不能形成類似的管束狀晶體呢? 以此推測,本文設計了一種新型納米管束狀結構的CO晶體.其內部由碳原子搭建成環狀結構,每個碳原子連接兩個氧原子構成一個結構單元,兩個結構單元之間通過氧?氧共價鍵連接.通過分析顯示,CO納米管束結構中,內部為碳五環時(Bundles?5),在能量上最穩定.在Bundles?5中,每個碳原子均為sp3雜化,且碳原子與碳原子的夾角約為109.5°,接近于金剛石的雜化方式,因此Bundles?5在所有管束狀結構中最穩定.計算分析表明,低壓下Bundles?5晶體結構的能量比空間群為Pnma和P21/m的CO鏈狀晶體結構更低.通過分析電子結構性質得知,管束狀晶體結構是寬帶隙半導體,而鏈狀CO晶體是金屬性質,因為密度泛函理論會低估帶隙的寬度,本文中用雜化泛函(HSE)理論對五環納米管的帶隙進行了校正,約為4.44 eV.新型納米管束狀結構的CO晶體,填補了CO晶體結構中無管束狀結構的空白,同時也打破了低壓下CO晶體結構僅為金屬性質的結論,這為研究低壓下CO的晶體結構提供了新的方向.
2 計算方法
本文運用基于密度泛函理論[28,29]的第一性原理軟件包VASP[30,31]計算分析了CO晶體的幾何結構、能量性質、電子性質以及管束狀結構的堆垛方式.第一性原理計算所選取的方法為投影綴加平面波方法,電子和電子之間的交換關聯泛函采用的是廣義梯度近似中的Perdew?Burke?Ernzerhof(PBE)泛函來描述電子之間的相互作用[32,33].在PBE交換關聯泛函的基礎上,通過雜化泛函理論[34,35]對晶體的電子結構性質進行了校正.通過測試,截斷能選取為600 eV;在結構優化的過程中,納米管結構的K點選為1 × 1 × 5;在電子結構性質的計算分析過程中,K點的選取更密集,為1 × 1 × 9.規定每種納米管結構在z方向是周期性的,而在x方向和y方向上,固定20 ?的真空層,以杜絕管與管之間的分子間相互作用力,從而達到分析納米管結構的目的.對于納米管束狀結構,依據納米管結構橫截面的不同,采用不同的密堆積方式將納米管堆積成納米管束狀結構,調整控制范德瓦耳斯力的參數使管與管之間存在范德瓦耳斯力.對于納米管束狀結構,在結構優化的過程中,K點選取為5 × 5 × 5,而在電子結構性質的計算中K點為7 × 7 × 7.通過VASP外接PHONPY軟件包的方法計算聲子譜,進一步證明結構的穩定性,聲子譜超胞選取為1 × 1 × 9,其高對稱性K點的選取與VASP計算分析能帶結構中K點的選取是一致的.在本文中,為體現分析的準確度,所有對比性分析的調控參數都是完全一致的.
3 研究內容分析
3.1 納米管結構的設計以及穩定性分析
根據碳原子與氧原子的成鍵方式,本文中搭建了六種不同的CO納米管.因為碳原子最外層有四個價電子,可以形成四條共價鍵,氧原子最外層有六個價電子,可以形成兩條共價鍵,因此納米管的內部均由碳原子構成,形成碳環,由3-8個碳原子組成,每個碳原子除構成碳環的兩條共價鍵,還有連接氧原子的一條碳?氧共價鍵,如圖1(a)的內插圖所示,氧原子作為橋梁連接兩個不同的碳環,按照這個規律就構成內部由碳原子構成碳環,通過氧原子連接碳環在z方向上形成無限長的CO納米管結構.根據Bader電荷分析可知,無論是何種納米管,每個原胞中,碳原子最外層的電子密度是相同的,即碳原子是等價的,同樣氧原子最外層的電子密度也是相同的,即原胞中每個氧原子也是等價的,每個原胞中,每個碳原子向與其連接的氧原子轉移0.95-0.99個電子,如表1所列,兩者形成共價鍵.在圖1(a)中每個氧原子連接兩個碳原子,原胞中一個碳原子,隔壁原胞中一個碳原子,每個碳原子為氧原子提供一個電子形成共價鍵,恰好與Bader分析相對應.按照內環碳原子的個數,這些納米管被命名為Tube?3,Tube?4,Tube?5,Tube?6,Tube?7,Tube?8,圖2(b)即為Tube?3-Tube?8的橫截面圖.

圖1 (a)每種CO納米管的相對能量;(b)每種CO納米管鍵角相對于直徑的函數圖像Fig.1.(a) Relative energy of each CO nanotube;(b) the bond angle as a function of the diameter of each CO nanotube.

表1 CO納米管的鍵長dC-C和dC-O,每個CO單元的總能量Etol和形成能Ecoh,以及納米管每個原胞中碳原子轉移給氧原子的電荷數CCHG-OCHGTable 1.Structural parameters of Tube?3?Tube?7,where dC-C is bond length between carbon atoms,dC-O is bond length between carbon atom and oxygen atom;total energy (Etol) and cohesive energy (Ecoh);electron transfer from carbon atom to oxygen atom (CCHG-OCHG).
每種納米管的重復單元(即原胞)的碳原子個數是不一樣的,碳環的直徑也是不一樣的,也就意味著環與環之間的橋梁,即氧原子的相對位置也是有區別的,為了解決這些問題,沿著周期性方向上的晶格掃描過程是必不可少的.按照納米管設計的原則,z方向為納米管的周期性方向,所以在此方向晶格基矢是放開的,在x方向和y方向晶格基矢均為固定值,20 ?的真空層,以隔絕納米管之間的相互作用.當然原胞中的原子坐標是放開的.通過晶格掃描,以納米管在z方向上的晶格基矢長度為橫坐標,以能量為縱坐標,做出不同納米管隨著z方向上晶格基矢長度變化的能量分析圖,如圖2(a)所示.通過圖像可知,構成納米管內部碳環的碳原子數越少即碳環直徑越細,環與環之間的距離越遠,當然,從能量上比較碳五環結構的納米管能量最低,即五環納米管結構(Tube?5)是最穩定的納米管結構,這與之前的研究有一定的相符性,CO氣體在低壓下容易形成五邊形結構[15].由圖2的能量分析圖還可以看出,碳四環和六環的CO納米管(Tube?4和Tube?6)能量相對較低,結構較穩定,而碳三環、七環和八環的納米管結構(Tube?3,Tube?7 和Tube?8)能量較高.根據形成能的計算公式Ecoh=Etol-Egas,其中Etol為體系平均到每個CO單位上的總能量,Egas為氣態CO分子的總能量,所得到的形成能平均到每個CO單位上為Ecoh,所得結果如表1所列,Tube?3和Tube?8的形成能大于零,雖然Tube?7的數值小于零,但是能量較高,而Tube?4,Tube?5和Tube?6納米管的形成能比較低,相對更穩定.基于以上能量分析,在接下來的研究過程中,本文僅對在能量上較穩定的Tube?4,Tube?5 和Tube?6進行對比討論,而Tube?3,Tube?7 和Tube?8納米管不再討論.
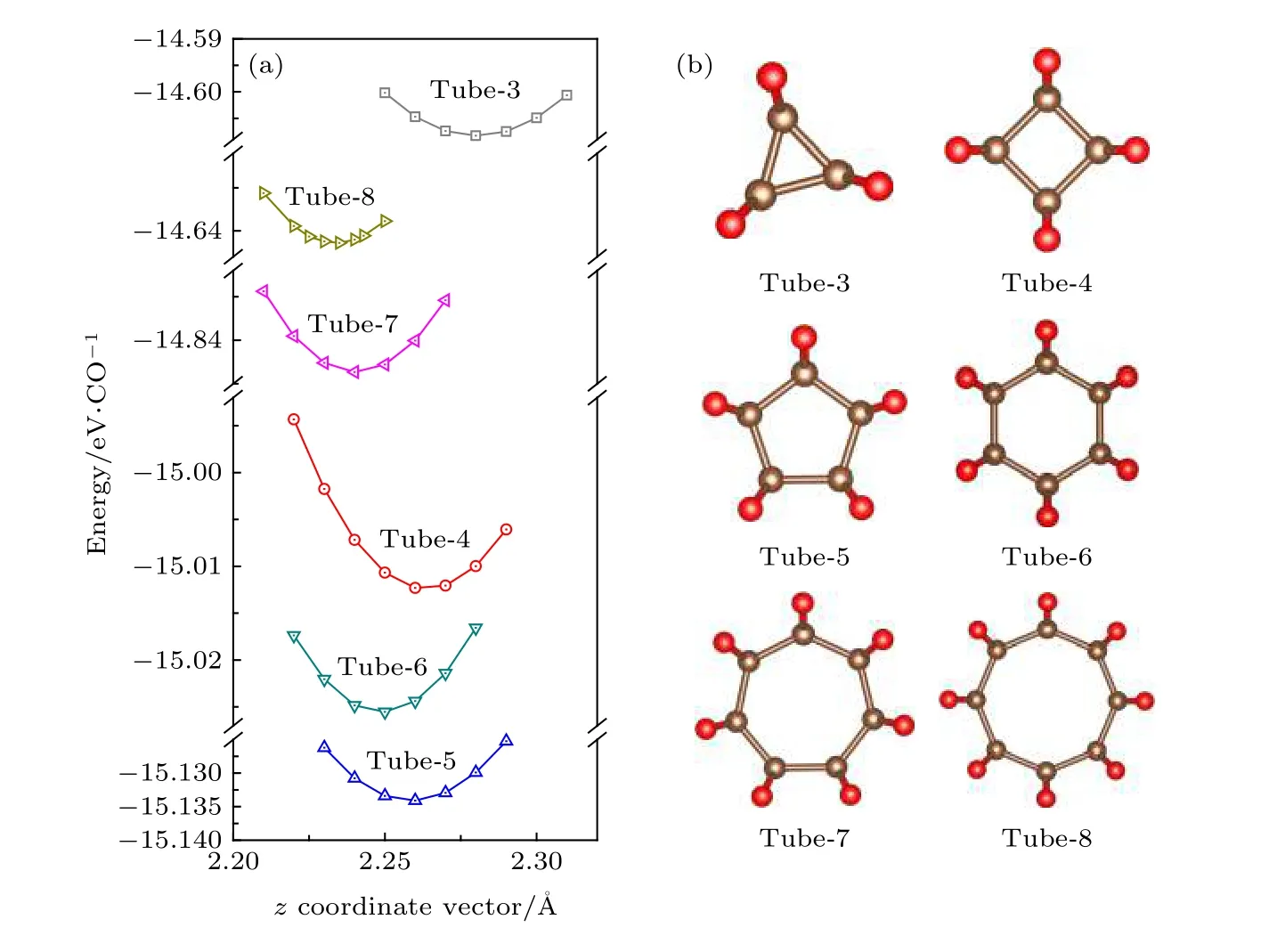
圖2 各納米管z方向晶格掃描能量圖(a)和橫截面圖(b)Fig.2.Lattice scanning energy diagrams (a) and cross sections (b) of various nanotubes according z direction.
通過晶格基矢的掃描得知,Tube?5納米管碳環與碳環之間的距離是2.26 ?,即z方向上的基矢即為2.26 ?.以碳環的碳原子個數為橫坐標,以每種納米管最穩定能量相對于Tube?5納米管的相對能量為縱坐標,即Tube?5納米管的能量為零,做出相對能量與碳環碳原子個數的曲線圖(圖1(a)).通過圖像可知,Tube?5納米管能量最低,即最穩定.
那么Tube?5 CO納米管最穩定的原因是什么呢? 圖1(a) 中,以Tube?5的結構為例,三個碳原子構成的正N邊形的內角,即碳?碳?碳角(∠1-∠CCC),每個碳原子與橋梁氧原子以及相鄰碳原子構成外角,即氧?碳?碳角(∠2-∠OCC).內角和外角隨CO納米管直徑的變化規律如圖1(b)所示.通過分析六種CO納米管中碳原子的兩種鍵角,得到以下結論: 隨著直徑的變大,內角越來越大,外角越來越小.而Tube?5納米管的內角和外角分別為108.0° 和110.5°,恰好與金剛石的鍵角(109.5°)最為相近.因此Tube?5 CO納米管中碳原子的雜化方式,最接近于金剛石中的碳原子,即sp3雜化,而其他納米管的碳原子雜化方式是不完全的sp3雜化.碳位于第四主族,具有三種截然不同的雜化方式: sp,sp2,sp3.自然界中目前發現的天然碳單質為石墨(sp2雜化)、金剛石(sp3雜化)和無定形碳.由圖1(b)分析可知,Tube?5納米管的雜化方式與金剛石最接近,這可以解釋為什么Tube?5納米管最穩定.與此同時,對于不同納米管的鍵長我們也進行了定量的分析,如表1所列,在不同的納米管中,碳?氧鍵的鍵長處于1.40-1.41 ?之間,并不受CO納米管直徑變化的影響,而碳?碳鍵的鍵長隨著納米管直徑的增大而增大,在相同的計算參數下,金剛石碳?碳鍵長為1.55 ?,其數值介于Tube?3-Tube?5鍵長之間.當然驗證新型材料是否穩定的方式有很多種,能量上是否收斂僅僅是一個方面.目前,用聲子譜是否有虛頻也是驗證能量穩定性的方式之一,為此,本文通過PHONOPY軟件包計算分析了Tube?4,Tube?5 和Tube?6三種納米管的聲子譜,如圖3(a)所示,這三種納米管均沒有虛頻,再一次驗證了Tube?4,Tube?5 和Tube?6三種CO納米管在能量上的穩定性.為證明納米管的熱力學穩定性,在室溫下(T=300 K),每種納米管以1 fs的速度振動5000步,納米管材料的結構保持不變,而且能量趨近于穩定值,如圖3(b)所示,雖然模擬時間很短,但也在一定程度上驗證了納米管材料的熱力學穩定性.
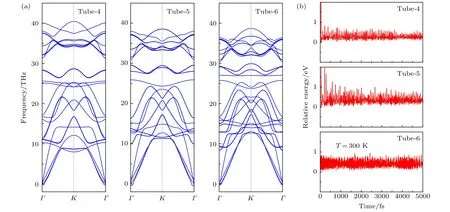
圖3 (a) Tube?4-Tube?6的聲子譜;(b)分子動力學模擬圖像Fig.3.(a) Phonon spectra and (b) evolution of energy as a function of time during the molecular dynamics simulations at 300 K of Tube?4? Tube?6.
3.2 CO納米管束的穩定性分析和電子結構性質預測
最新研究表明,通過范德瓦耳斯力堆垛而成的CO納米鏈的晶體結構,比CO分子晶體結構更穩定,其空間群為Pnma和P21/m,并且在低壓下,鏈狀晶體結構是目前發現的最穩定結構[16].而我們提出的CO納米管也可以通過范德瓦耳斯力堆垛形成三維晶體結構,類似于碳納米管束狀結構.表2列出了三種納米管按照不同的密堆積方式計算得出的總能量,通過計算分析能量的穩定性,三種較穩定的CO納米管堆垛方式如圖4所示,將CO納米管束狀晶體結構分別命名為Bundles?4,Bundles?5和Bundles?6.Bundles?4納米管束狀晶體是正方格子,而Bundles?5和Bundles?6通過六角密堆積方式構建而成.納米管內是共價鍵相互作用,而納米管之間是范德瓦耳斯力相互作用,這與碳納米管束是完全一致的.

表2 CO納米管束不同密堆積方式的總能量(單位: eV/CO)Table 2.Total energy of different dense packing modes of nanometer tube bundles (in eV/CO).

圖4 Tube?4-Tube?6納米管堆垛而成的納米管束結構Fig.4.Structure diagram of nanotube bundle.
之前的研究顯示鏈狀晶體結構在低壓下是最穩定的結構,比CO分子晶體還要穩定,而這兩種鏈狀結構和納米管束狀結構的共同點在于: 均有單條納米帶或者納米管通過范德瓦耳斯力堆垛形成晶體,內部主要是共價鍵的作用,鏈與鏈、管與管之間是范德瓦耳斯力的相互作用.為此,我們將CO納米管束狀晶體結構和Pnma和P21/m這兩種鏈狀結構進行分析對比,圖5(a)給出了這三種結構隨著壓強增大焓值的變化量.其中焓值是通過公式H=U+PV計算所得,U為0 K下結構的內能值,P為晶體結構外部環境的靜水壓強,V為每個CO單元的體積.通過圖5(a)的對比分析可知,在10 GPa以下的低壓下,Bundles?5 納米管束狀晶體結構比Pnma和P21/m兩種鏈狀晶體結構更穩定.在非常小的壓強下,如1 GPa以下,Bundles?4 和Bundles?6 納米管束狀晶體結構不如Pnma和P21/m兩種晶體結構穩定.但隨著壓強的增大,管束狀結構的晶體結構變得更穩定,特別是Bundles?6 納米管束晶體,當壓強大于1 GPa時,它的穩定性就大于P21/m和Pnma兩種鏈狀晶體.在壓強大于8.6 GPa時,其穩定性就超越了Bundles?5納米管束狀結構.因此通過焓值的變化可以判定,在低壓下CO納米管束狀結構更穩定.

圖5 (a)五種不同一氧化碳晶體的焓變函數;(b) Bundles?5帶隙和結構參數隨壓強的變化Fig.5.(a) Enthalpy function of five different kinds of car?bon monoxide crystals;(b) band gap and structural para?meters vary with pressure of Bundles?5.
晶體的電子結構性質受共價鍵的影響比較大,受分子間相互作用力的影響較小.如圖5(b) 所示,本文以Bundles?5 CO納米管結構為例,研究CO納米管的晶體結構參數隨壓強的變化.在圖5(b)中,納米管結構的共價鍵對于壓強的變化并不敏感,無論是碳?碳共價鍵還是碳?氧共價鍵在壓強增加時,其變化非常小,但是納米管間的距離對于壓強來說是十分敏感的,壓強越大,管間距越近,也就意味著晶格體積越小.雖然隨著壓強的增加,共價鍵變化很小,分子之間的相互作用力,即范德瓦耳斯力變化還是很大的.但眾所周知,范德瓦耳斯力對于材料的電子結構性質的影響是有限的,可以忽略,所以文中用納米管Tube?4,Tube?5,Tube?6的電子結構性質來預測納米管束Bundles?4,Bundles?5,Bundles?6的電子結構性質.如圖6所示,通過分析Tube?4-Tube?6 CO納米管能帶結構圖可知,CO納米管結構均為非直接帶隙的半導體,相應的帶隙大小分別為 2.60,2.93和 3.07 eV.由于PBE泛函的交換關聯算法一般都會低估材料的帶隙,因此本文采用雜化關聯泛函(HSE06)的方式校正了納米管結構的帶隙,校正后,Tube?5 CO納米管結構的帶隙為4.44 eV,但能帶隨高對稱性點的變化趨勢是一樣的.由此可以推斷出,CO的納米管束狀晶體結構應該是寬帶隙的半導體.相對于Pnma和P21/m兩種鏈狀晶體的金屬性質,CO納米管束狀晶體的電子結構與鏈狀晶體截然不同,CO納米管束狀結構為半導體性質.因此可知低壓下,CO的固態相既可以是金屬,也可以是半導體.

圖6 Tube?4-Tube?6的能帶結構Fig.6.Band gap of Tube?4?Tube?6.
4 結 論
本文設計提出一種新型CO低壓下的固態相-納米管束狀結構.通過晶格基矢的掃描分析,Tube?5 CO納米管具有能量的最穩定性,原因主要為Tube?5 CO納米管中碳原子的雜化方式與金剛石最相近.聲子譜的計算分析顯示Tube?4-Tube?6 CO納米管均沒有虛頻,從而驗證了CO納米管的穩定性.不同壓強下,焓值的結果證明CO納米管束狀材料比Pnma和P21/m空間群的鏈狀晶體在能量上更穩定.并且CO納米管束狀材料打破了CO固態僅為金屬的猜想,也可能是半導體,甚至未來還會存在絕緣體.CO納米管束狀晶體設計的提出不僅豐富了低壓下CO晶體結構與電子性質的多樣性,還為分析CO固態相提供了新的研究方向.
感謝山東大學物理學院趙明文教授、山東建筑大學楊博博士以及河南農業大學劉小標老師的討論.

