冠狀動脈粥樣硬化心臟病患者血清CTRP1水平與糖脂代謝、胰島素抵抗的關系
湯 巍
冠狀動脈粥樣硬化性心臟病(冠心病)為重要冠狀動脈血管發生動脈粥樣硬化病變引起的血管腔狹窄或阻塞[1],其中約有2/3患者合并糖代謝異常,部分糖尿病患者入院后才被確診,且是冠心病的危險因素。胰島素抵抗(insulin insistence,IR)為各種原因造成的胰島素促進葡萄糖攝取及轉化效率下降,機體為保持血糖穩定會代償性分泌過多胰島素,導致高胰島素血癥。有學者[2]指出IR為促進代謝綜合征的重要因素,為冠狀動脈粥樣硬化的重要機制。C1q/腫瘤壞死因子相關蛋白(complement C1q/tumor necrosis factor-related protein,CTRP)家族為結構同脂聯素(adiponectin,APN)相似的一組蛋白,有15個成員[3],其中補體C1q腫瘤壞死因子相關蛋白1(CTRP1)為新近發現的與APN有同源序列的蛋白質,其通過影響組織糖脂代謝、抗血栓等生物作用參與機體炎癥的調節。有研究[4]證實了CTRP1與冠狀動脈病變發生、發展相關,隨冠心病嚴重程度增加,CTRP1水平升高。但關于CTRP1與冠心病患者糖脂代謝、IR的關系研究較少。該文主要分析冠心病患者血清CTRP1水平與糖脂代謝、IR的關系,結果如下。
1 資料與方法
1.1 一般資料選取2017年5月—2019年4月筆者所在醫院心內科經冠狀動脈造影(CAG)確診的冠心病患者120例。納入標準:(1)符合1979年世界衛生組織(WHO)頒布的缺血性心臟病定義,經病史、體格檢查、心電圖、心臟超聲與CAG等確診;(2)臨床資料及相關實驗室檢查數據完整;(3)無嚴重器質性病變。排除標準:(1)急性心肌梗死、周圍血管性疾病、嚴重肝腎功能異常、慢性阻塞性肺疾病、結締組織疾病者;(2)合并冠心病以外的其他嚴重心臟病如心肌病、瓣膜病;(3)合并血液系統疾病、全身免疫系統疾病、惡性腫瘤、近期有手術史或精神障礙者。依據1997年美國糖尿病學會(ADA)的糖尿病診斷標準將其分為A組 (正常糖耐量,n=42)、B 組(糖耐量異常,n=35)、C 組(2 型糖尿病,n=43)。
1.2 方 法
1.2.1 基線資料搜集 搜集三組一般資料 (性別、年齡、高血壓史、吸煙史)、臨床資料[入院時測定的空腹血糖(FBG)、糖化血紅蛋白(HbA1c)、空腹胰島素(FINS)、胰島素抵抗指數(HOMA-IR)、三酰甘油(TG)、 總膽固醇 (TC)、血清 CTRP1、脂聯素(APN)]。 (1)常規生化指標檢測:FBG、FINS 以氧化酶法、酶法(Beckman CX9型全自動生化儀)測得,TG、TC也經全自動生化分析儀測定;(2)HOMA-IR計 算 方 法 :HOMA-IR=FBG×FINS/22.5, 正 常 人HOMA-IR水平為1;(3)CTPR1及APN水平測定:將抽取的靜脈血放置于普通玻璃管,在血液凝固后于4℃下高速離心 (2506×g),10 min后抽取上清液放入EP管,置于-80℃下保存,應用酶聯免疫吸附試驗(ELISA)測定CTRP1及APN水平,試劑盒均購自上海森雄科技實業有限公司。
1.2.2 冠狀動脈病變狹窄程度評估 應用數字減影心血管造影系統INNOVA 3100(美國GE公司),以標準Judkin法進行CAG檢查,≥2個垂直角度造影完全暴露病變,對CAG圖像進行定量分析,評估冠脈病變狹窄程度。Gensini積分方法[5]:對每支冠狀動脈病變狹窄程度進行定量評估,首先依據冠狀動脈狹窄程度確定基本評分,狹窄直徑<25%計1分,25%~50%計 2分,51%~75%計 4分,76%~90%計8分,91%~99%計16分,100%計32分,后依據不同冠狀動脈分支確定相應系數,其中左主干(LM)病變×5,左前降支(LAD)病變:近段×2.5,中段×1.5,遠段×1; 對角支病變:D1×1,D2×0.5; 左回旋支(LCX)病變:近段×2.5,鈍緣支×1,遠段×1,后降支×1,后側支×0.5;右冠狀動脈(RCA)病變:近、中、遠和后降支均×1。以每個冠狀動脈的狹窄基本評分乘以該病變部位系數,即為該病變血管評分,各病變血管得分總和即為該患者冠狀動脈病變狹窄程度總評分。
1.3 統計學方法采用SPSS 19.0軟件處理數據,計數資料以(%)表示,采取χ2檢驗;計量資料以()表示,行單因素方差分析及LSD-t檢驗,服從正態分布各變量間相關性采用Pearson相關分析。P<0.05為差異具有統計學意義。
2 結果
2.1 三組患者一般資料及臨床資料比較C組FBG、HbA1c、FINS、HOMA-IR、TG、TC、Gensini評分及血清CTRP1顯著高于A組、B組,C組APN顯著低于A組、B組(P<0.05)。見表1。
2.2 不同冠狀動脈病變患者糖脂代謝、胰島素抵抗指標比較不同冠狀動脈病變者FINS、TC比較差異無統計學意義(P>0.05),隨冠狀動脈病變支數增多, 患者 FBG、HbA1c、HOMA-IR、TG、Gensini評分及血清CTRP1增加,而APN下降(P<0.05);冠狀動脈多支病變者血 清 FBG、HbA1c、HOMA-IR、TG、Gensini評分及血清CTRP1高于單支病變者,而APN低于單支病變(P<0.05);多支病變者HbA1c、TG、Gensini評分及血清CTRP1高于雙支病變者,而APN低于雙支病變者(P<0.05);單支病變、雙支病變者血清 FBG、HbA1c、HOMA-IR、TG、Gensini評分、CTRP1、APN比較差異也有統計學意義 (P<0.05)。 見表2。
2.3 冠心病患者CTRP1水平與糖脂代謝、胰島素抵抗的關系分析Pearson相關分析顯示,冠心病患者血清 CTRP1 水平與其 FBG、HbA1c、TG、Gensini評分呈正相關,與APN呈負相關(P<0.05)。見表3。

表2 不同冠脈病變患者糖脂代謝、胰島素抵抗指標比較
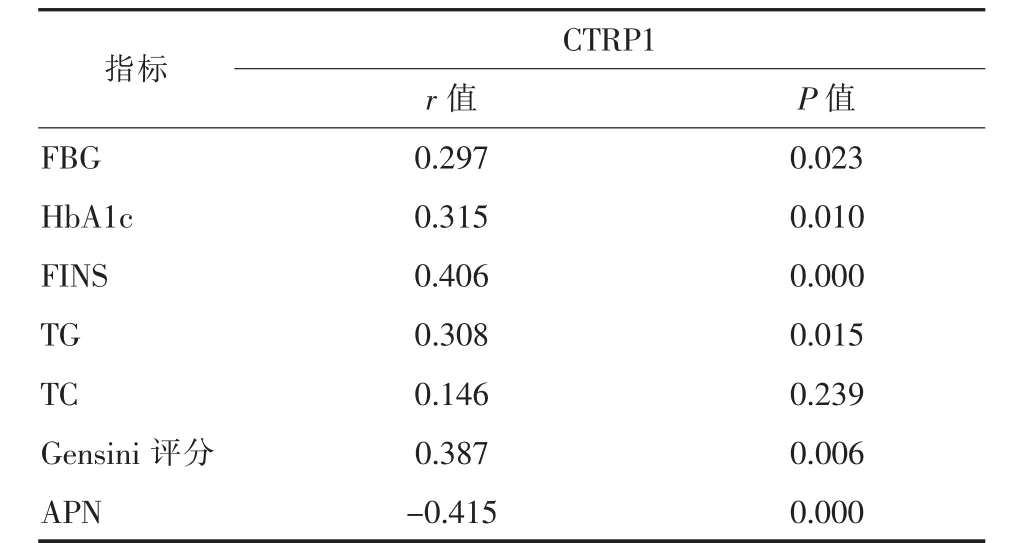
表3 冠心病患者CTRP1水平與糖脂代謝、胰島素抵抗的關系分析
3 討論
IR與心血管疾病密切相關,參與動脈粥樣硬化發生發展,尤其是與冠心病的嚴重程度強烈相關[6],有研究[7]發現IR與冠心病斑塊纖維帽弧度成明顯負相關性。脂肪組織可分泌多組織因子及激素參與機體代謝平衡的調節,其中APN研究較多,APN為有胰島素增敏性的脂肪因子,可在多方面發揮調節糖脂代謝作用[8]。CTRP蛋白為一類脂肪細胞源性細胞因子,其具有與APN高度相似的結構域及生化特征,近年來有不少研究[9,10]報道 CTRP3、CTRP12與冠心病、糖尿病患者有相關性,而CTRP1也是CTRP家族中一員,主要表達于心臟、肌肉與脂肪組織,同血管調節、血小板聚集、局部炎癥反應、免疫反應等有密切關系[11],但目前關于CTRP1與冠心病患者糖脂代謝、IR的關系研究甚少。
該研究中,C 組 FBG、HbA1c、FINS、HOMA-IR、TG、TC、Gensini評分及血清CTRP1顯著高于A組、B組,C組 APN顯著低于 A組、B組 (P<0.05);A組、B組上述指標差異也有統計學意義,表明冠心病患者存在糖脂代謝紊亂及IR,與常學偉等[12]報道的IR為判斷冠心病并糖耐量受損患者冠狀動脈狹窄程度重要指標的結論相似。IR導致動脈粥樣硬化的機制可能為增強氧化應激,使非感染性慢性炎癥反應持續過度激活,誘導細胞增殖,或放大心血管危險因子影響而加重動脈粥樣硬化,或餐后高血糖加重IR與胰島素分泌缺陷,損傷血管內皮細胞,促進動脈粥樣硬化,因此在冠心病患者中存在IR及糖脂代謝紊亂[13]。CTRP1為新近發現的脂肪因子,在冠心病合并糖耐量受損及冠心病患者中,IR的增強反饋性調節血清中CTRP1水平升高,而升高的CTRP1可特異性激活蛋白激酶B(Akt)與p44/42絲裂原活化蛋白激酶(MAPK)信號通路,從而增加葡萄糖轉運體4(GLUT4)向細胞膜轉運,增強肌肉組織對葡萄糖的吸收,繼而發揮降糖作用[14]。同時該研究中隨冠狀動脈病變支數增多,患者FBG、HbA1c、HOMA-IR、TG、Gensini評分及血清 CTRP1增加,而APN下降,其中多支病變者HbA1c、TG、Gensini評分及血清CTRP1高于單支、雙支病變者,而APN低于雙支病變者,與王輝宇[15]報道的IR與冠心病嚴重程度相關的結論一致,表明隨冠心病患者病變程度加重,其糖脂代謝紊亂及IR可能更嚴重,尤其是CTRP1與冠心病病變的關系值得關注。Wang等[16]的研究也發現,CTRP1與冠狀動脈病變發生、發展相關。
曹雪明等[17]的研究發現,冠心病患者側支循環程度與CTRP1、IR有密切關系,且CTRP1水平與FBG、HOMA-IR、TG、IL-6呈顯著正相關性。該研究Pearson相關分析顯示,冠心病患者血清CTRP1水平與其 FBG、HbA1c、TC、Gensini評分成正相關,與上述報道結果相近,說明CTRP1與冠心病患者糖脂代謝紊亂、IR有著密切關系。目前研究[18]證實CTRP1在炎癥反應中具有調節免疫、炎癥介質釋放、細胞分化凋亡等功能,因此CTRP1作為肥胖、IR與血糖升高的保護因素發揮作用,其在物質代謝、炎癥、免疫方面的功能將可能對糖尿病、冠心病等心血管疾病的治療提供一個新靶點[19]。動物實驗研究[20]也表明,CTRP1在糖脂代謝方面發揮作用為通過增強腺苷酸活化蛋白激酶磷酸化,抑制其下游乙酰輔酶A 羧化酶活性。Shabani等[21]發現,CTRP1參與患者脂肪肝疾病等慢性病發生發展,且作用機制可能與IR有關。該研究也發現,CTRP1與APN存在負相關關系,與既往研究[22]發現糖尿病患者血清中CTRP1與APN存在負相關關系的結果相符。此外,CTRP1與APN存在動態平衡,當血糖水平升高時APN水平下降,CTRP1水平升高進而起到拮抗血糖進一步升高,維持血糖的作用[23],但CTRP1在調節糖脂代謝中的確切分子機制與受體途徑尚不清楚,研究較有限,有待更多的試驗室深入研究。
綜上所述,CTRP1與冠心病患者糖脂代謝紊亂、IR有著密切關系,有望為冠心病患者的降糖治療提供一個新靶點,其作用機制值得深入研究。

