帕瑞昔布鈉對乳腺癌患者外周血CD4+CD25+調節性T 細胞的影響*
李志藝, 顏振藝, 劉曉燕, 李大桁
(廣東醫科大學附屬醫院 麻醉科, 廣東 湛江 524001)
乳腺癌是女性最常見的惡性腫瘤,其發病率逐年上升。在歐美國家,乳腺癌占女性惡性腫瘤的 25%~30%[1];在我國,乳腺癌發病率已經上升為女性惡性腫瘤的第1位,成為婦女健康的最大威脅[2]。手術仍是治療乳腺癌的常用方式,但術后復發率還是很高,手術和麻醉對機體的免疫系統的抑制作用是乳腺癌術后復發的主要原因之一[3]。近年來的研究發現, CD4+CD25+調節性 T 細胞(CD4+CD25+Treg)可抑制抗腫瘤免疫[4],還發現COX-2抑制劑對乳腺癌轉移的抑制作用可能與其減少 CD4+CD25+Treg細胞的產生有關[5]。帕瑞昔布鈉(parecoxib sodium)是一種高選擇性 COX-2 抑制劑,已被廣泛應用于臨床圍術期鎮痛,其臨床療效已在口腔科、婦科及骨科等多種手術術中及術后得到證實[6-8]。研究表明帕瑞昔布鈉能夠降低圍手術期的免疫抑制[9],但目前還未見帕瑞昔布鈉對 CD4+CD25+Treg 細胞影響的研究報道。本研究對術前的乳腺癌患者給予帕瑞昔布鈉用藥,觀察麻醉誘導前 30 min、術畢及術后48 h乳腺癌患者外周血 CD4+CD25+調節T細胞比例、血清轉化生長因子β(TGFβ)及白細胞介素-10(IL-10)水平變化,探討帕瑞昔布鈉降低術后免疫抑制的機制,為乳腺癌手術的麻醉用藥提供參考。
1 資料與方法
1.1 研究對象
女性乳腺癌患者40例,45~60歲,平均54歲。臨床分期為Ⅱ期,無注射帕瑞昔布鈉禁忌癥,排除術后病理不是Ⅱ期患者,患者或其家屬知情同意參與本研究。將患者隨機分為觀察組和對照組,每組各20例,兩組患者年齡、病情程度等方面比較,差異無統計學意義(P>0.05)。
1.2 方法
所有患者均進行麻醉誘導:靜脈注射咪唑安定、異丙酚、舒芬太尼、順阿曲庫銨,患者意識消失后經口氣管插管進行機械通氣;觀察組患者于手術切皮前 15 min 給予帕瑞昔布鈉 40 mg,對照組給予等量生理鹽水處理;兩組患者分別于麻醉誘導前 30 min(T1)、術畢(T2)和術后48 h(T3)抽取外周血進行后續研究。
1.3 觀察指標
1.3.1外周血CD4+CD25+Treg細胞比例 取患者新鮮外周血5 mL,加入淋巴細胞分離液,離心分離獲取外周血淋巴細胞。分別加入相應的熒光標記抗體:FITC-CD4抗體、PE-CD25抗體,避光孵育25 min,加入PBS洗滌2次,重懸后上流式細胞儀檢測CD4+CD25+Treg細胞含量,計算外周血CD4+CD25+Treg細胞比例。
1.3.2血清TGFβ和IL-10水平 取患者新鮮的外周血5 mL,2 500 r/min離心10 min分離血清,采用酶聯免疫吸附試驗(ELISA)檢測,按試劑盒操作說明檢測血清TGFβ和IL-10含量。
1.4 統計學分析
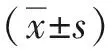
2 結果
2.1 CD4+CD25+Treg細胞占CD4+T細胞比例
結果顯示,對照組患者T2、T3時點外周血CD4+CD25+Treg細胞比例均顯著高于T1時點,差異有統計學意義(P<0.01);觀察組患者T2、T3時點CD4+CD25+Treg細胞比例均顯著低于對照組同時點,差異有統計學意義(P< 0.01)。見圖1。

注:(1)與同組T1時點比較,P<0.01;(2)與同時點對照組比較,P<0.01。圖1 兩組患者手術不同時點外周血CD4+CD25+Treg細胞占CD4+T細胞比例Fig.1 The proportion of CD4+CD25+Treg cells to CD4+T cells of breast cancer patients in the two groups at different time points of treatment
2.2 血清TGFβ及IL-10水平
結果顯示,對照組患者T2、T3時點血清TGFβ和IL-10含量均顯著高于T1時點,差異有統計學意義(P<0.01);觀察組患者T2、T3時點血清TGFβ和IL-10含量均顯著低于同時點對照組的數值,差異有統計學意義(P<0.01)。見圖2。
3 討論
在圍手術過程中,創傷和應激會引起的激素、前列腺素、花生四烯酸等物質釋放,抑制自然殺傷細胞(NK)細胞、T 淋巴細胞和樹突狀細胞的功能,導致殘余腫瘤病灶的生長及擴散[10]。而大部分靜脈麻醉藥和吸入麻醉藥都能降低NK等免疫細胞的活性及數量,促進腫瘤的生長及轉移[11]。圍術期免疫抑制發生的最高峰為術后第3天,這也許是術后乳腺腫瘤的微小殘留灶繼續發展和形成轉移的最佳時期,而完好的細胞免疫卻能夠有效地控制這種微小腫瘤轉移灶的發生概率。因此,制定合理的麻醉用藥和麻醉方案,降低機體免疫抑制,對乳腺腫瘤病人預后非常重要,具有重要的臨床意義。
機體抗腫瘤的免疫效應與腫瘤逃避免疫系統的攻擊之間形成一對此消彼長的矛盾關系體[12]。CD4+CD25+Treg細胞是 CD4+T 細胞中具有獨特免疫調節功能的T細胞亞群。研究表明 CD4+CD25+Treg 細胞與人體惡性腫瘤的發生密切相關,其不僅能通過細胞間的直接接觸抑制效應T細胞的功能,還能通過分泌細胞因子等多種方式發揮抑制作用,從而抑制抗腫瘤T細胞免疫,已被公認是一種潛在的腫瘤逃逸機制[13]。國內外研究也發現乳腺癌患者外周血和腫瘤組織CD4+CD25+Treg 細胞數目越多,其復發的可能性越大,預后也越差[14]。近年來,乳腺癌與COX-2的關系日益受到重視,大量的流行病學和實驗證據表明 CO X-2 抑制劑對治療早期和轉移性乳腺癌均有意義[15]。本研究發現對照組術畢和術后CD4+CD25+Treg細胞比例較術前顯著升高,表明手術可上調乳腺癌患者外周血CD4+CD25+Treg細胞含量,使腫瘤易于逃逸,而帕瑞昔布鈉能夠在一定程度上抑制其上調,從而抑制腫瘤逃逸,使乳腺癌患者獲益。帕瑞昔布鈉通過何種途徑抑制CD4+CD25+Treg細胞的上調還需要進一步研究。

注:(1)與同組T1時點比較,P<0.01;(2)與同時點對照組比較,P<0.01。圖2 兩組乳腺癌患者手術不同時點血清TGFβ和IL-10水平Fig.2 Serum levels of TGFβ and IL-10 of breast cancer patients in the two groups at different time points of treatment
TGF-β是一種重要的細胞因子,其參與調控細胞生長、分化和凋亡等過程,而最新研究發現TGF-β能夠促進癌癥逃避免疫,研究也顯示TGF-β抑制劑和可用的免疫治療藥物會增強這種抗腫瘤作用,從而允許免疫系統能夠高效地消除已經建立的轉移瘤[16]。IL-10是多細胞源多功能的細胞因子,參與調節細胞的生長、炎性反應和免疫反應,是公認的炎癥與免疫抑制因子。在腫瘤、造血系統及心血管系統中發揮重要作用[17]。研究表明,Treg能夠分泌TGF-β和IL-10,發揮其調節功能[18]。本研究結果顯示帕瑞昔布鈉在抑制CD4+CD25+Treg細胞含量的同時,還顯著降低了術畢和術后患者血清TGF-β和IL-10的含量,這進一步提示帕瑞昔布鈉可抑制乳腺癌術后的腫瘤逃逸,使帕瑞昔布鈉成為乳腺癌患者圍術期的理想用藥。
綜上所述,本研究發現帕瑞昔布鈉可抑制乳腺癌病人術畢和術后外周血CD4+CD25+Treg以及血清TGF-β、IL-10的水平上調,揭示了帕瑞昔布鈉對乳腺癌病人免疫系統的作用,為乳腺癌病人的麻醉用藥提供一個更好的選擇。

