槲皮素對人骨髓瘤細胞U266侵襲和遷移的影響
楊軍嶺 李曉晴 王莉 楊俠
[摘要]?目的?研究槲皮素對骨髓瘤細胞U266侵襲和遷移的影響及機制。
方法?用不同濃度的槲皮素處理人骨髓瘤細胞U266,噻唑藍(MTT)方法測定細胞存活變化,計算其半數抑制濃度。人骨髓瘤細胞U266分為空白對照組(不做藥物處理)、陽性對照組(用地西他濱處理)、槲皮素組(半數抑制濃度的槲皮素處理)、PDTC組(NF-κB信號抑制劑PDTC處理)、PDTC+槲皮素組(半數抑制濃度的槲皮素和PDTC處理)共5組進行細胞培養。各組以MTT檢測細胞存活能力,劃痕愈合實驗檢測細胞運動能力,Transwell小室檢測細胞侵襲和遷移能力,蛋白免疫印跡(Western blot)檢測細胞中基質金屬蛋白酶2(MMP-2)、核因子-κBp65亞型(NF-κBp65)和基質金屬蛋白酶9(MMP-9)蛋白表達水平。
結果?槲皮素組、PDTC組、PDTC+槲皮素組細胞存活、侵襲、遷移能力及細胞中MMP-2、MMP-9、NF-κBp65表達水低于空白對照組(F=28.419~167.394,P<0.001)。PDTC+槲皮素組細胞存活、侵襲、遷移能力及細胞中MMP-2、MMP-9、NF-κBp65表達水平低于槲皮素組和PDTC組(P<0.05)。
結論?槲皮素能夠通過抑制NF-κB信號通路降低骨髓瘤細胞的侵襲和遷移能力。
[關鍵詞]?多發性骨髓瘤;槲皮素;腫瘤侵潤;腫瘤轉移;NF-κB
[中圖分類號]?R733.3;R977.29
[文獻標志碼]?A
[文章編號]??2096-5532(2019)06-0643-05
doi:10.11712/jms201906004
[開放科學(資源服務)標識碼(OSID)]
EFFECT OF QUERCETIN ON THE INVASION AND MIGRATION OF HUMAN MYELOMA U266 CELLS
YANG Junling, LI Xiaoqing, WANG Li, YANG Xia
(Department of Pharmaceutical, Air Force 986 Hospital, Xi′an?710054, China)
[ABSTRACT] Objective To investigate the effect of quercetin on the invasion and migration of human myeloma U266 cells and related mechanisms.
Methods Human myeloma U266 cells were treated with different concentrations of quercetin. MTT assay was used to measure the change in cell viability, and median inhibitory concentration was calculated. Human myeloma U266 cells were divided into blank control group (without treatment), positive control group (treated with decitabine), quercetin group (treated with quercetin at its median inhibitory concentration), pyrrolidine dithiocarbamate (PDTC) group (treated with the NF-κB signaling pathway inhibitor pyrrolidine dithiocarbamate), and PDTC+quercetin group (treated with quercetin at its median inhibitory concentration and PDTC) for cell culture. MTT assay was used to measure cell viability; the wound healing test was used to evaluate the invasion and migration abilities of cells; Western blot was used to measure the protein expression of matrix metalloproteinase-2 (MMP-2), nuclear factor-kappa B (NF-κB) p65, and matrix metalloproteinase-9 (MMP-9).
Results Compared with the blank control group, the quercetin group, the PDTC group, and the PDTC+quercetin group had significantly lower cell viability, invasion and migration abilities, and expression of MMP-2, MMP-9, and NF-κBp65 (F=28.419-167.394,P<0.001). Compared with the quercetin group and the PDTC group, the PDTC+quercetin group had significantly lower cell viability, invasion and migration abilities, and expression of MMP-2, MMP-9, and NF-κBp65 (P<0.05).
Conclusion Quercetin can reduce the invasion and migration of myeloma cells by inhibiting the NF-κB signaling pathway.
[KEY WORDS] multiple myeloma; quercetin; neoplasm invasivenes; neoplasm metastasis;?NF-kappa B
骨髓瘤是一種惡性漿細胞增殖疾病,造血干細胞移植、新型藥物的應用等大大提高了骨髓瘤病人的生存期,但是由于骨髓瘤具有易復發、轉移快等特點,尋找有效的骨髓瘤治療方法對病人預后具有重要意義[1]。槲皮素具有抗腫瘤活性,其可以抑制乳癌、卵巢癌、胃癌等腫瘤細胞的生長和轉移,但其具體的作用機制尚不明確[2-4]。核因子-κB(NF-κB)是一種在人體內廣泛存在的信號轉導通路,參與炎癥、氧化應激、細胞生長、細胞遷移等多種生理和病理過程,其在惡性腫瘤組織中過度激活,NF-κB抑制劑能夠下調腫瘤細胞的惡性表型[5-7]。相關研究顯示,槲皮素能夠下調肺癌等細胞中NF-κB的激活水平,槲皮素抗腫瘤活性可能與NF-κB信號通路抑制有關[8-9]。有研究結果顯示,槲皮素具有抗多發性骨髓瘤細胞生長的作用,槲皮素處理后的NCI-H929細
胞株的存活能力降低[10]。因此,本研究探討了槲皮素對骨髓瘤細胞增殖、遷移及侵襲的影響及其機制,旨在為延長骨髓瘤病人生存期提供參考。
1 材料與方法
1.1?實驗材料
1.1.1?藥品、試劑和細胞?HRP標記的二抗購自北京索萊寶科技有限公司,槲皮素購自大連美侖生物技術有限公司,基質金屬蛋白酶-2(MMP-2)抗體購自美國Proteintech,基質金屬蛋白酶-9(MMP-9)抗體購自美國Santa Cruz公司,NF-κB信號抑制劑PDTC購自美國Sigma公司,核因子-κBp65亞型(NF-κBp65)抗體購自美國Abbkine,人骨髓瘤細胞U266購自上海江林生物科技有限公司(細胞以含體積分數0.10胎牛血清的RPMI 1640培養液培養。細胞培養參數為:37 ℃,飽和濕度,體積分數0.05 CO2培養箱)。
1.1.2?重要儀器?SpectraMax iD3酶標儀購自美國Molecular Devices,TE2000-U倒置顯微鏡購自日本尼康公司,TGL-18M離心機購自上海盧湘儀離心機儀器有限公司,1658001垂直電泳槽購自美國Bio-Rad。
1.2?實驗方法
1.2.1?噻唑藍(MTT)檢測槲皮素對骨髓瘤細胞存活影響?取生長至對數期的人骨髓瘤細胞U266,以2.5 g/L的胰蛋白酶消化后,接種到96孔培養板中(接種密度為2×107/L,每孔添加100 μL),放在37 ℃、飽和濕度、體積分數0.05的CO2培養箱中培養過夜。在細胞中添加槲皮素,使槲皮素終濃度分別為0、40、80、160、320 μmol/L,繼續培養24 h后,將培養板小心取出,添加20 μL的MTT,置于37 ℃結合4 h,棄上清液。添加二甲基亞砜溶液100 μL,放在振蕩器上反應10 min,以酶標儀測定490 nm波長處的光密度(OD)值。經空白孔調零以后,設置0 μmol/L作用組細胞存活率為100%,分析40、80、160、320 μmol/L濃度的槲皮素處理后細胞存活率變化。實驗設3個復孔,重復3次。
1.2.2?細胞分組?人骨髓瘤細胞U266依次分為:空白對照組(A組)、陽性對照組(B組)、槲皮素組(C組)以及PDTC組(D組)以及PDTC+槲皮素組(E組)共計5組。槲皮素組:采用含有槲皮素終濃度為130 μmol/L的細胞培養液培養;PDTC組:采用含有PDTC終濃度為50 μmol/L的細胞培養液進行培養;PDTC+槲皮素組:采用槲皮素終濃度為130 μmol/L和PDTC終濃度為50 μmol/L的細胞培養液培養;空白對照組:使用不添加槲皮素、地西他濱以及PDTC的細胞培養液培養;陽性對照組:在實驗0 h時用3.2 mmol/L的地西他濱細胞培養液培養。以MTT方法檢測各組細胞不同培養時間細胞存活率變化,步驟同1.2.1。
1.2.3?Transwell小室檢測細胞侵襲和遷移能力
在Transwell小室中添加RPMI 1640稀釋的濃度為100 mg/L的Matrigel,放在37 ℃濕化。取空白對照組、陽性對照組、槲皮素組、PDTC組、PDTC+槲皮素組細胞,用不含血清的培養液懸浮,在Transwell小室的上室內添加105個細胞(200 μL),分別在下室中添加600 μL的含體積分數0.10胎牛血清的RPMI 1640培養液,放在37℃、體積分數0.05 CO2培養箱中繼續培養24 h。將小室取出,用棉簽擦掉沒有穿膜的細胞。甲醇固定,吉姆薩染色,光鏡下選取5個視野觀察侵襲細胞數目。Transwell小室細胞遷移實驗同侵襲實驗,遷移實驗前不用Matrigel濕化。實驗設3個復孔,重復3次。
1.2.4?蛋白免疫印跡(Western blot)檢測細胞中MMP-2、MMP-9、NF-κBp65蛋白表達?空白對照組、陽性對照組、槲皮素組、PDTC組、PDTC+槲皮素組細胞按照上述方法培養24 h,用常規方法分別提取細胞中的總蛋白,蛋白樣品保存在-80 ℃。SDS-PAGE電泳后在冰上轉膜70 min。將電轉后的NC膜取出,置于含體積分數0.05牛血清清蛋白的封閉液中孵育結合2.0 h。NC膜再與MMP-2、MMP-9、NF-κBp65抗體稀釋液在4 ℃過夜反應以后,與HRP標記的二抗反應2.0 h,以ECL發光試劑盒發光。用Quantity One軟件掃描分析MMP-2、MMP-9、NF-κBp65條帶和內參β-actin條帶的灰度值,分析目的條帶表達水平。MMP-2、MMP-9、NF-κBp65抗體分別以1∶600、1∶600、1∶400稀釋,HRP標記的二抗以1∶4 000稀釋。
1.3?統計分析方法
采用SPSS 21.0統計軟件進行分析。計量資料數據以±s形式表示,多組間均數的比較采用單因素方差分析,組間兩兩比較采用SNK(Student-Newman-Keuls)法。
P<0.05為差異有統計學意義。
2?結?果
2.1?槲皮素對骨髓瘤細胞存活能力影響
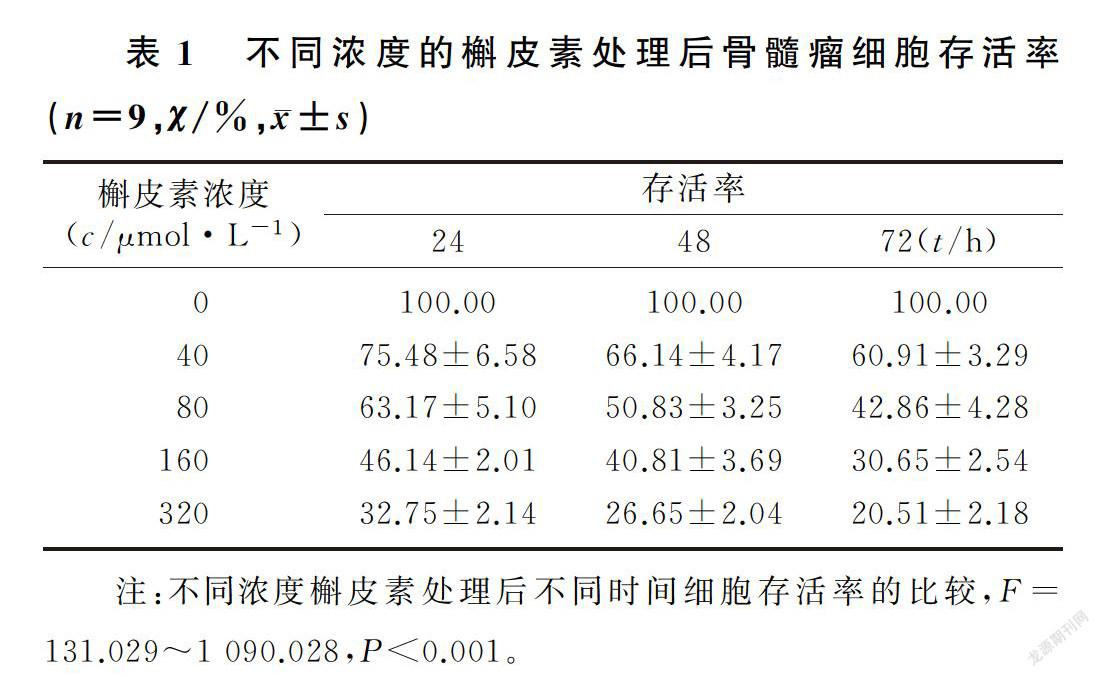
用40、80、160、320 μmol/L的槲皮素處理后的骨髓瘤細胞,在培養24、48、72 h細胞存活率均降低(F=131.029~1 090.028,P<0.001),槲皮素可以呈濃度依賴性地抑制骨髓瘤細胞存活。計算24 h其半數抑制濃度為(128.58±11.46)μmol/L,選用130 μmol/L的槲皮素處理骨髓瘤細胞做后續實驗。見表1。
2.2?槲皮素聯合PDTC對骨髓瘤細胞存活和運動能力影響
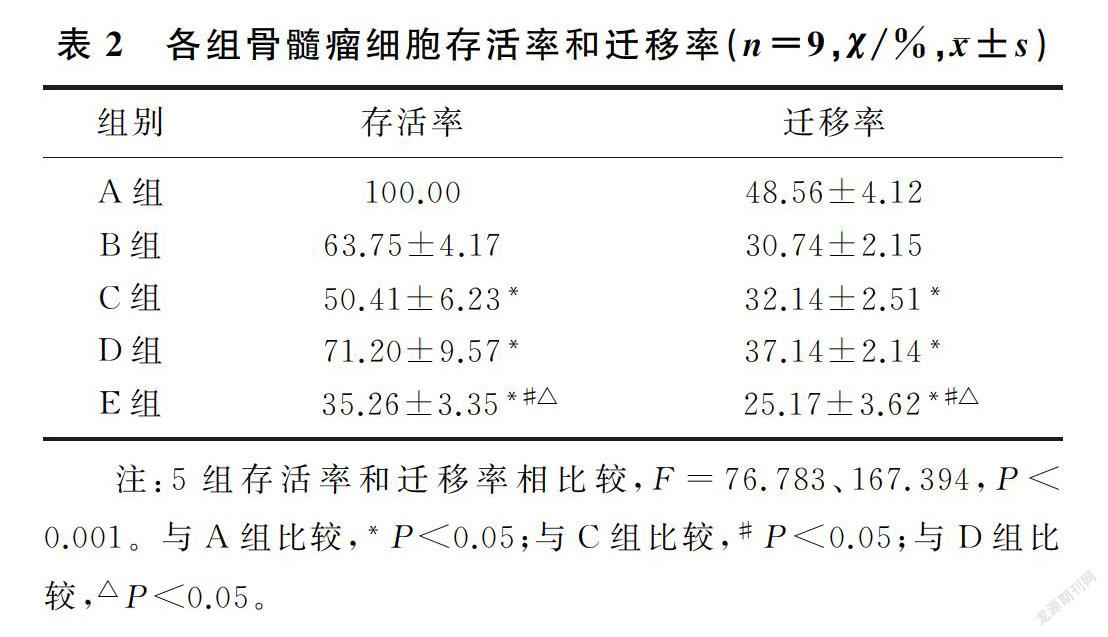
槲皮素和NF-κB信號通路抑制劑處理后的骨髓瘤細胞存活率和遷移率均降低,槲皮素和NF-κB信號通路抑制劑聯合處理后骨髓瘤細胞的存活率和遷移率低于槲皮素或NF-κB信號通路抑制劑單獨處理的細胞(F=28.419、66.610,P<0.001)。槲皮素聯合NF-κB信號通路抑制劑能夠協同降低骨髓瘤細胞存活和運動能力。見表2。
2.3?槲皮素聯合PDTC對骨髓瘤細胞侵襲遷移能力影響
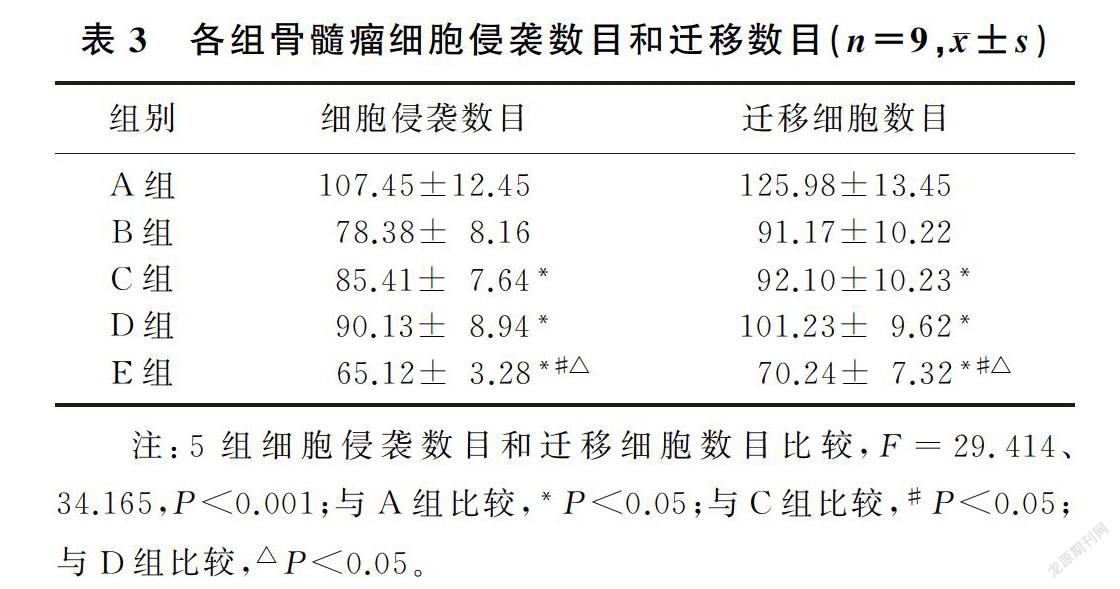
槲皮素和NF-κB信號通路抑制劑處理后的骨髓瘤細胞侵襲數目和遷移數目均降低,槲皮素和NF-κB信號通路抑制劑聯合處理后骨髓瘤細胞的侵襲數目和遷移數目低于槲皮素或NF-κB信號通路抑制劑單獨處理的細胞(F=29.414、34.165,P<0.001)。槲皮素聯合NF-κB信號通路抑制劑能夠協同降低骨髓瘤細胞侵襲和遷移能力。見表3。
2.4?槲皮素聯合PDTC對骨髓瘤細胞中相關蛋白表達影響
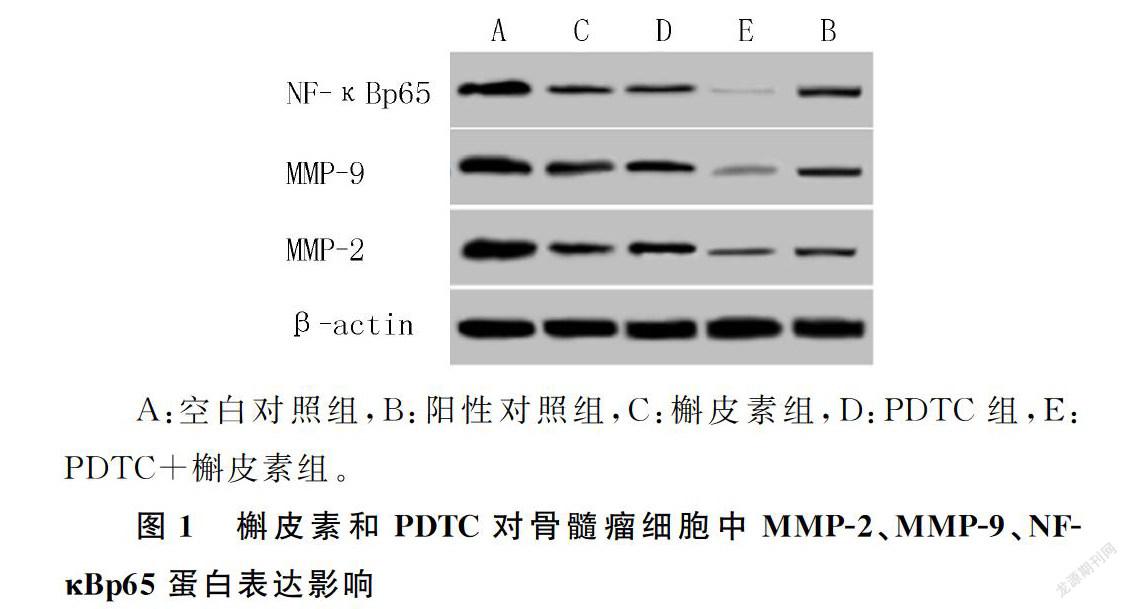
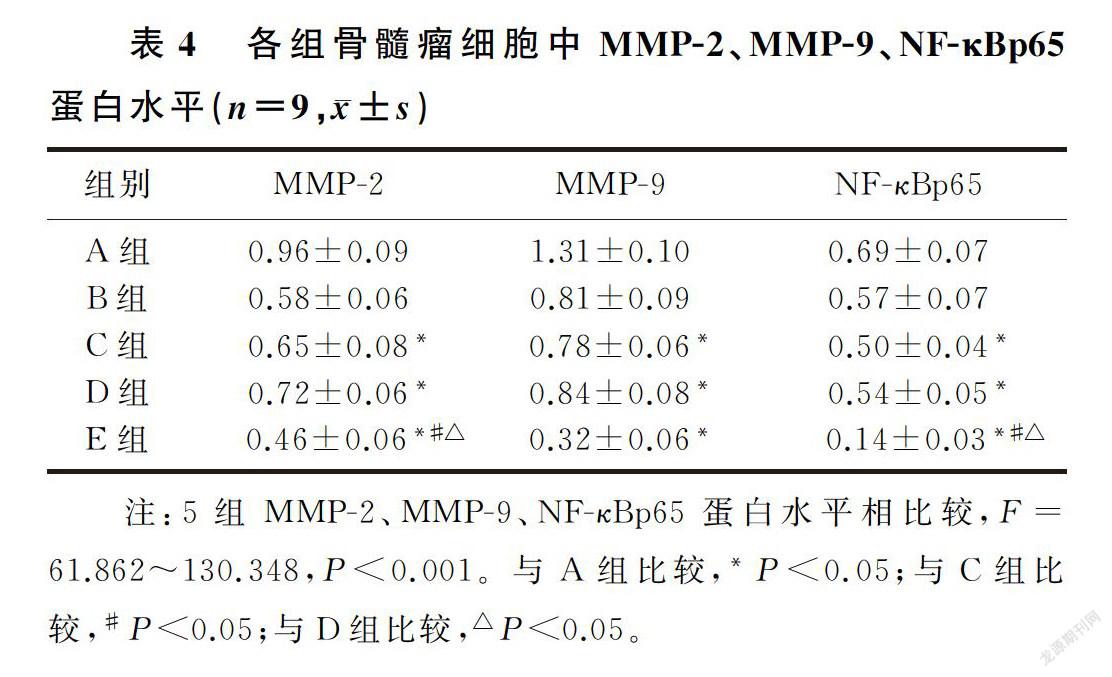
槲皮素和NF-κB信號通路抑制劑處理后的骨髓瘤細胞中MMP-2、MMP-9、NF-κBp65蛋白表達水平均降低,槲皮素和NF-κB信號通路抑制劑聯合處理后骨髓瘤細胞中MMP-2、MMP-9、NF-κBp65蛋白表達水平低于槲皮素或NF-κB信號通路抑制劑單獨處理的細胞(F=61.862~130.348,P<0.001)。槲皮素聯合NF-κB信號通路抑制劑能夠協同抑制骨髓瘤細胞中MMP-2、NF-κBp65、MMP-9蛋白表達。見圖1和表4。
3?討?論
槲皮素是一種黃酮類的化合物,具有擴張冠狀動脈、抗血小板聚集、抗過敏、鎮痛等藥理作用[11]。
目前的研究表明,槲皮素具有抗腫瘤細胞生長的作用,其可以下調前列腺癌、膀胱癌等腫瘤細胞的生長和侵襲能力[12-13]。本實驗的結果表明,不同濃度的槲皮素處理后的人骨髓瘤細胞U266的存活能力降低,細胞的侵襲、遷移和運動能力下降,說明槲皮素不僅具有抗骨髓瘤細胞生長的作用,還具有抑制骨髓瘤細胞轉移潛能的作用。
NF-κB是一種轉錄調控因子,是由多個亞單位組成的蛋白家族,包括Rel、RelB、NF-κBp52、NF-κBp65等,其中NF-κBp65是目前發現的NF-κB信號轉導中的必需成員,其表達水平高低與NF-κB信號的激活呈正相關[14-16]。NF-κB具有多種生物學作用,在炎癥、免疫調節等方面具有重要作用,NF-κB還參與動脈粥樣硬化、腫瘤、低氧復氧組織損傷等病理過程[17-19]。NF-κB在腫瘤組織中過度激活,抑制NF-κB信號通路能夠下調腫瘤細胞的惡性表型[20-22]。在肺腺癌等腫瘤病理過程中已經證實,槲皮素可以抑制NF-κB信號通路的激活[8]。本實驗的結果也表明,槲皮素能夠下調骨髓瘤細胞中NF-κBp65的表達,并且槲皮素和NF-κB信號通路抑制劑具有協同抗骨髓瘤細胞存活、運動、遷移和侵襲的作用,說明槲皮素可以通過抑制NF-κB信號通路的激活調控骨髓瘤細胞的惡性表型。
腫瘤轉移是腫瘤引起死亡的重要原因,腫瘤細胞合成的基質金屬蛋白酶是腫瘤細胞侵襲和遷移的基礎[23-26]。基質金屬蛋白酶含有多個蛋白家族成員,這些蛋白家族成員能夠降解幾乎所有的細胞外基質成分,其中MMP-2和MMP-9是目前研究發現的與腫瘤轉移關系最為密切的基質金屬蛋白酶成員,二者表達水平升高標志著腫瘤細胞轉移能力增加[27-29]。本實驗的結果顯示,槲皮素和NF-κB信號通路抑制劑能夠協同抑制骨髓瘤細胞中MMP-2和MMP-9蛋白表達水平,說明二者能夠通過抑制細胞合成MMP-2和MMP-9發揮抗骨髓瘤細胞遷移和侵襲的作用。
綜上所述,槲皮素能夠抑制骨髓瘤細胞的存活、侵襲、遷移和運動能力,其作用機制可能與抑制NF-κB信號激活和降低MMP-2、MMP-9蛋白表達水平有關。目前對于槲皮素靶向調控NF-κB信號通路的具體機制尚不清楚。本實驗結果為研究槲皮素在骨髓瘤細胞遷移中具體作用機制奠定了基礎,為研究槲皮素抗腫瘤機制提供了參考,為提高骨髓瘤的治愈率提供了新思路。本實驗存在一定的局限性,沒有在多株骨髓瘤細胞和體內進行驗證,在以后的實驗中會對上述部分以及槲皮素的具體作用機制進行探討。
[參考文獻]
[1]GAY F, ENGELHARDT M, TERPOS E, et al. From transplant to novel cellular therapies in multiple myeloma: Euro-
pean Myeloma Network guidelines and future perspectives[J].?Haematologica, 2018,103(2):197-211.
[2]WU Q, NEEDS P W, LU Y, et al. Different antitumor effects of quercetin,quercetin-3′-sulfate and quercetin-3-glucuronide in human breast cancer MCF-7 cells[J].?Food & Function, 2018,9(3):1736-1746.
[3]TIWARI H, KARKI N, PAL M, et al. Functionalized graphene oxide as a nanocarrier for dual drug delivery applications: the synergistic effect of quercetin and gefitinib against ovarian cancer cells[J].?Colloids and Surfaces B-Biointerfaces, 2019,178(1):452-459.
[4]SHANG H S, LU H F, LEE C H, et al. Quercetin induced cell apoptosis and altered gene expression in AGS human gastric cancer cells[J].?Environmental Toxicology, 2018,33(11):1168-1181.
[5]YANG Bin, YAN Ping, YANG Guangzhao, et al. Triptolide reduces ischemia/reperfusion injury in rats and H9C2 cells via inhibition of NF-κB, ROS and the ERK1/2 pathway[J].?International Journal of Molecular Medicine, 2018,41(6):3127-3136.
[6]LIU L, AHN K S, SHANMUGAM M K, et al. Oleuropein induces apoptosis via abrogating NF-kappa B activation cascade in estrogen receptor-negative breast cancer cells[J].?Journal of Cellular Biochemistry, 2019,120(3):4504-4513.
[7]GRINBERG-BLEYER Y, CARON R, SEELEY J J, et al. The alternative NF-κB pathway in regulatory T cell homeostasis and suppressive function[J].?The Journal of Immunology, 2018, 200(7):2362-2371.
[8]WU T C, CHAN S T, CHANG C N, et al. Quercetin and chrysin inhibit nickel-induced invasion and migration by downregulation of TLR4/NF-kappa B signaling in A549 cells[J].?Chemico-Biological Interactions, 2018,292(25):101-109.
[9]MENG Lingquan, YANG Feiya, WANG Mingshuai, et al. Quercetin protects against chronic prostatitis in rat model through NF-kappa B and MAPK signaling pathways[J].?The Prostate, 2018,78(11):790-800.
[10]FATMA G, ISSAM S, RAWYA S, et al. Antioxidant potential of four species of natural product and therapeutic strategies for cancer through suppression of viability in the human multiple myeloma cell line U266[J].?Biomedical and Environmental Sciences, 2019,32(1):22-33.
[11]KUNDUR S, PRAYAG A, SELVAKUMAR P, et al. Synergistic anticancer action of quercetin and curcumin against triple-negative breast cancer cell lines[J].?Journal of Cellular Physiology, 2019,234(7):11103-11118.
[12]SUN S, GONG F, LIU P, et al. Metformin combined with quercetin synergistically repressed prostate cancer cells via inhibition of VEGF/PI3K/Akt signaling pathway[J].?Gene, 2018,664(20):50-57.
[13]LEE Y H, TUYET P T. Synthesis and biological evaluation of quercetin-zinc (Ⅱ) complex for anti-cancer and anti-metastasis of human bladder cancer cells[J].?In Vitro Cellular & Developmental Biology-Animal, 2019,55(6):395-404.
[14]SINGH A K, FECHTNER S, CHOURASIA M, et al. Critical role of IL-1 in IL-1-induced inflammatory responses: coo-
peration with NF-κBp65 in transcriptional regulation[J].?FASEB Journal, 2019,33(2):2526-2536.
[15]陳亞利,歐陽軍,孟晶茜,等. 姜黃素對高尿酸血癥大鼠腎組織中TGF-β1,NF-κB表達的影響[J].?鄭州大學學報(醫學版), 2018,53(3):360-364.
[16]王宏,王瑞英,劉志紅,等. TGF-β1及NF-κBP65在妊娠期甲亢大鼠子代腎臟中的表達[J]. 河北醫科大學學報, 2019,40(3):281-285,291.
[17]YANG Shujun, LI Jian, CHEN Yu, et al. MicroRNA-216a promotes M1 macrophages polarization and atherosclerosis progression by activating telomerase via the Smad3/NF-kappa B pathway[J].?Biochimica et Biophysica Acta-Molecular Basis of Disease, 2019,1865(7, SI):1772-1781.
[18]陳偉,馬磊,楊立山. 甘草次酸對哮喘大鼠的抗氧化應激作用及 NF-κB 信號通路的調控[J].?鄭州大學學報(醫學版), 2016,51(6):762-765.
[19]NAN Jing, WANG Yuxin, YANG Jinbo, et al. IRF9 and unphosphorylated STAT2 cooperate with NF-kappa B to drive IL6 expression[J].?Proceedings of the National Academy of Sciences of the United States of America, 2018,115(15):3906-3911.
[20]MING Xiaoyan, ZHANG Xu, CAO Tingting, et al. RHCG suppresses tumorigenicity and metastasis in esophageal squamous cell carcinoma via inhibiting NF-κB signaling and MMP1 expression[J].?Theranostics, 2018,8(1):185-198.
[21]TANIGUCHI K, KARIN M. NF-kappa B, inflammation, immunity and cancer: coming of age[J].?Nature Reviews Immunology, 2018,18(5):309-324.
[22]REN L, LI Z, DAI C, et al. Chrysophanol inhibits proliferation and induces apoptosis through NF-κB/cyclin D1 and NF-κB/Bcl-2 signaling cascade in breast cancer cell lines[J].?Molecular Medicine Reports, 2018,17(3):4376-4382.
[23]ZHOU Yongping, CHEN Yigang, DING Wenzhou, et al. LncRNA UCA1 impacts cell proliferation, invasion, and migration of pancreatic cancer through regulating miR-96/FOXO3[J].?IUBMB Life, 2018,70(4):276-290.
[24]王善容,丁月云,朱宗平,等. SPECT/CT融合骨顯像診斷肺癌單發骨轉移的價值[J].?山東大學學報(醫學版), 2018,56(2):41-46.
[25]WOODCOCK C C, HUANG Y, WOODCOCK S R, et al. Nitro-fatty acid inhibition of triple-negative breast cancer cell viability,migration,invasion, and tumor growth[J].?Journal of Biological Chemistry, 2018,293(4):1120-1137.
[26]GUAN Yanxing, ZHANG Mengzhi, CHEN Xuezhong, et al. Lnc RNA SNHG20 participated in proliferation, invasion, and migration of breast cancer cells via miR-495[J].?Journal of Cellular Biochemistry, 2018,119(10):7971-7981.
[27]FENG S Q, ZHANG X Y, FAN H T, et al. Up-regulation of LncRNA MEG3 inhibits cell migration and invasion and enhances cisplatin chemosensitivity in bladder cancer cells[J].?Neoplasma, 2018,65(6):925-932.
[28]DINICOLA S, MASIELLO M G, PROIETTI S, et al. Nicotine increases colon cancer cell migration and invasion through epithelial to mesenchymal transition (EMT): COX-2 involvement[J].?Journal of Cellular Physiology, 2018,233(6):4935-4948.
[29]LIN C C, KUO C L, HUANG Y P, et al. Demethoxycurcumin suppresses migration and invasion of human cervical can-
cer HeLa cells via inhibition of NF-κB pathways NF-kappa B[J].?Anticancer Research, 2018,38(5):2761-2769.

