25G和27G玻璃體切除術聯合空氣填充治療RRD的療效比較
黃紅波,韓光杰
0引言
隨著25G和23G玻璃體切除術(pars planavitrectomy,PPV)的開展標志著玻璃體視網膜手術微創時代的到來。微創玻璃體視網膜手術不僅簡化了手術操作,而且也顯示出術后并發癥少、炎癥反應輕、術后恢復快等優勢。但隨著臨床手術例數的增多,與其無縫合相關的并發癥如低眼壓、脈絡膜脫離等的報告逐漸增多[1-2]。本著“越小越好”的原則,2010年切口更小的27G PPV微創手術系統也用于臨床[3],其適應證也從最初的局限于后極部的黃斑部疾病逐漸向更加復雜的如糖尿病視網膜病變、孔源性視網膜脫離(rhegmatogenous retinal detachment,RRD)等擴展[4-7]。現如今,對于RRD玻璃體手術中硅油、惰性氣體和空氣均可作為玻璃體腔填充物,與硅油填充需要進行二次手術取出硅油且可伴有多種并發癥相比,氣體填充的并發癥相對較少[8],在惰性氣體在我國應用受限的情況下,國內針對25G和27G玻璃體切割術聯合空氣填充治療RRD的報告較少,我們回顧性對比分析了25G和27G玻璃體切割術聯合空氣填充治療RRD的臨床療效和安全性,現將結果報告如下。
1對象和方法
1.1對象回顧性分析2016-05/2018-06在柳州市紅十字會醫院首次接受25G或27G玻璃體切除術治療的RRD患者63例63眼,根據手術方式不同進行分組,其中25G組33例33眼,男19例19眼,女14例14眼,年齡16~71歲;27G組30例30眼,其中男17例17眼,女13例13眼,年齡18~65歲。兩組患者年齡、性別、BCVA、眼壓、視網膜裂孔數等比較,差異均無統計學意義(P>0.05),見表1。納入標準:(1)經90D前置鏡或三面鏡檢查證實為孔源性視網膜脫離,且為馬蹄形裂孔;(2)裂孔位置偏后且裂孔位于8∶00~4∶00位方向;(3)裂孔較多且分布非同一圓周;(4)行27G或25G PPV后按照要求規律隨訪滿1mo以上者。排除標準:(1)巨大裂孔;(2)黃斑裂孔性視網膜脫離;(3)合并脈絡膜脫離;(4)增生性玻璃體視網膜病變(proliferative vitreousretinopathy,PVR)C1級以上;(5)既往行玻璃體切除術、抗青光眼手術等;(6)有嚴重全身疾病及不能配合手術體位的患者。本研究經醫院倫理委員會審核并批準。
1.2方法所有患者術前經詳細告知后均簽署手術知情同意書,本回顧性研究均使用Alcon Constellation玻璃體切割儀,在非接觸廣角鏡下行25G或27G玻璃體切割術,27G玻璃體切割速率為7500次/min,負壓600mmHg(1mmHg=0.133kPa),25G玻璃體切割速率為5000次/min,負壓450mmHg,術中灌注壓均維持為28mmHg。手術均由同一位經驗豐富的眼科副主任醫師完成。在球后局部麻醉下行玻璃體切除術,術前評估需行白內障手術的常規白內障超聲乳化摘除混濁的晶狀體。于角膜緣后3.5~4.0mm處將結膜錯位2~3mm,用套管穿刺針以30°左右斜行穿刺結膜和鞏膜到達穿刺套管的頂端,再以垂直方向進入玻璃體腔,切除中央部玻璃體,行玻璃體后脫離。結合鞏膜外頂壓,在曲安奈德染色下行全玻璃體切除后行氣液交換,引流視網膜下液,平伏視網膜,圍繞視網膜裂孔行視網膜激光光凝。手術結束時拔除鞏膜套管,檢查鞏膜切口滲漏情況,必要時行鞏膜切口縫合。術后保持俯臥位5~7d,地塞米松妥布霉素滴眼液點眼10d。患者手術后隨訪1mo。隨訪包括BCVA(LogMAR)、眼壓、視網膜復位率及并發癥發生情況。為便于視力的統計分析,光感記為4,手動記錄為3,數指記錄為2。
統計學分析:采用統計學軟件SPSS19.0進行分析。計量資料以均數±標準差表示。采用重復測量數據的方差分析,各時間點的組間差異比較,采用獨立樣本t檢驗;各組的時間差異比較,采用LSD-t檢驗。計數資料的組間比較采用χ檢驗、Fisher精確檢驗。以P<0.05為差異有統計學意義。
2結果
2.1兩組的手術時間比較25G組和27G組的平均手術時間分別為44.13±5.9、46.07±6.1min,差異無統計學意義(t=0.028,P=0.412)。
2.2兩組術后視力比較25G和27G組術前BCVA分別為1.03±0.44、1.07±0.38,隨訪到1mo時,25G和27G組BCVA分別為0.73±0.32、0.70±0.29,兩組均較手術前改善,差異均有統計學意義(P<0.01)。但25G和27G組BCVA提高幅度分別為-0.3±0.12、-0.31±0.14,差異無統計學意義(P>0.05)。
2.3兩組術后眼壓比較術后不同時間兩組眼壓比較,差異無統計學意義(F時間=5.16,P時間=0.25;F組間=1.32,P組間=0.31;F組間×時間=10.02;P組間×時間=0.11),見表2。25G和27G組術后1wk內發生一過性低眼壓(<6mmHg)的分別為5眼(15%)和3眼(10%),差異無統計學意義(χ=0.376,P=0.540)。發生低眼壓的患眼均于術后1wk內恢復正常(>6mmHg)。
2.4兩組視網膜復位率比較25G組和27G組隨訪至1mo時視網膜復位率分別為91%(30/33)、93%(28/30),兩組差異無統計學意義(P=0.902)。25G失敗的3眼中有2眼是發現新的視網膜裂孔,予以再次手術填充硅油,現取油后1mo視網膜復位良好,1眼因前段PVR,予以再次玻璃體切除后硅油填充。27G組有2眼是因為前段PVR導致視網膜再次脫離,予以25G玻璃體切除后填充硅油,1眼因為新發現視網膜裂孔,處理同上。兩組均未見脈絡膜脫離、眼內炎等嚴重并發癥。
3討論
經睫狀體平坦部的三通道玻璃體切除是目前眼底外科的經典術式。隨著2002年25G和2005年23G玻璃體切除系統的應用,開創了眼底外科的微創時代。那么23G、25G玻璃體切除術真的就是完美的眼底外科手術嗎?近年來,隨著23G、25G微創玻璃體切除術的普及,與未縫合的手術切口的相關并發癥逐漸引起廣大眼科醫生的關注,如術后低眼壓、眼內炎等[1-2]。為了應對這些問題,本著“越小越好”的原則,在2010年日本學者Oshima等[3]首次正式報道了27G玻璃體切除系統。其適應證也從最初的局限于后極部的黃斑部疾病逐漸向更加復雜如RRD、糖尿病視網膜病變等疾病擴展。
對于27G PPV,大家首先最關心的就是手術效率問題。理論上,流體經過管徑越小,阻力就越大,勢必影響液體流量。而我們的研究顯示兩組的手術時間無差異,這與國內的研究結果相同[7,9],分析其原因如下:(1)本研究術中采用的參數:27G玻璃體切割速率為7500次/min,負壓600mmHg,25G玻璃體切割速率為5000次/min,負壓450mmHg。眾所周知,液流率能夠隨切割速率和負壓的提高而提高[10],這就在一定程度上彌補了27G玻切頭管道細的劣勢。(2)27G玻璃體切割系統雙向氣動探頭的高速切割能夠降低管道內玻璃體的黏度,促進其分解和流動[11]。同時27G PPV系統探頭的高速切割和可控的開合比可保證玻璃體切割連續平穩地進行,緩解流量的下降,降低組織阻塞探頭口的發生率[12]。(3)術中我們發現在切除中央部玻璃體時27G確實慢于25G,但在處理裂孔周邊玻璃體時,由于25G開口和液流較大,對浮動視網膜的牽拉較強,為防止醫源性裂孔,術者會放慢切除速度。而27G在切除裂孔周邊的玻璃體時由于對視網膜牽拉作用較小,術者則可以“大膽”的切除。(4)27G切割頭更細,有利于眼內更加精細的操作,其開口更加接近切割頭的頂端,術中可將切割頭深入裂孔下抽吸視網膜下液,在一定程度上減少了笛針的使用,減少術中交換器械的次數,從而節約手術時間。在孔源性視網膜脫離手術中硅油、惰性氣體和無菌空氣均可作為玻璃體腔填充物,以輔助視網膜復位和平伏。與硅油填充需要進行二次手術取出硅油且可伴有多種并發癥相比,主要利于氣浮力和表面張力作用的氣體填充的并發癥較少,同時也能為患者節約經濟費用。在目前國內惰性氣體使用受限的情況下,我們采取無菌空氣作為填充物,術后1mo隨訪時27G組視網膜復位率達到93%,這與既往國內研究提及的27G PPV治療RRD的成功率接近[8]。
表1 兩組基線資料比較

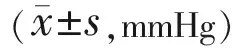

組別術后1d術后3d術后1wk術后1mo25G組11.19±3.1911.22±2.8812.11±3.2112.55±3.4427G組11.89±3.2512.09±3.0912.76±3.2812.79±3.78
我們認為玻璃體切除聯合無菌空氣填充可成功使視網膜復位的關鍵在于手術適應證的把握[8]和術者的手術技術:(1)術前仔細評估患者全身情況,看其是否能堅持術后的體位;(2)眼部要求:PVR C1級以下、視網膜活動度良好、裂孔位于視網膜上方;排除巨大裂孔、脈絡膜脫離等復雜眼部情況者;(3)術中應仔細檢查視網膜周邊部,不能遺漏裂孔,并充分處理所有視網膜裂孔以及視網膜變性區,徹底切除裂孔周邊的玻璃體,尤其是馬蹄形裂孔前緣處的玻璃體,對于視網膜裂孔行激光封閉要確實可靠,保證激光斑反應良好。
本研究結果顯示:在治療RRD上,27G和25G PPV具有同樣高的解剖復位率和手術效率,兩者均能夠提高術后視力,且術中術后并發癥無差異,是較為安全、有效的手術方式。但27G更細的切割頭有利于眼內更加精細的操作,其開口更加接近切割頭的頂端,術中可將切割頭深入裂孔下抽吸視網膜下液,在一定程度上減少笛針的使用,減少術中交換器械的次數[13]。由于其更小的切口,也能減輕術后的炎癥反應[14]。但27G玻切頭有個明顯的缺點,其工作距離相對25G玻切頭較短,不能用于高度近視等長眼軸的患眼[15]。本研究為單中心的回顧性研究,納入觀察的樣本量有限,其結果存在一定的局限性,期待更多中心更大樣本量的研究的報告。

