CdTe量子點熒光探針檢測血清和食品中Cr3+
龔婷婷,王秋月,吳一微
(湖北師范大學化學化工學院,湖北黃石435002)
Cr3+在脂肪、碳水化合物、核酸和蛋白質的代謝過程中起重要作用,是人體必需的微量元素之一。正常人每天需要攝入25~35μg的Cr3+來改善血糖、血脂的代謝,而Cr3+的缺乏可能會導致糖尿病和心血管疾病,但過量的Cr3+也會對細胞結構產生不利影響[1]。因此,建立一種簡單、靈敏度高和選擇性好的測定食品和生物樣品中痕量Cr3+的新方法至關重要。
目前,鉻的檢測方法主要有電化學方法[2]、原子吸收光譜法[3]、電感耦合等離子體質譜法[4]和熒光法[5],其中熒光法因具有選擇性好、靈敏度高和響應速度快等優點引起人們的極大興趣[6]。在熒光檢測技術中,熒光探針的選擇是關鍵。量子點(QDs)因具有量子產率高、光化學穩定性好、斯托克斯位移大、吸收光譜寬、抗漂白強和熒光壽命長等優點受到廣泛關注[7-9]。Abolhasani等[7]和Souza等[8]分別建立了基于Cr3+熒光猝滅巰基乙酸修飾的CdS QDs、CdSe QDs的傳感新方法。Han等[9]在CdTe QDs表面修飾上不同的配體,利用配體的識別差異,成功地鑒別了Cr3+和Cr6+。然而,利用CdTe QDs在不同緩沖體系中對Cr3+的響應差異,建立Cr3+的分析新方法尚未見報道。
本文采用一鍋法合成了尺寸均一且水溶性好的巰基乙酸修飾的CdTe QDs,基于Cr3+在不同介質中對該量子點熒光猝滅作用的差異,建立了食品和血清中痕量Cr3+的分析新方法。
1 實驗部分
1.1 儀器和試劑
LS45熒光光譜儀(美國,Perkin Elmer);U-3010紫外-可見分光光度計(日本,Hitachi);PB-10型精密pH 計(德國,Sartorius)。
CdTe QDs的合成及表征同本課題組前期工作[10]。Cd(Ac)2·2H2O、NaBH4、CrCl3·6H2O、NaOH(天津市科密歐化學試劑有限公司),K2TeO3(Aladdin),巰基乙酸(Alfa Aesar)。1mg·mL-1Cr3+、Ag+、Cu2+、Hg2+等金屬離子貯備液分別由相應的高純鹽 CrCl3·6H2O、AgNO3、CuCl2·2H2O和 Hg(NO3)2(上海化學試劑廠)配制而成。水為二次蒸餾水。
1.2 CdTe QDs探針檢測Cr3+
將55μL CdTe QDs和400μL 0.1mol·L-1HAc-NaAc緩沖溶液(pH=6.0)混合于比色管中,分別加入不同濃度的Cr3+標準溶液,用水定容至5.0mL,混勻,室溫下放置10min后,用熒光光度計測量其熒光強度(λex/λem=458/560nm,狹縫寬度均為10nm)。
1.3 樣品預處理
將血液樣品(黃石市二醫院檢驗科提供)高速離心(3 500r/min)后,收集血清,待用。橙汁和牛奶樣品(購于當地超市)高速離心(3 500r/min),棄掉大顆粒沉淀物后,再通過0.45μm濾膜過濾,收集濾液,待用。
2 結果與討論
2.1 CdTe QDs在不同介質中對金屬離子的選擇性
分別研究了不同金屬離子在B-R緩沖溶液和HAc-NaAc緩沖溶液中對CdTe QDs熒光強度的影響。從圖1A可知,在B-R緩沖溶液中,Ag+、Cu2+和Hg2+對CdTe QDs熒光強度有明顯的猝滅作用;而在HAc-NaAc緩沖溶液中(圖1B),除了Ag+、Cu2+和 Hg2+外,Cr3+也能猝滅CdTe QDs的熒光。因此,基于本課題組前期工作[10],本文實驗選擇HAc-NaAc緩沖體系。

圖1 在B-R緩沖溶液(A)和HAc-NaAc緩沖溶液(B)中不同金屬離子對CdTe QDs熒光強度的影響Fig.1 Effect of various metalions on fluorescence intensity of CdTe QDs in B-R buffer(pH=7.0)(A)and HAc-NaAc buffer(pH=7.0)(B)
2.2 pH值的影響
強酸或強堿會影響QDs表面基團的質子化或去質子化,導致其表面結構發生變化,進而影響QDs的性質[11]。因此,分別考察了在體系中加或不加Cr3+的條件下,pH對CdTe QDs熒光強度的影響。結果表明:Cr3+不存在時,當pH=5.0~6.0,CdTe QDs熒光強度逐漸增加,pH=7.0~11.0CdTe熒光強度基本保持穩定;而Cr3+存在時,當pH=5.0~11.0,CdTe QDs熒光強度總體呈現微弱上升的趨勢。比較兩種結果發現,在pH=6.0時熒光強度差值最大,故選擇pH=6.0為最優pH值。
2.3 HAc-NaAc緩沖溶液濃度的影響
在體系中分別加或不加Cr3+的條件下,考察了HAc-NaAc緩沖溶液濃度對CdTe QDs熒光強度的影響。結果表明,HAc-NaAc濃度在0.002~0.008mol·L-1范圍內,熒光猝滅程度逐漸增加;在0.012~0.080mol·L-1范圍內,熒光猝滅程度逐漸下降;在0.008mol·L-1時,熒光猝滅程度最大。因此,選擇0.008mol·L-1的pH=6.0的HAc-NaAc緩沖溶液。
2.4 CdTe QDs體積的影響
在最佳條件下,固定Cr3+的濃度為40ng·mL-1,考察了不同體積的CdTe QDs對熒光強度的影響。結果表明,CdTe QDs體積在15~55μL范圍內,熒光猝滅程度總體上逐漸增加;CdTe QDs體積在55~65μL范圍內,熒光猝滅程度逐漸減小。因此,55μL CdTe QDs為最佳體積。
2.5 干擾離子影響的消除
采用二乙基二硫代氨基甲酸鈉(DDTC)和NH4OH為掩蔽劑,消除Ag+、Hg2+和Cu2+對CdTe QDs檢測Cr3+的干擾,從而實現對Cr3+的選擇性檢測,見圖2。比較圖2中曲線b和曲線c可見,在掩蔽劑的存在下,Ag+、Cu2+和 Hg2+對CdTe QDs檢測Cr3+無明顯影響。
2.6 CdTe QDs探針測定Cr3+的分析性能
在最佳條件下,考察了不同濃度的Cr3+對CdTe QDs的熒光強度的影響。實驗結果顯示,隨著Cr3+濃度的增加,CdTe QDs的熒光強度逐漸減弱,熒光猝滅程度(F0/F)與Cr3+在0.50~45ng·mL-1范圍內呈現良好的線性關系(F0表示不存在Cr3+時的熒光強度,F表示存在Cr3+時的熒光強度),線性方程為:F0/F=0.04148c+1.004,相關系數為0.9962,檢出限為0.12ng·mL-1(2.3×10-9mol·L-1)。
表1列出了本方法與文獻方法的性能比較。與同為熒光分析方法相比,本法的檢出限比大多數方法低[12-14],但高于少數方 法[8];而 與 比 色 法[15-16]相 比,本 法 表 現 出 更 低的檢出限。表明本法具有簡單、廉價、靈敏度高和選擇性好等優點。

圖2 不同體系的熒光強度Fig.2 Fluorescence intensity(λex=458nm)of different systems(a)CdTe QDs:(b)CdTe QDs+Cr3+;(c)(b)+Ag+ +Cu2++Hg2+ +DDTC+NH4OH.[Ag+],[Cu2+]and[Hg2+]:10ng·mL-1;[DDTC]:2.0×10-6 mol·L-1;[NH4OH]:3.0×10-4 mol·L-1;CdTe QDs:55μL.
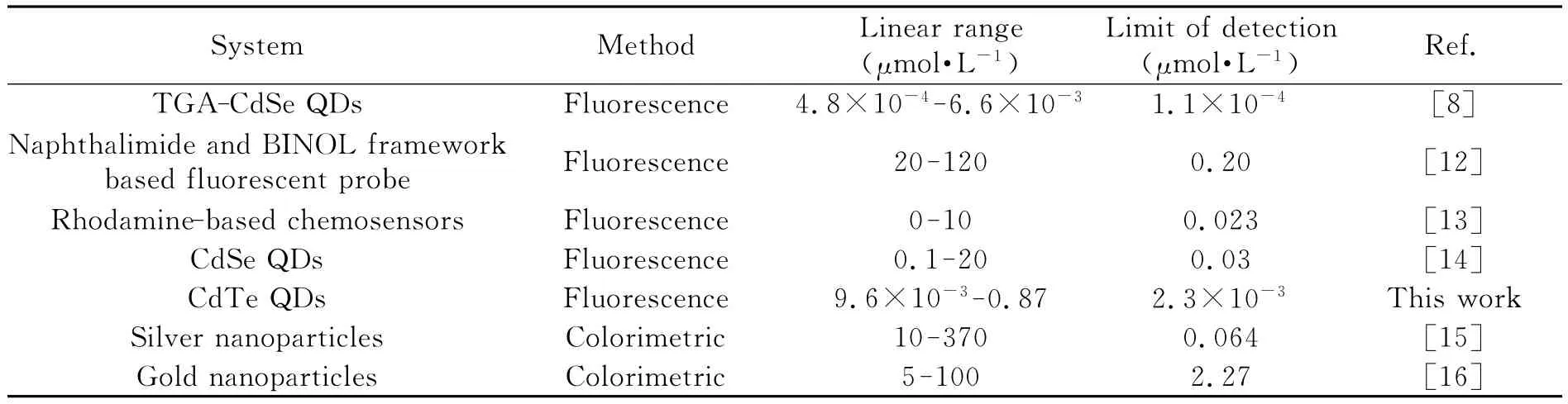
表1 本實驗方法與文獻方法對比Table 1 Comparison of this work with various reported methods
2.7 CdTe QDs檢測Cr3+的可能機理
Cr3+能顯著猝滅CdTe QDs的熒光,而Cr6+不能猝滅CdTe QDs的熒光原因可能如下:Cr3+和Cr6+在溶液中分別以陽離子和陰離子的形式存在,巰基乙酸包覆的CdTe QDs表面帶負電荷,因此由于靜電引力作用,CdTe QDs能吸附 Cr3+、排斥Cr6+[9],拉近了 Cr3+與CdTe QDs的距離,為電子轉移鋪平了道路[17],當CdTe QDs和Cr3+之間發生電子轉移時,QDs表面快速形成缺陷,從而導致熒光猝滅。
2.8 實際樣品分析
為探究CdTe QDs探針檢測Cr3+的可行性,在最佳條件下,考察了CdTe QDs熒光探針檢測血清、牛奶和果汁樣品中Cr3+的加標回收情況。結果如表2所示,除橙汁未檢測到Cr3+外,健康人、糖尿病人血清樣品和牛奶樣品中均檢測到Cr3+,且糖尿病人血清中的Cr3+含量明顯低于健康人。這是由于Cr3+對調節人體血糖至關重要,血糖越高,體內的Cr3+的含量越少,與實驗結果一致。方法的加標回收率在91.8%~106%之間,符合檢測要求。

表2 CdTe QDs應用于實際樣品中Cr3+的檢測Table 2 Detection of Cr3+in real samples by CdTe QDs
3 結論
基于CdTe QDs熒光探針,建立了一種簡單、價廉、靈敏度高和選擇性好的檢測血清和食物樣品中Cr3+的新方法,與大部分其他文獻報道的方法相比,本法表現出更優異的分析性能。已成功用于血清樣品,橙汁樣品和牛奶樣品中Cr3+含量的測定。

