乳腺癌患者BRCA1/2突變特點與臨床病理特征相關性
鄭春海 張祥宇
乳腺癌為臨床上常見的女性惡性腫瘤之一,在我國部分地區的發病率已位居第一位。而由于乳腺癌侵襲生長和播散轉移的存在,使得患者的晚期治愈率明顯減低[1-2]。早期診斷乳腺癌,加強相關位點與標志物的早期檢測,對于評估患者的預后具有重要意義[3-4]。現代研究表明乳腺癌的發生是1個多基因變異積累及相互作用的復雜的過程,原癌基因的激活和抑癌基因功能喪失與乳腺癌發生密切相關[5]。15%左右的乳腺癌有家族遺傳背景,部分是由于高外顯率基因突變造成的,主要就是乳腺癌易感基因1(breast cancer susceptible gene 1,BRCA1)和BRCA2[6]。BRCA1和BRCA2基因是目前所發現的最重要的乳腺癌易感基因之一,其突變形式主要為移碼突變、終止碼突變、錯義突變等,歐美人群中家族性乳腺癌的BRCA1突變率較高,并且突變率與家族中具有乳腺癌病史的人數呈正相關[7-9]。相關研究出了發現BRCA1和BRCA2的致病性突變外,還有許多位點存在單核苷酸多肽(SNP)的現象,可能與乳腺癌發病風險有關[10-11]。本文具體探討了乳腺癌患者BRCA1和BRCA2突變特點與臨床病理特征相關性,希望為闡述乳腺癌的遺傳病因機制以及為乳腺癌的早期診治奠定基礎。現總結報告如下。
1 資料與方法
1.1 研究對象
2016年2月到2018年2月選擇在我院腫瘤外科診治的乳腺癌患者140例作為研究對象,納入標準:經病理確診,采樣前未經放化療;女性;醫院倫理委員會批準了此次研究;患者在自愿條件下簽署了知情同意書;臨床與病理資料完整;單側發病;所有患者無血緣關系。排除標準:臨床資料不完整者;妊娠與哺乳期婦女;合并自身免疫性疾病等患者。年齡29~78歲,平均年齡(55.09±6.29)歲;分化程度:高分化74例,中分化36例,低分化30例;臨床分期:Ⅰ期40例,Ⅱ期45例,Ⅲ期40例,Ⅳ期15例;轉移情況:轉移100例,未轉移40例。
1.2 BRCA1和BRCA2突變檢測
取所有患者的癌組織樣本與癌旁組織標本,后者均肉眼下取自癌組織0.5 cm之外黏膜,且經組織病理學檢查均未見癌細胞浸潤。用酚/氯仿法提取組織樣本的DNA,操作按天根Genomic DNA Kit 說明書進行,選擇BRCA1和BRCA2的編碼區、5'和3'端非翻譯區、外顯子內含子拼接區用PCR(聚合酶鏈反應)進行擴增,由在線引物設計程序進行設計,由上海生工公司合成引物序列。PCR反應體系為25 μl,95 ℃ 3 min預變性后進行15個周期的溫度遞減循環,(94 ℃ 30 s,63 ℃~56 ℃ 1 min,每個周期遞減0.5 ℃,72 ℃ 1 min),隨后20個周期恒溫循環(94 ℃ 30 s,56 ℃ 1 min,72 ℃ 1 min),72 ℃延伸10 min。所有擴增的序列測序后進行Blast分析,所檢測到的位點在乳腺癌信息中心網站數據庫進行比對,確定突變情況。
1.3 統計學方法
應用SPSS 22.00軟件對所有數據進行分析,計數數據(BRCA1和BRCA2突變頻率)以%、百分比表示,對比為χ2檢驗,計量數據以均數±標準差表示,對比為t檢驗,相關性分析采用Logistic 回歸分析與Spearman相關分析,以α=0.05為檢驗水準。
2 結果
2.1 BRCA1和BRCA2突變對比
乳腺癌組織的BRCA1和BRCA2突變率分別為13.6%和14.3%,癌旁組織分別為0.7%和1.4%,對比差異有統計學意義(P<0.05)。見表1。
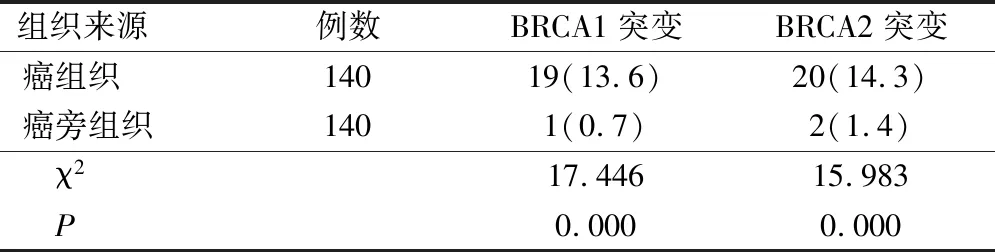
表1 不同組織的BRCA1和BRCA2突變情況對比(例,%)
2.2 BRCA1和BRCA2突變與與臨床病理特征的相關性
在140例癌組織中,不同臨床分期、分化程度與淋巴結轉移組織中的BRCA1、BRCA2突變率對比差異有統計學意義(P<0.05)。見表2。

表2 BRCA1和BRCA2突變與臨床病理特征的相關性(例,%)
2.3 相關性分析
Spearman相關分析顯示乳腺癌組織的BRCA1與BRCA2突變呈現顯著正相關性(γ=0.672,P=0.000)。Logistic回歸分析顯示乳腺癌的臨床分期、分化程度與淋巴結轉移都為影響BRCA1、BRCA2突變的獨立危險因素(P<0.05)。見表3與表4。
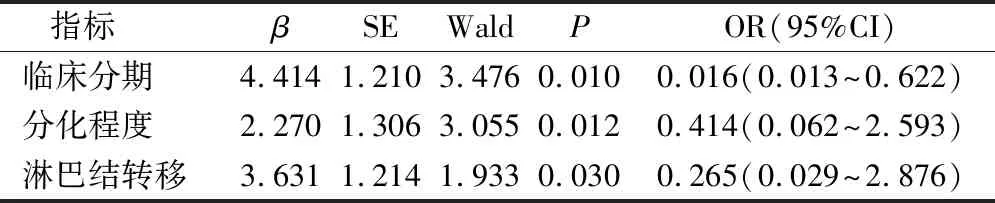
表3 影響乳腺癌組織BRCA1突變的主要因素
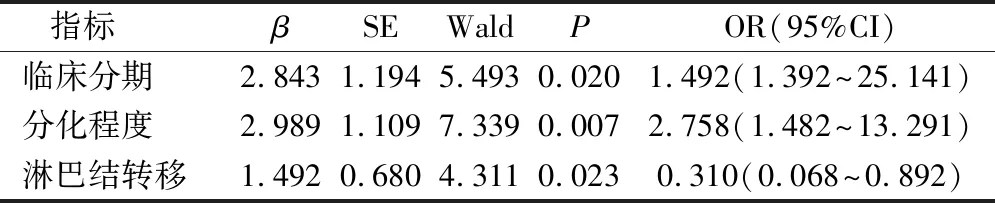
表4 影響乳腺癌組織BRCA2突變的主要因素
3 討論
乳腺癌是女性最常見的惡性腫瘤之一,在我國部分大城市已位居大城市女性腫瘤的第一位,乳腺癌的早發現、早診斷和早治療,是改善預后的有效途徑[12]。現代研究證明乳腺癌的發生是環境因素和遺傳因素共同作用的結果,部分乳腺癌的發生有一定的家族遺傳傾向,許多外顯基因參與其中,改變了個體對乳腺癌發病因素的易感性[13-14]。不過當前我國只有不到15%的遺傳性乳腺癌患者可檢測到BRCA1、BRCA2基因的致病性突變,多數遺傳性乳腺癌的遺傳因素并不明確[15]。
BRCA1和BRCA2是通過基因連鎖分析發現的與家族性發病密切相關的兩個基因。BRCA1位于人類染色體17q2l帶上,編碼1863個氨基酸,具有23個外顯子[16]。BRCA2位于人類染色體13q12帶上,編碼3418個氨基酸,包括27個外顯子。BRCA1和BRCA2是兩個功能復雜、涉及多條通路的關鍵基因,有研究顯示BRCA1突變攜帶者,在50歲時患乳腺癌的累計發病風險為30%左右,到70歲時累計發病風險為80%左右,特別是BRCA1突變組的對側乳腺癌發生率明顯升高,并且總生存期較短[17]。本研究顯示乳腺癌組織的BRCA1和BRCA2突變率分別為13.6%和14.3%,癌旁組織分別為0.7%和1.4%,對比差異有統計學意義(P<0.05)。還有研究顯示BRCA1和BRCA2是1個抑癌基因,BRCA1和BRCA2基因突變可造成機體對乳腺癌的易感性增高[18]。BRCA1和BRCA2基因突變原發乳腺癌患者對側乳腺癌的25年累積發病率為50%左右,BRCA1突變者乳腺癌的年齡與對側乳腺癌發病風險呈正相關[19]。
BRCA1和BRCA2相關性乳腺癌具有雌激素受體和孕激素受體陰性率高、CerbB-2陰性率高、p53陽性率高特點。有研究顯示在雌激素受體陰性且腫瘤分級為Ⅲ級的乳腺癌患者中,不論是否具有乳腺癌家族史,BRCA1突變的檢出率高達30%左右,BRCA1基因突變患者更容易出現發病年齡低、腫瘤組織的分化程度差、更容易發生腋窩淋巴結轉移等病理特征[20-21]。本研究顯示在140例癌組織中,不同臨床分期、分化程度與淋巴結轉移組織中的BRCA1、BRCA2突變率對比差異有統計學意義(P<0.05)。當前也有研究顯示不同種族人群BRCA1和BRCA2突變率的報道差別很大,來自遺傳性乳腺癌家族的個體表現出最高的BRCA突變頻率,BRCA突變可雙側乳腺癌中具有很高的突變率[22-23]。
本研究Spearman相關分析顯示乳腺癌組織的BRCA1與BRCA2突變呈現顯著正相關性(γ=0.672,P=0.000);Logistic回歸分析顯示乳腺癌的臨床分期、分化程度與淋巴結轉移都為影響BRCA1、BRCA2突變的獨立危險因素(P<0.05)。相關研究顯示遺傳性乳腺癌中BRCA1基因突變檢出率更高,可達90%,帶BRCA1基因的女性至70歲以前發生乳腺癌的機率為70%左右,且其發生乳腺癌或卵巢癌的時間較散發性患者要早[24]。通過對攜帶BRCA1或者BRCA2基因突變的高危人群進行篩查、隨訪和監測,有利于乳腺癌的早發現。不過未對BRCA1和BRCA2突變相關性乳腺癌的免疫組化及病理特點進行詳細回歸分析,主要由于是樣本數量比較少,待進一步加大樣本量進行分析。
總之,乳腺癌患者BRCA1和BRCA2突變比較常見,與臨床分期、組織學分化與淋巴結轉移等病理學特征顯著相關。

