COPD合并呼吸衰竭患者血清膽堿酯酶、前白蛋白水平及與預后的關系
劉京鶴 常宇飛 王建愉 秦 卓 馬剡芳
慢性阻塞性肺疾病(chronic odstructive pulmonary disease,COPD)是呼吸系統的常見病與多發病,且是一種破壞性的肺疾病并以發生率高、病情重、預后差等為主要特點[1]。其病因主要為小氣道發生相關病變或肺部的實質組織損傷,若不及時治療則可導致患者并發多種并發癥,呼吸衰竭作為COPD急性加重期的一種并發癥并可造成患者死亡[2]。COPD的急性加重期患者因體內嚴重缺氧會導致肝臟受到傷害,研究表明膽堿酯酶(cholinesterase,CHE)作為反應肝臟合成蛋白質功能的重要指標,可反映COPD合并呼吸衰竭患者的病情[3]。前白蛋白(prealbumin,PA)是由于肝臟合成的蛋白質并可反映早期肝細胞損害程度[4]。關于血清CHE、PA水平是否能夠作為COPD合并呼吸衰竭患者病情進展及判斷預后中的重要指標尚未見報道,因此本研究針對COPD合并呼吸衰竭患者血清CHE與PA水平變化及其與預后的關系進行探討。
資料與方法
1.一般資料:選取2015年3月~2016年6月期間筆者醫院收治的173例COPD患者作為研究對象,其中男性93例,女性80例,患者年齡為48~72歲,平均年齡55.26±9.68歲,平均BMI為22.37±3.58kg/m2,平均病程為15.36±5.34年。COPD緩解期組51例、COPD急性加重期組50例、COPD合并Ⅱ型呼吸衰竭組72例。根據住院期間COPD合并呼吸衰竭患者存活的53例患者作為生存組,死亡的19例作為死亡組,其中呼吸衰竭(Ⅱ型)診斷標準為海平面、靜息狀態、呼吸空氣條件下血氧分壓(PaO2)<60mmHg(1mmHg=0.133kPa),血二氧化碳分壓(PaCO2)>50mmHg。各組臨床資料比較,差異無統計學意義(P>0.05)。納入標準:①所有患者均符合中華醫學會制定的COPD診斷標準[5];②無高血壓或心力衰竭等疾病;③臨床資料完整者。排除標準:①心功能不全者;②患有惡性腫瘤者;③合并冠心病、肝臟、腎臟等器官功能嚴重障礙患者;④既往腦出血或腦梗死患者;⑤合并惡性疾病患者;⑥中途退出研究的患者。COPD急性加重期及其合并呼吸衰竭患者均于入院時給予廣譜抗生素、氧療、支氣管擴張劑及無創通氣等治療。
2.研究方法:(1)檢測血清CHE與PA水平:所有患者均于入組時清晨空腹狀態下抽取靜脈血3ml,離心后吸取血清,采用丁酰硫代膽堿法并選用試劑盒(北京利德曼生化技術有限公司)檢測血清CHE水平,正常參考值為(5~12)kU/L。采用免疫比濁法并選用試劑盒(浙江伊利康生物技術有限公司)檢測血清PA水平,正常參考值為250~400mg/L,儀器為AU 5800型全自動生化分析儀(美國貝克曼公司),所有操作均嚴格按照說明書進行操作。(2)指標檢測:所有受試者均在入院時抽取清晨空腹靜脈血5ml,3000r/min轉速離心15min,吸取血清置于-70℃冰箱保存。檢測血清白蛋白(ALB)、門冬氨酸氨基轉移酶(AST)、丙氨酸氨基轉移酶(ALT)、堿性磷酸酶(ALP)、總蛋白(TP),所有檢測試劑及標準品均購自上海北加生化試劑有限公司。采用乳膠免疫比濁法(日本SEKISUI公司)檢測血清超敏C反應蛋白(hs-CRP)水平。生存組與死亡組患者均進行急性生理學及慢性健康狀況評分系統評分(APACHEⅢ評分)。(3)肺功能指標檢測:應用日本福田公司生產的ST-75型肺功能檢測儀測定第1秒用力呼氣容積占預計值百分比(FEV1/Pred)與用力呼氣量占用力肺活量比值(FEV1/FVC)。
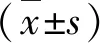
結 果
1.各組血清CHE與PA水平比較:各組患者血清CHE與PA水平存在明顯差異,COPD合并呼吸衰竭組患者血清CHE與PA水平顯著低于COPD急性加重期組與COPD緩解期組(t=2.945,P=0.004;t=7.936,P=0.001),COPD急性加重期組患者血清CHE與PA水平顯著低于COPD緩解期組(t=4.799,P=0.001),詳見表1。
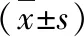
表1 各組血清CHE與PA水平比較
2.COPD合并呼吸衰竭組患者中生存組與死亡組間血清CHE與PA水平比較:COPD合并呼吸衰竭死亡組患者血清CHE與PA水平顯著低于生存組(P<0.05),詳見表2。
3.COPD合并呼吸衰竭生存組、死亡組患者臨床指標比較:COPD合并呼吸衰竭死亡組患者ALB、AST、 TP與FEV1/Pred均顯著低于生存組(P<0.05),而ALP、hs-CRP與APACHEⅢ評分均顯著高于生存組(P<0.05),詳見表3。
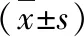
表2 COPD合并呼吸衰竭組患者中生存組與死亡組間血清CHE與PA水平比較
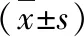
表3 生存組、死亡組患者臨床指標比較
4.COX比例風險回歸分析COPD合并呼吸衰竭患者預后的相關因素:將影響COPD合并呼吸衰竭患者預后的相關因素進行COX比例風險回歸分析,COX單因素分析結果顯示PA、CHE、TP與hs-CRP水平均為COPD合并呼吸衰竭患者預后的危險因素,COX多因素分析結果顯示血清PA與CHE水平均為COPD合并呼吸衰竭患者預后的獨立危險因素,詳見表4、表5。

表4 COX單因素回歸分析COPD合并呼吸衰竭患者預后因素
討 論
COPD以氣道與肺血管的慢性炎癥改變以及通氣功能阻塞為主要臨床表現,其臨床癥狀加重進而發

表5 COX多因素分析COPD合并呼吸衰竭患者預后因素
展為呼吸衰竭[6]。由于患者的肝功能受損引起CHE水平下降,而PA是一種負急性時相蛋白并與COPD急性加重期患者病情進展及嚴重程度呈顯著相關[7~9]。目前關于CHE、PA與COPD合并呼吸衰竭患者預后的相關性研究相對較少,因此本研究主要分析血清CHE、PA水平與COPD合并呼吸衰竭患者疾病進展及評估的關系,可為臨床早期診斷及預后評估提供理論依據。
CHE是由肝細胞產生的糖蛋白,可作為肝臟合成蛋白質功能的重要指標[10]。研究表明,COPD合并急性衰竭患者體內缺氧會抑制中樞神經性膽堿酯酶合成進而加快體內膽堿酯酶分解,缺氧、感染等因素可引發全身反應并釋放大量乙酰膽堿進而抑制膽堿酯酶的活性[11,12]。PA是由肝臟組織合成與分泌的急性相關性反應蛋白,其血清表達水平下降幅度與肝臟實質組織損害嚴重程度密切相關[13]。相關研究表明,血清CHE與PA的半衰期較短且不易受外源性因素的影響,并均可反映肝臟早期的儲備功能[14]。本研究結果顯示,COPD合并呼吸衰竭組患者血清CHE與PA水平顯著低于COPD急性加重期組與COPD緩解期組,COPD急性加重期組患者血清CHE與PA水平顯著低于COPD緩解期組,說明COPD合并呼吸衰竭患者血清CHE與PA水平顯著降低,隨著病情嚴重程度的增加而逐漸降低且差異有統計學意義,提示患者發生COPD合并呼吸衰竭時血清CHE與PA水平會迅速降低且隨著患者CHE與PA水平的降低幅度增大,其疾病嚴重程度甚至病死率就越高。
COPD合并呼吸衰竭是臨床危重癥,以氣流不完全可逆性限制為主要病理學特征,且常伴隨呼吸短促與痰液增多等炎性反應[15]。因此,早期診斷并及時治療COPD合并呼吸衰竭對改善患者預后具有重要意義。研究報道指出血清CHE含量可用于大面積腦梗死早期等急重癥患者的病情與預后評估,其含量越低患者病情越重且病死率越高[16]。相關研究表明,CHE與PA不僅可用于評估患者肝臟損傷,同時可作為判斷肝功能嚴重程度與預測預后的重要指標[17]。
本研究將COPD合并呼吸衰竭患者入院期間的生存情況分為生存組與死亡組,結果顯示死亡組患者血清CHE與PA水平顯著低于生存組,進一步分析發現死亡組ALB、AST、TP與FEV1/Pred均顯著低于生存組,而ALP、hs-CRP與APACHEⅢ評分均顯著高于生存組,其中上述指標可準確反映肝細胞合成的生理學構建功能并與肝臟實質組織及肺功能受損的嚴重程度密切相關[18]。同時本研究采用COX比例風險回歸分析COPD合并呼吸衰竭患者預后的相關因素,血清PA與CHE水平均為患者預后的獨立危險因素,提示血清PA、CHE水平與COPD合并呼吸衰竭患者預后密切相關,其表達水平越低患者預后越差。
綜上所述,血清CHE與PA水平對COPD合并呼吸衰竭患者疾病嚴重程度與預后均具有較高的評估價值,且均可作為預測患者疾病進展與評估預后的有效指標。

