高中化學圖像題解題思路及典型例析

摘? 要:隨著教育事業的發展,新課程改革不斷深入,此背景下我國高中化學課程也發生了較大程度的變化。圖像題解題為高中化學解題方式中較為常見的一種,此方法不但能夠幫助學生實現解題能力上的有效提升,還可針對不同題型進行不同解題方式的轉換,進而提高學生答題整體準確率。本文針對高中化學圖像題解題思路及典型例題進行分析。
關鍵詞:圖像題解題;高中化學;運用;思維
高中化學知識所涉及內容相對較多,并且難度相對較大,因此許多高中生在學習化學知識期間常受到阻礙,圖像能夠較大程度上幫助學生提高對于化學知識的認識,將化學知識進行直觀展現,不但激發學生學習興趣,還能幫助學生實現對化學知識的充分掌握。在高中化學中,圖像主要引導學生利用坐標知識,對理論知識進行弱化,使抽象化理論知識能夠更為直觀的展現于學生面前,進而實現學生化學解題能力的提升。
一、高中化學反應速率因素及化學平衡移動
(一)反應速率因素及化學平衡移動的典型例題
高中化學知識難點相對較多,其中主要包括平衡移動及反應速率相關知識,此兩項知識內容對學生解題能力要求相對較高,學生必須充分了解影響化學反應速率的條件,并在此基礎上實現對化學平衡移動及物質狀態的深入分析,才可實現對此化學類型題的有效解答。例如:可逆反應M+N? ? X+Y增大壓強時,化學反應速率將出現如圖1所示變化,那么M、Y、N、X四種物質的聚集狀態為(? ? )。
A.N、M同為氣體,Y、X僅有一種為氣體
B.M為非氣體,Y、X、N均為氣體
C.X、Y皆為非氣體,M、N均為氣體
D.N、M均為氣體,X、Y均為氣體
(二)解題思路
根據影響化學平衡及反應速率的因素進行分析,在壓強增加情況下,V1以及V2同時增大,表示生成物和反應物中均有氣態物質存在,但不能說明所有物質均為氣體。此時由于V2增大的幅度大于V1,平衡將向逆反應移動,從而可以確定生成物氣體計量數和大于反應物中氣體計量數的總和,由上述分析可知,此化學題的最終答案即為A。
高中化學學習過程較為繁瑣,因此學生在學習期間,應針對化學反應速率進行重點研究,明確影響其的內外因素。在化學反應速率因素中,物質本身存在的結構及性質的差異即為內因,而影響化學反應速率的主要因素即為外因,因此學生在化學知識探究期間,應針對內外因特點,分析反應物的壓強、體系溫度以及濃度等,如此才能實現解題能力的提升。
二、高中化學離子共存推斷題
(一)離子共存推斷例題
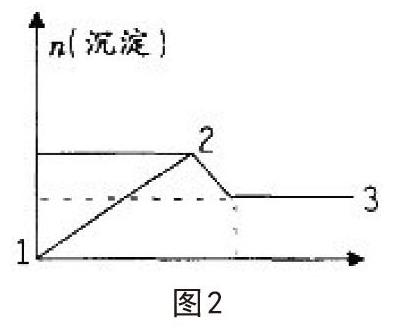
高中化學中的離子共存推斷題,難度相對較高,許多高中生實際解題時無法理解題意思。同時,此類題型所涉及內容相對較多,許多學生在學習期間常出現知識混淆現象,此現象在一定程度上降低了學生答題準確率,若無法對此問題進行及時解決,將打擊學生學習積極性。圖像解題方法能夠對化學題目進行分解,使其以更為直觀的方式呈現于學生,幫助學生理解化學知識,進而實現解題能力的提升。例如:某無色透明溶液中可能存在以下離子:A13+,K+,Fe3+,NH4+,Cu2+,Mg2+,若往溶液中加入Na2O2粉末,則溶液產生無色無味氣體及白色沉淀物。根據生成沉淀量以及Na2O2粉末含量之間的關系,如圖2所示,進行溶液離子的推算。
(二)解題思路
據題意,學生在解題時應注意以下幾點:應根據無色透明溶液將Cu2+以及Fe3+元素進行排除,而后根據溶液因Na2O2粉末加入后,出現氣體推斷,NH3并未出現,產生氣體中僅有O2,由此可推算出,溶液中并未存在NH4+。而后應針對本題的實際圖像進行深入探究可知,溶液就點1開始便以出現沉淀現象,而過氧化鈉及沉淀物的量呈現正比例上升趨勢,由此可知,溶液中存在A13+、Mg2+等離子。而由曲線以及點2可知,在點2處,沉淀的總量最大,但隨后沉淀卻開始減少可知,有A13+離子;比較點1以及點2,點3時沉淀的量不再改變,則知溶液內沉淀物為Mg(OH)2。
三、結語
綜上所述,高中化學知識點涉及內容相對較多,且知識點難度較大,若學生無法在學習期間建立知識結構,完善學習方法,將嚴重影響其實際解題思路。而圖像解題方法能夠較大程度上解決學生這一問題,并且幫助學生實現學習能力的提升。在學生將圖像解題方式應用于高中化學問題過程中,首先應及時分析題目的主要類型,而后明確題目所要傳達的具體內容,最后應用所學知識及圖像解題法對化學問題進行解答,如此不但能夠實現學習積極性的提升,還將有效提高解題能力,進而實現解題思維的有效拓展。
參考文獻
[1]黃元東,顏燕,閆春更,周青.化學教學設計能力評價量表的編制與應用研究[J].化學教育(中英文),2019,40(01):35-42.
[2]單斐.淺談高中化學課堂例題講解策略[J].名師在線,2016(10):26-27.
[3]宋婷,李遠蓉,秦小翕.高中化學教材章節圖像的特點分析及教學功能研究[J].化學教育,2014,35(05):11-13.
作者簡介
黃麗潔(1988.09—),女,漢族,廣西博白人,大學本科,中學二級教師。

