從VEGF和sVEGFR2探究分子靶向藥物舒尼替尼治療轉移性腎癌的機制
劉 暢,張 寧
(1.鶴壁市人民醫院泌尿外科,河南鶴壁 458030;2.北京大學腫瘤醫院泌尿外科,北京 100020)
腎細胞癌是泌尿外科常見惡性腫瘤,發病率在泌尿生殖系統腫瘤中排名第二[1]。該病起源于腎臟中泌尿小管上皮系統,發病隨年齡增加[2];男性發病率高于女性,多發于40至55歲的男性患者[3];主要臨床表現為血尿、發熱、貧血、腫塊和腰疼等[4]。目前發病機制尚不明確,可能與職業、生活習慣、飲食及其他疾病相關[5],臨床治療手段有手術治療、化學治療、免疫治療和分子靶向治療[6]。靶向治療已成為轉移性腎癌的有效輔助治療手段,可提升患者的生存率[7]。激酶抑制劑舒尼替尼(Sunitinib)是臨床最常見的治療腎癌的藥物[8],其治療晚期腎癌的藥物,作用機制明確。而腎門淋巴結對腎癌的轉移有指示性意義。本研究通過血管內皮生長因子(vascular endothelial growth factor,VEGF)和可溶性血管內皮生長因子受體2(solubility vascular endothelial growth factor receptor 2,sVEGFR2)兩種生物標志物,解析分子靶向藥物Sunitinib在治療轉移性腎癌過程中的作用機制,探究分子靶向治療過程的關鍵因素。
1 資料與方法
1.1 一般資料選取2015年6月至2017年6月間在鶴壁市人民醫院泌尿外科住院治療的100例轉移性腎癌患者作為研究對象,按照不同治療方案,分為服用Sunitinib輔助治療組(Sunitinib組,n=50)和未服用Sunitinib輔助治療組(不服藥組,n=50)。
1.2 納入和排除標準納入標準:① 年齡40~60歲的患者;②根據WHO《腎細胞癌的病理分類和診斷標準(2004版)》[9]確診為轉移性腎癌;③經影像學/病理學確認已轉移并至少有1處可測量病灶,TNM分期為T1~3N0~1M0期;④Karnofsky功能狀態評分[10]在60~90分之間;⑤未接受過系統治療。排除標準:①心、肝、腎等重要臟器功能衰竭或移植者;②嚴重自身免疫性疾病者;③伴有其他惡性腫瘤者;④過敏體質及對研究用藥過敏者;⑤有認知功能障礙或精神異常,無法配合完成研究者。倫理學考量:①患者簽署參知情同意書;②保障患者的醫療安全和隱私權;③試驗遵循《渥太華工作組關于臨床試驗注冊的聲明》。
1.3 服藥情況Sunitinib(美國輝瑞公司,批準文號:H2013025,規格:12.5 mg×28 s)按照標準的4/2治療方案,每天1次口服50 mg,服藥4周停藥2周為1個周期[11]。每周評估患者的不良反應,根據具體情況給予藥物減量至下一劑量水平或停藥。
1.4 療效評價治療4個周期后進行評價,直至治療結束。按實體瘤療效評價標準(response evaluation criteria in solid tumour,RECIST)進行評價。完全緩解(complete regression,CR):所有靶病灶消失;部分緩解(partial regression,PR):靶病灶最長徑之和與基線狀態比較,縮小≥ 30%;病變進展(progressive disease,PD):靶病灶最長徑之和與治療開始后所記錄到的最小靶病灶最長徑之和比較,增加≥20%,或者出現1個或多個新病灶。病情穩定(stable disease,SD):縮小未達PR,增加未達PD。
1.5 評估治療后的不良反應情況根據腫瘤化療藥物不良反應評價標準[12](Common Terminoloy Criteria adverse Events Version 3.0,CTCAE v3.0),評估電解質紊亂、發熱、腎功能減退、胃腸道反應(惡心、腹瀉、嘔吐)、中重度貧血、左室射血分數降低等不良反應。
1.6 VEGF和sVEGFR2檢測使用VEGF和sVEGFR2試劑盒(美國RB公司),按照試劑盒說明書進行嚴格操作,使用ELISA方法,檢測患者血清中兩種生物標記物的濃度。檢測使用多功能酶標儀進行(日本Thermo公司),檢測波長450 nm,每個樣品進行6次重復試驗,計算平均值,利用不同生物標記物的標準曲線測定不同標記物的濃度。
1.7 測量腎癌轉移前哨淋巴結(hilar lymph nodes,HLN)的數值采用電子計算機斷層掃描(computed tomography,CT)測量腎癌轉移前哨淋巴結HLN的總徑值,推測病灶的縮小比例。
2 結 果
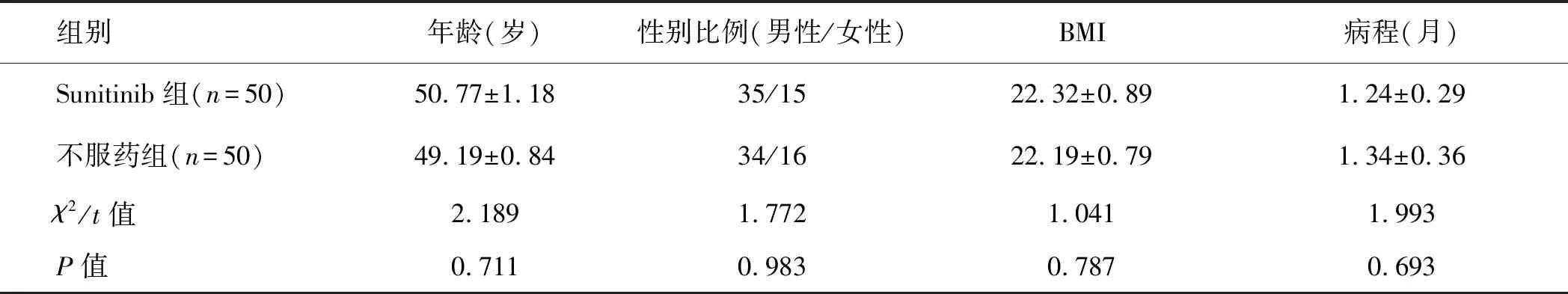
2.1 受試者一般情況首先,對本研究中的各組受試者的一般情況進行比較,結果顯示兩組患者的年齡、性別比例、體質量指數(body mass index,BMI)和病程均無統計學差異(P0.05)。此外,研究過程中所有受試者均完成了全部試驗,無中途退出者,亦無改用其他療法者(表1)。
表1 受試者一般情況(n=100)
BMI:體質量指數。
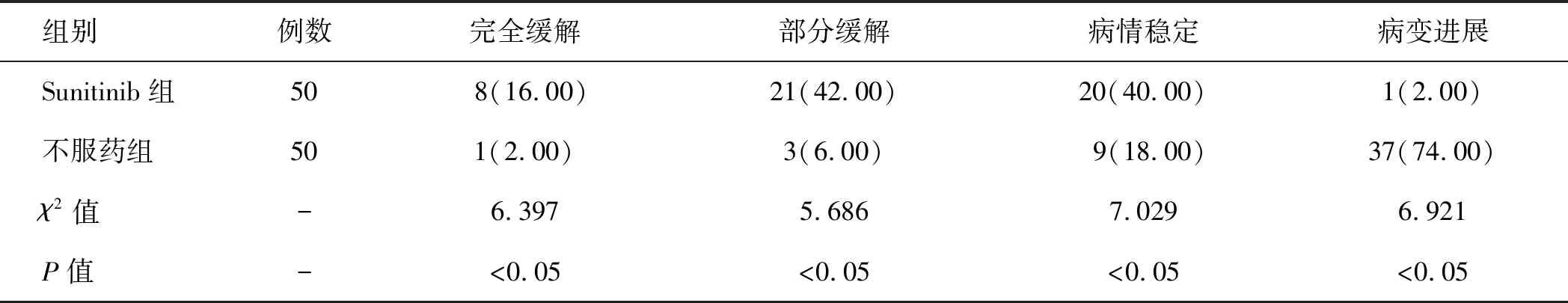
2.2 受試者治療效果比較Sunitinib組患者的治療效果中,完全緩解的例數和比例為8/50(16%),部分緩解的例數和比例為21/50(42%),病情穩定的例數和比例為20/50(40%),病變進展的例數和比例為1/50(2%);不服藥組患者中,治療效果完全緩解的例數和比例為1/50(2%),部分緩解的例數和比例為3/50(6%),病情穩定的例數和比例為9/50(18%),病變進展的例數和比例為37/50(74%)。Sunitinib組患者的治療效果高于不服藥組患者(P<0.05,表2)。
表2 受試者治療效果比較[例(%)]
2.3 患者并發癥發生的情況Sunitinib組中的獲益組、非獲益組與不服藥組的并發癥有明顯差異(P<0.05),獲益組、非獲益組患者主要存在電解質紊亂、發熱、腎功能減退、胃腸道反應(惡心、腹瀉、嘔吐)、中重度貧血、左室射血分數降低等不良反應(表3)。
表3 患者并發癥發生的情況[n(%)]
2.4 受試者生物標記物水平比較獲益組患者比非獲益組和不服藥組的VEGF水平升高、sVEGFR2水平降低,這表明VEGF和sVEGFR2是Sunitinib治療轉移性腎癌患者過程中的關鍵參數(P<0.05,表4)。
表4 受試者生物標記物水平變化值的比較(n=50)

VEGF:血管內皮生長因子;sVEGFR2:可溶性血管內皮生長因子受體2;與非獲益組比較,*P<0.05,與不服藥組比較,#P<0.05。
2.5 受試者腫瘤轉移灶(HLN)與生物標記物濃度的相關性分析
2.5.1治療前 Sunitinib組患者的HLN與VEGF的相關系數-0.996,P值為0.015,與sVEGFR2的相關系數為0.984,P值為0.018;不服藥組患者的HLN與VEGF的相關系數0.101,P值為0.829,與sVEGFR2的相關系數為0.484,P值為0.528。結果表明,HLN與VEGF呈負相關(P<0.05),與sVEGFR2呈正相關(P<0.05,表5)。
表5 受試者治療初期腫瘤轉移灶與生物標記物濃度的相關性分析(n=50)

HLN:前哨淋巴結;VEGF:血管內皮生長因子;sVEGFR2:可溶性血管內皮生長因子受體2。
2.5.2治療后 舒尼替尼治療晚期腎癌的臨床緩解率為36.00%。治療后,Sunitinib組患者的HLN與血管內皮生長因子的相關系數-0.931,P值為0.059,與可溶性血管內皮生長因子受體2的相關系數為0.802,P值為0.218;不服藥組患者的HLN與血管內皮生長因子的相關系數0.185,P值為0.814,與可溶性血管內皮生長因子受體2的相關系數為0.384,P值為0.611。結果表明,HLN與血管內皮生長因子水平呈負相關(P<0.05),與可溶性血管內皮生長因子受體2無相關性(P0.05,表6)。
表6 受試者治療末期腫瘤轉移灶與生物標記物濃度的相關性分析(n=50)
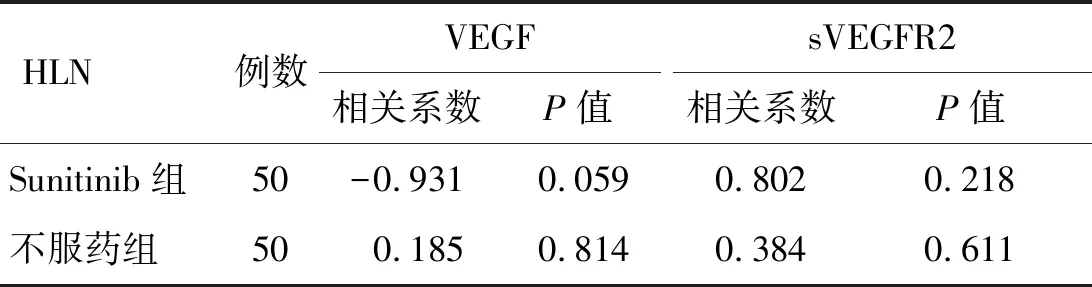
HLN:前哨淋巴結;VEGF:血管內皮生長因子;sVEGFR2:可溶性血管內皮生長因子受體2。
3 討 論
目前,小分子靶向藥物治療腎癌等惡性腫瘤已經廣泛應用于臨床,并取得了一定的治療效果[13],可提升患者生存率。Sunitinib具有抑制腫瘤血管生成和腫瘤細胞生長的多重抗癌作用,其靶點有:VEGFR(VEGFR1、VEGFR2、VEGFR3),及血小板源生長因子受體(platelet-derived growth factor receptor,PDGFR)α和β等[14]。同時,Sunitinib由于受體較多,其在臨床使用過程中易產生手足綜合征、口腔炎、其他皮膚和皮下組織異常等副作用。本次研究的結果顯示,服用Sunitinib輔助治療的患者其療效優于對照組,但發生不良反應的幾率也相應增高。
HLN是腎腫瘤患者引流腫瘤淋巴液并最先發生轉移的淋巴結,按照解剖學及“由近及遠”的轉移原則,如未檢測到此淋巴結轉移,患者可免于行規范的根治性切除和廣泛性淋巴結清掃。本次研究還發現,治療前后HLN與VEGF水平均呈顯著負相關;治療前HLN與sVEGFR2呈顯著正相關,治療后HLN與sVEGFR2無顯著相關。VEGF和sVEGFR2均可有效指示Sunitinib的治療過程,VEGF的作用過程需要借助其受體sVEGFR2的信號通路完成,同時其作用過程下調了sVEGFR2的表達水平[15];患者治療后病情緩解,無需要通過sVEGFR2的水平變化調控,故sVEGFR2水平與HLN無顯著相關。可以認為,VEGF表達水平越高,腫瘤血管更加豐富,腫瘤生長更快、侵襲性更強[16],Sunitinib等小分子靶向藥物治療的效果也越好。VEGF和sVEGFR2因子在小分子靶向藥物治療腎細胞癌的臨床過程中可成為其遠期療效的預測因子[17]。進一步分析其原因,Sunitinib作為抗腫瘤治療的新型藥物,主要通過抑制腫瘤內血管生長產生作用,直接抗腫瘤細胞效應相對較弱[18];抑制血管生成的過程復雜、受多種因素影響。隨著對腫瘤血管形成過程認識的深入及檢測技術的發展,盡早篩選出抗VEGF 藥物療效的、靈敏度高的預測因子,以界定優勢人群,達到個體化治療目的;同時可以更準確地區分不同的腫瘤類型,避免無效甚至有害的治療。
綜上所述,Sunitinib可有效控制轉移性腎癌患者的病情,并與VEGF等受體的調節有關,VEGF是評估其療效的有效預測指標。本研究闡述了Sunitinib治療轉移性腎癌的部分作用機制,具有一定的臨床研究與應用價值。