基于水滑石的全蛋液中磷吸附與解吸及動力學模型研究
遲玉杰 何 晶 趙 英 馬艷秋 安瑞琪
(1.東北農業大學食品學院, 哈爾濱 150030; 2.東北農業大學農學院, 哈爾濱 150030)
0 引言
腎臟是人體內磷代謝的重要場所,當其發生病變時,機體就會出現磷代謝紊亂,并伴隨許多并發癥[1]。慢性腎臟病(Chronic kidncy discase, CKD)高磷血癥是世界上高發病率和高死亡率的疾病之一,國外有46.7%的腎病患者存在高磷血癥,國內情況更為嚴重,發生率高達81%[2-4]。目前,患者主要依靠透析和藥物治療維持機體的磷代謝水平,其專用飲食較為短缺,腎病患者飲食既需要優質蛋白質,又同時要求磷含量較低,磷/蛋白質(Phosphorus/Protein, P/Pro)質量比值要求控制在10~12 mg/g范圍內[5-6],要求日常膳食磷的攝入量為3.3~16.0 mg/(100 kJ),透析治療后磷的攝入量為6.0~16.0 mg/(100 kJ)[7]。全蛋液營養全面且豐富,其蛋白質生物價高達100,易被人體吸收[8-10],是患者優選的蛋白來源。全蛋液中磷質量濃度為2 268~2 289 mg/L,P/Pro質量比值為16.15~19.09 mg/g[11],基于腎病患者低磷飲食的需求,需進行全蛋液脫磷技術的開發,制備適于腎病患者的專用型食品配料。
目前,關于磷酸基團的去除方法已有一定的研究,主要包括酶法、超濾膜、離子交換樹脂及吸附法等[12-16]。其中,采用吸附劑進行磷的去除易于工業化生產,是一種方便、快速的加工方式。水滑石(Layered double hydroxide, LDH)是一種常見的用于吸附磷酸鹽離子的材料[17],其由帶正電荷的主體層板和層間陰離子通過非共價鍵相互作用組裝而成,層間陰離子可與各種陰離子,包括無機離子、有機離子、雜多酸離子以及配位化合物的陰離子進行交換[18]。本實驗采用的吸附劑為Mg-Al LDH,是一種典型的天然礦物,其層板由鎂八面體和鋁氧八面體組成,具有較強的堿性[19]。相比其他吸附劑,LDH對陰離子如磷酸根離子具有吸附效率高、無二次污染及價格低廉等優點,且在高溫焙燒時具有記憶效應,高溫形成的無定形物可以通過水合重構結構,利于進行循環使用[20]。LDH是一種堿性材料,已廣泛應用于醫藥和食品行業,且已作為胃藥成分被收入英國藥典[20]。LDH在藥物緩釋方面已有大量研究[20-23]。同時,利用LDH制備的食品包材具有良好的抗菌特性,可有效延長食品貨架期[23]。目前,采用LDH進行磷吸附已具備一定的研究基礎,學者們進行了不同層次吸附機理的探究。賈云生等[24]采用Ca-Al LDH進行磷吸附,吸附規律符合Langmuir 吸附等溫方程,吸附動力學過程符合準二級動力學方程。FROST等[25]則研究了LDH吸附磷的機理,研究表明,熱處理可以提高LDH對磷的吸附效率,同時層間陰離子的組成受pH值影響較大,且堿性條件下吸附較高價態的磷酸根離子。
本文通過吸附等溫線、吸附動力學、吸附熱力學表征LDH除磷機理,測定吸附過程中全蛋液蛋白質溶解度的變化及氨基酸含量變化,分析LDH進行全蛋液磷吸附的適用性。同時基于綠色、經濟的實驗原則,對LDH進行循環利用。
1 材料與方法
1.1 原料與儀器
新鮮雞蛋,市售;Mg-Al LDH,邵陽天堂助劑化工有限公司;磷酸二氫鉀標準品,純度99.99%以上,上海阿拉丁生化科技股份有限公司;鄰苯二酚、鉬酸銨、亞硫酸鈉、硫酸銅、氯化鈉、氫氧化鈉、鹽酸及硫酸等均為國產分析純。
KSW-5-12A型馬弗爐,天津市中環實驗電爐有限公司;日立L-8800型氨基酸自動分析儀,日本日立公司;TU-1810型紫外可見分光光度計,北京普析通用儀器有限責任公司;SHA-B型水浴恒溫振蕩器,常州億通分析儀器制造有限公司;高速臺式冷凍離心機,上海安亭科學儀器廠。
1.2 樣品的制備
將新鮮雞蛋經清洗、打蛋,轉速135 r/min下攪拌至均勻,采用尼龍網紗(篩分粒度100目)過濾系帶等雜質得到全蛋液。加入0.20 mol/L NaOH溶液,40℃攪拌(135 r/min)1.5 h,冷卻恢復至室溫(20℃)后采用0.10 mol/L HCl溶液調節pH值至8.5。按國家標準進行全蛋液中磷含量的測定[26],樣品磷質量濃度為2 200 mg/L。采用去離子水稀釋全蛋液樣品,制備一系列磷質量濃度梯度的全蛋液,分別為25、50、75、100、125、150 mg/L。
1.3 LDH吸附實驗
參照SHIN等[27]的方法,取稀釋全蛋液100 mL至錐形瓶中,分別加入2.5、5.0、7.5、10.0、12.5、15.0 g/L的LDH,吸附溫度為20、25、30、35、40、45℃,吸附時間為0、1、2、3、4、5、6、7 h,攪拌(轉速135 r/min)吸附后采用尼龍網紗(篩分粒度300目)過濾混合物,并分別收集全蛋液樣品和LDH,測定全蛋液中磷含量及蛋白質溶解度,LDH對全蛋液中磷的吸附量以及蛋白質溶解度[28]計算公式為
Qt=(C0-Ci)V0/m
(1)
式中Qt——t時刻吸附量,mg/g
C0——吸附初始吸附質的質量濃度,mg/L
Ci——吸附后吸附質的質量濃度,mg/L
V0——樣品初始體積,L
m——吸附劑質量,g
(2)
式中S——蛋白質溶解度,%
P——樣品中總蛋白質質量,g
P1——上清液中蛋白質質量,g
1.4 吸附等溫式
Langmuir吸附等溫式的前提條件是吸附表面均勻并且為單分子層,其線性表達式為
(3)
式中Ce——吸附質的平衡質量濃度,mg/L
Qe——吸附劑的實驗平衡吸附量,mg/g
Qm——最大吸附量,mg/g
b——Langmuir常數,L/mg
Langmuir吸附等溫式重要的平衡參數為RL,定義為
(4)
Freundlich吸附等溫式應用于非均勻吸附劑的多層吸附,其線性表達式為
(5)
式中KF——吸附能力Freundlich常數
n——吸附強度Freundlich常數
1.5 吸附動力學及熱力學模型
準一級動力學模型即Lagergren一級動力學模型,用于研究液相-固相體系的吸附過程,公式為
ln(Qe-Qt)=lnQe-tK1
(6)
式中t——吸附時間,min
K1——準一級動力學模型常數,min-1
準二級動力學模型由HO和MCKAY提出[29],方程線性化后為
(7)
式中K2——準二級動力學模型常數,g/(mg·min)
熱力學參數是吸附過程實際應用中的重要指標,包括Gibbs自由能變(ΔG)、焓變(ΔH)和熵變(ΔS)。
ΔG=ΔH-TΔS
(8)
ΔG=ΔH-RTlnK
(9)
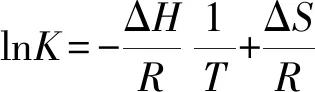
(10)
(11)
式中 ΔG——吸附自由能變,kJ/mol
ΔH——吸附焓變,kJ/mol
ΔS——吸附熵變,J/(mol·K)
R——摩爾氣體常數,取8.314 J/(mol·K)
T——熱力學溫度,K
K——固液分配系數
1.6 LDH的解吸及重復利用
1.6.1解吸實驗
將吸附后分離得到的LDH,在室溫下利用0.6 mol/L的NaCl進行解吸,液料比(解吸液體積與LDH質量比)分別為0.25、0.50、0.75、1.00、1.25、1.50 L/g,解吸時間為1~8 h,解吸率計算公式為
(12)
式中Rd——解吸率,%
Cd——解吸液中吸附質的質量濃度,mg/L
Vd——解吸液的體積,L
Qd——吸附-解吸平衡的吸附量,mg/g
1.6.2重復利用
經過NaCl解吸后的LDH進行500℃焙燒4 h,冷卻后使用[19],其添加量為7.5 g/L,吸附時間5 h,全蛋液磷初始質量濃度125 mg/L,吸附溫度30℃,pH值8.5。按式(1)計算Qt。
1.7 氨基酸含量測定
精確稱取10 mL全蛋液/脫磷全蛋液,參照WANG等[9]方法測定蛋液中各氨基酸含量。
1.8 數據處理
實驗中所有結果都是3次測定的平均值,計算標準偏差,采用SPSS 19.0進行顯著性分析。采用Origin 8.6軟件對數據進行分析與制圖,模型擬合采用Curve Expert 32軟件。
2 結果與分析
2.1 LDH吸附時間對吸附量及溶解度的影響
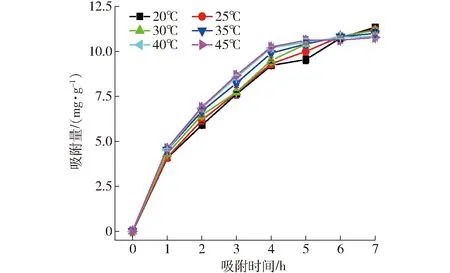
圖1 LDH吸附時間對全蛋液中磷吸附量的影響Fig.1 Effect of LDH adsorption time on quantity of adsorption of phosphate in whole egg liquid
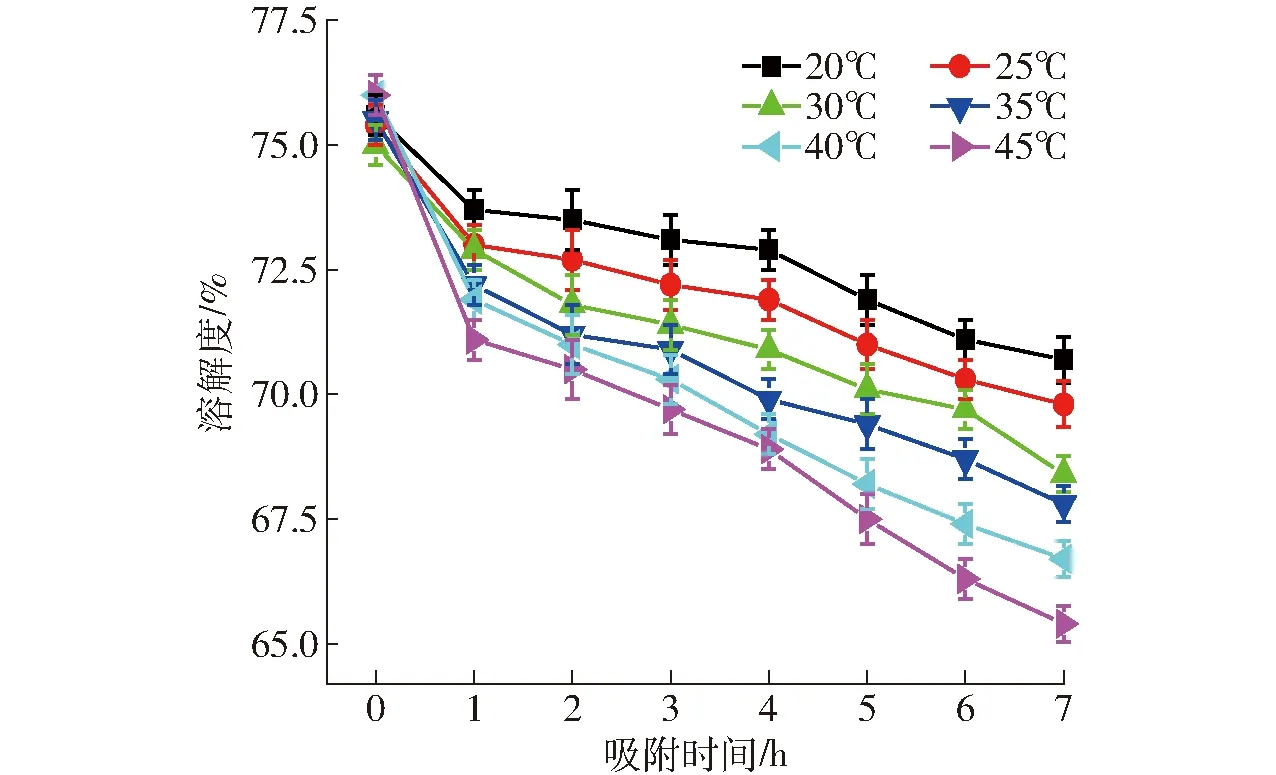
圖2 LDH吸附時間對全蛋液溶解度的影響Fig.2 Effect of LDH adsorption time on solubility in whole egg liquid
圖1、2分別為溫度20~45℃范圍內,不同吸附時間(1~7 h)LDH對吸附量及溶解度影響結果。由圖1可知,隨著吸附時間的增加,LDH的吸附量逐漸增加(P<0.05),實驗中LDH對全蛋液中磷的最大吸附量超過10 mg/g。SHIN等[27]的研究中也采用LDH進行磷的吸附,研究得到相同的吸附趨勢,隨著吸附時間的增加吸附效果逐漸提高。本實驗中5~7 h吸附時間內的吸附量曲線交叉重疊較多,吸附時間達到6 h時,40℃和45℃的吸附趨于飽和。LI等[30]的研究中采用天然磁黃鐵礦進行磷的吸附,得到了與本實驗相似的結論,較長時間吸附后增長率降低,吸附接近飽和。同時,實驗中發現LDH吸附前6 h內較高溫度吸附量較大,而6 h后較低溫度的吸附量超過較高溫度的吸附。這可能是由于在吸附初期,溫度越高,分子運動越快,吸附強度也越大(P<0.05)。而長時間吸附后,熱處理的蛋液發生凝固現象[31-34],嚴重影響吸附劑與吸附質的接觸,且溫度越高熱凝固的影響越大。吸附6 h后各溫度下吸附量數值接近,差異不顯著(P>0.05)。
不同溫度下,利用LDH進行全蛋液中磷的吸附,溶解度呈下降趨勢(P<0.05),且各溫度吸附的下降趨勢相似,較低溫度吸附時溶解度始終高于高溫吸附(P<0.05),這也與全蛋液的熱凝固密切相關。蛋白質受熱后形成網狀交聯結構,甚至出現不溶性熱聚合體,導致溶解度下降[35]。AMR等[36]研究了熱處理對溶解度的影響,升高20℃溶解度損失13%。本實驗中溫度升高20℃后,溶解度損失不超過10%。這主要是由于全蛋液含水率高于AMR的實驗,在一定程度上較高的含水率利于蛋白質穩定存在于體系中,宏觀表現為溶解度較高。
2.2 初始質量濃度對吸附量及溶解度的影響
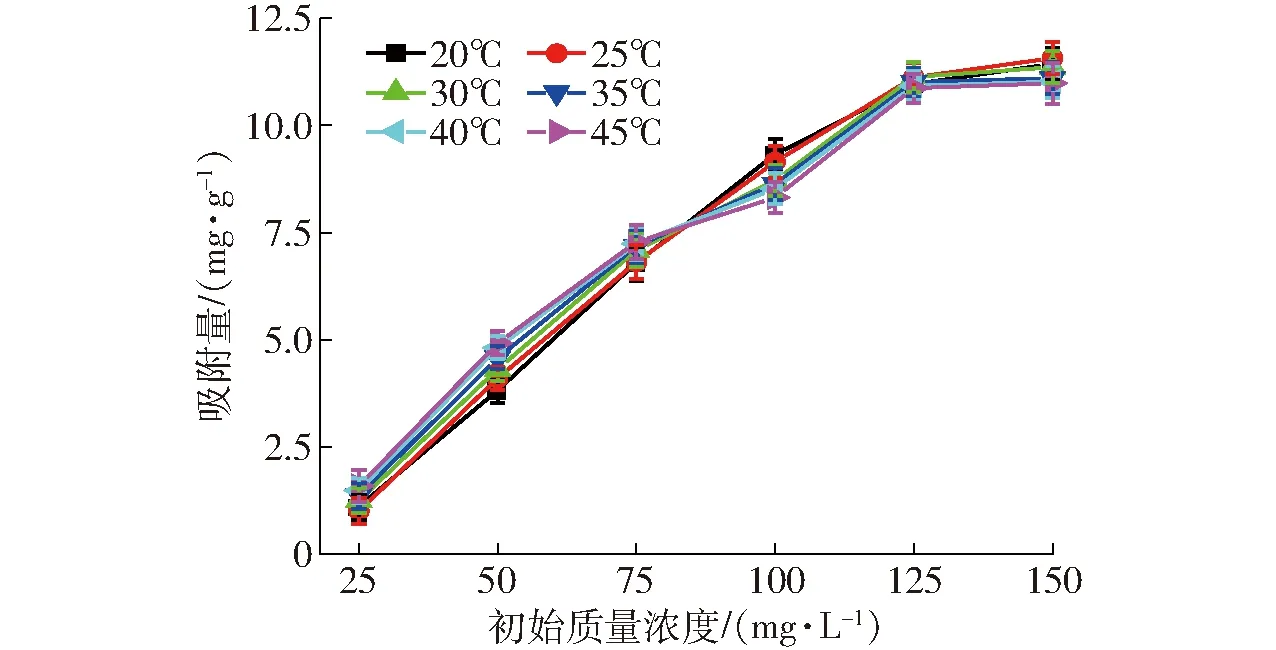
圖3 磷的初始質量濃度對LDH吸附量的影響Fig.3 Effect of initial concentration of phosphate on its quantity of adsorption of LDH adsorption
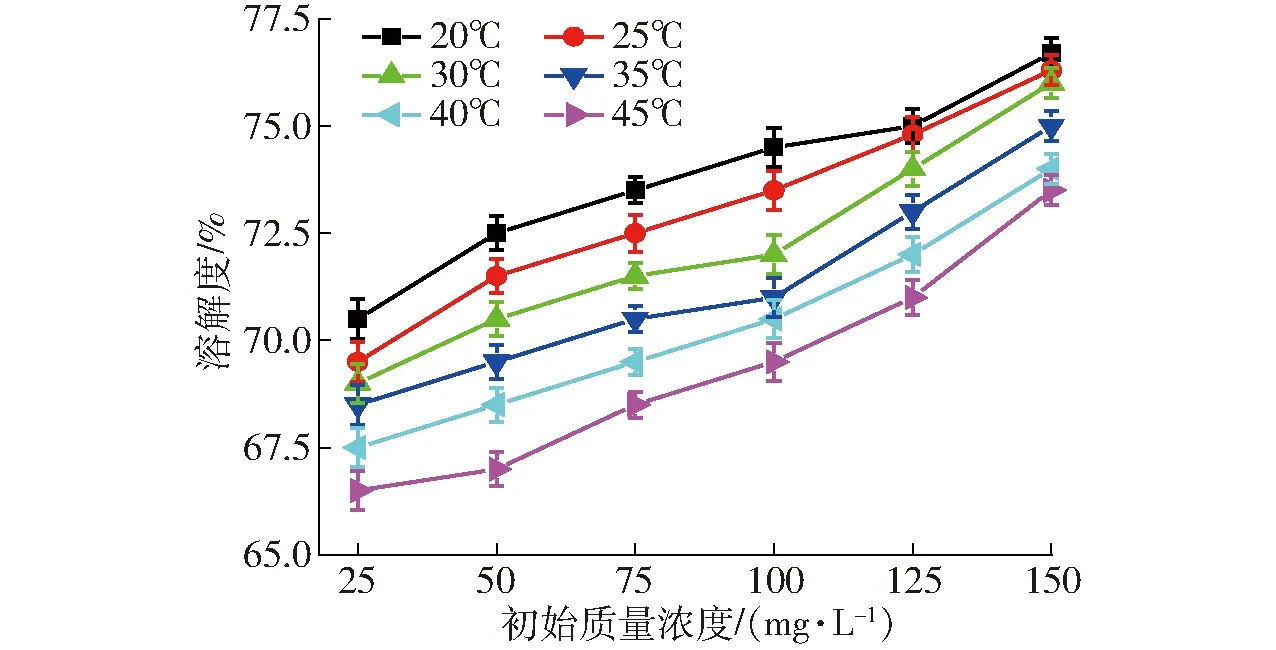
圖4 磷的初始質量濃度對全蛋液溶解度的影響Fig.4 Effect of initial concentration of phosphate on solubility in whole egg liquid
通過去離子水稀釋得到一系列磷質量濃度梯度的全蛋液,分別為25、50、75、100、125、150 mg/L。圖3、4分別為全蛋液中磷的初始質量濃度對LDH吸附量和溶解度的影響,較低初始質量濃度時,LDH分散性好,溫度高的全蛋液中磷的吸附效果相對較好,但各溫度下吸附量差異不顯著(P>0.05)。當初始質量濃度達到75 mg/L后,較低溫度(20、25、30℃)的吸附量高于較高溫度吸附量(35、40、45℃)。初始質量濃度超過125 mg/L后,較高溫度的吸附增長率顯著降低,吸附趨于平衡,而相對低溫的吸附仍具有較高的增長率。這主要是與蛋液的耐熱性有關,全蛋液濃度較高時易造成熱聚集,稀釋的蛋液熱聚集程度相對較低[31]。隨著蛋液中磷質量濃度的增加,LDH對磷的吸附量逐漸增大(P<0.05)。在YAO等[37]的研究中采用紅色和灰色陶瓷黏土進行磷吸附,認為磷的初始質量濃度、吸附溫度、吸附量三者間的相關性較強。而本實驗中磷初始質量濃度對吸附影響顯著,而溫度對吸附量影響較弱。這可能是由于實驗所用材料的不同,本實驗采用的LDH具有熱穩定性,而YAO等[37]的研究中采用的陶瓷黏土更易受溫度影響。在SARKAR等[38]的研究中發現吸附濃度對吸附的影響程度較弱,這可能與吸附質性質有關,SARKAR等研究中吸附質為酚類有機物(如苯酚、1,2-二羥基苯、1,3-二羥基苯和1-羥基-4-硝基苯),所帶電荷小于本實驗中的吸附質磷。吸附質所帶電荷越高,吸附強度越大[13]。從圖4可知,溶解度受磷初始質量濃度的影響顯著(P<0.05),均為逐漸增加的趨勢。同時,磷的初始質量濃度越小溶解度越低,這是由于過度稀釋蛋液會造成蛋白質水合膜的破壞,蛋白質可溶性降低[31]。溶解度的變化與圖2結果接近,且溫度較低時全蛋液中溶解度較高(P<0.05)。
2.3 LDH添加量對吸附量及溶解度的影響
圖5、6分別為LDH的添加量對全蛋液中磷的吸附量和溶解度的影響,隨著添加量的增加,LDH對全蛋液中磷的吸附量先增加后降低,溶解度逐漸降低。當LDH的添加量在2.5~10 g/L范圍內,溫度對LDH吸附效果影響顯著(P<0.05),且吸附溫度越高其磷酸根吸附量越高。當添加量為10 g/L時,各溫度下磷的吸附量均達到最高值。LDH的添加量超過10 g/L后,其對全蛋液中磷的吸附量顯著下降,但此時溫度對吸附效果影響不顯著,各溫度下LDH的吸附量無明顯差異(P>0.05)。這可能是由于當添加量較大時,造成LDH的聚集現象,減小了吸附質與LDH的接觸面積,降低其吸附效果。實驗中發現添加量達到10 g/L時,出現結塊現象,需通過攪拌輔助其分散于全蛋液體系中。陳蘅莉等[16]也研究了吸附劑添加量對吸附量的影響,其研究也表明添加量較大時,可得到較好的吸附效果。本實驗還研究了全蛋液中溶解度的變化,LDH添加量對溶解度的影響與圖2結果相似,隨著添加量的增加溶解度逐漸下降。這可能是大量的LDH加入到全蛋液中,會造成全蛋液體系黏度增加,隨著攪拌的進行,全蛋液中蛋白質等組分形成絮狀物,可溶性降低[39]。與圖2、4結論相似,溫度對全蛋液中溶解度影響顯著(P<0.05),溫度較低時全蛋液中溶解度相對較高。
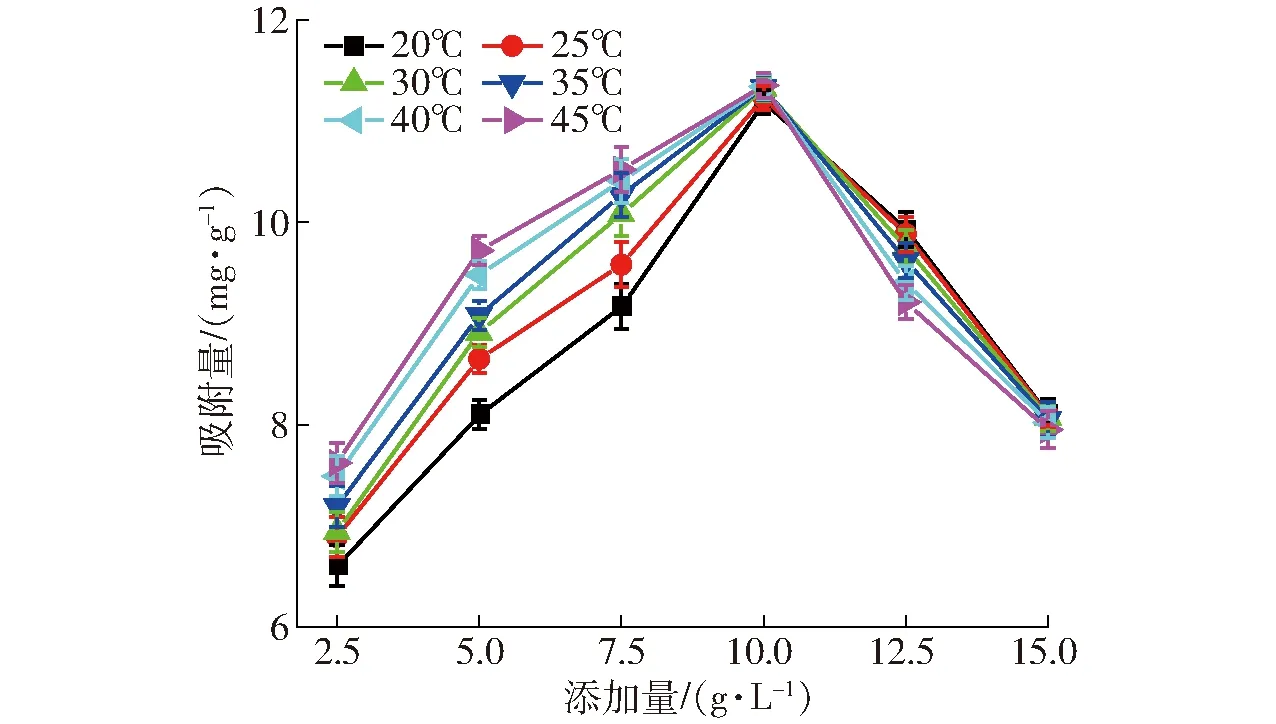
圖5 LDH添加量對全蛋液中磷吸附量的影響Fig.5 Effect of LDH addition on quantity of adsorption of phosphate in whole egg liquid
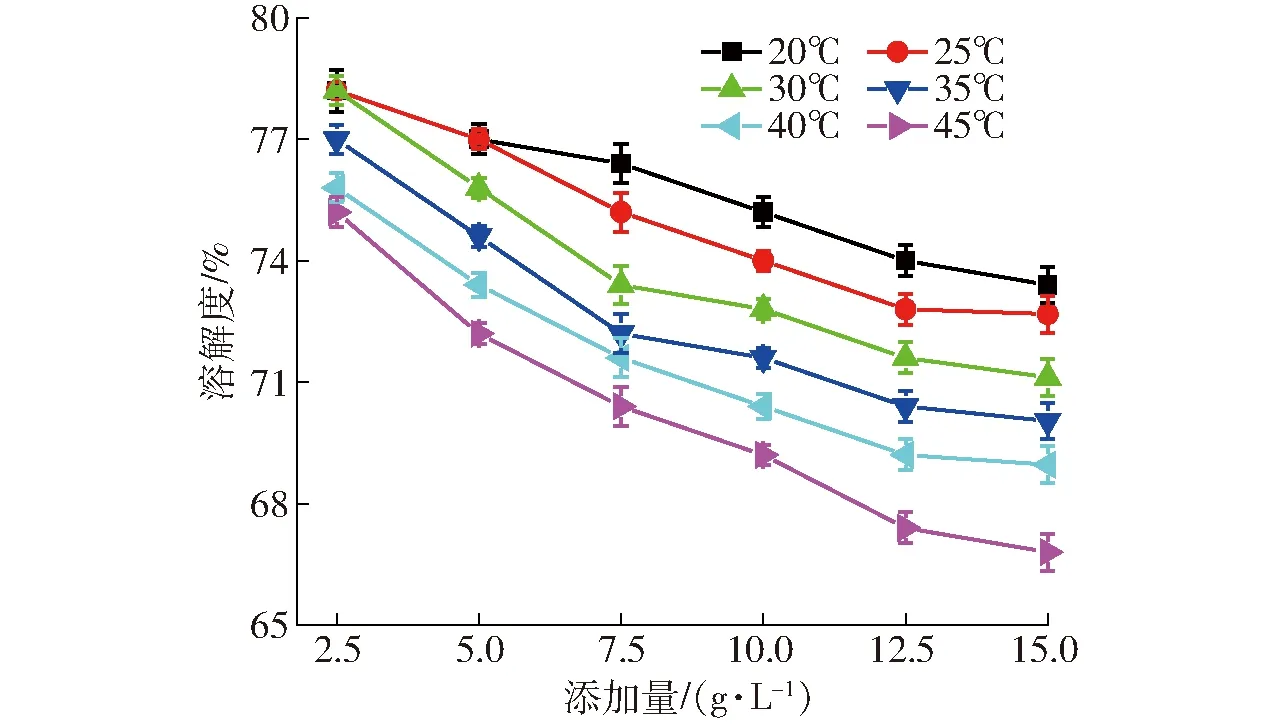
圖6 LDH添加量對全蛋液溶解度的影響Fig.6 Effect of LDH addition on solubility in whole egg liquid
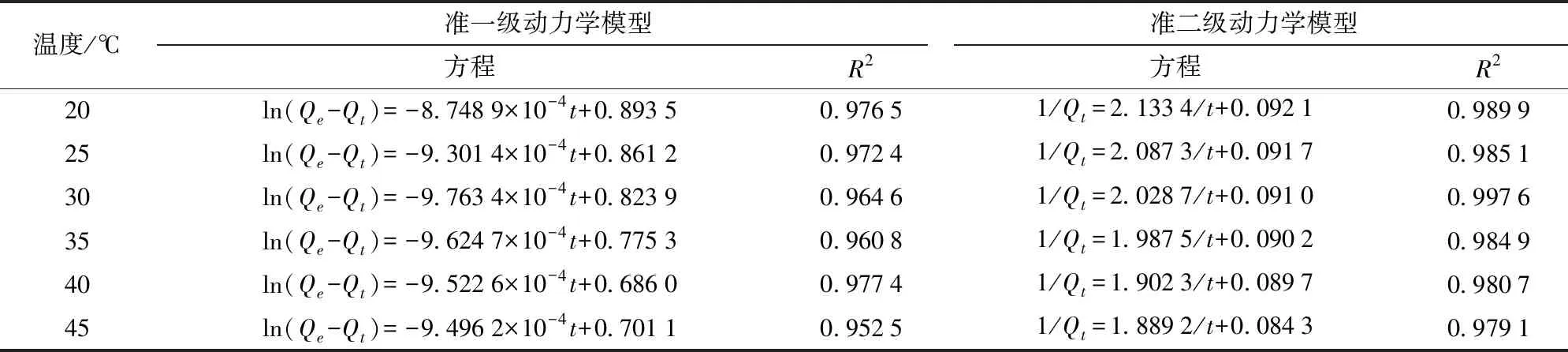
2.4 LDH吸附等溫式、吸附熱力學及吸附動力學
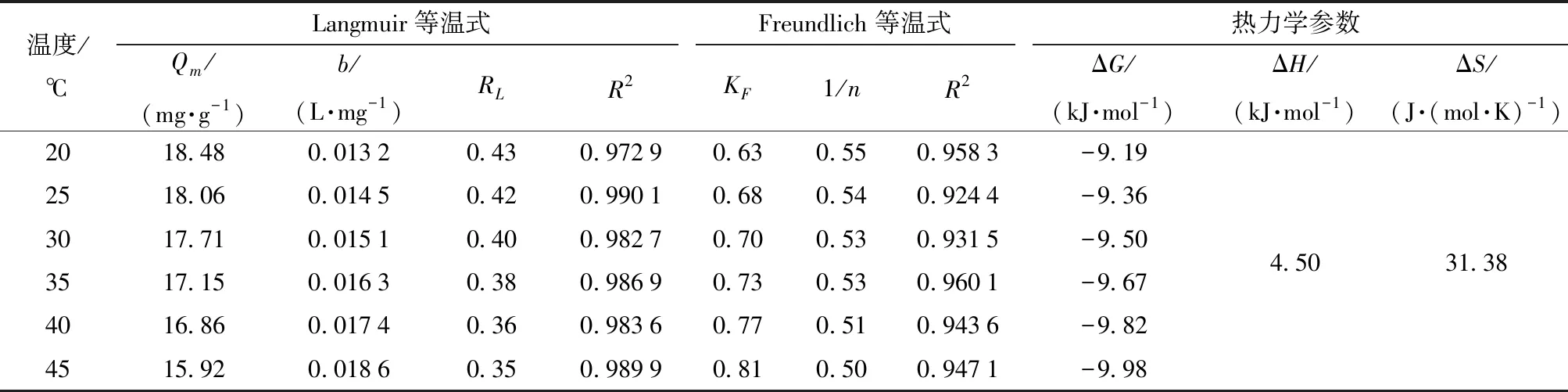
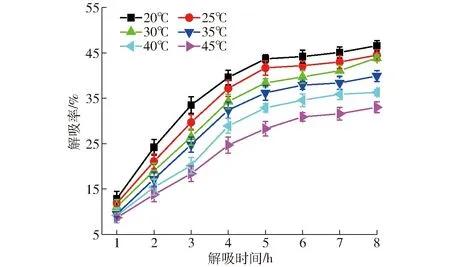
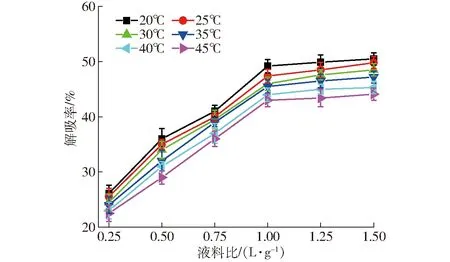
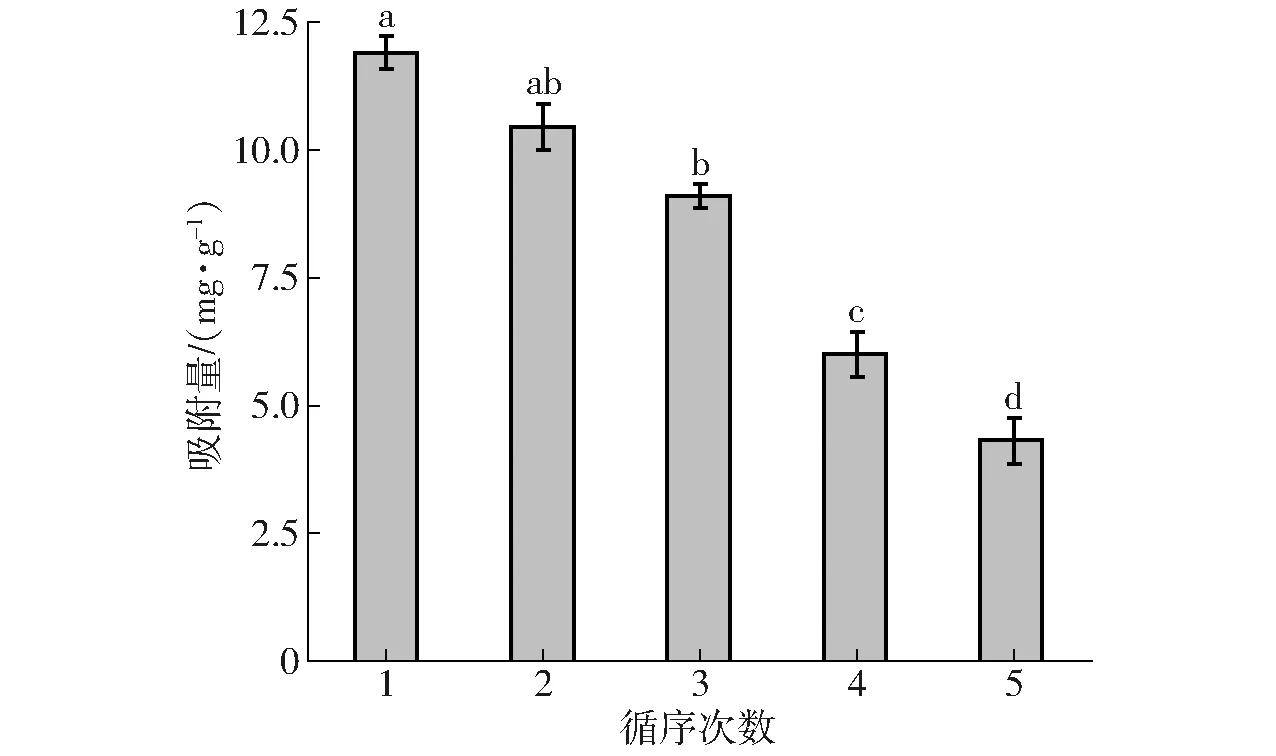
Langmuir吸附等溫式的前提條件是吸附表面均勻并且為單分子層,而Freundlich吸附等溫式應用于非均勻吸附劑的多層吸附[40]。Langmuir吸附等溫式中根據RL的值判斷吸附過程是否良好,0 圖7、8為LDH解吸實驗結果,由實驗數據可知吸附溫度對NaCl解吸磷的影響顯著(P<0.05),吸附溫度越低,LDH上吸附的磷的解吸效果越好,具有更大的解吸率。這是由于較低溫度吸附時,磷與LDH結合方式主要為物理結合,磷吸附于LDH層板表面,結合力較低,易于解吸。吸附溫度越高,化學吸附程度越大,磷與LDH層間鎂離子、鋁離子的結合越多,解吸難度增大。圖7中隨著解吸時間的增加,磷酸根解吸率逐漸增加(P<0.05),解吸5 h后解吸率增長緩慢。李克超等[47]采用LDH對棉酚進行解吸的研究中,解吸時間長達12 h。本實驗達到解吸最大的時間相對較短,這可能與吸附質的性質有關。相對于棉酚,磷離子更易于被NaCl溶液解吸。通過李克超的研究可知棉酚在解吸的同時發生降解,重新吸附于LDH表面,所以需要更長的解吸時間。如圖8所示,隨著解吸液的增加,解吸率逐漸增加(P<0.05),各溫度下初始增長呈線性,吸附溫度對解吸率影響顯著(P<0.05),溫度越低解吸效果越好。當液料比超過1.00 L/g后解吸率增長緩慢。此時,LDH中結合較弱的磷都已脫除,繼續增加解吸液用量,不能達到很好的解吸效果又會造成試劑的浪費。因此,最佳的解吸條件為:1 g LDH采用1 L NaCl解吸液進行磷解吸,解吸時間為5 h。 表1 LDH對全蛋液中磷的吸附等溫式及熱力學參數Tab.1 Adsorption isotherm and thermodynamic parameters of phosphorus in whole egg liquid by LDH 表2 LDH對全蛋液中磷的吸附動力學模型參數Tab.2 Adsorption kinetic model parameters of phosphate in whole egg liquid by LDH 圖7 LDH解吸時間對磷解吸率的影響Fig.7 Effect of desorption time of LDH on rate of desorption of phosphate 圖8 液料比對磷解吸率的影響Fig.8 Effect of ratio of desorption liquid to LDH on rate of desorption of phosphate 圖9 LDH循環次數對全蛋液中磷吸附量的影響Fig.9 Effect of cycle times of LDH on quantity of adsorption of phosphate in whole egg liquid 為探究LDH的可再生性,對LDH進行循環使用,經過NaCl解吸后的LDH進行500℃焙燒4 h,冷卻后使用。焙燒溫度為500℃時,可以將影響磷酸根吸附的層間陰離子釋放出來,增加材料的比表面積,同時焙燒產物與水混合后可以恢復原有結構[19]。將LDH焙燒產物應用于全蛋液吸附實驗中,其對磷的吸附效果如圖9所示。隨著使用次數的增加,LDH對磷的吸附量逐漸降低。前2次對磷的吸附量差異不顯著,第3次使用時降低為10 mg/g以下,在第4次和第5次使用時吸附量降低到6 mg/g以下。在循環使用中,采用高溫處理水滑石,LDH片層發生斷裂、移位和重排[17],形成大量微孔結構,利于物理吸附的進行。相似地,殷實等[48]研究中采用微波預處理和傳統焙燒加熱相結合的方式處理生物炭,形成豐富的微孔和介孔,形成了多級孔道結構。本實驗進行多次循環使用時,LDH表面的吸附位點被占用,對陰離子磷的吸附效果降低。目前,關于吸附劑循環使用的研究較少,李克超等[47]對LDH進行了循環利用,在前3次吸附棉酚的效果較好。一定次數的循環使用,可以較大程度地發揮吸附劑的吸附作用。本實驗中LDH最佳使用次數為2次,使用3次也基本滿足吸附要求。 雞蛋中氨基酸含量豐富,且蛋白模式與人體的蛋白模式相似,可以被人體全面吸收[49]。實驗中測定了各溫度下(20~45℃)磷吸附處理對全蛋液中氨基酸的影響,進而研究脫磷對蛋白質營養性的影響,如表3所示。實驗結果表明氨基酸中絲氨酸含量有一定程度的降低,這是由于雞蛋蛋白質中含有高度磷酸化的絲氨酸,特別是Ser128~Ser141之間,有14個絲氨酸殘基連續排列[50]。王芳[13]的研究中得到了相同的結論,雞蛋蛋白質脫除的磷主要來自于絲氨酸,脫磷對側鏈含磷酸基團的氨基酸影響顯著。根據FAO/WHO提出的優蛋白質組成條件,8種必需氨基酸占總氨基酸質量分數應在40%以上,必需氨基酸與非必需氨基酸質量百分比應超過60%。由表3可知,采用LDH進行磷吸附后全蛋液中必需氨基酸占總氨基酸質量分數始終大于40%,必需氨基酸與非必需氨基酸質量百分比也一直高于60%,表明LDH脫磷對全蛋液中蛋白質營養性的影響較小,這也對應了圖2、4、6中溶解度的結果。綜上可知,采用LDH進行脫磷的同時可以保持全蛋液中蛋白質的營養性,適用于低磷液蛋制品的開發。 表3 全蛋液及脫磷全蛋液的氨基酸質量分數Tab.3 Analysis of amino acids in whole egg liquid and dephosphorization whole egg liquid % (1)采用LDH進行全蛋液中磷的吸附,最佳吸附條件為:吸附時間6 h,磷初始質量濃度125 mg/L,LDH添加量10 g/L。 (2)實驗中LDH的最大吸附量超過10 mg/g,同時溶解度下降幅度在10%以內;Langmuir等溫式、Freundlich等溫式、準一級動力學和準二級動力學模型均可表征LDH對磷的吸附,Langmuir等溫式和準二級動力學模型擬合度較高,尤其在25℃和30℃吸附溫度時擬合效果最佳。 (3)ΔS為31.38 J/(mol·K),ΔH為4.50 kJ/mol,ΔG小于-9 kJ/mol,在溫度20~45℃范圍下均能自發反應且為吸熱反應。 (4)解吸實驗中,最佳條件為解吸時間5 h,液料比為1.00 L/g。循環利用時,LDH最佳使用次數為2次。 (5)脫磷后全蛋液必需氨基酸占總氨基酸的質量分數大于40%,必需氨基酸與非必需氨基酸的質量百分比大于60%,LDH脫磷對蛋白質營養性的影響較小。 (6)LDH適用于全蛋液中磷的去除,其對磷的吸附效果良好且可保持蛋白質的營養性,吸附過程簡單又可以進行重復使用,有利于低磷全蛋液的工業化開發。2.5 LDH的解吸特性
2.6 LDH的循環使用
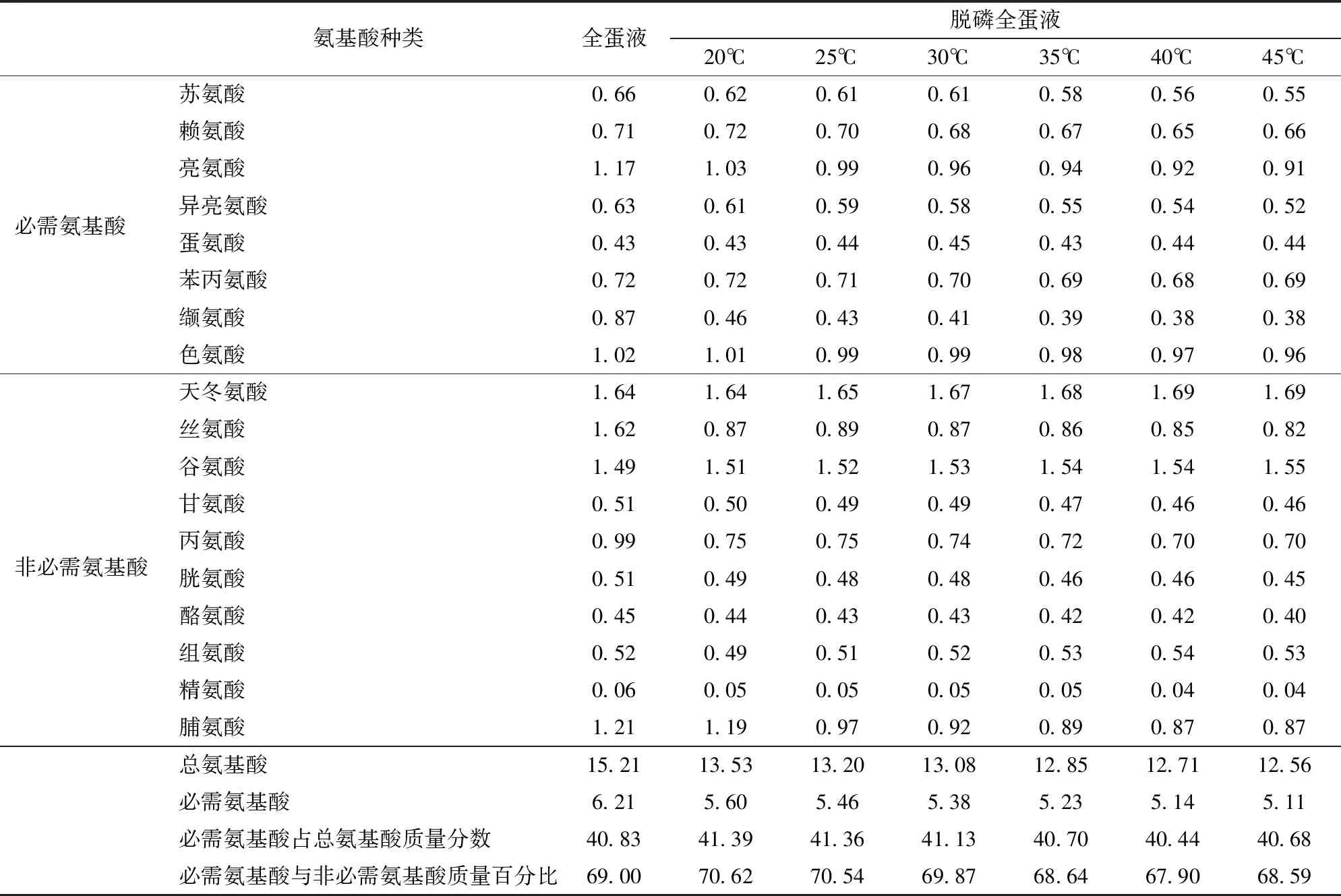
2.7 對氨基酸含量的影響
3 結論

