高分辨率磁共振指導下的孤立皮質下梗死的CISS分型及相關臨床研究
陳蓓蕾, 李 威, 楊 柳, 于海龍, 葉 靖, 王 鈺
孤立皮質下梗死(Single subcortical infarction,SSI)通常是指在穿支動脈供血區域發生的,位于大腦半球深部的梗死病灶,包括半卵圓中心、放射冠、基底節、丘腦、腦干等部位,病灶直徑通常小于20 mm[1]。以往認為,孤立皮質下梗死是由于小穿支動脈的脂質玻璃樣變造成的,然而近來研究發現,載體動脈動脈粥樣硬化阻塞穿支動脈口,導致穿支動脈閉塞或狹窄,也可導致孤立皮質下梗死[2]。根據CISS(Chinese ischemic stroke subclassification)分型,載體動脈病變導致的孤立皮質下梗死屬于大動脈粥樣硬化型腦梗死,但是根據目前常用的TOAST分類標準,往往會將該類患者歸類為小血管病型甚至不明原因型[3],從而無法對患者的病因和發病機制進行準確的評估。高分辨磁共振(High Resolution Magnetic Resonance Imaging,HRMRI)是利用磁共振原理抑制血管內流動血液信號獲取血管壁等靜態組織圖像的一種成像方法,可以更準確的提供腦梗死責任血管壁和動脈粥樣硬化斑塊成分的信息。HRMRI已經被廣泛應用于顱內動脈壁的分析,我們采用該技術,分析不同卒中亞型的孤立皮質下梗死患者的相關危險因素及預后,從而有益于制定個體化診療方案。
1 對象和方法
1.1 研究對象 連續納入2015年1月~2018年4月江蘇省蘇北人民醫院符合孤立皮質下梗死的患者共78例。納入標準:(1)年齡18~90歲;(2)發病72 h內的急性腦梗死患者;(3)頭部CT排除出血;(4)DWI提示符合孤立皮質下梗死。排除標準:(1)多發性腦梗死(2)腦出血(3)腦炎(4)多發性硬化患者。
1.2 方法
1.2.1 一般臨床資料 入院時采集患者的基線資料,包括年齡、性別、高血壓、糖尿病、心房顫動、吸煙史、飲酒史、空腹血糖、糖化血紅蛋白、血脂、血壓(舒張壓和收縮壓)、NIHSS評分等。入院后完善心電圖/動態心電圖,頸部血管彩超、顱內多普勒血流圖/頭頸CTA檢查。
1.2.2 預后和隨訪 起病3 d對患者進行NIHSS評分評估,早期神經系統功能惡化(Early neurological deterioration,END)被定義為在72 h內NIHSS的運動部分評分增加≥2分[4]。3 m后進行隨訪,行NIHSS評分及改良Rankin量表評分(mRS評分),評估患者的遠期預后。
1.3 MRI檢查 對入組患者行頭部MRI掃描(包括T1、T2、DWI、FLAIR等序列)、三維時間飛躍法磁共振血管成像(3D TOF Magnetic Resonance Angiography,3D TOF MRA)、高分辨率磁共振 (high resolution magnetic resonance imaging,HRMRI)血管壁分析、動脈自旋標記技術(arterial spin labeling,ASL)、磁敏感成像(susceptibility weighted imaging,SWI)等檢查項目。腦梗死病灶大小定義為DWI所顯示腦梗死病灶面積最大層面的病灶直徑;根據Pullicino公式,梗死病灶體積=長×寬×MRI掃面陽性層數×π/6,計算三次取平均值[5]。
1.4 CISS分型標準 (1)大動脈粥樣硬化(Large artery atherosclerosis,LAA):①對于除了穿支動脈區孤立梗死以外的其他任何類型梗死灶,有梗死病灶相對應的顱內或顱外大動脈粥樣硬化證據(易損斑塊或狹窄≥50%);②對于穿支動脈區孤立梗死灶類型,以下情形也歸到此類:其高分辨率磁共振(HRMRI)提示載體動脈有粥樣硬化斑塊或血管檢查(TCD、MRA、CTA 或DSA)提示任何程度的粥樣硬化性狹窄;③需排除心源性卒中;④排除其他可能的病因。(2)穿支動脈疾病(Penetrating artery disease,PAD):①與臨床癥狀相吻合的發生在穿支動脈區的急性孤立梗死灶,不考慮梗死灶大小;②高分辨率磁共振(HRMRI)載體動脈無粥樣硬化斑塊或血管檢查(TCD、MRA、CTA 或DSA)未發現任何程度狹窄;③同側近端顱內或顱外動脈有易損斑塊或>50%的狹窄,孤立穿支動脈急性梗死灶歸類到不明原因(多病因);④需排除心源性卒中;⑤排除其他可能的病因[6]。
1.5 近端孤立皮質下梗死(proximal single subcortical infarction,pSSI)和遠端孤立皮質下梗死(distal single subcortical infarction,dSSI)的標準 根據病灶位置與動脈主干(大腦中動脈或基底動脈)的相對關系,將pSSI定義為梗死病灶位于動脈主干的穿支動脈供血的近端區域,即延伸至主干分支處;dSSI定義為梗死病灶位于動脈主干的穿支動脈供血的遠端區域,即未延伸至主干分支處[7]。

2 結 果
共連續入組78例患者,結合高分辨率磁共振,根據CISS分型標準進行分型,其中大動脈粥樣硬化型46例(見圖1~圖6),穿支動脈型30例(見圖7~圖12),心源性栓塞型1例,其他原因型1例。
2.1 不同卒中分型患者基線資料的比較 單因素分析顯示,大動脈粥樣硬化型孤立皮質下梗死患者中,高齡(P=0.002)、高血壓(P=0.019)患者的比例以及脂蛋白a(P=0.033)、糖化血紅蛋白(P=0.049)水平,均高于穿支動脈型孤立皮質下梗死患者,結果具有統計學意義(見表1)。
2.2 不同卒中分型患者的多因素分析 多因素回歸分析顯示,年齡與大動脈粥樣硬化型腦梗死患者孤立性皮質下梗死的發生獨立相關(P=0.021),差異具有統計學意義(見表2)。
2.3 不同卒中分型患者影像學特點比較 大動脈粥樣硬化型與穿支動脈型孤立皮質下梗死患者的病灶大小(P=0.685)及病灶體積(P=0.867)均無明顯統計學差異(見表3)。
2.4 不同病因分型和病灶部位的關系 大動脈粥樣硬化型與穿支動脈型孤立皮質下梗死患者,其病灶部位在兩組間無明顯統計學差異(見表4)。
2.5 不同卒中分型患者預后的比較 大動脈粥樣硬化型孤立皮質下梗死的患者在起病早期(72 h)更容易出現神經系統癥狀的進展(P=0.003),差異具有統計學意義;而兩組的遠期3 m臨床預后(mRS評分)無明顯統計學意義(見表5)。



圖1 DWI提示左側放射冠急性腦梗死,其病灶直徑26.50 mm; 圖2 MRA提示左側大腦中動脈M段閉塞; 圖3 HRMRI提示左側大腦中動脈粥樣硬化斑塊,阻塞管腔,血管閉塞。根據CISS分型標準也歸類于大動脈粥樣硬化型



圖4 DWI提示左側放射冠區孤立皮質下梗死,位于左側大腦中動脈穿支供血區,病灶直徑14.31 mm; 圖5 MRA未見左側大腦中動脈狹窄; 圖6 HRMRI提示左側大腦中動脈存在新月形動脈粥樣硬化斑塊,并且阻塞穿支動脈。根據CISS分型標準歸類于大動脈粥樣硬化型

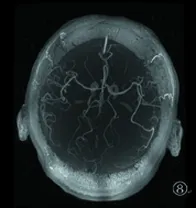

圖7 DWI提示右側基底節區孤立皮質下梗死,病灶直徑12.75 mm; 圖8 MRA未見明顯異常; 圖9 HRMRI未發現載體動脈粥樣硬化斑塊。根據CISS分型標準歸類于穿支動脈疾病型



圖10 DWI提示左側基底節區孤立皮質下梗死,病灶直徑37.73 mm; 圖11 MRA未提示血管狹窄; 圖12 HRMRI無載體動脈粥樣硬化斑塊,可見其大腦中動脈穿支動脈存在動脈粥樣硬化,內膜增厚。該患者CTA排除顱外血管狹窄,根據CISS分型標準也應歸類于穿支動脈型

表1 不同卒中分型患者基線資料

表2 不同卒中分型患者的多因素分析

表3 不同卒中分型患者影像學特點

表4 不同病因分型和病灶部位的關系

表5 不同卒中分型患者的預后
3 討 論
孤立皮質下梗死是缺血性腦卒中的一個重要類型,是指穿支動脈供血區域的腦白質深部的孤立梗死病灶,通常被認為是由于小穿支動脈動脈病變所致,但近來研究發現,其病因也可以是大動脈病變[2]。目前國際公認的卒中分型方法為TOAST(Trial of Org 10 172 in acute stroke treatment)分型,根據TOAST分型標準,大動脈粥樣硬化型腦梗死要求存在由于動脈粥樣硬化所致的頸動脈、大腦前動脈、大腦中動脈、大腦后動脈、椎-基底動脈的狹窄程度大于等于50%,而小血管閉塞型腦梗死則要求其病灶直徑小于15 mm[8]。因此,存在輕度(<50%)載體動脈狹窄的SSIs,以及病灶直徑大于15 mm的SSIs,可能會分別被歸類為小血管疾病和隱源性卒中。近年來HRMRI的研究顯示,部分顱內血管有輕度狹窄,甚至在MRA上沒有狹窄,但在HRMRI上有明顯的斑塊的血管,可以由于其分支閉塞導致SSIs,而且這些血管的病變與動脈粥樣硬化有關,因此應該被歸類為大動脈粥樣硬化型[3]。CISS分型則不將血管狹窄程度或病灶大小作為卒中分型的標準,而是通過病因或發病機制對卒中進行分型,并且提出了穿支動脈疾病的概念,將動脈粥樣硬化正式引入到穿支動脈的病因診斷中。通過血管影像學,其將大動脈粥樣硬化型腦梗死的發病機制區分為:(1)載體動脈斑塊或血栓堵塞穿支動脈;(2)動脈到動脈栓塞;(3)低灌注或栓子清除下降或混合型。根據動脈粥樣硬化部位來區分大動脈粥樣硬化型和穿支動脈型腦梗死[6]。針對病灶直徑通常較小的孤立皮質下梗死患者來說,這種分型標準可能能更加準確的從病因學上對其進行分型。HRMRI與傳統MRI相比,可以使幾毫米的動脈壁可視化[9],并能夠分析顱內血管斑塊位置及性質,從而比一般影像學手段如CT及超聲等更靈敏的發現血管病變,確認孤立皮質下梗死的責任血管,并更加準確的對孤立皮質下梗死進行卒中分型。本研究通過HRMRI,對患者責任血管血管壁進行分析,發現孤立皮質下梗死患者的CISS卒中分型,主要是以是大動脈粥樣硬化型和穿支動脈病變型,少量患者為心源性栓塞或其他類型。
本研究針對大動脈粥樣硬化型和穿支動脈型的孤立皮質下梗死患者,進行了相關危險因素分析,并比較兩種類型孤立皮質下梗死患者的預后。研究發現,在單因素分析中,大動脈粥樣硬化型孤立皮質下梗死的患者中,存在更多高齡及高血壓的患者,并且其脂蛋白a、糖化血紅蛋白水平均高于穿支動脈型孤立皮質下梗死患者。而多因素分析顯示,年齡是大動脈粥樣硬化型孤立性皮質下梗死的獨立危險因素。Choi等研究發現,載體動脈病變導致的孤立皮質下梗死與高齡和其他非顱內血管的動脈粥樣硬化相關[10]。這與我們的研究結果相符。以往研究發現,近端孤立皮質下梗死(pSSI)和遠端孤立皮質下梗死(dSSI)的臨床特點及預后存在一定差異,通常pSSI的梗死體積較大,入院時NIHSS評分也較高,dSS 1 y內復發或惡化風險較低,預后較好[11,12]。此外,有研究指出,大腦中動脈(MCA)粥樣硬化更易導致孤立皮質下梗死進展或預后不佳[13,14],但也有研究發現卒中進展可能與梗死體積相關,而與是否存在MCA動脈粥樣硬化無明顯關聯[15]。本研究主要是根據病變血管進行分組研究,研究結果并未提示病灶大小及病灶體積在兩組間存在顯著差異,并且未提示大動脈粥樣硬化型孤立皮質下梗死患者更多是dSSI。我們發現大動脈粥樣硬化型孤立皮質下梗死的患者在起病早期(72 h)更容易出現臨床癥狀的進展,即神經系統癥狀的加重,而兩組的3 m臨床預后無明顯統計學意義,從而提示發病72 h內的卒中進展可能與其病因及病變血管部位相關,大動脈病變導致的孤立皮質下梗死更容易表現為早期進展型腦卒中。
本研究通過高分辨率磁共振血管壁成像,根據血管病變部位對孤立皮質下梗死進行了分型,能從病因上更準確的將不同類型孤立皮質下梗死進行分組;并分析了不同卒中分型的相關危險因素,結果顯示高齡是大動脈粥樣硬化型孤立性皮質下梗死的獨立危險因素;大動脈粥樣硬化型梗死患者早期更容易出現卒中進展,但兩者的遠期預后并沒有明顯的差異。該研究的結論對孤立皮質下梗死患者的病因及早期進展的預測有一定的臨床指導意義。但本研究為小樣本單中心研究,樣本量較少,研究結果存在一定的局限性。擴充樣本量或進行多中心研究,可能得出更準確及更有意義的研究結果。

