Child-Pugh C級患者伏立康唑血藥濃度監測結果分析
趙慶國,任秋霞,杜春輝,王艷紅(.中國人民解放軍30醫院藥學部,北京 00039;.山東大學附屬山東省腫瘤醫院藥學部,山東 濟南 507)
伏立康唑是一種新型合成的三唑類抗真菌藥物,抗菌譜廣,抗菌效力強,是治療侵襲性真菌感染的首選藥物。伏立康唑主要通過肝臟CYP450同工酶CYP2C19、CYP2C9和CYP3A4代謝,CYP2C19的基因多態性及藥物代謝的特征是伏立康唑個體差異的主要原因[1-2]。
血藥濃度監測是實現伏立康唑個體化給藥的重要手段,也是提高伏立康唑臨床療效和降低其不良反應發生率的重要保證。近年來,伏立康唑血藥濃度監測的必要性已得到確認[3]。臨床上對伏立康唑血藥濃度的監測也越來越重視,HPLC-UV、GC-MS、UPLCMS等各種方法被開發以監測伏立康唑血藥濃度[4-7]。然而,目前尚無Child-Pugh評分C級的患者應用伏立康唑的用藥研究,同時根據血藥濃度監測結果調整伏立康唑給藥方案的研究也甚少。本研究從應用伏立康唑并進行血藥濃度監測的患者中篩選出117例嚴重肝功能不全的患者,探討Child-Pugh C級患者用藥及根據血藥濃度監測進行伏立康唑劑量調整的經驗,旨為臨床肝損傷嚴重、Child-Pugh C級患者提供合理使用伏立康唑的必要依據。
1 研究對象與方法
1.1 研究對象
收集整理我院2014年7月- 2018年1月使用伏立康唑并進行血藥濃度監測的患者,查閱病歷記錄基本資料及藥物應用情況。排除Child-Pugh評分未達C級以及使用伏立康唑未達穩態或采血期間有血液凈化的患者。為獲得穩態谷濃度結果,本實驗所有患者的采血時間均在接受靜注或口服伏立康唑負荷劑量,維持劑量2次或大于2次之后。所有患者均為簽署了知情同意書的住院患者。伏立康唑劑型分為注射劑和片劑兩種,未區分不同商品名稱。
1.2 方法
1.2.1 血藥濃度測定方法 采用Agilent 1290超高效液相色譜儀進行測定,色譜柱為Zorbax SB-C18柱(2.1 mm×100 mm,1.8 μm),流動相為乙腈-0.05%三氟乙酸水溶液(40∶60,v/v),流速0.2 mL·min-1,柱溫30 ℃,檢測波長256 nm[8]。
1.2.2 統計分析方法 采用SPSS統計軟件進行分析,計量資料以(均數±標準差)表示,計量資料兩組間比較采用t檢驗,以P< 0.05為差異有統計學意義。
2 結果
2.1 患者基本資料
本研究共納入患者117例,其中男性95例(81.2%),女性22例(18.8%);平均年齡50.9歲,44歲以下青年患者37例(31.6%),45 ~ 59歲中年患者47例(40.2%),60歲以上老年患者33例(28.2%)。117例患者中大部分來自于我院急診重癥監護室,另外還包括肝衰科、移植科以及感染科等其他科室。患者均為肝硬化患者且Child-Pugh評分為C級,包括乙型肝炎肝硬化,丙型肝炎肝硬化,膽汁淤積性肝硬化,酒精性肝硬化,藥物性肝硬化等。
2.2 血藥濃度分布情況
本研究分析的117例患者所測血藥濃度均為穩態谷濃度值。根據文獻報道[9]的有效濃度范圍(1.0 ~5.5 μg·mL-1)及給予的維持劑量進行分析,濃度分布情況詳見表1。
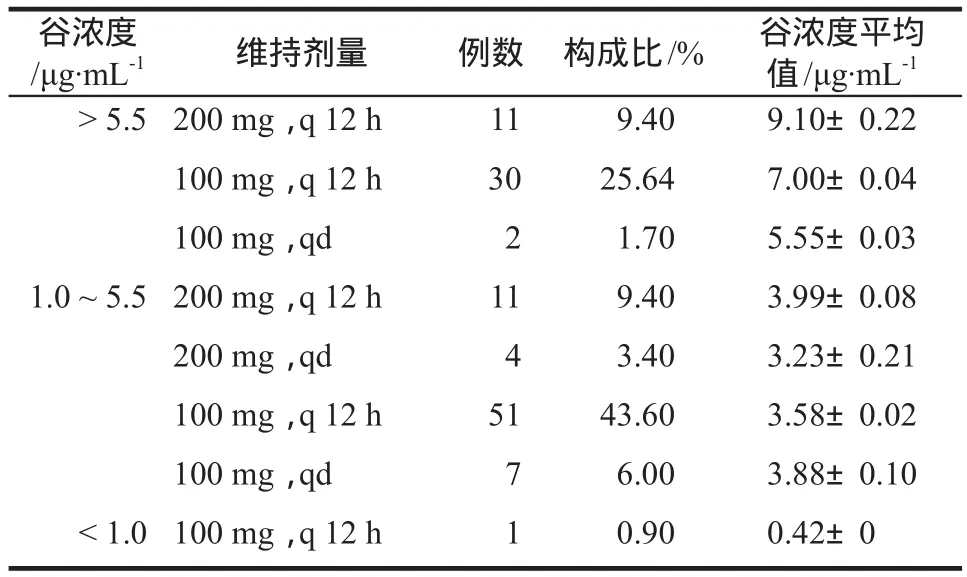
表1 伏立康唑血藥濃度分布情況Tab 1 Distribution of voriconazole plasma concentrations
117例患者中應用維持劑量200 mg,q 12 h的22例,此給藥方案高于推薦濃度上限占比50%;維持劑量100 mg,q 12 h的82例,高于推薦濃度上限的占比36.58%。維持劑量200 mg,qd和100 mg,qd的給藥方案較少僅13例,其中有2例略高于推薦濃度上限。由圖1可知,維持劑量為200 mg,q 12 h的患者伏立康唑血藥濃度往往嚴重偏高,維持劑量100 mg,q 12 h則具有更高的安全性。但同時需要注意的是對于嚴重肝功能不全的患者而言,維持劑量100 mg,q 12 h雖然大部分患者在推薦濃度范圍內(62.20%),但仍有37.80%的患者血藥濃度未在推薦濃度范圍內,需要及時監測血藥濃度進行給藥方案調整,以減少不良反應發生率,確保藥物的安全性及有效性。
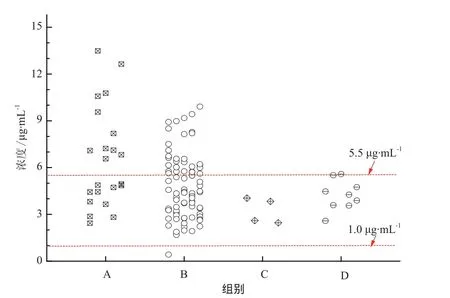
圖1 不同維持劑量患者伏立康唑血藥濃度分布情況A - 200 mg,q 12 h;B - 100 mg,q 12 h;C - 200 mg,qd;D - 100 mg,qdFig 1 Distribution of voriconazole plasma concentration in patients with different maintenance doses A - 200 mg,q 12 h; B - 100 mg,q 12 h; C - 200 mg,qd; D - 100 mg,qd
2.3 性別
本次納入的病例中男性95例,血藥濃度平均值為(5.13±0.03)μg·mL-1;女性22例,女性組血藥濃度平均值為(4.60±0.09)μg·mL-1,將男性組血藥濃度結果與女性組血藥濃度結果分析比較發現無統計學意義(P= 0.35)。
2.4 年齡
將患者按年齡分為青年組、中年組和老年組,并進行血藥濃度結果比較分析(見表2)。將青年組、中年組和老年組伏立康唑血藥濃度平均值進行兩兩比較發現,各組之間無統計學意義(P> 0.05)。

表2 不同年齡組血藥濃度比較Tab 2 Comparison of plasma concentrations between different age groups
2.5 體質量
117例患者按體質量分為40 ~ 60 kg組、60 ~ 80 kg組、80 ~ 100 kg組,各組伏立康唑穩態血藥谷濃度測定結果見表3。結果顯示隨著體質量增加,伏立康唑血藥濃度呈下降趨勢,與孟冬梅等[10]研究結果相一致。將40 ~ 60 kg、60 ~ 80 kg及80 ~ 100 kg組血藥濃度結果進行兩兩比較,結果表明60 ~ 80 kg組與80 ~100 kg組有統計學差異(P= 0.04)。
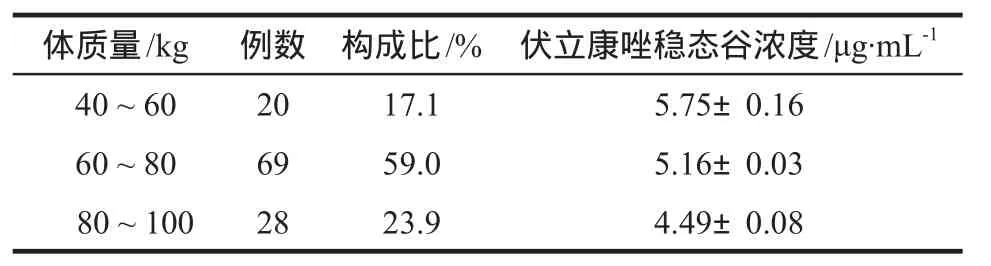
表3 不同體質量組血藥濃度比較Tab 3 Comparison of plasma concentrations between different body weight groups
2.6 給藥途徑
納入的患者中65例為靜脈給藥(55.6%);52例為口服給藥(44.4%)。將口服組與靜脈組血藥濃度比較分析發現,靜脈組伏立康唑谷濃度平均值為(5.05±0.03)μg·mL-1,口服組伏立康唑谷濃度平均值為(5.00±0.05)μg·mL,兩組比較無統計學意義(P= 0.90)。
2.7 合并用藥
伏立康唑不僅是CYP2C19、CYP2C9和CYP3A4的底物也是其抑制劑,而體內多數藥物由這幾種酶代謝,因此伏立康唑與很多藥物存在潛在的相互作用,包括利福平、苯妥英、卡馬西平、大環內酯類及質子泵抑制劑等。本研究納入的117例患者中除了質子泵抑制劑,未使用其他與伏立康唑具有潛在相互作用的藥物。117例患者使用伏立康唑的同時使用質子泵抑制劑的90例,伏立康唑平均血藥濃度為(5.69±0.04)μg·mL-1,其中使用蘭索拉唑的70例,奧美拉唑10例,雷貝拉唑6例,泮托拉唑4例;未使用質子泵抑制劑的27例,伏立康唑平均血藥濃度為(4.53±0.08)μg·mL-1。對同時使用質子泵抑制劑和未使用質子泵抑制劑的兩組進行分析,結果顯示兩組比較具有統計學意義(P= 0.04)。
3 討論
對于肝損傷嚴重、Child-Pugh評分C級的患者,此類患者按常規劑量給藥很容易造成患者體內藥物蓄積,導致伏立康唑發生谷濃度高于推薦血藥濃度上限,不良反應發生的風險增大。目前尚未有此類患者應用伏立康唑安全性及有效性的相關研究數據,因此根據血藥濃度監測結果調整伏立康唑的給藥劑量,總結對于肝損傷嚴重、Child-Pugh C級患者伏立康唑的用藥經驗尤為重要。
此類患者應考慮參照伏立康唑說明書中中度肝硬化患者(Child-Pugh B)的給藥方案(負荷劑量不變維持劑量減半),給予比Child-Pugh B級患者更低的維持劑量。對合并使用質子泵抑制劑的患者應密切監測其血藥濃度,避免因藥物相互作用而導致的伏立康唑血藥濃度過高。同時,由于個體差異在利用伏立康唑血藥濃度監測調整給藥方案過程中,不能盲目參照安全濃度范圍,必須結合臨床患者實際情況制定合理的治療方案,必要時應考慮停藥或換藥治療。
本研究納入的均為肝功能嚴重損害的患者,研究結果為該類患者伏立康唑的應用及用藥調整提供了臨床依據。不足之處是本研究僅參考了該類患者的穩態谷濃度值并沒有完整的藥代動力學數據,且研究病例只有本院患者數據具有一定的局限性。

