Keap1-Nrf2/ARE信號通路在腫瘤中的雙重作用及其與耐藥性的關系
李曉強,隋峰,王洋,趙麗鳳,李慧杰,譚余慶
中國中醫科學院 中藥研究所,北京100029
惡性腫瘤是嚴重威脅人類健康的重大致死疾病,隨著人類居住環境的惡化,惡性腫瘤的種類越來越多,隨之產生的腫瘤耐藥性等問題也越來越受到研究者的重視。Keap1-Nrf2/ARE 信號通路是機體在抵抗外來應激時最重要的內源性氧化應激通路,其誘導產生的Ⅱ相代謝酶和抗氧化酶等蛋白在保護正常細胞中發揮重要作用[1]。但與此同時,Keap1-Nrf2/ARE 信號通路對某些腫瘤細胞也表現出促進作用,而對另外某些腫瘤細胞卻表現出抑制作用,這種雙重作用使得以Keap1-Nrf2/ARE 信號通路為作用靶點的藥物研發必須得到足夠的重視。我們就Keap1-Nrf2/ARE 信號通路在腫瘤發生發展中的雙重作用及其在腫瘤耐藥性中的影響做簡要綜述,為以此信號通路為作用靶點的藥物研發提供新思路。
1 Nrf2、Keapl、ARE的基本結構
1.1 Nrf2的結構
核因子E2 相關因子2(nuclear factor E2 re?lated factor 2,Nrf2)屬于Cap-n-Collar(CNC)蛋白家族,該家族成員均具有高度保守的堿性亮氨酸拉鏈(basic leucine zipper,bZip)結構[2]。基于其保守序列,Nrf2 分為7個結構功能域(圖1),即Neh1~Neh7(Nrf2-ECH homology)[3-4]。Neh1 結 構域包含bZIP 結構,其與細胞核內小Maf 蛋白形成異源二聚體,使Nrf2 能夠識別并結合抗氧化反應元件(antioxidant response element,ARE),繼而啟動下游相關基因轉錄[5]。Neh2 結構域含有2個重要保守區域DLG和ETGE,是Nrf2與Kelch 樣環氧氯丙烷相關蛋白1(Kelch-like ECH-associated protein-1,Keap1)結合的區域,正是基于這2個區域與Keap1的相互作用,才使得Nrf2 能夠穩定存在于細胞質[6]。位于C端的Neh3 結構域對Nrf2的轉錄活性非常重要,該蛋白最后16個氨基酸殘基的缺失會完全破壞其激活報告基因和內源性基因表達的能力[7]。Neh4和Neh5 結構域是Nrf2的2個獨立激活區,它們分別與cAMP 反應元件結合蛋白(CREB)結合,并與之協同作用起到活化轉錄的作 用[8]。Neh6 包 含2個 模 序,即DSGIS和DSAPGS,是一段非依賴于Keap1 調控Nrf2 降解的結構域[9]。Neh7 是新發現的結構域,可特異性地與維甲酸X 受體α(retinoid X receptor α,RXRα)作用從而抑制Keap1-Nrf2/ARE 信號通路[3]。
1.2 Keap1的結構
Keap1 是Cullin3與泛素連接酶E3 復合物的底物結合蛋白,該復合物可識別Nrf2,也可作為細胞外源性物質和氧化應激的傳感器[10]。Keap1屬于Kelch 家族多區域阻遏蛋白,包含5個主要的功能結構域(圖1),分別為N端結構域(N-termi?nal region,NTR)、干 預 區(intervening region,IVR)、BTB(broad complex, tramtrack and Bric-a-Brac)區、雙甘氨酸重復區(double glycine repeats,DGR)和C端結構域(C-terminal region,CTR)。其中DGR 區 也叫Kelch 區,是Keap1與Nrf2的Neh2部位結合區[11]。
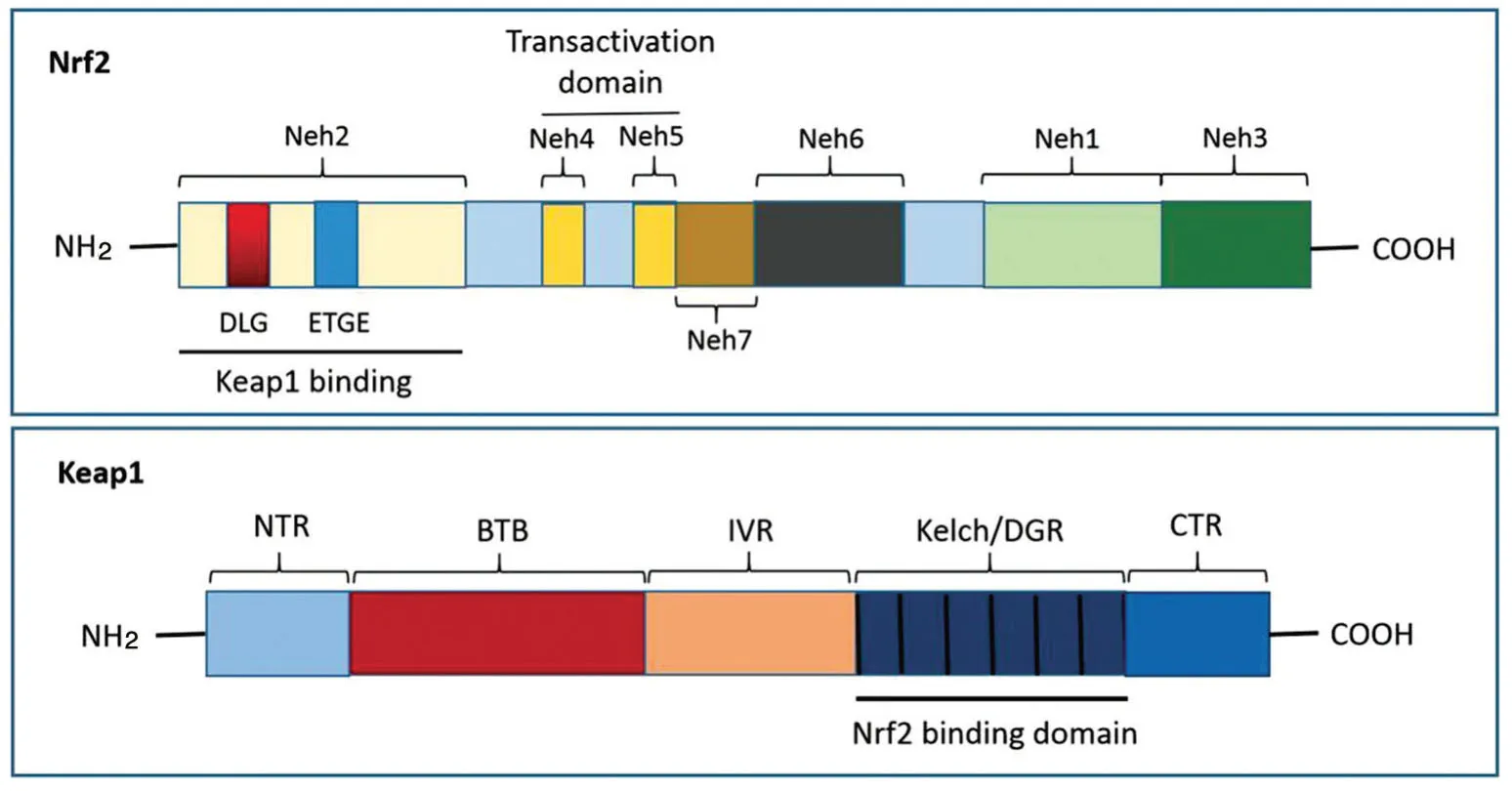
圖1 Nrf2和Keap1 結構示意圖
1.3 ARE的結構
ARE 是一種順式作用元件,核心序列為5'-(G/A)TGA(G/C)nnnGC(G/A)-3'。研究證實,Bach1和Nrf2 互相競爭結合ARE,從而調節ARE介導的基因表達[12]。
2 Keap1-Nrf2/ARE 信號通路的調控機制
在正常生理狀態下,Nrf2 通過其Neh2 結構域與負調控蛋白Keap1的Kelch 區相互作用,穩定存在于細胞質中,Nrf2 經泛素蛋白酶體途徑被降解,因此Nrf2的表達水平得以維持在較低的水平,機體處于一個氧化-抗氧化平衡的狀態。當細胞受到活性氧(ROS)或其他親核劑刺激后,Nrf2與Keap1 解偶聯,活化的Nrf2 轉運進入細胞核,與小Maf 蛋白結合成異質二聚體后與ARE 結合,激活靶基因表達,調控Ⅱ相代謝酶和抗氧化酶等蛋白的轉錄活性(圖2)[13],從而發揮抗氧化損傷作用,使細胞恢復氧化-抗氧化平衡狀態。
Keap1-Nrf2/ARE 信號通路的激活主要取決于Nrf2的激活,而Nrf2的激活主要由Keap1 介導及Nrf2 自身的磷酸化等調控。目前,由Keap1 介導的Nrf2 激活機制有一種比較流行的學說,即所謂的“鉸鏈和門閂”機制[14-15]。該機制認為以二聚體形式存在的Keap1的2個DGR 區通過與Nrf2的DLG和ETGE 結構域錨定在一起。親和力相對高的ETGE 區和親和力相對弱的DLG 區分別扮演著“鉸鏈”和“門閂”的角色。氧化應激等刺激使得Nrf2的DLG 區與Keap1的DGR 區解 離,而Nrf2的ETGE 區仍然與Keap1的DGR 區穩定結合在一起,使得Keap1-Nrf2 復合物穩定存在于細胞質;而同時新生成的Nrf2的ETGE 區由于無法和Keap1 結合,從而在細胞質中累積并陸續轉入核內與Maf蛋白結合成二聚體,進而結合ARE 促進下游相關靶基因的表達。
另外,還有一些學者認為一些蛋白激酶使Nrf2 發生磷酸化,致使其構象發生改變,從而促使Nrf2與Keap1 發生解離。例如,蛋白激酶C(PKC)可使Nrf2的Ser40 位點發生磷酸化,從而改變Nrf2的構象,避免E3 泛素化連接酶對Nrf2的識別而阻礙降解,增加其在細胞質中的含量并且增強其轉錄活性[16]。
3 Keap1-Nrf2/ARE 信號通路在腫瘤發展中的雙重作用
3.1 Keap1-Nrf2/ARE 信號通路對腫瘤的抑制作用
正常狀態下,細胞質中的Nrf2與Keap1 結合并處于活性相對抑制狀態。當用一些外源物質處理正常細胞時,引起Nrf2與Keap1 解偶聯,激活此信號轉導通路,并啟動靶基因如醌氧化還原酶1(NQO1)、超氧化物歧化酶(SOD)、谷胱甘肽過氧化物酶(GSH-Px)、血紅素氧合酶1(HO-l)等的轉錄及表達,提高了細胞的氧化應激及修復功能,避免了腫瘤的發生[17]。
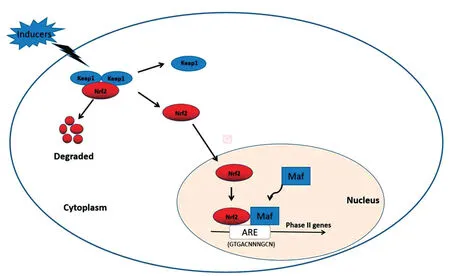
圖2 Keap1-Nrf2/ARE 信號通路
Keap1-Nrf2/ARE 信號通路能防止正常細胞發生癌變,使某些腫瘤細胞發生凋亡。Wang 等合成了一種新的化合物PBQC,發現其高濃度條件下可通過增強Nrf2 活性從而抑制HeLa、A549、U87和HUVECs 等腫瘤細胞生長,而不抑制正常的血管內皮細胞生長。此外,PBQC 可以引起Keap-1蛋白s-谷胱甘肽酰化,促進Nrf2 核易位和促凋亡基因的表達,從而使癌細胞發生凋亡[18]。
這些研究結果表明Keap1-Nrf2/ARE 信號通路對某些腫瘤細胞具有抑制作用,其機制主要是通過增強Nrf2的活性,促進其核異位來誘導相關保護蛋白抵抗正常細胞發生惡變的能力,同時提高腫瘤細胞中某些促凋亡蛋白的表達進而促使其發生凋亡。
3.2 Keap1-Nrf2/ARE 信號通路對腫瘤的促進作用
臨床研究統計分析表明,Keap1-Nrf2/ARE 信號通路與多種癌癥的發生、發展密切相關。Nrf2的異常高表達會促進食管鱗狀細胞癌、喉癌、肝癌細胞SMMC-7721 等的發展[19-21]。
CDK20 是一種新發現的蛋白激酶,在多種癌癥的細胞生長和增殖中發揮重要作用,研究證明CDK20 通過自身保守的ETGE 結構域與Nrf2 競爭結合Keap1,從而增強Nrf2的轉錄活性,降低細胞內ROS 水平,增強肺癌細胞的放化療耐藥性[22]。這些發現說明Keap1-Nrf2/ARE 信號通路能促進腫瘤的生長和發展,其機制主要通過增強Nrf2的活性,進而增強下游抗氧化蛋白的表達,加強細胞抵抗外來應激及其耐藥性的能力。
4 Keap1-Nrf2/ARE 信號通路介導的腫瘤耐藥性
腫瘤耐藥性(multidrug resistance,MDR)是影響腫瘤化療效果的絆腳石。MDR的形成機制非常復雜,目前大多數研究表明這些機制主要包括多藥耐藥性相關蛋白(multidrug resistance associ?ated protein,MRP)等膜轉運蛋白介導的化療藥物外排、GST 同工酶介導的化療藥物外排、DNA 拓撲異構酶介導的MDR表達水平改變、凋亡途徑相關基因表達下降等[23]。越來越多的研究證實MDR與Keap1-Nrf2/ARE 信號通路密切相關,這與其能間接影響MDR 及相關酶的表達水平有關。
Hu 等發現位于細胞質的新抗氧化因子iASPP(inhibitor of apoptosis stimulating protein of p53)不依賴p53,而通過其N端DLT 氨基酸序列與Nrf2經典DLG 序列競爭性結合Keap1的DGR 結構域,提高Nrf2 蛋白穩定性,激活Nrf2 抗氧化系統,促進其抗氧化靶基因(如NQO1、HMOX1、FTH1)表達,顯著抑制腫瘤細胞內ROS 水平,從而促進腫瘤細胞的生長和耐藥[24]。Tian 等發現,在膽管癌細胞中,非典型的蛋白激酶Cι(aPKCι)能夠促進Nrf2 累積、核轉移及激活相關目的基因表達,從而促進膽管癌的腫瘤發生和化藥耐藥性,這種作用是通過aPKCι與Nrf2 競爭結合Keap1 中一個高度保守的DLL 結構域來實現的[25]。另外,其他一些蛋白如PALB2、DPP3 等也都可通過與Nrf2 競爭性結合Keap1 來促進Nrf2 轉核,從而促進腫瘤細胞在不利環境下的生存,增強其對化療藥物的耐藥性[26-27]。
這些研究結果表明,Keap1-Nrf2/ARE 信號通路與腫瘤耐藥性密切相關,藥物通過競爭性結合Keap1 或Nrf2 關鍵結構域,激活Nrf2 并促進其轉核,從而促使一些耐藥蛋白的表達,增強腫瘤的耐藥性。
5 基于Keap1-Nrf2/ARE 信號通路治療腫瘤的策略
化療在癌癥綜合治療中帶來的毒副作用和耐藥性是不容忽視的重要問題。鑒于Keap1-Nrf2/ARE 信號通路能夠增強腫瘤細胞耐藥性,抑制Keap1-Nrf2/ARE 信號通路已成為逆轉癌細胞耐藥的重要靶點之一。采用Keap1-Nrf2/ARE 信號通路抑制劑與抗癌藥聯用,增強癌細胞對化療藥的敏感性,改善化療藥物的治療效果,為癌癥治療提供了新途徑。
呂慧等的研究證實,多柔比星(DOX)可以誘導K562細胞中Nrf2 蛋白累積,而聯合鴉膽子苦醇處理K562細胞可抑制Nrf2-Keap1 信號通路及其下游靶蛋白表達,進而降低K562細胞抗氧化應激能力,增強DOX誘導K562細胞凋亡作用[28]。另外,從基因水平對Keap1-Nrf2/ARE 信號通路加以干擾或抑制,也可增敏腫瘤細胞。例如,研究發現一些miRNA可與此信號通路中Keap1 或Nrf2 相互作用,從而抑制此信號通路的激活。Chang 等發現miRNA-141 可能通過靶向負調控Keap1 激活Keap1-Nrf2/ARE 信號通路,誘導抗氧化酶的表達,以降低細胞氧化應激水平,從而抑制乳腺癌細胞T47D的活力[29]。還有一種可能是利用人工合成某些小分子多肽作為誘導劑[18],這些多肽可以特異性結合Keap1 中DGR 結構域或者Nrf2 中DLG 或ETGE 結構域的氨基酸序列,從而能破壞Keap1-Nrf2 復合物的穩定性,促進Nrf2與Keap1發生解離,進而促使Nrf2 核異位促進下游靶基因的表達。
6 結語
Keap1-Nrf2/ARE 信號通路在機體抵抗外源性物質和氧化損傷方面發揮著重要的作用,越來越多的研究證實,Keap1-Nrf2/ARE 信號通路與多種癌癥的發生發展有著密切的聯系。在癌癥治療中,Nrf2 有作為藥物靶點的巨大潛力,Nrf2誘導劑和NRF2 抑制劑都有望作為抗癌藥物發揮作用,其中一種可能是將Nrf2誘導劑或NRF2 抑制劑與傳統的抗癌藥物聯用[30]。但鑒于Keap1-Nrf2/ARE信號通路對腫瘤細胞的雙重作用,不同癌癥中Nrf2表達水平對癌癥的作用以及癌癥所處的發展階段都應被考慮進去[31]。長期使用Nrf2誘導劑是否會促使正常細胞發生惡變目前也尚未有確切定論,需要通過更深入的研究驗證。另外,腫瘤細胞產生耐藥性的機制十分復雜,可能涉及到多種機制共同作用,仍須進行更廣泛的研究加以理解。相信隨著對Keap1-Nrf2/ARE 信號通路的不斷深入研究,其在抗腫瘤方面也會發揮越來越重要的作用。

