匹伐他汀聯合乙酰半胱氨酸對PCI患者對比劑腎功能損傷的干預作用
祖玉剛,趙淑君,張芳,陳春紅,賈辛未,解俊敏,張小瓊,范學秀,文艷彬,胡素欣
(1河北大學附屬醫院,河北保定 071000;2保定市第二醫院;3保定市第一醫院;4保定市容城縣人民醫院;5保定市博野縣醫院)
對比劑腎病(CIN)是指血管內注射對比劑72 h內引起的血清肌酐(Cr)異常升高,同時排除其他原因引起的急性腎功能損傷[1]。CIN早期多表現為少尿或非少尿型腎功能損傷,臨床癥狀隱匿且不典型,早期診斷困難且缺乏有效治療方法,因此對CIN的預防則尤為重要[2,3]。近年來研究發現,氧化應激反應和腎髓質缺血是CIN主要的發病機制[4]。匹伐他汀屬于羥甲基戊二酸單酰輔酶A還原酶(HMG-COA)抑制劑,具有顯著的抗炎、抗氧化作用[5];而乙酰半胱氨酸(NAC)是一種含有巰基的抗氧化劑,通過參與調控腎素-血管緊張素轉化酶系統,發揮擴張腎血管、增加腎血流量的作用[2]。本研究通過探討匹伐他汀聯合NAC對PCI患者血清氧化應激因子水平的影響及腎保護作用,為CIN的臨床預防提供科學的理論依據。
1 資料與方法
1.1 臨床資料 選擇2016年5月~2017年10月在河北大學附屬醫院接受PCI治療患者200例,男121例、女79例,年齡38~79(63.59±10.42)歲。入選標準: ①符合1999年歐洲泌尿生殖放射學會制定的關于CIN的診斷標準[6];②臨床資料完整;③由患者或家屬簽署本次研究知情同意書。排除標準: ①不符合上述納入標準的患者;②PCI術前2周接受他汀類、非甾體類抗炎藥物、環氧化酶-2抑制劑、氨基糖苷類藥物、二甲雙胍、抗氧化維生素或乙酰半胱氨酸治療者;③PCI術前1周使用對比劑者;④術前接受腎透析者;⑤合并急性感染、創傷、惡性腫瘤或各種應激情況的患者;⑥合并嚴重的心、肝、腎功能不全者;⑦原發性腎病、早期糖尿病腎病者;⑧精神障礙、智力異常的患者;⑨對他汀類藥物及血管緊張素II受體拮抗劑(ARB)或對比劑過敏及不能耐受者。按照隨機數字表法,將200例患者分為四組各50例。四組年齡、性別、BMI、臨床癥狀體征、腎小球濾過率估計值(eGFR)、PCI分期、對比劑類型比較無統計學差異(P均>0.05)。本項研究獲得醫院倫理委員會審查批準。
1.2 治療方法 四組術前12 h給予水化治療(0.9%氯化鈉500 mL持續緩慢靜脈滴注),術后繼續水化治療24 h。A組:術前1 d給予口服匹伐他汀(華潤雙鶴藥業股份有限公司生產,國藥準字H20080736)4 mg/d,1次/d,PCI術后相同劑量再連續服用3 d。B組:術前1 d服用NAC泡騰片(浙江金華康恩貝生物制藥有限公司生產,國藥準字H20057334)l 200 mg,2次/d,PCI術后相同劑量再連續服用3 d。C組:PCI術前術后不作進一步處理。D組:術前術后同時給于匹伐他汀及NAC泡騰片,方法A組和B組患者。四組患者經橈動脈或尺動脈入徑行PCI,均使用低滲透壓非離子型造影劑碘海醇(揚子江藥業有限公司生產,滲透濃度為800 mOsm /kg)。術前常規應用降糖藥、低分子肝素、抗血小板藥、β受體阻滯劑等。
1.3 檢測方法 分別于介入術前2 d和術后第3天、第7天采集患者晨起肘靜脈血5mL,加入枸櫞酸鈉抗凝,4 ℃ 3 000r/min離心10 min,分離血清,-80 ℃冰箱保存。采用AU5800全自動生化分析儀(美國Beckman coulter)檢測血清Cr、胱抑素C(CysC)水平,采用ELISA法檢測血清氧化低密度脂蛋白(ox-LDL)、同型半胱氨酸(Hcy)水平。試劑盒購均自中生北控生物科技股份有限公司。
2 結果
2.1 四組PCI前后血清Cr、CysC水平比較 術后3 d,四組血清Cr和CysC水平均較治療前升高,C組血清Cr和CysC水平高于A組和B組,D組血清Cr、CysC水平均低于A、B、C組,差異均有統計學意義(P均<0.05)。術后7 d,A、B、C組血清Cr和CysC水平仍然高于術前,D組血清Cr、CysC水平低于A、B、C組,差異均有統計學意義(P均<0.05)。見表1。
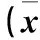
表1 四組PCI前后血清Cr、CysC水平比較±s)
注:與術前2 d比較,*P<0.05;與A、B、D組同時間比較,aP<0.05;與A、B組同時間比較,bP<0.05。
2.2 四組PCI前后血清ox-LDL和Hcy水平比較 術后3 d,四組血清ox-LDL和Hcy水平均較治療前升高,A、B、D組血清ox-LDL和Hcy水平均低于C組,D組血清ox-LDL和Hcy低于A組和B組,差異均有統計學意義(P均<0.05)。術后7 d,D組血清ox-LDL和Hcy水平仍低于其他三組(P均<0.05)。見表2。
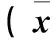
表2 四組PCI前后血清ox-LDL和Hcy水平比較±s)
注:與術前2 d比較,*P<0.05;與A、B、D組同時間比較,aP<0.05;與A、B組同時間比較,bP<0.05。
2.3 四組PCI前后eGFR變化及其與ox-LDL、Hcy的相關性 PCI術前2 d、術后7 d,A組eGFR分別為(85.91±11.06)、(79.62±11.87)mg/ (min·1.73 m2),B組eGFR分別為(83.08±11.57)、(78.76±10.71)mg/ (min·1.73 m2),C組eGFR分別為(85.75±13.72)、(71.28±10.39)mg/ (min·1.73 m2),D組eGFR分別為(87.84±11.93)、(82.34±9.45)mg/ (min·1.73 m2)。與術前比較,PCI患者術后eGFR均降低(P均<0.05);術后7 d ,A、B、C組eGFR均低于D組(P均<0.05)。相關性分析顯示,血清ox-LDL、Hcy水平與eGFR均呈負相關關系(r分別為-0.639、-0.577,P均<0.05);血清ox-LDL、hcy水平越高,即腎功能損傷越嚴重。
2.4 四組PCI術后CIN發生情況 根據CIN診斷標準:血管內注射對比劑后3 d內出現新發生腎功能障礙或原有的腎功能障礙加重并除外其他因,血清Cr水平較基線絕對值升高44.2 μmol/L或相對增加超過基線的25%[7]。A、B、C、D組術后7 d發生CIN分別為2例(4.0%)、3例(6.0%)、6例(12.0%)、1例(2.0%)。D組CIN發生率低于其他三組(P均<0.05)。
3 討論
隨著影像學和介入放射學診斷和治療領域大量應用碘對比劑,其引發的腎功能損傷也逐漸成為威脅人類健康的重要原因之一。目前,臨床上腎臟損傷的診斷主要依靠血清Cr、BUN及eGFR等指標[7],其早期診斷腎臟損傷的敏感性、特異性均不夠理想。CIN發病早期臨床癥狀不明顯,易被忽視造成漏診、誤診,同時CIN發病確診后臨床上也缺乏有效的治療措施。因此PCI患者使用對比劑之前進行CIN危險因素分型評估,充分進行水化治療,以及采用相應藥物進行腎臟損傷的預防十分重要。
CIN發病機制十分復雜。目前大多數研究認為,CIN發生與氧化應激反應和腎素-血管緊張素系統(RAS)密切相關[8]。由于對比劑含有碘離子或其他毒性分子,其進入血管后可通過抑制抗氧化酶的活性,大量釋放氧自由基,促使線粒體大量產生超氧陰離子,從而引起脂質過氧化反應造成腎臟組織微血管病變[9]。另一方面,對比劑還可以抑制前列腺素的合成和分泌,從而作用于RAS系統,引起腎血管收縮,導致腎髓質缺血性損傷甚至壞死[10]。有研究顯示,ox-LDL和Hcy與CIN的發生密切相關[11]。ox-LDL是糖基化的低密度脂蛋白膽固醇(LDL-C)在超氧陰離子的作用下被氧化修飾所生成的過氧化分子。正常情況下,LDL-C不會被巨核細胞所吞噬,但是ox-LDL卻易被巨核細胞吞噬,在血管壁上形成動脈粥樣硬化斑塊,導致腎小球損傷[12]。Hcy屬于甲硫氨酸循環的含硫代謝產物,易被超氧陰離子所氧化,導致血管內皮細胞清除率下降,同時促使血小板聚集,激活凝血因子,促使動脈粥樣硬化斑塊的形成,損傷腎臟內皮細胞和腎小球,引起早期腎臟損傷[13]。有研究顯示,在對比劑腎病發生初期,出現蛋白尿的時間遠遠早于血清Cr和BUN 的改變[14],因此,可將ox-LDL和Hcy作為CIN早期診斷標志物。
目前臨床上特異性預防CIN發生的藥物相對缺乏,抗氧化劑是常用的預防性用藥。NAC可與氧自由基發生還原反應,同時抑制血管緊張素轉化酶活性,減少血管緊張素的生成,促使一氧化氮等擴血管因子大量釋放,對降低蛋白尿和增加腎血流量具有一定保護作用[15]。,為增強抗氧化劑的干預效果,臨床建議對于CIN患者應聯合其他藥物協同發揮腎功能保護作用。匹伐他汀屬于臨床上常用的HMG-COA抑制劑,該藥除了具有強效降脂作用以外,還可以通過清除氧自由基發揮抗氧化作用,抑制腎小管間質損傷、緩解腎臟系膜區細胞增殖、調節腎小球血流量等從而直接或間接保護腎臟[16]。本研究顯示,與匹伐他汀或NAC單獨干預者比較,匹伐他汀聯合NAC治療患者血清Cr、CysC、ox-LDL和Hcy水平降低,eGFR升高,CIN的發生率顯著降低。
綜上所述,匹伐他汀聯合NAC可有效改善PCI患者機體氧化應激反應,減輕對比劑引起的圍手術期腎功能損傷,是降低CIN發生的有效干預措施。

