分泌型卷曲相關蛋白5與慢性阻塞性肺疾病嚴重程度的關系
朱珍 殷少軍 魏麗 左晟 孔志斌 柳毅 李虹 宋爽 劉華
慢性阻塞性肺疾病(chronic obstructive pulmonary disease, COPD)是一種以持續氣流受限為特征的疾病,新的指南強調COPD存在全身炎癥反應,表現有全身氧化負荷異常增高、循環血液中促炎癥細胞因子濃度異常增高及炎癥細胞異常活化等[1-2]。越來越多的研究表明血液中某些抗炎脂肪因子與COPD相關,包括脂聯素、瘦素等[3-6]。
2010年,分泌型卷曲相關蛋白5(secreted frizzled-related protein-5, sfrp5)首次作為抗炎脂肪因子在脂肪細胞中發現,證明sfrp5可抑制脂肪組織巨噬細胞炎癥[7]。sfrp5在肺部疾病中的研究很少,僅在非小細胞肺癌、胸膜間皮瘤中有報道[8-10]。目前為止,國內外尚無關于sfrp5與COPD方面的研究報道,sfrp5與COPD的關系尚不明確,基于sfrp5對脂肪組織巨噬細胞的作用,我們初步推測sfrp5可能與巨噬細胞主要參與的COPD相關。為此,我們觀察了COPD患者血清sfrp5水平的變化,旨在探討sfrp5水平與COPD嚴重程度的關系。
資料與方法
一、 研究對象
收集2016年2月至2017年2月在上海市第六人民醫院東院呼吸內科門診隨診的COPD穩定期患者共計370例,其中男性287例,平均年齡(64.9±11.4)歲;女性83例,平均年齡(65.1±9.6)歲。納入體檢中心健康體檢者205例,均為同期肺功能正常的健康體檢者,其中男性150例,平均年齡(64.4±11.0)歲;女性55例,平均年齡(65.4±12.1)歲。2組性別、年齡及病程差異均無差異,具有可比性。本研究經上海第六人民醫院臨床倫理委員會審核批準,研究對象均簽署知情同意書。
二、COPD穩定期的納入與排除標準
1. 納入標準:①COPD診斷標準參照中華醫學會呼吸病學分會制定的“慢性阻塞性肺疾病診治指南(2013年修訂版)”:診斷COPD需要進行肺功能檢查,吸人支氣管舒張劑后第1 s用力呼氣容積/用力肺活量%(forced expiratory volume in one second/forced vital capacity, FEV1/FVC%)<70%即明確存在持續的氣流受限;②除外哮喘、支氣管擴張癥、充血性心力衰竭、肺結核和彌漫性泛細支氣管炎等疾病后可確診為COPD;③所有患者均處于臨床穩定期:患者的咳嗽、咳痰和氣短等癥狀穩定或癥狀輕微,病情基本恢復到急性加重前的狀態[2];④所有患者接受正規治療,納入試驗前6周內未使用抗生素,并且吸入藥物劑型劑量維持不變。
2. 排除標準:①肺功能提示合并有限制性通氣功能障礙者;②胸部CT 提示肺炎、肺膿腫、活動性肺結核、支氣管擴張、肺部腫瘤、肺間質疾病、彌漫性泛細支氣管炎、胸腔積液、氣胸等其他呼吸系統疾病;③合并代謝系統疾病:糖尿病、高脂血癥、肥胖等;④合并心血管疾病:包括心功能不全、高血壓、動脈粥樣硬化等;⑤全身其他各系統疾病包括肝硬化、非酒精性肝硬化、慢性腎臟疾病等;⑥認知障礙或精神異常無法完成COPD患者自我評估測試(COPD assessment test, CAT)問卷和改良版英國醫學研究委員會 (modified British Medical Reseach Council, mMRC) 呼吸問卷者。
三、研究方法
1. 患者臨床癥狀評估: 用mMRC呼吸問卷進行呼吸困難評分,記錄過去1年急性加重次數。mMRC呼吸困難分級:依據英國醫學研究會修訂的呼吸困難量表進行測試,其主要分為0~6級,級數越高,呼吸困難越嚴重。為明確COPD的嚴重程度,包括氣流受限的嚴重程度,患者的健康狀況和未來急性加重的風險程度,最終改善COPD患者的治療和疾病管理,我們按照中華醫學會呼吸病學分會制定的“慢性阻塞性肺疾病診治指南(2013年修訂版)”,根據患者的臨床癥狀、急性加重風險、肺功能異常的嚴重程度及并發癥情況進行綜合評估分組:將入選患者分為4組:A組:mMRC 0~1分、FEV1占預計值%≥50%且近一年急性加重次數<2次;B組:mMRC≥2分、FEV1占預計值%≥50%且近一年急性加重次數<2次;C組:mMRC 0~1分、FEV1占預計值%<50%或近一年急性加重次數2次;D組:mMRC≥2分、FEV1占預計值%<50%或近一年急性加重次數2次。肺功能評估的風險與急性加重評估的風險結果不一致時,以最高風險為準。
2. 生化指標測定: 測量所有研究對象血壓、身高、體重,計算體質量指數(Body mass index, BMI)。甘油三酯、膽固醇、血糖由全自動生化分析儀測定;糖化血紅蛋白(glycosylated hemoglobin A1c, HbA1C)采用高效液相色譜法檢測。所有研究對象在入選當天整夜禁食,次日清晨靜臥位,采集外周靜脈血10 ml,以離心半徑8 cm,3 000 r/min離心5 min,分離血清,-80 ℃冰箱儲存備檢。
3. 酶聯免疫吸附試驗法測定: sfrp5酶聯免疫吸附測定(enzyme-linked immunosorbent assay, ELISA)試劑盒由美國Biosource公司提供,其檢測靈敏度為100 ng/L,批內變異2.97%~3.84%,批間變異3.97%~5.50%,操作嚴格按說明書。用酶聯免疫吸附測定(ELISA)法測定血清腫瘤壞死因子-α(tumor necrosis factor-α, TNF-α)、白細胞介素-6(interleukin-6, IL-6)濃度,試劑盒由美國R&D公司生產。測定方法按照說明書進行。所有研究對象接受肺功能檢查(瑞士席勒Spirovit SP-1肺功能儀)。
四、 統計學方法
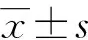
結 果
一、COPD患者一般情況比較
按綜合評估把COPD組再分為4組:A組98例,B組71例,C組75例,D組126例,各組性別、年齡及病程差異均無統計學意義(P>0.05),吸煙指數、體重指數存在差異(P<0.01),前一年急性加重頻率和CAT評分存在差異(P<0.01),用藥情況組間差異無統計學意義(P>0.05,見表1。
二、各組人群的生化指標及炎癥因子比較
各組患者的甘油三酯、膽固醇無明顯統計學差異(P>0.05),空腹血糖和HbA1C、血清IL-6、TNF-α存在顯著差異(P<0.01)。各組患者sfrp5水平差異很大(P<0.01)。COPD患者sfrp5水平顯著低于正常對照組,各組COPD患者sfrp5水平存在顯著差異:A組>B組>C組>D組,見表2。
三、 各組人群的肺功能參數比較
FEV1/FVC、FEV1占預計值%、肺一氧化碳彌散量(diffusion of the lungs for carbon monoxide, DLCO)、殘氣容積/肺總量(residual volume/total lung capacity, RV/TLC)組間差異均有統計學意義(P<0.01),見表2。
四、COPD患者的相關性分析
COPD患者血清sfrp5與BMI、甘油三酯、FBG均呈顯著負相關(r值分別為-0.346、-0.244、-0.501,均P<0.01),與炎癥因子IL-6、TNF-α水平也呈顯著負相關(r值分別為-0.401、-0.382,均P<0.01),與肺功能參數FEV1/FVC%、FEV1占預計值%均呈顯著正相關(r值分別為0.472、0.579,均P<0.01)。總體而言,較低的sfrp5水平者肺功能較差。

表1 各組人群的臨床特征
注:NAa統計學結果不包含對照組

表2 各組人群的生化指標、肺功能參數及sfrp5水平、炎癥因子水平
注:與對照組比較,aP<0.05
討 論
COPD綜合評估主要是根據患者的臨床表現、急性加重次數、肺功能分級及并發癥情況進行評價,具有重要的治療指導意義。過去單一用FEV1評估氣流受限程度,但其與患者的臨床癥狀、病理改變等情況并不符,不能完全反映臨床癥狀程度及不能預測急性加重風險。將肺功能分級作為判斷慢COPD嚴重程度的金標準,在老年患者可致過度診斷,而在年輕患者又可能導致漏診,因此,在臨床工作中受到一定限制。CAT量表能有效用于評價COPD患者的臨床癥狀和生活質量[11],mMRC呼吸困難評分量表是評估COPD患者呼吸困難程度的主要方法之一。研究表明,CAT評分與mMRC評分具有良好的相關性,說明mMRC評分能有效的評估COPD患者病情嚴重程度及預后情況[12]。本研究為更好地評估sfrp5水平與COPD嚴重程度的關系,根據mMRC呼吸困難評分、近一年急性加重次數、FEV1占預計值%來對COPD患者進行綜合評估分組,觀察A、B、C、D4組COPD患者血清sfrp5水平的變化。
巨噬細胞參與COPD的發病機制,在COPD的發生發展過程中,巨噬細胞及各種炎癥細胞釋放各種炎癥介質,表現為循環血液中細胞因子水平異常增加尤為明顯,其中CRP、IL-8、TNF-α、IL-6、瘦素等多種促炎因子水平增加。本研究也提示促炎因子水平TNF-α、IL-6在健康對照組和COPD組中存在顯著差異,COPD患者的促炎因子TNF-α、IL-6水平分別顯著高于健康對照組,且各組COPD患者促炎因子TNF-α、IL-6水平分別存在顯著差異:A組 sfrp5是一種新鑒定的脂肪因子,廣泛表達于脂肪組織、胰腺、肺等組織[7]。Ouchi等[7]在對胰島素抵抗小鼠模型的研究中發現,Sfrp5與Frz蛋白受體競爭結合Wnt5a,阻斷下游信號JNKl的激活,調控脂肪組織巨噬細胞的炎癥反應,故被認為是一種抗炎脂肪因子。Sfrp5基因轉染胰島素抵抗小鼠模型治療2周后,其脂肪組織巨噬細胞產生的炎癥因子水平下降。胃上皮細胞來源的Sfrp5可抑制Wnt5a誘導CCL2表達和巨噬細胞趨化作用,還可抑制巨噬細胞產生的炎癥因子和COX-2/PGE2的表達[13]。由此可見,sfrp5參與巨噬細胞的炎癥反應,因此,我們猜測sfrp5在巨噬細胞參與的COPD發病中可能發揮抗炎作用。本文結果顯示,COPD患者sfrp5水平顯著低于正常對照組,各組COPD患者sfrp5水平存在顯著差異:A組>B組>C組>D組,且sfrp5水平與促炎因子TNF-α、IL-6水平均呈負相關,提示sfrp5隨著炎癥嚴重程度的增加而下降,這可能是由于隨著COPD促炎效應不斷放大,而抗炎作用受到抑制的結果;本研究還顯示COPD患者血清sfrp5與FEV1/FVC%、FEV1占預計值%呈正相關,提示sfrp5與COPD患者氣流受限程度呈負相關,而氣道持續炎癥最終導致氣道重塑和氣流受限,sfrp5可能通過抗氣道炎癥的作用而抑制氣流受限,這與之前的研究結果提示sfrp5是一種抗炎因子相一致。 但是,本文存在一定的局限,血循環中sfrp5會受到多種因素影響。Hu等[14]發現糖耐量受損(Impaired glucose tolerance, IGT)、2型糖尿病(type 2 diabetes mellitus, T2DM)患者及肥胖人群血漿sfrp5水平明顯降低,并與肥胖相關指標(如BMI、WHR等)、血脂、血糖等代謝性指標及HOMA-IR等明顯呈負相關。瞿華等[15]在對新診斷的T2DM患者研究中發現,血漿sfrp5水平與HbA1C、甘油三酯、空腹血糖、ln(HOMA-IR)及體重指數均呈負相關。本研究結果顯示,COPD患者血清sfrp5與BMI、甘油三酯、FBG均呈顯著負相關。這與之前的研究結果相一致,提示sfrp5參與了脂代謝和糖代謝的發生機制。血糖血脂均和COPD的嚴重程度密切相關[16-20],是否脂代謝、糖代謝和COPD全身炎癥之間存在某種炎癥關聯機制,這一問題尚有待深入探討。

