2型糖尿病下肢血管病變患者血清Vaspin、RET水平變化及意義
陳建平,浦江,楊曙梅,王敬春,王旭東
(南通大學附屬醫院,江蘇南通226001)
糖尿病是嚴重危害人類健康的疾病,患病率逐年升高,且日趨年輕化[1]。下肢血管病變是糖尿病較常見的血管并發癥之一,致殘、致死率較高,其病理基礎為動脈粥樣硬化,胰島素抵抗、脂質代謝異常、炎癥反應、肥胖、高血壓是目前較為明確的高危因素[2]。腹腔脂肪型絲氨酸蛋白酶抑制劑(Vaspin)是新近發現的一種脂肪細胞因子,具有較強的胰島素增敏效用。抵抗素(RET)是脂肪細胞分泌的多肽類激素,具有抗胰島素作用。目前對Vaspin、RET在糖尿病下肢血管病變中水平變化的研究較少。2014年6月~2016年6月,我們檢測了糖尿病有無下肢血管病變患者的血清Vspin和RET水平變化,探討二者與糖尿病下肢血管病變的關系。
1 資料與方法
1.1 臨床資料 選擇同期南通大學附屬醫院內分泌科收治的2型糖尿病(T2DM)住院患者80例,根據踝肱指數(ABI)分為非下肢血管病變組(NON-LVD組)45例(ABI≥0.9)和下肢血管病變組(LVD組)35例(ABI<0.9)。NON-LVD組中,男26例、女19例,年齡(52.31±6.53)歲,糖尿病病程(3.58±1.70)年;LVD組中,男23例、女12例,年齡(51.72±5.71)歲,糖尿病病程(5.74±2.52)年。納入標準:符合糖尿病診斷標準[3],即空腹血糖(FBG)>7.0 mmol/L,口服葡萄糖耐量試驗(OGTT)血糖≥11.1 mmol/L;符合下肢血管病變分型標準[4];病例資料齊全;患者知情同意。排除標準:心肌梗死、慢性心力衰竭、急性腦血管病、嚴重肝腎功能異常、庫欣綜合征、惡性腫瘤等疾病。另選取同期行體檢的健康者50例作為對照組,男29例、女21例,年齡(50.16±5.70)歲。三組年齡、性別具有可比性。本研究經我院倫理委員會批準。
1.2 ABI檢測方法 T2DM患者仰臥位,采用GE多普勒超聲,測量肱動脈血壓并取其高限,測量足背動脈、脛后動脈收縮壓(SBP),取其高限作為踝動脈壓,二者比值即為ABI。
1.3 血糖、血脂、血清Vaspin、RET水平檢測 入院清晨采集各組空腹靜脈血,肝素抗凝,室溫下密封保存,避免劇烈震蕩引發溶血現象,3 000 r/min離心后,應用自動生化儀檢測NON-LVD組、LVD組治療前后及對照組FBG、甘油三酯(TG)、總膽固醇(TC),采用放射免疫分析法測定空腹胰島素(FINS)、采用比色法測定糖化血紅蛋白(HbA1c),采用ELISA法檢測血清Vaspin、RET及游離脂肪酸(FFA)水平。計算HOMA-IR。以上操作均嚴格按照試劑盒步驟操作。血清Vaspin、RET及FFA試劑盒購自美國Rapidbio公司。
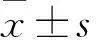
2 結果
2.1 各組血糖指標水平比較 LVD組和NON-LVD組FBG均高于對照組(P均<0.05)。LVD組和NON-LVD組HbA1c、FINS、HOMA-IR均高于對照組,且LVD組均高于NON-LVD組(P均<0.05)。見表1。
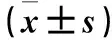
表1 各組血糖指標水平比較
2.2 各組血脂、Vaspin、RET水平比較 LVD組和NON-LVD組TG、FFA水平均高于對照組(P均<0.05)。NON-LVD組、LVD組血清Vaspin水平均低于對照組,且LVD組低于NON-LVD組(P均<0.05)。NON-LVD組、LVD組血清RET水平均高于對照組,且LVD組高于NON-LVD組(P均<0.05)。見表2。
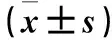
表2 各組血脂、Vaspin、RET水平比較
2.3 血清Vaspin、RET水平的相關性 血清RET與Vaspin水平呈負相關(r=-0.495,P<0.05)。
2.4 T2DM患者發生下肢血管病變的多因素Logistic回歸分析結果 血清RET(β=0.194,OR=1.161)、HbA1c(β=0.133,OR=0.405)是T2DM患者發生LVD的獨立危險因素,而血清Vaspin(β=-0.141,OR=1.159)是保護因素(P均<0.01)。見表3。

表3 T2DM患者發生下肢血管病變的多因素Logistic回歸分析
3 討論
下肢血管病變是常T2DM常見的并發癥之一,是糖尿病足發病的主要因素,早期因癥狀不典型,可耐受,易與骨關節病等病變相混淆,因而往往容易誤診、漏診。當患者出現明顯癥狀如靜息痛、壞疽等,往往已經處于病變晚期,難以達到滿意的治療效果,最終需截肢甚至危及生命[5]。研究發現,早期、及時、正確的診斷和定期監測,可使40%~85%的患者免于截肢,因此早期診斷至關重要[6]。但目前對于下肢血管病變的診斷主要依靠血管超聲學檢查,缺乏必要、特異性高的血清學標記物。
Vaspin最初是由Hida等[7]從肥胖OLETF大鼠內臟脂肪組織分離出的脂肪因子,后在人體內發現亦存在,并證實其為絲氨酸蛋白酶抑制劑Serpin家族的重要成員。Vaspin內含415個氨基酸殘基,其二級結構由9個α-螺旋、3個β-折疊、1個反應中心環組成。研究證實,Vaspin可通過抑制IL-1、IL-6、THF-α等炎性因子的分泌和血管平滑肌細胞的炎癥反應狀態,并通過誘導血管內皮細胞凋亡、影響糖脂代謝、改善胰島素敏感性等多種機制,發揮抗動脈粥樣硬化病變發生、發展的作用[8,9]。此外,Lin等[10]研究表明,Vaspin能通過抑制Apo E小鼠內質網應激誘導的巨噬細胞凋亡,從而延緩動脈粥樣硬化的進展,對血管起正性保護作用。Liu等[11]通過體外研究發現,Vaspin能夠抑制細胞因子誘導的核因子κB的活化和血管內皮細胞血管細胞黏附分子-1等諸多黏附分子的表達,增強胰島素敏感性,降低血糖,抑制血管平滑肌細胞增殖。Yang等[12]研究顯示,T2DM患者血清Vaspin水平低于健康人群,且在T2DM組中肥胖患者、伴血管病變患者血清Vaspin水平均降低。李振作等[13]研究證實,SBP、ABI和Vaspin水平是糖尿病發生下肢血管病變的獨立危險因素,血清Vaspin水平降低可能與T2DM患者下肢血管病變有關。本研究結果表明,NON-LVD組、LVD組血清Vaspin水平均低于對照組,提示血清Vaspin水平下降可能是T2DM患者下肢血管病變發生、發展的標志物。
眾多研究證實,RET有較強的胰島素抵抗效應,能促進血糖升高、誘導脂肪細胞增生,并通過上調VCAM-1、單核細胞趨化蛋白-1(MCP-1)、IL-1、IL-6的水平,促進內皮素-1(ET-1)釋放和減少一氧化氮(NO)生成,誘導全身各血管強烈收縮痙攣,損傷內皮細胞,從而加速動脈粥樣硬化的形成[14,15]。吳民松等[16]報道,血清RET水平可能作為一個獨立的危險因素誘發糖尿病足的發生,且伴有高血清RET水平的糖尿病患者或高血壓患者發生下肢缺血的風險大大增加。本研究顯示,NON-LVD組、LVD組血清RET水平均高于對照組,LVD組血清RET水平高于NON-LVD組,與楊偉等[17]研究結果一致,表明血清RET水平升高參與糖尿病及血管并發癥的發生、發展。
本研究進一步證實,血清RET水平與Vaspin呈負相關,血清RET水平、HbA1c是T2DM患者發生下肢血管病變的獨立危險因素,而血清Vaspin水平則是保護因素。機體血清Vaspin升高,有助于降低血糖,增強胰島素的敏感性,從而反饋抑制血清RET的分泌,阻止脂質沉積于血管內皮細胞,延緩動脈粥樣硬化的進程,相反,一旦Vaspin水平降低,其正性保護作用減弱,降低胰島素的敏感性,則促進血清RET升高,進一步誘導糖尿病及血管病變進一步發展,但二者具體的作用機制仍不明確[18]。
綜上所述,血清Vaspin、RET參與了糖尿病發生和演進,是T2DM患者發生下肢血管病變的獨立危險因素,隨著二者水平的異常變化,胰島素抵抗逐漸加重,直至發生下肢血管病變。然而血清Vaspin、RET在T2DM及下肢血管病變中的相互作用機制仍未完全闡明,這也將是本課題今后的研究方向。

