鉛陽極泥蘇打渣中Te、Bi、Cu浸出試驗研究
汪金良,胡華舟,陳亞州
(江西理工大學 工程研究院,江西 贛州 341000)
目前,鉛陽極泥主要采用火法工藝處理,其中的Te、Bi、Cu等有價金屬在氧化精煉后期富集進入蘇打渣中[1-3]。從蘇打渣中浸出Te、Bi、Cu主要有中性浸出[4]、堿浸[5-8]、酸浸[9-11]、硫化物浸出[12]和酸堿聯合浸出[13]等方法。但這些方法存在或有價金屬被浸出的同時其他金屬雜質也被同時浸出,或回收元素單一不能實現綜合回收,或工藝流程長、廢水產生量大,或設備腐蝕嚴重、操作環境差等問題。為此,根據鉛陽極泥蘇打渣的物相組成特點,在分析浸出熱力學基礎上,研究提出采用兩段鹽酸浸出工藝回收有價金屬,以期解決高酸度和高液固體積質量比帶來的問題,實現有價金屬的高效浸出與富集。
1 試驗部分
1.1 試驗原料
試驗所用蘇打渣取自某鉛冶煉廠鉛陽極泥處理工段,干燥后的ICP-MS、XRD表征結果分別見表1、圖1。由表1可知,蘇打渣中Te、Bi、Cu分別占14.32%、40.00%、7.37%。由圖1看出,物相以Bi2O3、TeO2、Bi2TeO6和CuBi2O4為主,具有較高的綜合回收價值。

表1 蘇打渣的化學成分 %
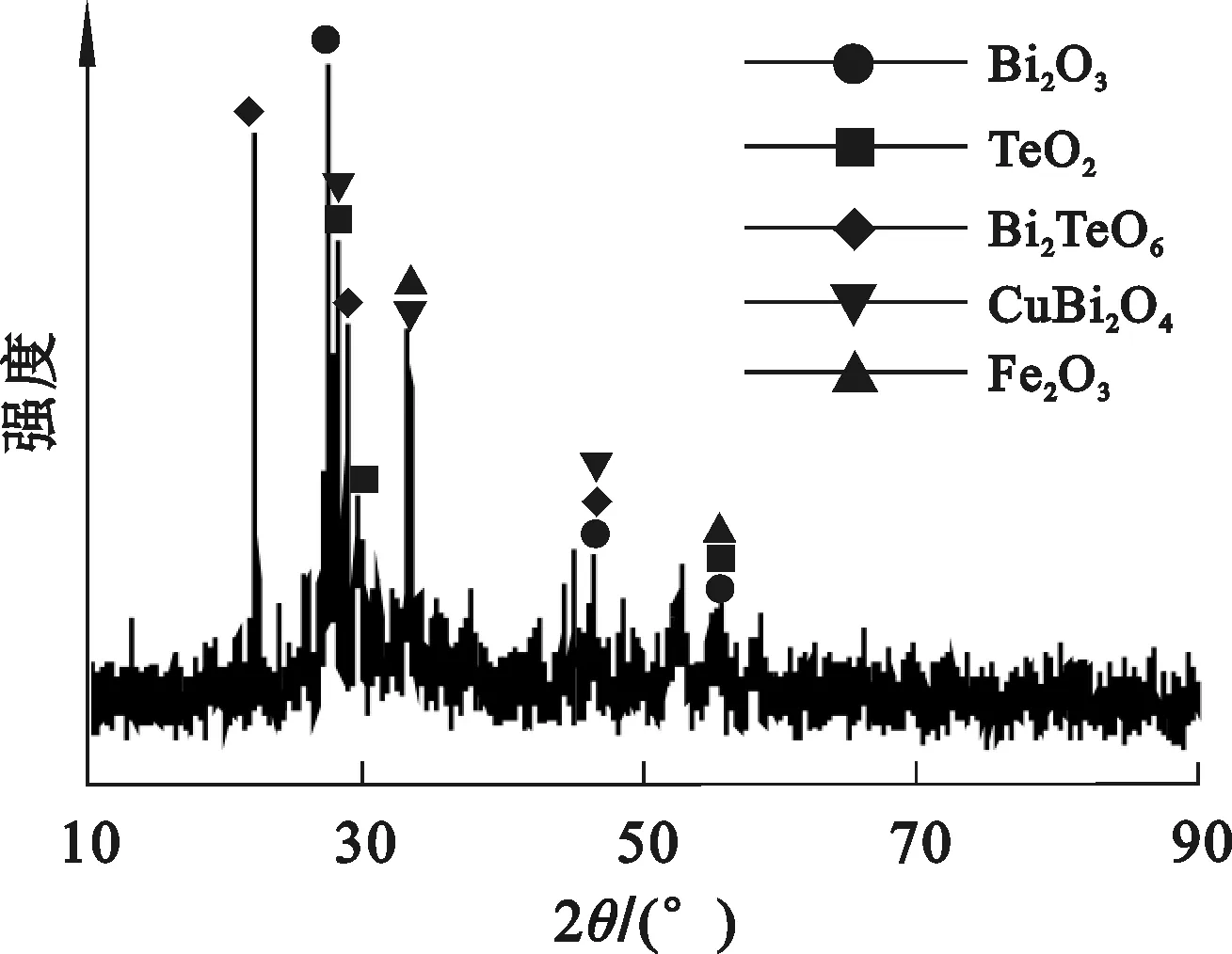
圖1 蘇打渣的XRD圖譜
1.2 試驗方法
蘇打渣鹽酸浸出試驗在同步數顯恒速電動攪拌器(RHYG-4S)中進行。取50 g蘇打渣,于500 mL燒杯中進行浸出。浸出率計算公式為
(1)
式中:μ(Me)為Me浸出率,%;m0為蘇打渣質量,g;w(Me)為蘇打渣中某元素質量分數,%;ρ(Me)為浸出液中某金屬元素質量濃度,g/L;V1為浸出液體積,mL。
2 浸出熱力學分析
2.1 浸出反應
基于蘇打渣XRD圖譜和鉛陽極泥回收工藝,選擇鹽酸體系進行浸出。發生的反應如下:

(2)

(3)

(4)

(5)

(6)

(7)

(8)
2.2 浸出熱力學計算
鹽酸體系浸出蘇打渣過程中,金屬元素價態沒有發生變化,因此浸出反應可概括為

(9)
則反應平衡常數K和ΔrGm分別為:
(10)
(11)
(12)
蘇打渣浸出過程中,各化合物在不同溫度下的標準摩爾自由能見表2[14]。
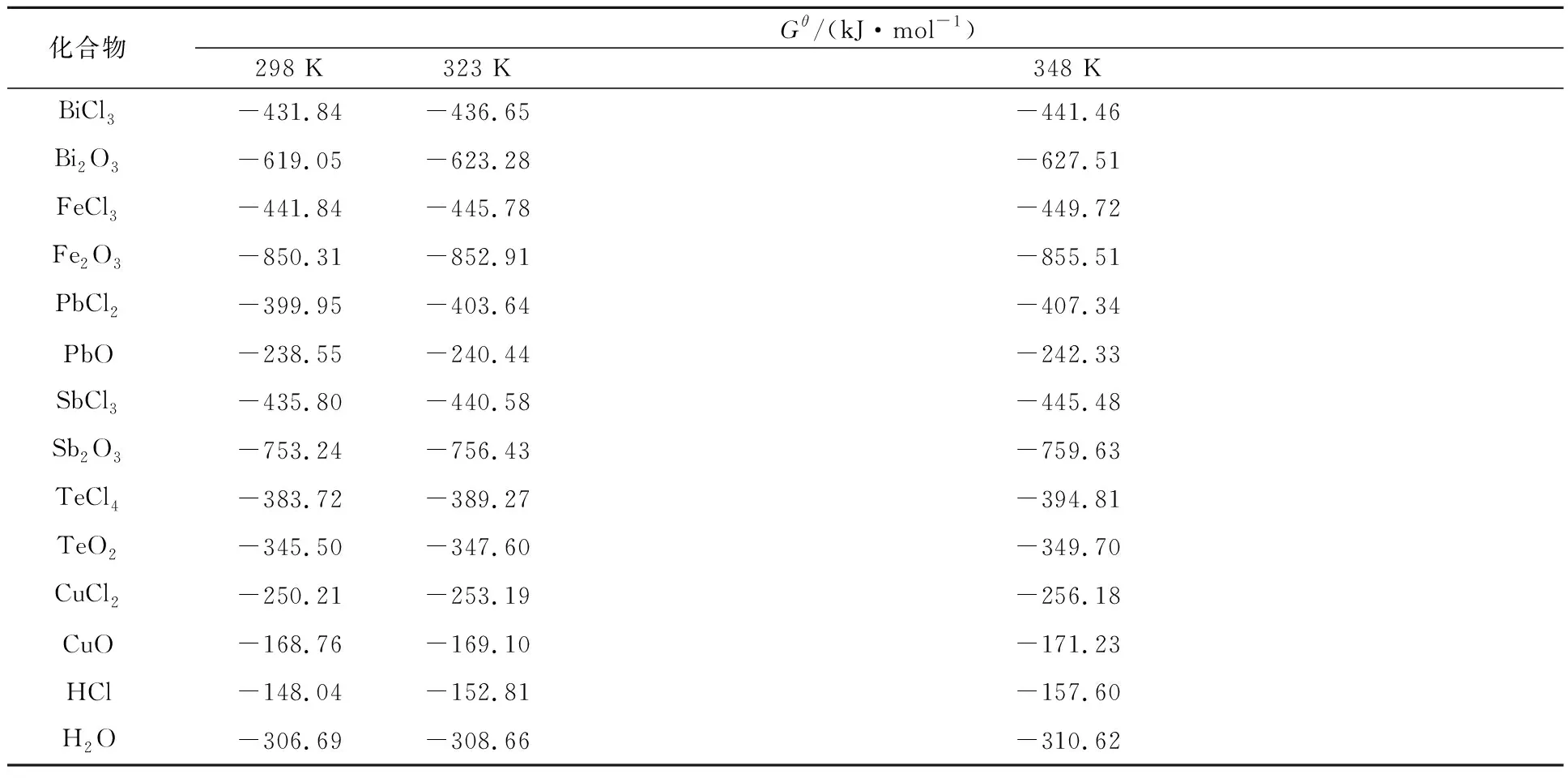
表2 主要化合物的標準摩爾自由能
將表2數據代入式(12)中,可得不同溫度下lg[Men+]與pH之間的關系,如圖2所示。
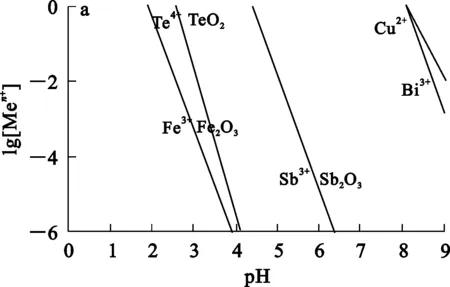
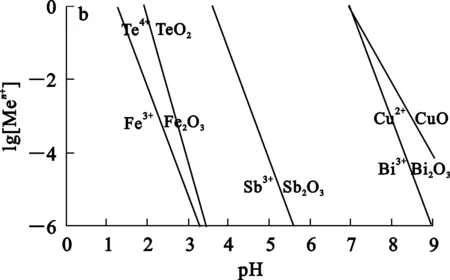
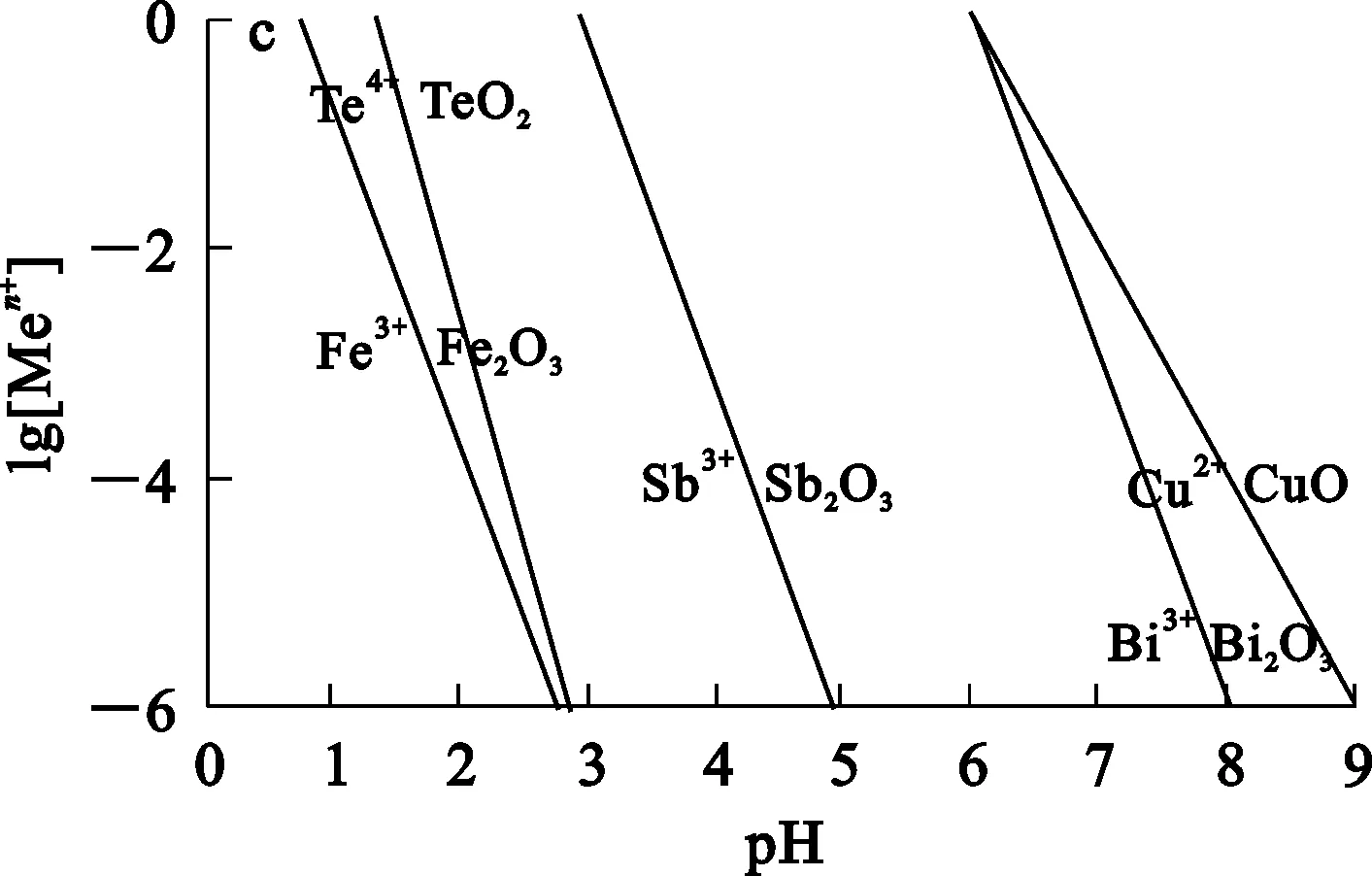
a—298 K;b—323 K;c—348 K。
由圖2看出:在同一溫度條件下,隨pH降低,浸出液中各Men+濃度不斷升高;從熱力學角度考慮,升溫不利于有價金屬的浸出;Te被浸出時,Bi、Cu等也被一并浸出,其他元素在高酸度下也被一并浸出。所以,在高酸度和較低溫度下共浸出Te、Bi、Cu在熱力學上是可行的。
3 試驗結果與討論
3.1 鹽酸濃度對蘇打渣浸出的影響
在溫度55 ℃、液固體積質量比5/1、攪拌速度300 r/min條件下浸出2 h,鹽酸濃度對蘇打渣浸出的影響試驗結果如圖3所示。
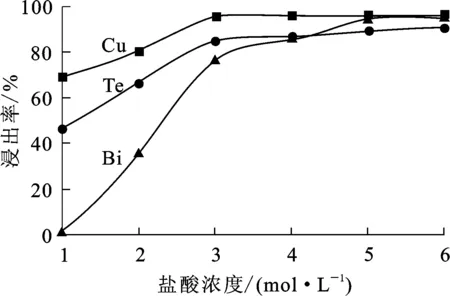
圖3 鹽酸濃度對蘇打渣浸出的影響
由圖3看出,鹽酸濃度為5 mol/L時,Te、Bi、Cu浸出率均達最大,分別為89.06%、94.10%、95.77%。為保證反應充分進行,可適當提高酸度;但若酸度過高,設備腐蝕加重、操作環境惡劣:因此,鹽酸濃度以不超過5 mol/L為宜。
3.2 溫度對蘇打渣浸出的影響
在鹽酸濃度5 mol/L、液固體積質量比5/1、攪拌速度300 r/min條件下浸出2 h,溫度對蘇打渣浸出的影響試驗結果如圖4所示。
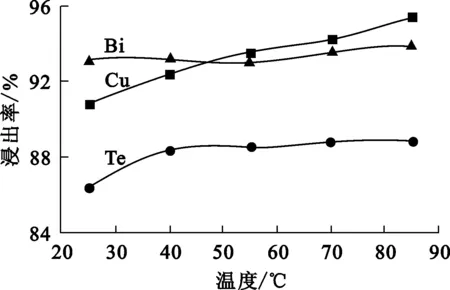
圖4 溫度對蘇打渣浸出的影響
由圖4看出:溫度對浸出的影響與上述熱力學分析結果一致,在常溫基礎上,適當升高溫度,可在一定范圍內強化浸出過程,促進鹽酸與生成物的擴散;隨溫度升高,Cu、Te浸出率有所提高,而Bi浸出率變化不大。但溫度過高,鹽酸揮發量加大,操作環境變差,綜合考慮,確定溫度以40 ℃為宜。
3.3 反應時間對蘇打渣浸出的影響
在鹽酸濃度5 mol/L、液固體積質量比5/1、溫度40 ℃、攪拌速度300 r/min條件下,反應時間對蘇打渣浸出的影響試驗結果如圖5所示。
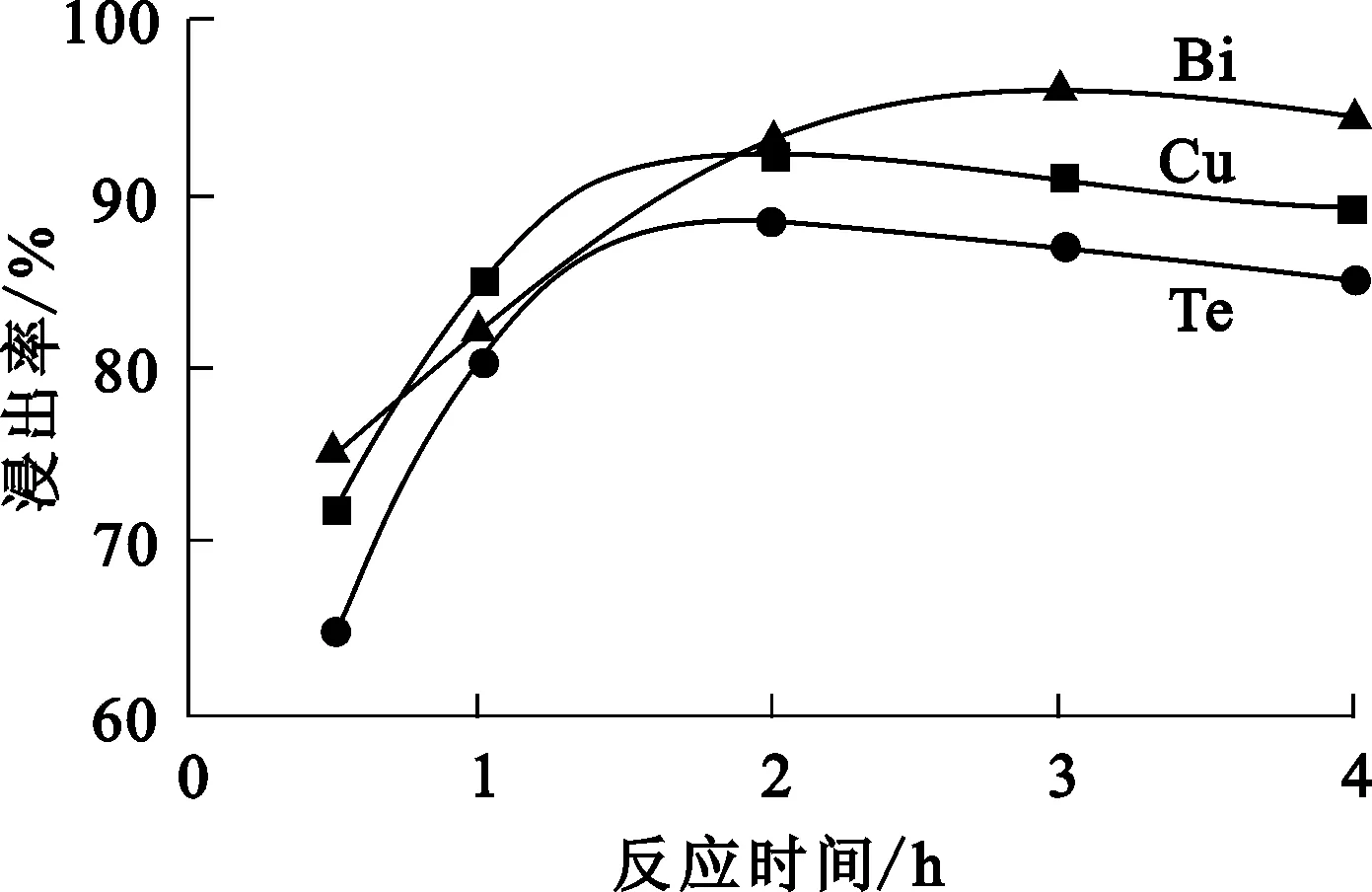
圖5 反應時間對蘇打渣浸出的影響
由圖5看出,反應2 h時,Te、Bi、Cu浸出率分別達88.39%、93.16%、92.38%,浸出效果較好。為保證有價金屬充分浸出,可適當延長反應時間;但反應時間過長,鹽酸揮發量加大,且生產效率會降低;而Bi浸出率隨反應時間從2 h延長至3 h提高不明顯:綜合考慮,確定反應時間以2 h為宜。
3.4 攪拌速度對蘇打渣浸出的影響
在鹽酸濃度5 mol/L、液固體積質量比5/1、溫度40 ℃條件浸出2 h,攪拌速度對蘇打渣浸出的影響試驗結果如圖6所示。
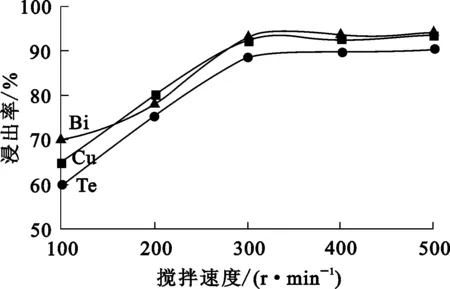
圖6 攪拌速度對蘇打渣浸出的影響
由圖6看出:隨攪拌速度增大,鹽酸與蘇打渣的傳質過程得以加強,有利于金屬離子與氯離子之間反應,Te、Bi、Cu浸出率提高;攪拌速度增至300 r/min時,Te、Bi、Cu浸出率穩定在90%左右;再繼續增大攪拌速度,對浸出過程無明顯促進作用。因此,確定攪拌速度以300 r/min為宜。
3.5 液固體積質量比對蘇打渣浸出的影響
在鹽酸濃度5 mol/L、浸出溫度40 ℃和攪拌速度300 r/min條件下浸出2 h,液固體積質量比對蘇打渣浸出的影響試驗結果如圖7所示。
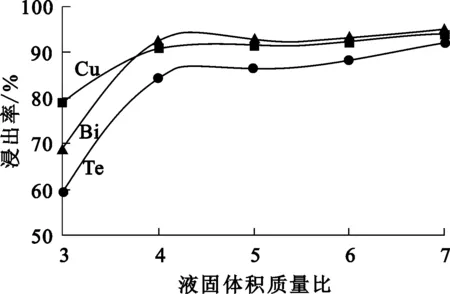
圖7 液固體積質量比對蘇打渣浸出的影響
由圖7看出:Te、Bi、Cu浸出率隨液固體積質量比增大均顯著提高;液固體積質量比增大至7/1后,Te、Bi、Cu浸出率趨于穩定,分別達92.23%、95.10%、94.05%。隨液固體積質量比增大,浸出液黏度降低、流動性變好,同時也提供了足夠的氯離子,有利于有價金屬的浸出和金屬配離子的形成。
用鹽酸體系浸出蘇打渣可實現有價金屬的共同浸出,但只有在高液固體積質量比條件下有價金屬浸出率才達90%,這樣浸出液中Te、Bi、Cu濃度較低、酸耗較大;而在低液固體積質量比(4/1)條件下浸出,Te浸出率不高。所以,對低液固體積質量比條件下的浸出渣進行高液固體積質量比條件下的二次浸出。
液固體積質量比為4/1時所得浸出渣的ICP-MS分析結果表明,Te、Bi、Cu質量分數分別為5.21%、13.69%和4.61%。增大液固體積質量比對一次浸出渣進行二次浸出。二次浸出條件:鹽酸濃度5.0 mol/L,浸出時間2 h,溫度40 ℃,液固體積質量比7/1,攪拌速度300 r/min。試驗結果見表3,二次浸出渣的ICP-MS分析結果見表4。

表3 一次浸出渣的二次浸出試驗結果

表4 二次浸出渣的化學成分分析結果 %
由表3、4看出:二次浸出可有效浸出一次浸出渣中殘留的Te、Bi、Cu元素;經過二次浸出,Te、Bi、Cu總浸出率明顯提高,Te、Bi、Cu得到有效浸出和富集;但部分Fe、Pb、As等也進入浸出液。
3.6 浸出液循環利用
兩次浸出過程中,其他浸出條件都相同,僅液固體積質量比不同,因此,在二次浸出液體積較小前提下,補充一定量鹽酸后可返回浸出蘇打渣,不會影響浸出液體積平衡,可實現浸出液循環利用和廢水零排放。蘇打渣兩次逆流浸出試驗結果見表5。可以看出,二次浸出液補充一定量鹽酸后返回一次浸出是可行的,而且避免了體系高酸度對設備的腐蝕。
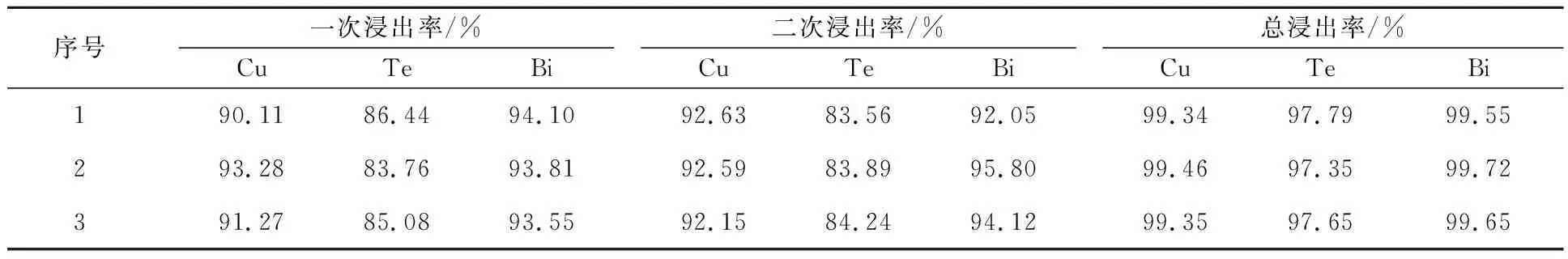
表5 蘇打渣的兩次逆流浸出試驗結果
4 結論
用鹽酸體系可實現蘇打渣中Te、Bi、Cu等有價金屬的一步浸出。在鹽酸濃度5.0 mol/L、溫度40 ℃、攪拌速度300 r/min、一段浸出液固體積質量比4/1、二段浸出液固體積質量比7/1條件下浸出2 h,Te、Bi、Cu浸出率分別達97.60%、99.64%、99.38%。此兩段浸出工藝流程簡單、操作方便,蘇打渣中Te、Bi、Cu實現有效回收,解決了鉛陽極泥蘇打渣處理流程長、金屬回收率低等問題。該工藝已實現工業化應用,蘇打渣處理效果較為理想。

