基于整合證據鏈的中草藥相關肝損傷診斷方法解讀
——以何首烏為例
景 婧,王睿林,朱 云,牛 明,宋雪艾,何婷婷,肖小河,王伽伯
近年來,中草藥相關肝損傷(herb-induced liver injury,HILI)的報道呈逐年增多趨勢,引起了醫務人員、制藥企業、政府部門和社會公眾的廣泛關注。由于中藥自身組成的多樣性和臨床用藥的復雜性,使HILI難以客觀辨識,其因果關系難以判斷。針對HILI診斷的復雜性,中華中醫藥學會發布的《中草藥相關肝損傷臨床診療指南》推薦采用基于整合證據鏈(integrated evidence chain,iEC)法的因果關系評價法[1],以“iEC”為診斷和因果關系評價的核心思想,評價流程以常規應用的羅素優克福因果關系評估方法(Roussel-Uclaf causality assessment method,RUCAM)為組成部分,并在RUCAM基礎上,通過多方面構建證據鏈,提高HILI診斷和因果關系評價的可信度。
本研究以報道較多的何首烏相關肝損傷為例[2-7],回顧性分析2007年1月—2016年12月解放軍第三〇二醫院收治的HILI患者的臨床資料,比較分析iEC法和RUCAM對診斷效能和因果關系判斷的異同,解讀HILI客觀診斷iEC法的適用性和優勢。
1 對象與方法
1.1 研究對象 選取2007年1月—2016年12月解放軍第三〇二醫院收治的診斷為HILI的住院患者。本研究方案通過了解放軍第三〇二醫院倫理委員會的審批。
1.2 診斷標準 參照中華中醫藥學會《中草藥相關肝損傷臨床診療指南》推薦的基于iEC法的HILI診斷策略(圖1)[1]。①發病前有中草藥及其相關制劑應用史,生化學診斷標準須滿足以下情況之一:ALT≥5×ULN;ALP≥2×ULN,特別是伴有谷氨酰轉肽酶(γ-glutamyl transpeptidase,γ-GGT)升高且排除骨病引起的ALP升高;ALT≥3×ULN且TBIL≥2×ULN;若患者有慢性肝病(chronic liver diseases,CLDs)時,須用服藥前肝功能基線水平代替ULN[8]。②排除其他導致肝損傷的原因,如:病毒、免疫、酒精、遺傳代謝、膽管、血管等;當患者有CLDs時,僅排除藥物因素以外的可引起急性肝損傷的其他原因,如病毒感染、急性酒精濫用等。③RUCAM評分≥3分。④排除聯合用藥中有明確肝毒性或相互作用引起藥物肝毒性的西藥。⑤能夠記錄并核實引起肝損傷的中草藥及其相關制劑資料(包括余留藥材、批準文號、處方組成及用法用量等)。⑥能夠鑒定中草藥基原,排除中草藥混偽品以及有害物質污染。⑦檢測出體內中草藥特征代謝物。⑧發生中草藥及其相關制劑再激發事件。⑨檢測出HILI的體內特異性生物標志物。
診斷結果判定:當同時出現上述①、②、③時判斷結果為“疑似診斷”;當具備疑似診斷特征及上述④、⑤[或⑥或⑦]時,判斷結果為“臨床診斷”;當具備疑似診斷特征及上述⑧時,或者具備臨床診斷特征及上述⑨時,判斷結果為“確定診斷”。由于本文為回顧性研究,無法獲取⑥、⑦、⑨三項。納入標準:①符合基于iEC法的HILI診斷標準;②發病前有何首烏及其制劑應用史。排除標準:①發病前6個月內服用其他不含何首烏的中藥制劑;②抗HAV-IgM、抗HBV-IgM、HBV DNA定量、抗HCV、HCV RNA定量、抗HEV-IgM、抗HEVIgG、非嗜肝病毒感染等陽性結果[8-12];③急性酒精中毒[13]。RUCAM評分法用于判斷HILI的因果關聯強度,相關性評價結果分為“極可能”(≥9)、“很可能”(6~8)、“可能”(3~5)、“不可能”(1~2)、“排除”(≤0)[14-16]。本研究的診斷流程見圖2。
1.3 研究方法 記錄研究對象的人口學資料、用藥信息、實驗室指標及結局,對比分析新建立的iEC法和常規應用的RUCAM的診斷效能和因果關系判斷的異同。
1.4 統計學處理 采用SPSS 19.0統計軟件對數據進行處理,計量資料采用±s或中位數(第一四分位數,第三四分位數)進行統計描述,計數資料采用百分比(%)進行統計描述。不同組間差異性比較采用t檢驗、非參數檢驗和Chi-Square檢驗。P<0.05為差異具有統計學意義。
2 結 果
2.1 臨床特征 2007年1月—2016年12月解放軍第三〇二醫院收治的193 714例肝病住院患者中,5710例發病前有可疑藥物服用史,經排除聯合用藥后有152例患者在肝功能異常前服用了何首烏及其制劑。利用iEC法客觀辨識后,145例發病前服用何首烏及其制劑的患者被診斷為HILI,其中男女比例約為1∶1.16,平均年齡為(43.29±13.68)歲,服藥時間為37.50(30.00,91.00)d,住 院 時 間 是 21.25(3.00,79.00) d,其中33例(22.8%)患者有CLDs基礎。145例患者的生化學分型以肝細胞損傷型為主(94.5%),其次是膽汁淤積型(2.8%)和混合型(2.8%)。
2.2 iEC法與RUCAM的診斷結果及一致性評價 145例HILI患者中,iEC法的診斷結果為:7例(4.8%)為“確定診斷”,101例(69.7%)為“臨床診斷”,37例(25.5%)為“疑似診斷”。145例患者的RUCAM相關性評分中位數為6(5,7)分,范圍:3~10分,其中“極可能”、“很可能”和“可能”分別占2.1%、51.0%和46.9%。經iEC法辨識為“確定診斷”和“臨床診斷”的患者中,RUCAM相關性評分以“很可能”的占比最高,分別為71.4%和53.5%;而iEC法構建證據鏈達到“疑似診斷”的患者中,RUCAM相關性評分以“可能”的比例最高,為59.5%,“很可能”僅占40.5%(見表1)。iEC的診斷可信度級別與RUCAM相關性評分級別之間的趨勢基本一致。
盡管如此,iEC診斷可信度級別和RUCAM相關性評分級別在部分HILI病例中仍有不一致的情況。RUCAM相關性評分僅為“很可能”(n=5)和“可能”(n=2)級別的7例患者,通過iEC法構建證據鏈可達到“確定診斷”;而RUCAM相關性評分為“可能”的44例患者,經iEC法構建證據鏈可達到“臨床診斷”(表1)。
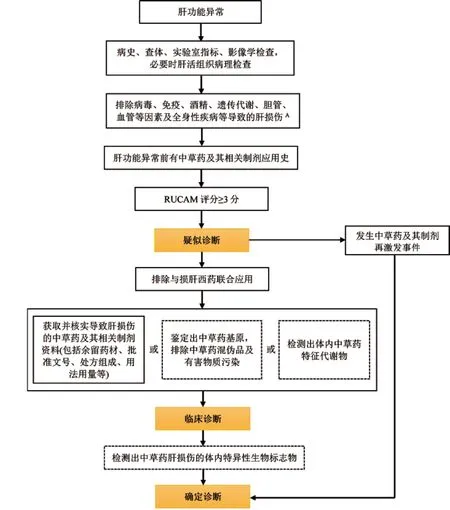
圖1 基于iEC法的HILI診斷方法注:虛框內部分可在有條件的實驗室開展;A.當針對有慢性肝病基礎人群進行HILI診斷時,僅須排除病毒感染、急性酒精濫用等非藥物因素引起的急性肝損傷即可Figure 1 Diagnostic method for HILI based on the iEC
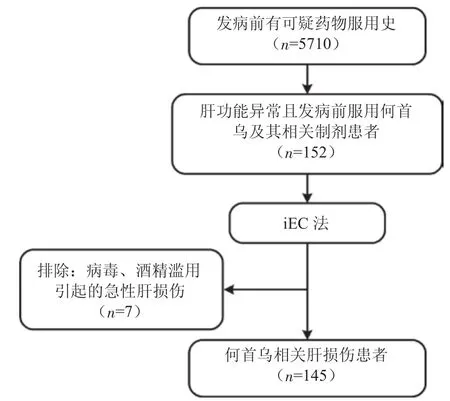
圖2 何首烏相關肝損傷診斷流程Figure 2 Flowchat depicting the diagnosis of HILI associated with Polygonum multiflorum
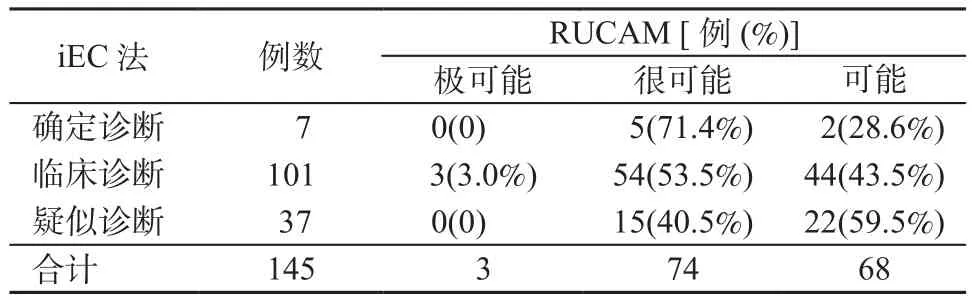
表1 iEC法與RUCAM的診斷結果(例)Table 1 Diagnosis results by iEC and RUCAM(cases)
2.3 基礎肝病對iEC法和RUCAM結果的影響 經iEC法構建證據鏈,112例無CLDs基礎HILI患者的診斷結果為:6例(5.3%)為“確定診斷”,77例(68.8%)為“臨床診斷”,29例(25.9%)為“疑似診斷”;33例有CLDs基礎HILI患者經iEC法辨識后,1例(3.0%)達到“確定診斷”,24例(72.7%)達到“臨床診斷”,8例(24.3%)達到“疑似診斷”。無CLDs基礎HILI患者的RUCAM相關性評分的判斷結果包括“極可能”(n=3)、“很可能”(n=71)和“可能”(n=38),其比例分別占2.7%、63.4%和33.9%;而在有CLDs基礎HILI患者的RUCAM相關性評分中,3例(9.1%)為“很可能”,30例為“可能”(90.9%)(表2)。經iEC法客觀辨識后,無CLDs基礎HILI患者與有CLDs基礎HILI患者的診斷可信度級別變化不大(χ2=0.371,P=0.831),而有CLDs基礎HILI患者的RUCAM相關性評分級別較無CLDs基礎HILI患者明顯下降(χ2=33.259,P=0.000)。

表2 2種方法對有無CLDs基礎HILI患者的診斷結果[例(%)]Table 2 Diagnosis results of HILI patients with or without CLDs by 2 methods[cases(%)]
3 討 論
由于特異性診斷標志物的缺乏,加上中藥自身的復雜性,使HILI診斷和因果關系評價面臨著挑戰,容易發生誤診和漏診[17]。同時,有CLDs基礎的HILI患者由于基礎肝病的干擾,使HILI因果關系的判斷難度較無CLDs基礎的HILI患者明顯增加[10]。因此,針對這些難點,急須開展適用于HILI自身特點的診斷和因果關系評價的研究。
常規應用的RUCAM相關性評分通過判斷DILI因果關系來達到辨識和診斷的目的,因操作性強而被廣泛推薦,但針對HILI診斷和因果關系評價仍存在一定的局限性[9,18]。Zhu等[19]利用RUCAM相關性評分對單一藥物相關肝損傷進行因果關系評價,發現“極可能”的比例在西藥致肝損傷中最高,占60.3%,而在HILI中僅占16.6%(P<0.001)。iEC法以RUCAM為組成部分,圍繞“證據鏈”核心思想,在RUCAM基礎上強調中草藥信息收集的完整性,突出HILI因果關系評價的客觀性,使HILI診斷和因果關系評價更為可靠[1]。
本研究145例HILI患者中,RUCAM的相關性評分結果以“很可能”為主,占51.0%。而這些RUCAM相關性評分為“很可能”的患者,經iEC法構建證據鏈后,5例(71.4%)達到“確定診斷”,54例(53.5%)達到“臨床診斷”,15例(40.5%)為“疑似診斷”,分別占iEC法相同診斷級別HILI患者的71.4%,53.5%和40.5%。此外,RUCAM相關性評分為“可能”的患者中,隨著iEC診斷可信度級別下降,RUCAM結果為“可能”的HILI比例在不同iEC診斷級別升高。這表明,針對HILI診斷時,iEC法的診斷級別越高,診斷可信度越強,所對應RUCAM評分的因果相關性就越強,且更傾向于很可能相關。由此可見,iEC法的診斷可信度級別和RUCAM相關性評分級別的趨勢基本一致,2種方法總體一致性較好。
盡管如此,部分HILI病例經iEC法辨識的診斷可信度級別和RUCAM相關性評分級別仍存在不一致。7例經iEC法構建證據鏈達到“確定診斷”的患者中,沒有1例的RUCAM相關性評分為“極可能”,最強因果相關性僅達到“很可能”;而44例RUCAM相關性評分為“可能”的患者,經iEC法構建證據鏈能夠達到“臨床診斷”。這很可能與中草藥自身復雜性強、HILI臨床影響因素眾多有關,大部分中草藥制劑是由多種草藥配伍組成,藥物之間的相互作用對RUCAM相關性評分結果影響較大,使RUCAM評分法在判斷HILI的因果關系時存在一定局限性。而iEC法以RUCAM相關性評分為組成部分,強調從藥物、機體等多方面構建證據鏈,能夠解決因影響因素復雜而使HILI診斷難度增大的問題。同時,醫務人員利用iEC法對HILI進行辨識后,能夠獲得確定診斷和臨床診斷病例。然而,這是否表明iEC在RUCAM相關性評分的基礎上能夠進一步提升HILI的診斷和因果關系評價的可信度,還須要進一步研究加以驗證。
基礎肝病對iEC法的診斷效能影響不大,但可導致RUCAM相關性評分的級別顯著下降。無CLDs基礎和有CLDs基礎的HILI患者通過iEC法構建證據鏈,達到“確定診斷”的病例分別占5.3%和3.0%,達到“臨床診斷”的病例分別占68.8%和72.7%,診斷效能變化不大(P>0.05);而RUCAM相關性評分在無CLDs基礎HILI因果關系評價中以“很可能”為主(63.4%),但在有CLDs基礎HILI患者中以“可能”為主(90.9%),“很可能”僅占9.1%,因果關系評價的級別明顯下降(P<0.001)。iEC法以RUCAM相關性評分為組成部分,在RUCAM基礎上不僅加強對藥物信息與機體因素的詳細調查,還對肝損傷的原因是藥物因素還是非藥物因素加以甄別,能夠對有CLDs基礎HILI患者進行客觀辨識和診斷;而RUCAM相關性評分更適合評價藥物與肝損傷的因果關系,而對藥物因素還是非藥物因素引起肝損傷的診斷區分度較低[14,20]。因此,iEC法不僅是無CLDs基礎HILI患者可靠的診斷方法,還同樣適用于有CLDs基礎的HILI患者的診斷和因果關系評價。
綜上所述,iEC法與RUCAM的總體一致性較好,iEC法是適用于臨床影響因素較為復雜的HILI診斷和因果關系評價,對有基礎肝病的HILI患者也可較好地應用。基于iEC法的診斷策略和因果關系評價模式不僅適用于HILI,也同樣適用于西藥相關肝損傷。亟需針對不同種類的藥物相關肝損傷,擴大樣本量,開展前瞻性、多中心研究,進一步驗證iEC法的適用性和優勢,為DILI的預警、診斷、治療和防控打下堅實的基礎。
【參考文獻】
[1]中華中醫藥學會肝膽病分會,中華中醫藥學會中成藥分會.中草藥相關肝損傷臨床診療指南[J].臨床肝膽病雜志,2016,32(5):835-843.
[2]朱云,劉樹紅,王伽伯,等.何首烏及其制劑導致藥物性肝損傷的臨床分析[J].中國中西醫結合雜志,2015,35(12):1442-1447.
[3]But PP,Tomlinson B,Lee KL.Hepatitis related to the Chinese medicine Shou-wu-pian manufactured from Polygonum multiflorum[J].Vet Hum Toxicol,1996,38(4):280-282.
[4]Park GJ,Mann SP,Ngu MC.Acute hepatitis induced by Shou-Wu-Pian,a herbal product derived from Polygonum multiflorum[J].J Gastroenterol Hepatol,2001,16(1):115-117.
[5]Mazzanti G,Battinelli L,Daniele C,et al.New case of acute hepatitis following the consumption of Shou Wu Pian,a Chinese herbal product derived from Polygonum multiflorum[J].Ann Intern Med,2004,140(7):W30.
[6]Cárdenas A,Restrepo JC,Sierra F,et al.Acute hepatitis due to shen-min: a herbal product derived from Polygonum multiflorum[J].J Clin Gastroenterol,2006,40(7):629-632.
[7]Dong H,Slain D,Cheng J,et al.Eighteen cases of liver injury following ingestion of Polygonum multiflorum[J].Complement Ther Med,2014,22(1):70-74.
[8]Aithal GP,Watkins PB,Andrade RJ,et al.Case definition and phenotype standardization in drug-induced liver injury[J].Clin Pharmacol Ther,2011,89(6):806-815.
[9]Chalasani NP,Hayashi PH,Bonkovsky HL,et al.ACG Clinical Guideline: the diagnosis and management of idiosyncratic druginduced liver injury[J].Am J Gastroenterol,2014,109(7):950-967.
[10]Teschke R,Danan G.Diagnosis and management of drug-induced liver injury (DILI) in patients with pre-existing liver disease[J].Drug Saf,2016,39(8): 729-744.
[11]Chalasani N,Bonkovsky HL,Fontana R,et al.Features and Outcomes of 899 patients with drug-induced liver injury: the DILIN prospective study[J].Gastroenterology,2015,148(7):1340-1352.
[12]Chalasani N,Regev A.Drug-Induced liver injury in patients with preexisting chronic liver disease in drug development: how to identify and manage? [J].Gastroenterology,2016,151(6):1046-1051.
[13]急性酒精中毒診治共識專家組.急性酒精中毒診治共識[J].中華急診醫學雜志,2014,23(2):135-138.
[14]Danan G,Teschke R.RUCAM in drug and herb induced liver injury: the update[J].Int J Mol Sci,2015,17(1):1-33.
[15]Danan G,Benichou C.Causality assessment of adverse reactions to drugs-I.A novel method based on the conclusions of international consensus meetings: application to drug-induced liver injuries[J].J Clin Epidemiol,1993,46(11):1323-1330.
[16]Benichou C1,Danan G,Flahault A.Causality assessment of adverse reactions to drugs-II.An original model for validation of drug causality assessment methods: case reports with positive rechallenge[J].J Clin Epidemiol,1993,46(11):1331-1336.
[17]孫穎,謝歡,王春紅,等.特異質型藥物性肝損傷病因評估及生物標志物的研究進展[J].傳染病信息,2017,30(4):203-208.
[18]Teschke R,Frenzel C,Schulze J,et al.Herbal hepatotoxicity:challenges and pitfalls of causality assessment methods[J].World J Gastroenterol,2013,19(19):2864-2882.
[19]Zhu Y,Niu M,Chen J,et al.Comparison between Chinese herbal medicine and Western medicine-induced liver injury of 1985 patients[J].J Gastroenterol Hepatol,2016,31(8):1476-1482.
[20]Teschke R,Schulze J,Schwarzenboeck A,et al.Herbal hepatotoxicity: suspected cases assessed for alternative causes[J].Eur J Gastroenterol Hepatol,2013,25(9):1093-1098.

