曲妥珠單抗聯合紫杉醇治療對轉移性乳腺癌患者血清CEA、CA-125及CA15-3的影響
陳亮 肖棟 梁明 翟超 張亦磊 鄭明華 韓拓
(西安交通大學醫學院附屬3201醫院腫瘤外科,陜西 漢中 723000)
乳腺癌在臨床上較為常見,是女性惡性腫瘤之一[1],有文獻報道,乳腺癌占各種女性惡性腫瘤的25%左右[2],其臨床轉移率和復發率較高。有資料統計,乳腺癌的臨床發病率與各種女性惡性腫瘤相比,發病率最高[3]。近年來患者的發病年齡趨于年輕化,乳腺癌危害著女性患者的身體健康,臨床上診斷乳腺癌主要通過病理學的方式,患者一旦確診為乳腺癌,常常為癌癥晚期,最佳的治療時機已經錯過[4]。有研究認為,早期診斷、發現并及時進行治療能提高臨床療效和改善預后[5]。臨床研究發現,腫瘤標志物的檢測能有效反映機體因癌癥而導致腫瘤標志物水平異常[6],能為乳腺癌的診斷、治療、復發以及轉移監測等提供依據。本研究旨在分析曲妥珠單抗聯合紫杉醇對轉移性乳腺癌患者血清CEA、CA-125及CA15-3的影響,現報告如下。
1 資料與方法
1.1 一般資料 收集2014年3月~2016年3月來我院接受診治的患者中,選取80例轉移性乳腺癌患者進行研究,回顧性分析所有患者的臨床資料,將患者按隨機數表法均分為兩組,每組各40例。觀察組患者實行曲妥珠單抗聯合紫杉醇治療,對照組患者使用單純的曲妥珠單抗進行治療,本次入選的患者納入標準[7]:①經X線、B超證實為轉移性乳腺癌,并且原發性腫瘤大于2cm;②患者生存期在3個月以上;③患者的超聲檢查顯示具有可評價的病灶;④患者的血常規、心電圖以及肝腎功能基本正常;⑤本次研究內容所有患者均知情并簽署同意書,我院倫理委員會同意并批準本次研究。排除標準:①在治療前接受過放療或化療的患者;②患者經檢測顯示肝腎功能異常;③患者還患有其他的惡性腫瘤;④對本次研究涉及的有關藥物過敏。其中,觀察組患者年齡18~66歲,平均年齡為(48.71±5.30)歲,轉移部位數:1個6例,2個12例,3個19例,4個3例。對照組患者年齡在19~67歲,平均年齡為(49.10±5.44)歲,轉移部位數:1個5例,2個13例,3個17例,4個5例。兩組患者的一般資料比較差異無統計學意義(P>0.05),兩組具有可比性。
1.2 方法 觀察組和對照組患者采用的曲妥珠單抗(赫賽汀,Genentech Inc,批準文號:國藥準字J20110020)使用方法和劑量等均相同,曲妥珠單抗使用劑量和方法具體如下:首次使用劑量為9mg/kg,之后的劑量保持在6mg/kg,將其溶于生理鹽水中,在90min內滴完,藥物不可快速滴注或靜脈注射。在首次滴注曲妥珠單抗時,要對患者進行6小時的觀察,如無不良事件的發生,則可以開始后續用藥,第二次用藥的觀察期可以縮短到2小時。根據患者的實際體重,計算曲妥珠單抗使用的總量,并且無上限和下限,除此之外,治療期間患者體重變化在10%以上,無論其體重是增加或減少,均應重新計算曲妥珠單抗的總量,3周重復一次。
觀察組患者為聯合用藥,在患者首次給予曲妥珠單抗的前一天,靜脈給予患者175mg/m2的紫杉醇(安素泰,Hospira Australia Pty Ltd,批準文號:進口藥品注冊證號H20090175),之后的紫杉醇用藥與曲妥珠單抗均為同一天,間隔3周,并且曲妥珠單抗給予30min后在進行紫杉醇滴注。3周重復一次,為一個療程,并且每位患者均治療2個療程以上。患者在每個療程后進行一次常規檢查。如果用藥后有效的患者,應該連續進行治療,直到病情發生變化或者達到相應的基線標準。每位患者均要進行3個療程以上的治療,治療后記錄患者的臨床療效及不良反應等。兩組患者的血清CEA、CA-125及CA15-3水平檢測,在清晨空腹采集其靜脈血5ml,使用電化學發光法進行檢測,檢測均按照說明書進行。
1.3 觀察指標 兩組患者治療后的血清CEA、CA-125及CA15-3水平變化情況比較;兩組患者治療后的近期臨床療效情況比較;兩組患者治療后發生的不良反應情況比較。
1.4 評定標準 近期臨床療效根據WHO實體瘤治療后的療效標準進行評定[8]:(完全緩解(CR),腫瘤病灶消失,并無新病灶出現;(部分緩解(PR),腫瘤病灶最大徑減少大于30%;(穩定(SD),腫瘤病灶最大徑減少大小于于30%,或增大小于20%;進展(PD),腫瘤病灶最大徑增大大于20%,或者有新病灶出現。總有效率=(CR+PR)例數/總例數。血清CEA基線水平大于5ng/ml為異常,小于等于5ng/ml為正常;血清CA-125基線水平大于35U/ml為異常,小于等于35U/ml為正常;血清CA15-3基線水平大于32U/ml為異常,小于等于32U/ml為正常[9]。
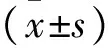
2 結果
2.1 兩組治療后血清CEA、CA-125及CA15-3水平變化情況比較 兩組治療前后的血清CEA、CA-125及CA15-3水平差異變化明顯,并且觀察組治療后的血清CEA、CA-125及CA15-3水平低于對照組,差異有統計學意義(P<0.05),見表1。
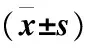
表1 兩組治療后的血清CEA、CA-125及CA15-3水平變化情況比較Table 1 Changes of serum CEA, CA-125 and CA15-3 levels in the two groups after treatment
注:t、P為觀察組和對照組經過治療后的血清CEA、CA-125及CA15-3水平對比,P<0.05
2.2 兩組治療后的近期臨床療效情況比較 觀察組的有效率高于對照組,差異有統計學意義(P<0.05),見表2。
2.3 兩組發生的不良反應比較 兩組治療后均有皮疹、惡心嘔吐、中性粒細胞減少以及腹瀉不良反應的情況發生;兩組不良反應比較差異無統計學意義(P>0.05),見表3。

表2 兩組治療后的近期臨床療效情況比較[n×(10-2)]Table 2 Comparison of the short-term clinical efficacy of the two groups after treatment

表3 兩組發生的不良反應比較[n×(10-2)]Table 3 Comparison of adverse reactions between the two groups
3 討論
女性惡性腫瘤中乳腺癌的發病率為第一位,其威脅著女性患者的身體健康,臨床上診斷乳腺癌主要通過病理學的方式,患者一旦確診為乳腺癌,常常為癌癥晚期,最佳的治療時機已經錯過[10]。臨床常采用放療、手術、化療和生物治療等方法治療乳腺癌,其中綜合治療在乳腺癌有著重要地位[11-12]。有文獻報道顯示,生物治療治療乳腺癌應用較為廣泛的藥物主要有曲妥珠單抗、阿瓦斯汀以及拉帕替尼等[13-14]。曲妥珠單抗是第一個用于臨床靶向治療的人源化單抗藥物,常用于轉移性乳腺癌的治療,其主要作用機制為與機體內的受體相結合,防止機體自身磷酸化和形成異源二聚體,從而抑制患者腫瘤細胞發生增殖[15]。
乳腺癌的臨床轉移率和復發率較高。因此,及早預防、診斷及治療,對患者的臨床療效、生存期以及生活質量都有十分重要的意義[16]。目前常用的診斷乳腺癌的方法有病理學方法、影像診斷技術、腫瘤標志物檢測法等[17-18]。有研究報道,腫瘤標志物的種類較多,主要有癌胎抗原性、酶類、糖類抗原志物等[19]。大量的研究顯示,臨床上常用的較為理想的腫瘤標志物均有以下幾個特征[20]:①特異性較好,此類標志物可以很好的將腫瘤與非腫瘤區分出來;②衰期較短,此類標志物其水平的上升或下降,可以作為判斷治療效果、腫瘤的轉移以及復發等情況;③靈敏度較高,此類標志物能使腫瘤盡早的被發現,進行早期診斷;④有器官特異性,此類標志物可以用于腫瘤定位;⑤檢測其水平能判斷腫瘤的分期、大小、預后等情況。CEA屬于酸性糖蛋白,是非特異性腫瘤標志物之一,其對乳腺癌雖無特異性,但是其水平的異常與檢測腫瘤標志物來預防、診斷、療效評定以及預后分析患者的生存率相關,是檢測腫瘤臨床分期、治療的療效以及預后的重要指標,有較高臨床價值[21]。CA-125是光譜標志物的一種,在癌癥患者中其水平會顯示不同程度的升高,其用于臨床判斷乳腺癌的價值較高[22]。CA15-3位于患者腫瘤細胞表面,當患者細胞癌變時,其含量升高,CA15-3水平能反映腫瘤的惡化或者緩解情況,可用于監測乳腺癌術后是否復發[23]。
研究顯示,單獨使用曲妥珠單抗的有效率在40%左右[24],但其與紫杉醇、多西他賽以及鉑類藥物聯合使用具有協同增效的作用,聯合使用的臨床療效更加顯著[25]。本次研究顯示聯合使用藥物的協同作用;另外,本次研究發現聯合使用藥物和單獨使用藥物均有皮疹、惡心嘔吐、中性粒細胞減少以及腹瀉不良反應情況發生。聯合使用藥物的患者與單獨使用藥物的患者不良反應比較間差異并不明顯,所有患者的不良反應均在可控范圍之內,以上的結果均與以往的報道相符。
4 結論
采用曲妥珠單抗聯合紫杉醇的方案治療轉移性乳腺癌患者,可有效降低患者血清CEA、CA-125及CA15-3水平,兩種藥物聯合使用能發揮協同作用,副作用較小,不良反應發生的幾率較低,值得臨床推廣使用。
【參考文獻】
[1]胡愛玲.曲妥珠單抗聯合含紫杉類方案治療HER -2陽性晚期乳腺癌療效觀察[J].現代中西醫結合雜志,2015 ,1(35):3948-3950.
[2]劉立川,袁欣.曲妥珠單抗聯合紫杉醇治療CerbB-2基因過表達的轉移性乳腺癌[J].中國藥物與臨床,2014,14(2) :248-249.
[3]王坤.帕妥珠單抗聯合曲妥珠單抗和多西紫杉醇一線治療轉移性乳腺癌提高患者的總生存期[J].循證醫學,2015,15(2):66.
[4]魏娜,倪青,戴民.術前應用曲妥珠單抗聯合新輔助化療對乳腺癌患者血清中血管新生因子及乳腺組織中凋亡相關分子的影響[J].中國現代醫學雜志,2015,25(22):46-49.
[5]黃香,吳昊,李薇等.曲妥珠單抗聯合紫杉醇脂質體和卡培他濱治療HER-2陽性復發轉移性乳腺癌[J].實用腫瘤雜志,2016,31(6):550-554.
[6]郝立群, 趙輝, 楊永凈,等.Her-2陽性轉移性乳腺癌的生物靶向治療[J].現代腫瘤醫學,2016,24(8):1227-1229.
[7]田奕,王平,馬麗君.應用曲妥珠單抗聯合多西紫杉醇治療HER-2過表達乳腺癌患者的療效觀察及不良反應的護理[J].中國煤炭工業醫學雜志,2014,17 (7):1178-1179.
[8]張鋼齡,張培禮,朱敬軍,等. 紫杉醇聯合卡鉑單周新輔助化療加曲妥珠單抗在HER2陽性乳腺癌的探討[J].中國中西醫結合外科雜志,2015,21(5):463-466.
[9]朱華云,孫小峰,陳嘉,等.曲妥珠單抗聯合白蛋白結合型紫杉醇治療晚期乳腺癌的療效和安全性[J].徐州醫學院學報,2015,2 (11):752-755.
[10] Ikeda T,Jinno A,Matsu A. The role of neoadjuvant chemotherapy for breast cancer treatment[J].Breast Cancer,2014,9(1):1535-1537.
[11] 楊立平.曲妥珠單抗聯合不同化療藥物治療乳腺癌的臨床療效[J].醫學臨床研究,2015,3(8):1684-1686.
[12] Castaneda SA, Strasser J. Updates in the Treatment of Breast Cancer with Radiotherapy[J]. Surg Oncol Clin N Am, 2017, 26(3):371-382.
[13] 嚴穎,李惠平,邸立軍,等.曲妥珠單抗治療后進展的轉移性乳腺癌繼續曲妥珠單抗治療的療效及安全性分析[J].癌癥進展.2016,14 (12):796-798.
[14] Ma S, Henson ES, Chen Y,etal. Ferroptosis is induced following siramesine and lapatinib treatment of breast cancer cells[J]. Cell Death Dis, 2016, 7(7):e2307.
[15] 李麗,秦建偉,韋達,等.曲妥珠單抗在乳腺癌新輔助化療中的應用[J].腫瘤,2014 ,34 (11):396-398.
[16] 陳士華.聯合檢測CA15-3、CA125、CEA對乳腺癌的臨床價值探討[J].檢驗醫學,2016,28(3):235-237.
[17] Taylor D, Lazberger J, Ives A,etal. Reducing delay in the diagnosis of pregnancy-associated breast cancer: How imaging can help us[J]. J Med Imaging Radiat Oncol, 2015, 55(1):33-42.
[18] Brouckaert O,Laenen A,Wildiers H,etal.The prognostic role of preoperative and (early) postoperatively change in CA15.3 serum levels in a single hospital cohort of primary operable breast cancers[J].The Breast,2013,3(3):320-325.
[19] 廖洪宇,龔建.血清CA15-3、CA125、CEA和PRL水平與乳腺癌及骨轉移的關系[J].蚌埠醫學院學報,2014,1(10):1418-1420.
[20] 吳曉燕,朱自力,張金業.腫瘤標志物檢測在肺癌診斷中的臨床應用價值探討[J].檢驗醫學,2014,2(5):578-580.
[21] 聶書偉,呂勇剛,易軍.肺癌臨床分期與腫瘤標志物CEA、CA15-3、NSE和CYFRA21-1相關性分析[J].臨床軍醫雜志,2015,40(2):395-398.
[22] 劉苑歡,魏榮興,邱群芳.聯合檢測 CA15-3、CA125、CEA對乳腺癌臨床診斷價值探討[J].實用癌癥雜志,2014,1(4):406-408.
[23] Sandri T,Salvatici M,Botteri E,etal. Prognostic role of CA15.3 in 7942 patients with operable breast cancer [J].Breast cancer research and treatment,2013,1(1):618-622.
[24] 仲崇明,卞光榮,劉小林,等.血清相關腫瘤標志物在乳腺癌診斷的性能評價[J].中國實驗診斷學,2013,15(2):254-256.
[25] 丁金旺,羅定存,葉柳青,等.血清TBX3、CA15-3及CEA聯合檢測對乳腺癌的診斷價值[J].醫學研究雜志,2013,42(4):118-121.

