靜脈注射人免疫球蛋白治療新生兒急性肺損傷/呼吸窘迫綜合征的效果
新生兒急性肺損傷/呼吸窘迫綜合征(acute lung injury/acute respiratory distress syndrome,ALI/ARDS)是新生兒期的危重癥之一,臨床表現為進行性呼吸困難和難以糾正的低氧血癥,病情重,病死率高。ALI/ARDS目前治療以機械通氣+肺表面活性物質(pulmonary surfactant,PS)、抗感染、限制性液體管理策略等綜合治療為主,由于新生兒特殊的病理生理特征,限制了糖皮質激素的使用,因此目前新生兒ALI/ARDS治療大都是機械通氣、PS應用方面的研究報告,而有關抗炎免疫調節治療方面研究甚少。本文旨在探討靜注人免疫球蛋白(intravenous immunoglobulin,IVIG)在新生兒ALI/ARDS抗炎治療中的臨床效果,現報道如下。
1 資料與方法
1.1一般資料選取2014年1月2016年12月在東南大學附屬鹽城醫院兒科收治的ALI/ARDS新生兒 患者60例,所有患兒根據急性肺損傷/急性呼吸窘迫綜合征診斷標準確診[1],患兒入院后均行胸部X線、氧合指數、氧分壓檢查。其中男性35例,女性25例。
原發病包括:新生兒窒息21例、胎糞吸入綜合征11例、新生兒肺炎15例、新生兒膿毒血癥8例、新生兒休克5例。按入院順序將研究對象按隨機數字表法分為治療組和對照組,每組30例,兩組患兒在性別、胎齡、出生體質量、入院時病情嚴重程度:氧合指數(oxygenation index,OI)、動脈/肺泡氧分壓比值(the ratio of arterial/pulmonary oxygen partial pressure, a/A PO2)、胸片病情分級[2](neonatal respiratory distress syndrome,NRDS 等級),差異無統計學意義(P>0.05)。詳見表1。本研究獲得醫院醫學倫理委員會批準及家長知情同意。
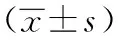
表1 兩組患兒一般情況比較
1.2方法兩組患兒入院后均予機械通氣[同步間歇指令通氣(synchronized imntermittent mandatory ventilation, SIMV)+呼氣末正壓(positive end-expiratory pressure, PEEP),呼吸機參數根據患兒的胎齡、體質量和NRDS病情分級設定]+PS[意大利Chiesi公司生產的固爾蘇(Curosurf),單次劑量100 mg/kg,經氣管插管給藥],同時給予哌拉西林鈉他唑巴坦鈉(華北制藥股份有限公司,50 mg/kg 靜脈滴注2次/天,連用5~7 d)抗感染及營養支持[按照熱卡70~90 cal/(kg·d)給予鼻飼喂養或靜脈腸外營養支持]等對癥治療;治療組加用IVIG(山東泰邦生物制品有限公司,國藥準字S20013001)靜脈滴注治療1 g/(kg·d),連用2天。
1.3觀察指標及檢測方法記錄兩組患兒機械通氣時間、住院時間、病死率及機械通氣前、通氣后 24、48及72小時抽取靜脈血2 mL檢測血清白細胞介素6(interleukin 6,IL-6)、IL-10、腫瘤壞死因子(tumor necrosis factor, TNF-α)值,觀察兩組患兒癥狀、體征,比較病情改善情況,根據病情需要檢查血常規、胸片、心臟彩超、顱腦CT等,觀察并明確是否有血細胞減少、皮疹、心動過速、腹脹、痙攣等不良反應,以及氣胸、呼吸機相關的肺炎、肺出血、顱內出血、動脈導管未閉等并發癥。IL-6、IL-10、TNF-α采用酶聯免疫吸附法(enzyme-linked immune sorbent assay, ELISA)檢測,試劑盒為北京博凌科為生物科技有限公司生產,嚴格按操作說明書操作。
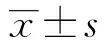
2 結果
2.1兩組患兒治療前后血IL-6、TNF-α、IL-10值比較兩組患兒血清IL-6、TNF-α水平均隨治療時間逐漸減低,且治療組較對照組降低幅度大(P<0.05);而IL-10水平隨治療時間而增高,且治療組患兒增高幅度較對照組大(P<0.05)。詳見表2。
2.2兩組患兒呼吸機機械通氣時間、住院時間比較治療組機械通氣時間、住院時間均低于對照組,差異有統計學意義 (P<0.05)。 詳見表3。
2.3兩組患兒住院期間不良反應、并發癥及病死率比較治療組有2例患兒在滴注IVIG時有面色發紅,減慢滴注速度自行緩解;治療組并發癥5例(氣胸1例,肺炎3例,顱內出血1例),對照組并發癥6例(氣胸2例,肺炎2例,顱內出血1例,肺出血1例),并發癥的發生率差異無統計學意義(χ2=0.111,P>0.05)。治療組住院期間死亡2例,對照組死亡8例,治療組患兒住院病死率低于對照組,差異有統計學意義(χ2=4.32,P<0.05)。
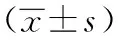
表2 兩組ALI/ARDS患兒治療前后炎癥指標變化
表3兩組患兒呼吸機機械通氣時間、住院時間比較

組別例數機械通氣時間(h)住院時間(d)對照組3075.70±13.3022.46±4.47治療組3055.33±13.1717.46±4.71t值5.9594.217P值<0.001<0.001
3 討論
ALI/ARDS是指由心源性以外的各種肺內、外致病因素導致的急性、進行性呼吸衰竭。ALI/ARDS發病機制雖然尚不十分明確,但目前公認ALI/ARDS是全身炎癥反應綜合征(systemic inflammatory response syndrome,SIRS)[3]和多臟器功能障礙綜合征(multiple organ dysfunction syndrome, MODS)最常見的靶器官損害表現,換言之,ALI/ARDS是全身性的綜合征[4]。在ALI和ARDS發作時機體存在SIRS和宿主過分的防御反應,如果SIRS和宿主過分的防御反應不能得到有效控制,會導致持續的嚴重反應(免疫反應、組織及內皮細胞的損傷、微血栓形成、高代謝狀態、循環異常等)、細胞的增殖和肺纖維化,引起肺部不可逆損傷。因此,在ALI/ARDS治療中除機械通氣呼吸支持治療,全身的抗炎治療也越來越引起臨床的重視。全身性非特異性抗炎治療包括使用糖皮質激素、免疫球蛋白、非類固醇抗炎制劑治療。在成人ICU中ALI/ARDS患者糖皮質激素治療使用廣泛而且療效肯定。但由于新生兒特殊的病理生理特點,使用糖皮質激素可能存在一系列不良反應,包括高血壓、高血糖、應激性潰瘍、新生兒壞死性小腸結腸炎和遠期的神經系統損害等,新生兒尤其是早產兒應避免使用糖皮質激素。而非類固醇抗炎制劑因其對胃腸道粘膜的損傷和肝腎毒性也不宜在新生兒中使用。
IVIG是從健康人血液中提取的血漿制品,含有正常人血漿中所含有部分特異性抗體成分,其中主要是IgG及少許的IgA、IgM。IVIG具有免疫調節的功能,因此,廣泛應用于各種感染性疾病和自身免疫性疾病如膿毒血癥[5]、特發性血小板減少性紫癜[6]、川崎病[7]等。本研究治療組加用IVIG治療后,血清中促炎性細胞因子IL-6、TNF-α在治療后24、48及72小時較對照組降低,而血清中抗炎性細胞因子IL-10則升高(P<0.05),表明使用IVIG可抑制新生兒ALI/ARDS機體過度的炎癥反應,阻止病情進展、惡化。其作用機理可能是:①ALI/ARDS發作時,由于存在肺組織的損傷,引起大量的中性粒細胞在短時間內聚集、激活,釋放過多的氧自由基、蛋白酶和炎性細胞因子 (IL-1、IL-6、IL-8、TNF-α等),以及巨噬細胞、肺毛細血管內皮細胞的參與是ALI/ARDS發病的重要細胞學機制。 IVIG具有封閉Fc受體的作用[8],加用IVIG治療后可阻斷中性粒細胞聚結激活,減少促炎癥因子的釋放,減輕機體的炎癥反應,使得治療組血清IL-6、TNF-α隨之降低。②ALI和ARDS為同一疾病過程的2個階段,ALI代表早期和病情相對較輕的階段,而ARDS代表后期病情較嚴重的階段。肺內炎性介質和抗炎介質的平衡失調,是ALI/ARDS發生、發展的關鍵環節。在ALI/ARDS發病時除了促炎性介質增加外,還有IL-4、IL-10、IL-13等抗炎性細胞因子釋放不足。IVIG具有調節炎癥性細胞因子的合成和釋放的作用[6],使用IVIG后不但可以抑制促炎癥介質的分泌,還可以促進抗炎癥介質的釋放,從而調節體內的炎癥介質失衡,阻斷病情的發生發展。③IVIG含有大量的特異性抗體,可以中和多種細胞因子。
本研究結果顯示,新生兒ALI/ARDS在機械通氣等治療的基礎上加用靜注IVIG治療,治療組病死率低于對照組(P<0.05)。而且治療組患兒機械通氣時間、住院天數比對照組顯著縮短(P<0.05)。這是因為IVIG抑制了ALI/ARDS患兒全身過度的炎癥反應,在早期抑制了病情的進展惡化;同時新生兒使用IVIG可以彌補體內免疫球蛋白的不足,特別是大分子的不能通過胎盤屏障的IgM、IgA,通過抗體與抗原的相互作用中和毒素和直接殺死細菌和病毒。
本研究尚有不足之處,首先不同病因所致的ALI/ARDS血液和組織中參與炎癥反應的介質其水平和組成(如TNF-α、IL-1、可溶性黏附分子等)是不同的,其次,納入的研究病例較少,未對ALI/ARDS患兒作肺內源性和肺外源性病因分類,ALI/ARDS遠期后遺癥方面:支氣管肺發育不良(bronchopulmonary dysplasia,BPD)、腦癱等有無差異,還需今后大樣本、長時間的觀察隨訪。
總之,IVIG可縮短新生兒ALI/ARDS的病程,降低病死率,且用藥安全可靠,有望成為新生兒ALI/ARDS的重要治療措施之一。
[1]中華醫學會呼吸學會分會. 急性肺損傷/急性呼吸窘迫綜合癥的診斷標準(草案)[J]. 中華結核和呼吸雜志, 2000(23):203-204.
[4]江載芳,申昆玲,沈穎.諸福棠實用兒科學[M].8版.北京:人民衛生出版社, 2015:453-456.
[3]李敏,劉曉琳. 足月新生兒呼吸窘迫綜合征危險因素分析[J].安徽醫學, 2016,37(3):320-322.
[4]江載芳.實用小兒呼吸病學[M].北京:人民衛生出版社, 2010:145-152.
[5]FRANCO A C, TORRICO A C, MOREIRA F T, et al. Adjuvant use of intravenous immunoglobulin in the treatment of neonatal sepsis:a systematic review with a meta-analysis[J]. J Pediatr (Rio J),2012,88(5):377-383.
[6]ALIOGLU B, ERCAN S, TAPCI A E, et al. A comparison of intravenous immunoglobulin (2 g/kg totally) and single doses of anti-D immunoglobulin at 50 μg/kg, 75 μg/kg in newly diagnosed children with idiopathic thrombocytopenic purpura:Ankara hospital experience[J].Blood Coagul Fibrinolysis, 2013,24(5):505-509.
[7]SEO E, YU J J, JUN H O, et al. Prediction of unresponsiveness to second intravenous immunoglobulin treatment in patients with Kawasaki disease refractory to initial treatment[J]. J Korean J Pediatr, 2016,59(10):408-413.
[8]王玉書, 金吉子,關宏锏. 免疫球蛋白的作用機制及臨床應用研究進展[J]. 延邊大學醫學學報, 2007,30(2):143-145.

