烴分子在H-FAU分子篩上吸附模擬研究
鳳孟龍,龍 軍,周 涵,田輝平,趙 毅
(中國石化石油化工科學研究院,北京 100083)
烴分子在H-FAU分子篩上吸附模擬研究
鳳孟龍,龍 軍,周 涵,田輝平,趙 毅
(中國石化石油化工科學研究院,北京 100083)
利用量子力學與分子力學結合的方法研究C14,C22,C30的直鏈2-烯烴、芳烴、直鏈烷烴、環烷烴在H-FAU分子篩上的吸附特性,烴分子吸附能隨碳數的增加而增大。烴分子吸附在H-FAU分子篩上,烯烴和芳烴雙鍵碳原子因具有π電子與分子篩B酸中心間形成π-H鍵,烷烴、環烷烴與B酸中心間有電子誘導作用,烴分子與分子篩骨架間有范德華作用。烴分子碳數的增加會增大分子與分子篩骨架間的范德華作用,不影響烯烴、芳烴與B酸中心間π-H鍵作用或烷烴、環烷烴與B酸中心間電子誘導作用。不同類型烴分子與分子篩B酸中心間相互作用由大到小的順序為直鏈2-烯烴>芳烴>直鏈烷烴>環烷烴。
吸附能 π-H鍵 電子誘導作用 范德華作用
催化裂化反應中難裂化的稠環芳烴對易裂化組分的競爭吸附效應會降低催化劑活性中心利用率,導致原料油轉化率和輕質油收率降低[1]。增加劑油比,可以增加活性中心數量消除競爭吸附效應,但受到裝置熱平衡的限制,劑油比不能過高。過高劑油比還會造成過度裂化導致干氣、焦炭產率上升,汽油、柴油等輕質油收率降低[2]。因此應對烴分子在分子篩上吸附進行研究,尋找削弱競爭吸附效應的方法,使易裂化烴分子能更容易與活性中心接觸,進行裂化反應,提高催化裂化原料油的轉化率和輕質油收率。現階段關于烴分子在分子篩上的吸附研究方法主要有實驗法(微量熱法[3]、重量法[4]、色譜法[5]、程序升溫脫附法[6]、紅外光譜法[7]和核磁共振法[8]等)和分子模擬法(分子力學法[9]、分子動力學法[10]、蒙特卡羅法[11]、量子力學法和分子力學結合法[12])。利用分子模擬法,在獲得宏觀吸附數據的同時,還能獲得吸附構型、吸附時發生的電子轉移、化學鍵變化等數據,在研究烴分子在分子篩吸附有更廣泛的應用。本課題通過量子力學和分子力學結合法研究C14,C22,C30的直鏈2-烯烴、芳烴、直鏈烷烴、環烷烴在H-FAU分子篩上的吸附特性。
1 模型和模擬方法
1.1 模型化合物的選擇
以C14,C22,C30的直鏈烷烴、直鏈2-烯烴、環烷烴、芳烴為模型化合物,利用 Materials Studio8.0中基于密度泛函理論的Dmol3模塊,對模型化合物的立體構型、電子結構進行優化。計算精度選擇Fine,選用廣義梯度近似GGA的PBE泛函,機組選用DNP,自洽場(SCF)迭代收斂的閥值設為:能量收斂精度1.0×10-5Ha,受力收斂精度0.000 2 Ha/nm,位移收斂精度0.000 5 nm。
1.2 H-FAU型分子篩模型的建立
建立636T(2022個原子)的具有FAU分子篩完整正弦孔道的模型,不飽和的Si原子用H原子飽和,Si—H鍵長固定為0.147 nm。將模型中一個Si原子替換成Al原子,并在與之相連的位于六方棱柱的四元環上O1位置[13-14]的O原子增加一個H原子作為電荷補償,形成B酸中心,見圖1。選取模型中40T(107個原子,球棍模型顯示區域),規定為量子力學區域,模型中其余原子為分子力學區域(線性模型顯示區域),利用Qmera模塊對分子篩模型進行優化,計算精度選擇Fine。

圖1 H-FAU分子篩模型○—H; ●—O; ●—Si; ●—Al
1.3 吸附能計算
利用Qmera模塊對吸附構型進行結構優化,優化后得到吸附構型能量Eadsorption,精度選擇Fine。利用Qmera模塊計算吸附前分子篩的能量Ezeolits和烴分子的能量Emoleculars,根據式(1)計算吸附能Eads:
Eads=Eadsorption-Ezeolits-Emoleculars
(1)
式中:Eads為吸附能;Eadsorption為吸附后吸附構型能量;Ezeolits為吸附前分子篩能量;Emoleculars為吸附前烴分子能量。
1.4 π-H鍵作用能、電子誘導能、范德華作用能的計算

(2)

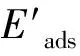
根據式(3)計算Eπ -H(或Eind):
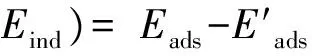
(3)
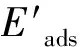
2 結果與討論
2.1 烯烴在H-FAU分子篩上的吸附
直鏈2-烯烴分子吸附在H-FAU分子篩時,烯烴雙鍵與B酸中心形成π-H鍵,烯烴與分子篩骨架間存在長程的范德華作用,因此吸附能(Eads)可以分解為π-H鍵作用能(Eπ -H)和范德華作用能(Evdw)。計算不同碳數的烯烴在H-FAU 分子篩的Eads,Eπ -H,Evdw,結果見表1。由表1可知:隨著碳數的增加烯烴分子的總吸附能增大;比較Eπ -H和Evdw可以看出,Eπ-H隨著碳數的增加基本不變,而Evdw隨著碳數增加顯著增大。這表明烯烴分子碳數的增加并不會增強烯烴分子雙鍵與B酸中心之間的π-H鍵強度而是增強了烯烴分子與分子篩骨架之間的范德華相互作用。比較烯烴分子吸附前后H-FAU分子篩上H1原子的電荷和O1—H1鍵長變化,見圖2和表1。從表1可以看出,2-烯烴分子吸附在H-FAU上形成π-H鍵時,分子篩上的H1原子得到電子,O1—H1鍵伸長。不同碳數2-烯烴分子吸附時分子篩H1原子得電子數和O1—H1鍵長變化量也基本相等。

表1 直鏈2-烯烴在H-FAU上的吸附
2.2 芳烴在H-FAU分子篩上的吸附
芳烴分子吸附在H-FAU分子篩上時,芳烴π電子與B酸中心同樣形成π-H鍵,同時芳烴與分子篩骨架間存在長程的范德華作用。計算不同碳數的烷基苯在H-FAU 分子篩的Eads、Eπ -H和Evdw,結果見表2。由表2可以看出:隨碳數的增加烷基苯的Eads增大;比較Eπ -H和Evdw可以看出,隨著碳數的增加Eπ -H基本保持不變,而Evdw顯著增大。這表明烷基苯分子中側鏈碳數的增加并不會增強烷基苯與活性中心之間的π -H鍵強度而是增強了烷基苯與分子篩骨架之間的范德華相互作用。分析烷基苯分子吸附前后H-FAU分子篩H1原子的電荷和O1—H1鍵長變化,結果見圖3、表2。烷基苯在H-FAU上吸附形成π -H鍵時,分子篩上的H1原子得到電子,O1—H1鍵伸長。不同碳數烷基苯分子吸附時分子篩H1原子得電子數和O1—H1鍵長變化量也基本相等。

表2 烷基苯在H-FAU上的吸附
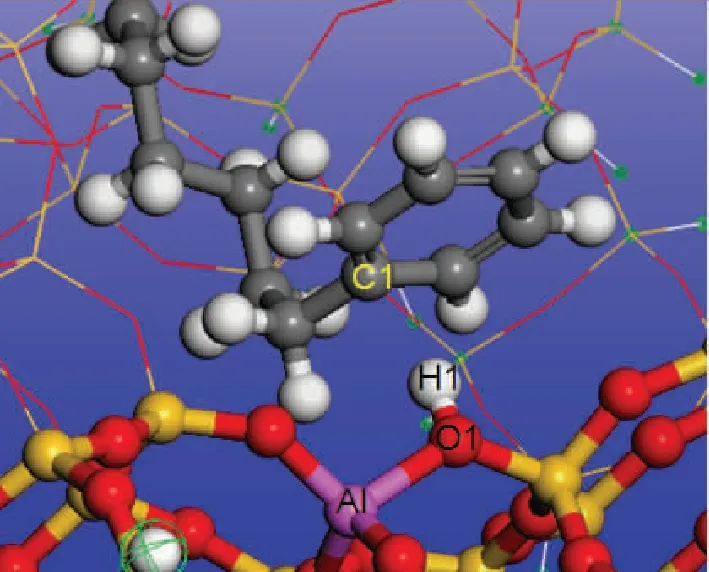
圖3 烷基苯在H-FAU分子篩上的吸附示意
計算不同碳數的烷基萘和烷基蒽在H-FAU分子篩上的Eads,Eπ -H,Evdw,結果見表3,吸附示意見圖4、圖5。由表3可知:隨著碳數的增加,烷基萘和烷基蒽在H-FAU分子篩上Eads增大;比較Eπ -H和Evdw可以看出,烷基萘和烷基蒽與分子篩B酸中心間的Eπ -H隨著碳數的增加基本不變,而Evdw隨著碳數增加顯著增大。這表明側鏈碳數的增加并不會增強烷基萘和烷基蒽與B酸中心之間的π-H鍵作用,而是增強與分子篩骨架之間的范德華相互作用。從表3、圖4、圖5可以看出,不同碳數烷基萘和烷基蒽吸附時,分子篩上H1原子得電子數、O1—H1鍵長變化量基本相等。

表3 烷基萘、烷基蒽在H-FAU上的吸附
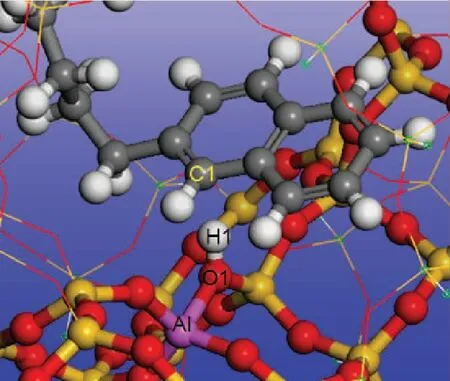
圖4 烷基萘在H-FAU分子篩上的吸附示意

圖5 烷基蒽在H-FAU分子篩上的吸附示意
比較烷基苯、烷基萘和烷基蒽在H-FAU吸附時的Eπ -H可以看出:隨著芳烴環數的增加,π-H鍵作用降低;進一步比較芳烴吸附時分子篩上H1原子的得電子數和O1—H1鍵長變化量可以看出,芳環數量的增加,芳烴在分子篩B酸中心上吸附時H1原子的得電子數和O1—H1鍵長變化量均降低。
2.3 直鏈烷烴在H-FAU分子篩上的吸附
直鏈烷烴分子吸附在H-FAU分子篩上時,分子篩B酸中心通過誘導作用使分布在直鏈烷烴C—H鍵間的電子云發生極化從而得到部分電子,形成電子誘導作用(Eind),直鏈烷烴與分子篩骨架間也存在長程的范德華作用(Evdw)。吸附能(Eads)可以分解為誘導作用能(Eind)和范德華作用能(Evdw)。計算不同碳數的直鏈烷烴在H-FAU 分子篩的Eads,Eind,Evdw,結果見表4。由表4可知:隨著碳數增加,烴分子的總吸附能增大;比較Eind和Evdw可以看出,Eind隨碳數增加變化不大,而Evdw隨碳數增加顯著增大。這表明碳數的增加并不會增強直鏈烷烴分子與B酸中心之間的電子誘導作用而是增強了直鏈烷烴分子與分子篩骨架之間的范德華相互作用。分析直鏈烷烴分子吸附前后H-FAU分子篩上H1原子的電荷和O1—H1鍵長變化,如圖6、表4所示,烴分子吸附在H-FAU上時,分子篩上的H1原子得到電子,O1—H1鍵伸長。不同碳數直鏈烷烴吸附時,分子篩H1原子得電子數和O1—H1鍵長變化量也基本相等。

表4 直連烷烴在H-FAU分子篩上的吸附
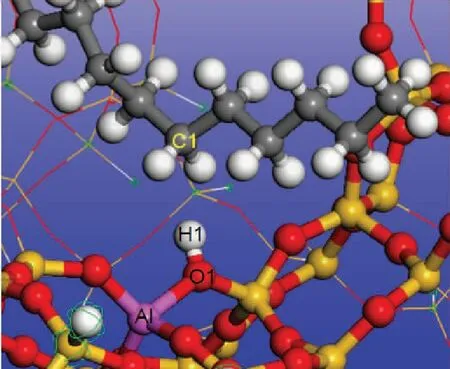
圖6 直鏈烷烴在H-FAU分子篩上的吸附示意
2.4 環烷烴在H-FAU分子篩上的吸附
烷基環己烷吸附在H-FAU分子篩上時,與直鏈烷烴類似,吸附能(Eads)可以分解為誘導作用能(Eind)和范德華作用能(Evdw)。計算不同碳數的烷基環己烷吸附在H-FAU 分子篩的Eads,Eind,Evdw,結果見表5。由表5可知:隨著碳數的增加Eads增大;Eind隨碳數增加基本保持不變,而范德華作用Evdw隨碳數增加顯著增大。這表明烷基環己烷側鏈碳數的增加并不會增強烷基環己烷與B酸中心之間的電子誘導作用而是增強了烷基環己烷與分子篩骨架之間的范德華作用。分析烷基環己烷吸附前后H-FAU分子篩上H1原子的電荷變化和O1—H1鍵長變化,如表5、圖7所示,烷基環己烷在H-FAU上吸附時,分子篩上的H1原子得到電子,O1—H1鍵伸長。不同碳數烷基環己烷吸附時,分子篩H1原子得電子數和O1—H1鍵長變化量也基本一致。

表5 烷基環己烷在H-FAU分子篩上的吸附

圖7 烷基環己烷在H-FAU分子篩上的吸附示意
計算不同碳數的烷基萘烷、烷基全氫蒽在H-FAU分子篩上的Eads,Eind,Evdw,結果見表6。由表6可知:隨著碳數的增加,烷基萘烷和烷基全氫蒽在H-FAU分子篩上Eads增大;比較Eind和Evdw可以看出,烷基萘烷和烷基全氫蒽與分子篩活性中心間的Eind隨著碳數的增加基本保持不變,而Evdw隨著碳數增加顯著增大;這表明側鏈碳數的增加并不會增強烷基萘烷和烷基全氫蒽與B酸中心之間的電子誘導作用而是增強與分子篩骨架之間的范德華作用。烷基萘烷、烷基全氫蒽在H-FAU分子篩上的吸附示意見圖8、圖9。從圖8、圖9、表6可以看出,不同碳數烷基萘烷和烷基全氫蒽吸附時,分子篩上H1原子得電子數、O1—H1鍵長變化量基本相等。

表6 烷基萘烷、烷基全氫蒽在H-FAU上的吸附

圖8 烷基萘烷在H-FAU分子篩上的吸附示意

圖9 烷基全氫蒽在H-FAU分子篩上的吸附示意
比較烷基環己烷與烷基萘烷和烷基全氫蒽與分子篩間的Eind,烷基萘烷和烷基全氫蒽的Eind大于烷基環己烷。比較環烷烴吸附時分子篩上H1原子的得電子數和O1—H1鍵長變化量可以看出,烷基萘烷和烷基全氫蒽吸附時分子篩H1原子得到電子數和O1—H1鍵長變化量均大于烷基環己烷。
2.5不同類型烴分子吸附比較
比較直連2-烯烴、芳烴、直連烷烴和環烷烴在H-FAU上的吸附可以看出,不同類型烴分子吸附能均隨著碳數的增加而增大,但碳數的變化對烴分子與分子篩B酸中心之間的相互作用能影響較小。不同類型烴分子與分子篩B酸中心間相互作用強度存在較大差異,烯烴、芳烴由于其π電子與B酸中心形成π-H鍵作用,與活性中心間相互作用較強。芳烴分子與B酸中心間相互作用弱于烯烴。直連烷烴、環烷烴與B酸中心間具有電子誘導作用,弱于烯烴、芳烴與活性中心形成的π-H鍵作用。直鏈烷烴與B酸中心間的電子誘導作用強于環烷烴。環烷烴中,烷基環己烷與B酸中心間電子誘導作用弱于烷基萘烷、烷基全氫蒽。不同類型烴分子與B酸中心相互作用強度順序為:烯烴>芳烴>直鏈烷烴>環烷烴。
3 結 論
(1)烴分子吸附在H-FAU分子篩上,烯烴、芳烴、直連烷烴、環烷烴分子吸附能均隨著分子碳數的增加逐漸增大。
(2)烯烴、芳烴、直連烷烴、環烷烴分子吸附在H-FAU上,分子碳數的增加只會增加烴分子與分子篩骨架間的范德華作用,對B酸中心與烴分子間的π-H鍵作用或電子誘導作用影響較小。
(3)烴分子與分子篩B酸中心間的相互作用強弱順序為:烯烴>芳烴>直鏈烷烴>環烷烴。
[1] 陳小博,辛利,李楠,等.焦化蠟油中芳香分的催化裂化特性及其對飽和分裂化性能的阻滯作用[J].中國石油大學學報,2014,38(5):190-195
[2] 劉銀東,李澤坤,王剛,等.競爭吸附對催化裂化反應過程的影響[J].化工學報,2008,59(11):2794-2799
[3] Coker E N,Jia Chunjuan,Karge H G.Adsorption of benzene and benzene derivatives onto zeolite H-Y studied by microcalorimetry[J].Langmuir ,2000,16(3):1205-1210
[4] Makowski W,Majda D.Equilibrated thermodesorption studies of adsorption of n-hexane and n-heptane on zeolitesY,ZSM-5 and ZSM-11[J].Applied Surface Science,2005,252(3):707-715
[5] Denayer J F,Souverijns W,Jacobs P A,et al.High-temperature low-pressure adsorption of branched C5—C8alkanes on zeolite beta,ZSM-5,ZSM-22,zeolite Y,and mordenite[J].Phys Chem B ,1998,102(23):4588-4597
[6] Makowski W ,Ogorzalek L.Determination of the adsorption heat ofn-hexane andn-heptane on zeolites beta,L,5A,13X,Y and ZSM-5 by means of quasi-equilibrated temperature-programmed desorption and adsorption(QE-TPDA)[J].Thermochimica Acta ,2007,465(12):30-39
[7] Benaliouche F,Boucheffa Y,Thibault-Starzyk F.In situ FTIR studies of propene adsorption over Ag- and Cu-exchanged Y zeolites[J].Microporous and Mesoporous Materials,2012,147(1):10-16
[8] Zhu Jianfeng,Mosey N,Woo T.Study of the adsorption of toluene in zeolite LiNa-Y by solid-state NMR spectroscopy[J].Phys Chem C,2007,111(36):13427-13436
[9] Nascimento M A C.Computer simulations of the adsorption process of light alkanes in high-silica zeolites[J].Journal of Molecular Structure(Theochem),1999,464(123):239-247
[10] Krishna R,Baten J M.Diffusion of hydrocarbon mixtures in MFI zeolite:Influence of intersection blocking[J].Chemical Engineering Journal,2008,140(1):614-620
[11] Khettar A ,Jalili S E ,Dunne L J.Monte-carlo simulation and mean-field theoryinterpretation of adsorption preference reversal in isotherms of alkane binary mixtures in zeolites at elevated pressures[J].Chemical Physics Letters,2002,362(56):414-418
[12] Raksakoon C,Limtrakul J.Adsorption of aromatic hydrocarbon onto H-ZSM-5 zeolite investigated by Oniom study[J].Journal of Molecular Structure(Theochem),2003,631(123):147-156
[13] Liengme B V,Hall W K.Studies of hydrogen held by solids.Part 11—Interaction of simple olefins and pyridine with decationated zeolites[J].Trans Farady Soc,1966,62:3229-3243
[14] Olson D H ,Dempsey E.The crystal structure of the zeolite hydrogen faujasite[J].Journal of Catalysis ,1969 ,13(2):221-231
SIMULATIONSTUDYOFHYDROCARBONADSORPTIONONH-FAUZEOLITEWTBZ
Feng Menglong, Long Jun, Zhou Han, Tian Huiping, Zhao Yi
(SINOPECResearchInstituteofPetroleumProcessing,Beijing100083)
Molecular simulation methods were used to study the adsorption of different types of hydrocarbons (2-olefins,aromatics,alkanes and cycloalkanes with carbon chain of C14,C22,C30) on H-FAU zeolite.The results show that the adsorption energy increases as the chain length extends from 14 to 30.The π-H bond is formed between the Bronsted acid sites on the zeolite and the π-electronics of olefins and aromatics,while Van der Waals interaction exists between zeolite framework and molecules through the electronic induction between Bronsted acid sites and σ-electronics of alkanes and cycloalkanes.The increase of carbon number in molecular chain has little effect on π-H interaction or electronic induction interaction,but increases the Van der Waals interactions.The intensity of interactions between molecules and acid sites decreases in the following order:olefins>aromatics>alkanes>cycloalkanes.
adsorption energy; π-H bond;electronic induction; Van der Waals interaction
2017-04-21;修改稿收到日期2017-08-09。
鳳孟龍,博士研究生,主要研究VGO分子在FAU分子篩上的擴散和吸附過程。
周涵,E-mail:zhouhan.ripp@sinopec.com。
中國石油化工股份有限公司合同項目(No.YK515026)。

