重組人透明質酸酶促皮下注射擴散研究
姜廷,楊偉,張金龍,呂鵬,侯利華,陳薇
軍事醫學科學院 生物工程研究所,北京 100071
重組人透明質酸酶促皮下注射擴散研究
姜廷,楊偉,張金龍,呂鵬,侯利華,陳薇
軍事醫學科學院 生物工程研究所,北京 100071
目的:探究重組人透明質酸酶(rHuPH20)促皮下注射藥物的擴散能力,解決皮下快速給藥和大體量給藥難題。方法:以臺盼藍模擬聯用藥物作為可視化示蹤劑,研究rHuPH20對皮下注射藥物擴散速率的影響;用生理鹽水造新西蘭兔水腫模型,研究rHuPH20對皮下注射輸液量的影響。結果:rHuPH20可極大地增加皮下注射藥物的擴散速率和輸液量。結論:rHuPH20作為擴散劑使用,可彌補傳統皮下注射微小輸液量的缺陷,滿足皮下注射不同輸液量的需求,在替代藥物靜脈輸液方面具有潛在應用價值。
透明質酸;透明質酸酶;皮下輸液;擴散作用
皮下注射是經典的微量體積注射方式,注射液必須經由皮膚間質進入作用靶點,而這種由膠原蛋白、彈性蛋白、纖維連接蛋白和透明質酸(hy?aluronic acid,HA)等結構性大分子組成的皮膚間質,具有復雜的三維立體結構,限制了皮下注射的擴散速率和輸液量[1]。其中HA是皮膚間質復雜立體結構的“基架”,同時HA的親水性促使水分子嵌入網狀結構內部,構成網狀實體彈性結構,阻礙了注射液的擴散吸收[2]。我們利用重組人透明質酸酶rHuPH20對皮下HA的酶解作用[3],破壞皮膚間質立體結構,降低其結構致密性和黏彈性,進而增加了皮下注射藥物的擴散速率和輸液量。rHuPH20作為擴散劑輔助皮下注射是一種新的皮下給藥方式,相比于傳統皮下注射具有快速擴散吸收、大體量輸液和高生物利用度等優勢,滿足了大體量皮下注射和快速給藥的需求。
1 材料與方法
1.1 材料
新西蘭兔(雄性,3 kg)購自中國食品藥品檢定研究院;BALB/c裸鼠(雄性,7周齡)購自北京維通利華實驗動物技術有限公司;rHuPH20(1.1×105U/mg)由軍事醫學科學院生物工程研究所抗體與疫苗研究室制備和提供;移液器為Gilson公司產品;臺式離心機為Hitachi公司產品;鹽酸氯胺酮購自福建古田藥業有限公司;臺盼藍購自Sigma公司;注射用生理鹽水購自國藥集團化學試劑有限公司;其他試劑為國產分析純產品。
1.2 rHuPH20促皮下注射擴散效果觀察
以BALB/c裸鼠為研究對象,以臺盼藍模擬聯用藥物作為可視化示蹤劑,通過監測臺盼藍的擴散速率,評價rHuPH20的促擴散作用。將BALB/c裸鼠隨機分成5組,每組8只(表1),稱重后,腹腔注射鹽酸氯胺酮(150 mg/kg)麻醉,標記背部正中左側1 cm處為給藥位點,各組給藥位點處皮下注射示蹤染料2%臺盼藍20 μL,1 min后皮下注射rHuPH20,注射結束立刻用卡尺測量臺盼藍染色面積,并以此為初始時間節點,觀察并記錄2、5、10、20、30 min時染色擴散橫向直徑D1和縱向直徑D2,根據面積計算公式(Area=D1×D2×π/4)計算各時間節點的臺盼藍擴散面積。

表1 rHuPH20促皮下注射擴散實驗
1.3 rHuPH20增加皮下注射輸液量和治療皮下水腫藥效評價
以新西蘭兔為研究對象,皮下注射大體量生理鹽水制造水腫模型。造模前預注射rHuPH20,評價rHuPH20對皮下注射輸液量的影響;造模后注射rHuPH20,以水腫體積為指標,評價rHuPH20治療水腫的藥效。耳緣靜脈注射鹽酸氯胺酮(150 mg/kg)麻醉新西蘭兔,徹底麻醉后用剃毛器剃除背部及左側絨毛,裸露表皮,背部正中左側2 cm處標記注射位點,進行皮下注射,記錄水腫體積。實驗分為3組:第1組皮下注射生理鹽水125 mL(對照);第2組皮下注射生理鹽水125 mL,水腫模型完成后,注射 100 μL rHuPH20(1000 IU/mL)(考察rHuPH20治療皮下水腫效果);第3組預先注射100 μL rHuPH20(1000 IU/mL),2 min后皮下注射生理鹽水125 mL(考察rHuPH20對皮下注射輸液量的影響)。
2 結果
2.1 rHuPH20促皮下注射擴散作用
如圖1,時間節點為10 min時,注射rHuPH20各組示蹤染料擴散面積顯著大于對照組,且高劑量rHuPH20組示蹤染料擴散面積高于低劑量組,證明rHuPH20促進皮下注射藥物擴散,且具有一定的劑量依賴性。
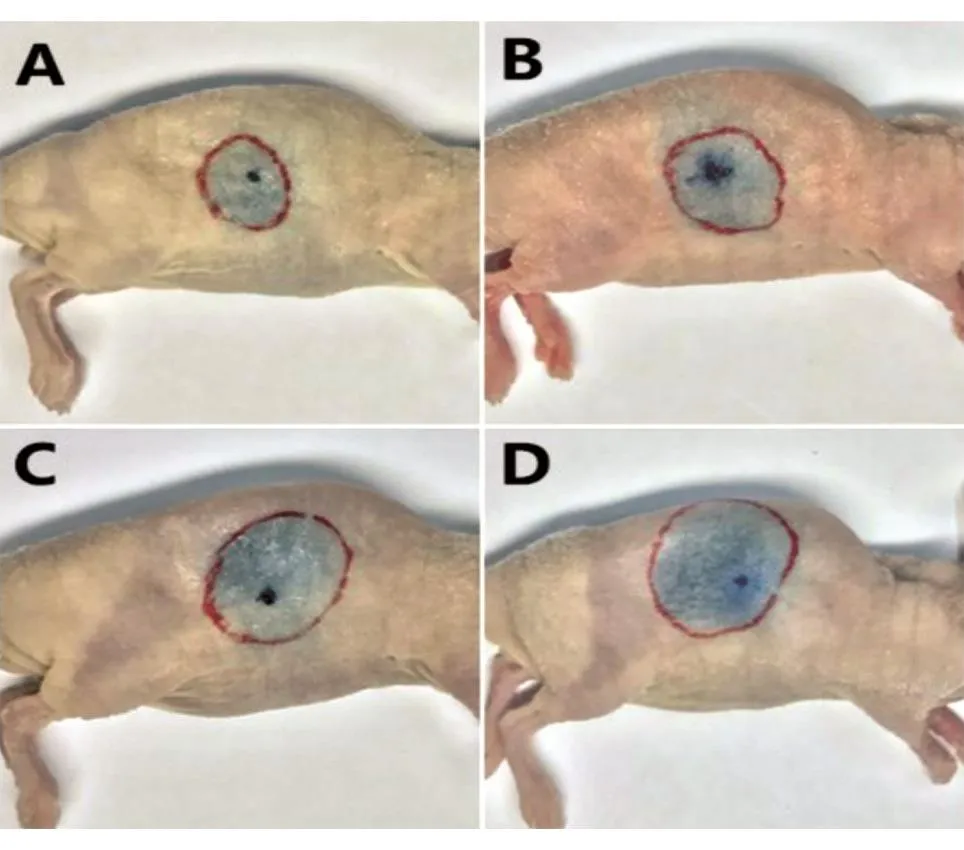
圖1 rHuPH20促皮下注射藥物擴散實驗
采用二維測量法測定不同時間皮下注射示蹤染料的擴散面積(表2)。0 min時,各組之間的臺盼藍擴散面積差異無統計學意義(P>0.05),即初始擴散面積無顯著性差異;測量擴散終點(30 min)時,各rHuPH20注射組與對照組示蹤染料擴散面積差異有統計學意義(P<0.05),其中10 U、50 U和100 U rHuPH20組分別為對照組擴散面積的157%、173%和173%。表明rHuPH20具有良好的促擴散作用。

表2 不同劑量rHuPH20對臺盼藍擴散的影響
為進一步研究rHuPH20酶活濃度與擴散速率的關系,對各組數據進行了深度分析。統計不同酶解時間臺盼藍擴散面積增加量與初始面積的百分比,獲得各組在不同時間節點內臺盼藍的擴散速率,并繪制擴散速率曲線圖(圖2)。不同酶解時間示蹤染料擴散速率數據類型為一個重復測量因素的兩因素設計一元定量資料,統計方法為混合效應模型法(mixed effects model),以P<0.05為差異有統計學意義,統計軟件為SAS 9.2(表3)。各酶解時間節點組間兩兩比較結果表明,2 min時,各組之間的臺盼藍擴散速率有顯著性差異(P<0.05),表明擴散速率與rHuPH20酶活濃度具有劑量關系,經100 U rHuPH20處理后臺盼藍擴散速率為對照組的748%;10、20和30 min時,50 U和100 U rHuPH20組促臺盼藍擴散速率無顯著差異(P>0.05);30 min時,10 U 和 50 U rHuPH20組、50 U和100 U rHuPH20組擴散作用無顯著性差異(P>0.05),表明rHuPH20促擴散作用隨時間推移逐漸降低。

圖2 不同時間節點擴散面積增加量與初始面積的百分比
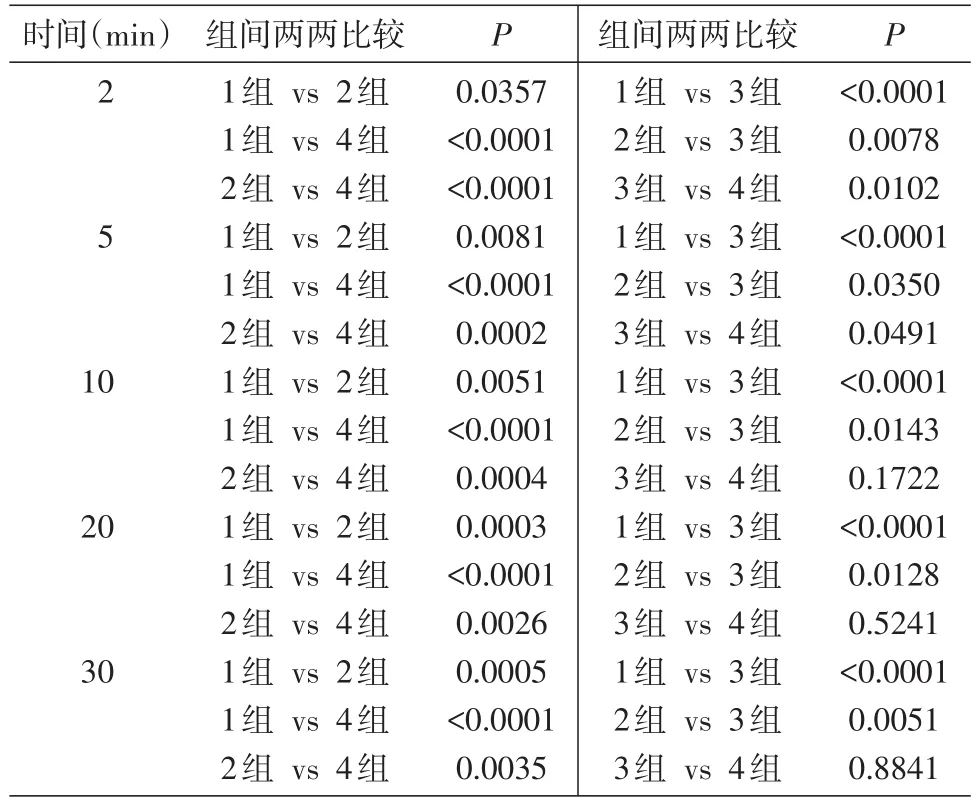
表3 組間兩兩比較統計結果
2.2 rHuPH20治療皮下水腫和增加皮下注射輸液量
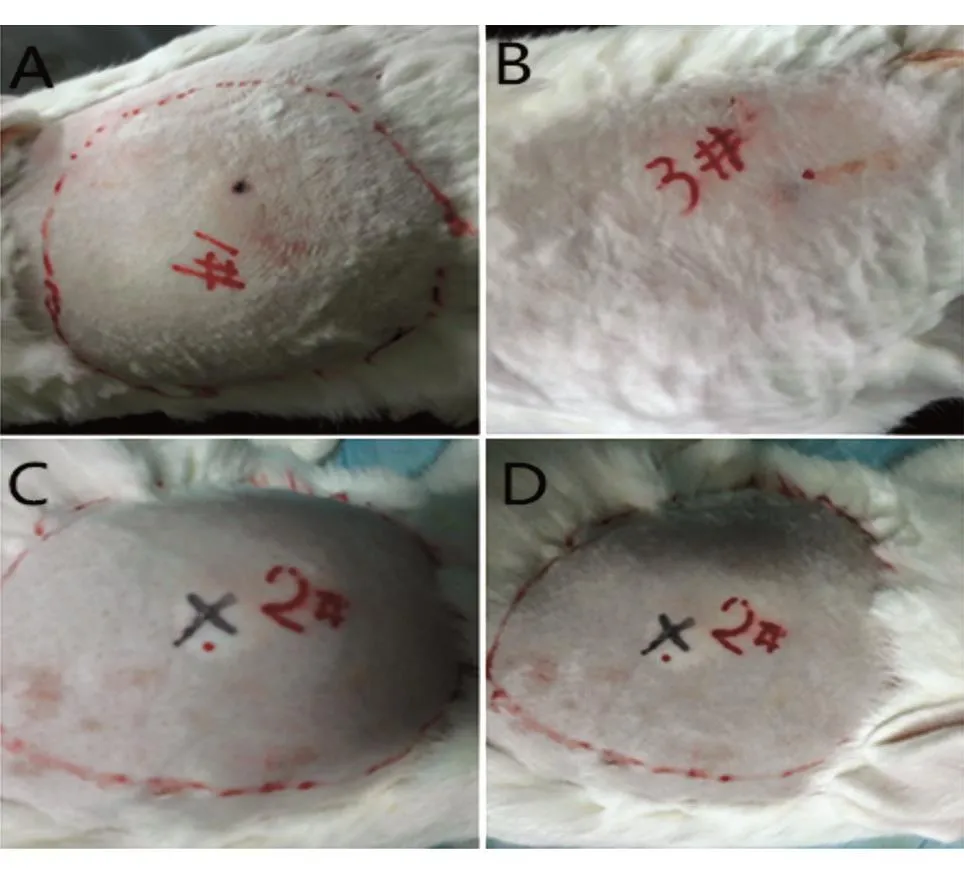
圖3 新西蘭兔脊背左側大體量注射生理鹽水制造水腫模型,造模前注射和造模后注射rHuPH20對水腫體積的影響
如圖3A所示,皮下注射生理鹽水125 mL造成局部皮下水腫,水腫體積為60.2 cm3(約10 h后水腫消失,解剖發現皮下有塊狀白色凝膠);而造模前預注射 100 μL rHuPH20(1000 IU/mL)2 min后,皮下注射生理鹽水125 mL未發生組織形變和腫脹(圖3B),表明在不引起組織損傷的條件下,rHuPH20可顯著提高皮下注射輸液量。皮下注射生理鹽水125 mL后,造成局部皮下水腫,水腫體積為70.2 cm3(圖3C);而造模后注射100 μL rHuPH20(1000 IU/mL),局部皮下水腫逐漸減小,20 min后水腫消失(圖3D),證明rHuPH20可以有效治療局部皮下水腫。
3 討論
自1940年始,從動物組織提取的透明質酸酶已應用于臨床實驗性治療,但低純度引起的高免疫原性和毒性作用限制了其在臨床上的推廣。21世紀初,美國Halozym公司利用基因重組技術在CHO細胞中表達了rHuPH20,并于2005年經美國FDA批準成為第一個上市的rHuPH20藥物,隨后rHuPH20注射劑和PEG-rHuPH20相繼于2010和2016年上市,但國內在rHuPH20制劑上還存在空白。本實驗室建立了高純度rHuPH20制備方法,擬利用rHuPH20解決皮下注射快速給藥和大體量輸液難題。我們用rHuPH20酶解皮膚間質中的HA,破壞了皮膚間質結構致密性和黏彈性,顯著提高了皮下注射藥物的擴散速率和輸液量。在本實驗條件下,100 U rHuPH20預處理后皮下注射示蹤染料初始擴散速率可提高6.48倍,經條件優化后可得到10倍甚至幾十倍初始擴散速率,在急性病癥治療和三防(防生、防化、防核)解毒中具有潛在應用價值。同時,rHuPH20在體內半衰期較短[4],意味著rHuPH20可能帶來的皮膚組織損傷和炎癥反應極小。
rHuPH20作為輔助擴散劑用于皮下注射是一種新型的“大體量皮下給藥方式”,相比于靜脈注射,具有技術要求低、操作簡單、成本低廉和輸液效率高等優勢,可替代靜脈注射而成為慢性疾病患者自助型注射類藥物給藥方式,如糖尿病患者注射胰島素[5];替代不便于靜脈注射環境和條件的大體量注射方式,如皮膚燒傷患者的輸液[6];為因溶解度、生物利用度和穩定性等因素限制而不能進行靜脈注射的藥物提供新的給藥途徑。這種大體量注射方式可彌補傳統皮下注射微小輸液量的缺陷,滿足皮下注射不同輸液量的需求。
[1]Bookbinder L H,Hofer A,Haller M F,et al.A re?combinanthuman enzyme for enhanced interstitial transport of therapeutics[J].J Control Rel,2006,114(2):230-241.
[2]Bian S,He M,Sui J,et al.The self-crosslinking smart hyaluronic acid hydrogels as injectable three-di?mensional scaffolds for cell culture[J].Colloids Surf B Biointerfaces,2016,140:392-402.
[3]Chen K J,Sabrina S,Safory N S,et al.Constitutive expression of recombinant human hyaluronidase PH20 by Pichia pastoris[J].J Biosc iBioeng,2016,122(6):673-678.
[4]Vaughn D E,Muchmore D B.Use of recombinant hu?man hyaluronidase to accelerate rapid insulin ana?logue absorption:experience with subcutaneous injec?tion and continuous infusion[J].Endocr Pract,2011,17(6):914-921.
[5]Garg S K,Buse J B,Skyler J S,et al.Subcutaneous injection of hyaluronidase with recombinant human in?sulin compared with insulin lispro in type 1 diabetes[J].Diabetes,Obes Metab,2014,16(11):1065-1069.
[6]Buehner M,Pamplin J,Studer L,et al.Oxalate ne?phropathy after continuous infusion of high-dose vita?min C as an adjunct to burn resuscitation[J].J Burn Care Res,2016,37(4):374-383.
Study of rHuPH20 Pharmacological Property on Facilitat?ing Diffusion of Subcutaneous Injection
JIANG Ting,YANG Wei,ZHANG Jin-Long,LYU Peng,HOU Li-Hua*,CHEN Wei*
Beijing Institute of Biotechnology,Beijing 100071,China
Objective:To study the recombinant human hyaluronidase rHuPH20 property of improving the diffu?sion of subcutaneous injection so as to realize quick subcutaneous injection and high-dose subcutaneous injection.Methods:Trypan blue was used as a visualized tracer to simulate combined medicine to study influence of rH?uPH20 on diffusion rate of subcutaneous injection.The New Zealand rabbit model of subcutaneous oedema was made by subcutaneous injection of saline to study influence of rHuPH20 on doses of subcutaneous injection.Re?sults:Subcutaneous co-administration of rHuPH20 greatly improves diffusion rate and doses of subcutaneous infu?sion.Conclusion:rHuPH20 can be co-administraed as diffusion agent to makes up the defects of traditional sub?cutaneous injection and meet the needs of various doses of subcutaneous injection,which has potential to replace the intravenous infusion.
hyaluronic acid;hyaluronidase;subcutaneous delivery;diffusion
R91;Q75
A
1009-0002(2017)05-0647-04
10.3969/j.issn.1009-
*Co-corresponding authors,HOU Li-Hua,E-mail:houlihua@sina.com;CHEN Wei,E-mail:cw0226@foxmail.com
2017-04-17
姜廷(1986- ),女,碩士研究生,(E-mail)18518920805@163.com
侯利華,(E-mail)houlihua@sina.com;陳薇,(E-mail)cw0226@foxmail.com

