pSilencer 3.1-Sirt3基因RNA干擾表達載體的構建及鑒定
曲 璇,李 軍,馬曉軍,韓洛川,史海龍
(陜西中醫藥大學基礎醫學院生物學教研室,咸陽 712046;*通訊作者,E-mail:quxuan519@163.com)
pSilencer 3.1-Sirt3基因RNA干擾表達載體的構建及鑒定
曲 璇*,李 軍,馬曉軍,韓洛川,史海龍
(陜西中醫藥大學基礎醫學院生物學教研室,咸陽 712046;*通訊作者,E-mail:quxuan519@163.com)
目的 構建Sirt3基因的RNA干擾載體,并在真核細胞中進行pSilencer 3.1-Sirt3的功能鑒定。 方法 利用體外DNA合成技術及液相色譜純化技術合成Sirt3干擾序列,通過酶切將干擾序列連接至pSilencer 3.1載體中,將陽性克隆載體轉入感受態大腸桿菌細胞后,篩選陽性克隆,通過第二代體外DNA測序技術進行序列測定。將測序正確的克隆用于Western blot實驗和real time PCR實驗,以對其在真核細胞中的正確表達和內源性Sirt3的干涉效果進行鑒定。 結果 PCR擴增得到序列測定結果與干擾序列完全一致。構建的pSilencer 3.1-Sirt3質粒在AGS和SGC-7901細胞中進行基因的轉染,pSilencer 3.1-Sirt3能夠有效抑制內源性Sirt3的mRNA水平和蛋白質水平的表達。 結論 成功構建獲得Sirt3干擾載體,并有效降低Sirt3的mRNA和蛋白質水平的表達,為今后Sirt3的功能研究提供良好的基礎。
Sirtuin-3; RNA干擾; 載體構建
自從20世紀70年代在酵母中首次發現兩種組蛋白去乙酰化酶以來,組蛋白乙酰化和去乙酰化的研究越來越受到關注。近年來,人們發現去乙酰化酶Sirtuin-3(Sirt3)具有依賴于NAD的組蛋白去乙酰化酶活性,能夠對乙酰化的線粒體蛋白進行脫乙酰基[1-3]。目前已發現Sirt3主要定位于肝、腦、腎和心臟等富含線粒體的組織器官中[3,4],Sirt3的作用底物有AceCS2、琥珀酸脫氫酶和谷氨酸脫氫酶等重要的能量代謝相關酶類,這對于維持和調節線粒體的正常生理功能具有重要意義[5,6]。大量研究表明,Sirt3可能與細胞生長、衰老、應激反應、能量代謝、DNA的損傷修復、細胞周期調控以及細胞的凋亡密切相關[2,7,8]。
RNA干擾(RNA interference, RNAi)是由雙鏈RNA(double stranded RNA)分子在mRNA水平關閉相應序列基因表達,誘發的特定基因沉默的過程。RNAi技術可造成特異性基因沉默,廣泛應用于基因功能研究中。
因此,基于Sirt3對細胞的重要意義,本研究構建了針對人Sirt3基因的特異性短發卡RNA(short hairpin RNA, shRNA)真核表達載體,并觀察了其在胃癌細胞AGS和SGC-7901中對Sirt3基因表達的抑制作用。這對于進一步研究Sirt3與疾病發生的關系、解讀相關機制、探討其生物學功能均具有重要意義。
1 材料與方法
1.1 細胞及主要試劑
HEK293、AGS和SGC-7901細胞購自中科院細胞庫,由本實驗室凍存;大腸桿菌XL10由第四軍醫大學生物化學與分子生物學實驗室惠贈;干擾質粒pSilencer 3.1-H1 neo及pSilencer 3.1陰性對照載體購自Ambion公司,BamHⅠ和HindⅢ等限制性核酸內切酶、DNA連接酶均購自TaKaRa;質粒提取試劑盒及凝膠回收純化試劑盒均購自U-gene公司;Sirt3單克隆抗體為CST公司產品。
1.2 人Sirt3基因特異性RNAi片段的設計及合成
采用Vector NTI 5.0軟件,根據人Sirt3的cDNA序列和干擾載體的設計要求,設計3對siRNA寡核苷酸鏈(Sirt3-938:5′-CUUGCUGCUGUGGUUGAUTT-3′;Sirt3-1211:5′-GCUUGAUGGACCAGACAAATT-3′;Sirt3-2419:5′-GCGCCUUAAUAAGAACAAATT-3′)。序列由上海生工生物工程公司合成。
1.3 人Sirt3基因siRNA干擾序列的鑒定
將合成的3對Sirt3的siRNA干擾序列轉染胃癌細胞AGS和SGC-7901,按LipofectAMINE2000脂質體轉染試劑盒說明書進行操作。將5×105個AGS和SGC-7901細胞/每孔接種于6孔板,接種后24 h取三對100 nmol/L siRNA序列分別與10 μl的LipofectAMINE2000混勻,進行瞬時轉染。轉染后24 h,收集蛋白檢測Sirt3蛋白水平的表達。
1.4 pSilencer 3.1-Sirt3載體的構建

1.5 LipofectAMINE2000瞬時轉染真核細胞
按LipofectAMINE2000脂質體轉染試劑盒說明書進行操作。將AGS和SGC-7901細胞5×105個/孔接種于6孔板,接種后24 h,取4 μg陰性對照空載體、pSilencer 3.1-Sirt3質粒分別與10 μl的LipofectAMINE2000混勻,20 min后進行瞬時轉染。
1.6 Western blot檢測Sirt3的蛋白水平表達
分別收集25 cm2培養瓶中陰性對照組、pSilencer 3.1-Sirt3干擾組的細胞樣品,用RIPA裂解液裂解細胞,提取蛋白進行定量,加入5×SDS凝膠加樣緩沖液,煮沸5 min,按照蛋白定量結果進行加樣,行12% SDS-PAGE凝膠電泳,采用半干法將蛋白轉移至NC膜上。將NC膜用5%脫脂奶封閉,分別加入Sirt3多抗(1 ∶1 000)和β-actin單抗(1 ∶1 000),室溫孵育1 h,用山羊抗兔或山羊抗小鼠二抗(1 ∶5 000),室溫孵育1 h,用ECL發光,膠片顯色,分析結果。以β-actin為內參照。
1.7 Real-time PCR檢測Sirt3的mRNA水平表達
按TRIzol試劑盒說明書分別提取AGS和SGC-7901細胞組、pcDNA3.1陰性對照載體、pcDNA3.1-Sirt3過表達實驗組樣品的總RNA。按說明書進行RT-PCR,反轉錄合成cDNA的第一條鏈,Sirt3的擴增引物(上游引物:5′-CCCCAAGCCCTTTTTCACTTT-3′;下游引物:5′-CGACACTCTCTC AAGCCCA-3′),PCR擴增條件為:預變性94 ℃持續5 min,變性94 ℃ 30 s、退火55 ℃ 30 s、延伸72 ℃ 30 s,共30個循環,72 ℃延伸7 min。以GAPDH為內參照(上游引物為5′-ACCCAGAAGACTGTGGATGG-3′,下游引物為5′-TCTAGACGGCAGGTCAGGTC-3′)。PCR擴增條件同Sirt3擴增條件相同。以上2對PCR引物均由上海生工生物工程公司合成。PCR結束后,將所得結果按照公式進行數據分析。
2 結果
2.1 人Sirt3干擾序列對Sirt3蛋白水平表達的鑒定
相對于陰性對照組,Sirt3-938、Sirt3-1211和Sirt3-2419三組siRNA轉染至胃癌細胞中,均有效抑制Sirt3蛋白表達(見圖1)。其中Sirt3-938干擾序列作用最明顯,可用于后期實驗研究。
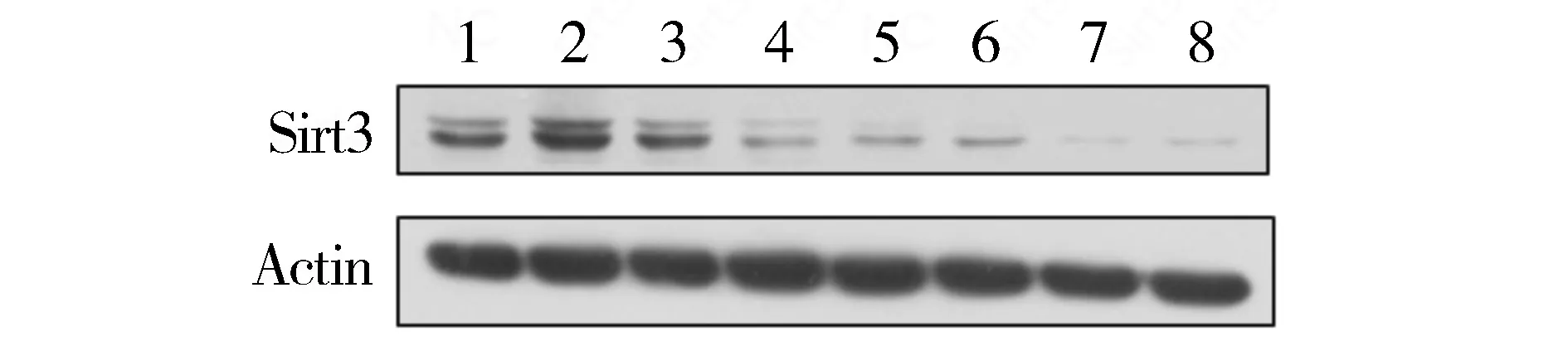
1-4.AGS細胞;5-8.SGC-7901細胞;1,5.陰性對照;2,6.轉染Sirt3-1211;3,7.轉染Sirt3-2419;4,8.轉染Sirt3-938圖1 Sirt3-938、Sirt3-1211 and Sirt3-2419降低Sirt3蛋白水平的表達Figure 1 Sirt3-938,Sirt3-1211 and Sirt3-2419 decreased the protein expression of Sirt3
2.2 人Sirt3基因真核干擾表達載體pSilencer 3.1-Sirt3的構建和鑒定
合成的2條寡核苷酸鏈退火后形成雙黏端的雙鏈DNA片段,將該片段和pSilencer 3.1-H1 neo分別用BamHⅠ和Hind Ⅲ進行雙酶切。最終由T4DNA連接酶將兩者連接后,構成質粒pSilencer 3.1-Sirt3(構建過程見圖2)。為了驗證載體構建是否正確,首先用內切酶BamHⅠ和Hind Ⅲ對pSilencer 3.1-Sirt3進行酶切鑒定,在小于100 bp的位置觀察到目的片段經2%瓊脂糖凝膠電泳,初步證明克隆構建成功。為了進一步驗證,將得到的陽性菌株送上海生工生物工程技術公司測序,證實干擾序列成功插入載體中,pSilencer 3.1-Sirt3干擾載體構建成功。
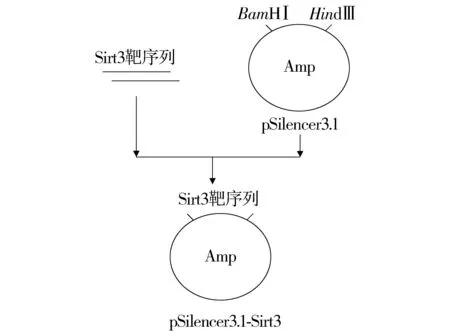
圖2 pSilencer3.1-Sirt3載體的構建Figure 2 The construction of pSilencer3.1-Sirt3
2.3 實時定量PCR檢測Sirt3的mRNA表達水平
按TRIzol試劑盒說明書分別提取AGS和SGC-7901細胞組、陰性對照載體、pSilencer 3.1-Sirt3轉染組樣品的總RNA。按說明書進行RT-PCR,反轉錄合成cDNA的第一條鏈,Sirt3的擴增引物(上游引物:5′-CCGCGGTACCATGGCGTTCTGGGGTTG-3′;下游引物:5′-CCGCTCTAGACTATTTGTCTGGTCCATCAAGC-3′)。PCR擴增條件為:預變性94 ℃ 5 min,變性94 ℃ 30 s、退火55 ℃ 30 s、延伸72 ℃ 30 s,共30個循環,72 ℃延伸7 min。以GAPDH為內參照。PCR結束后,將所得結果按照公式進行數據分析。結果顯示Sirt3干擾載體有效降低Sirt3的mRNA水平(見圖3)。

與對照組比較,*P<0.000 1圖3 pSilencer 3.1-Sirt3在AGS和SGC-7901細胞均能夠顯著降低Sirt3mRNA的表達Figure 3 The pSilencer 3.1-Sirt3 down-regulated the mRNA level of Sirt3 in both AGS and SGC-7901 cells
2.4 Western blot檢測Sirt3蛋白水平的表達
結果表明,干擾載體轉染組細胞的Sirt3蛋白的表達水平明顯受到抑制(見圖4)。這與RNA水平的檢測結果一致,證實Sirt3干擾載體在兩種腫瘤細胞中有效地抑制了Sirt3的蛋白表達。以上結果證明Sirt3干擾載體構建成功,可用于后期實驗研究。
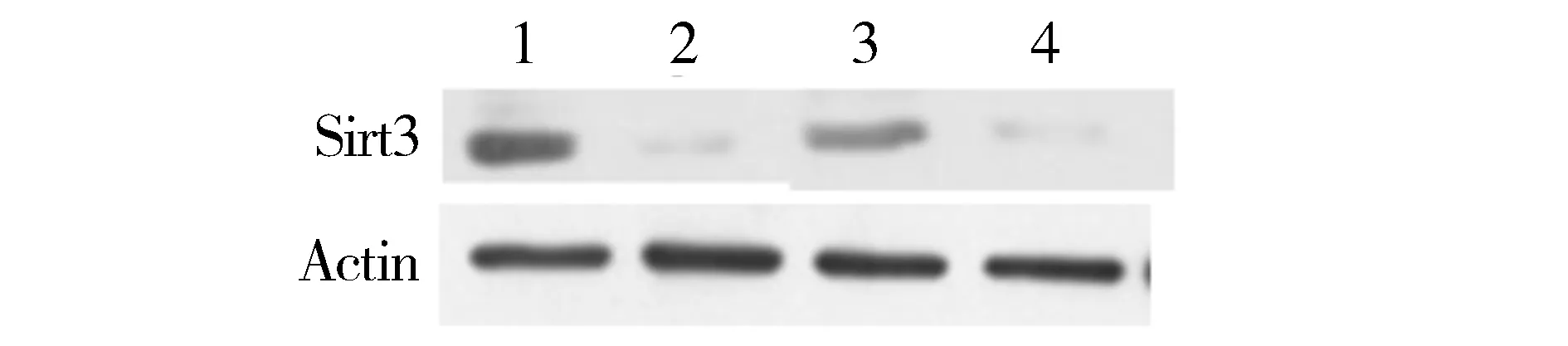
1.AGS陰性對照; 2.AGS細胞轉染pSilencer 3.1-Sirt3;3.SGC-7901陰性對照;4.SGC-7901細胞轉染pSilencer-3.1-Sirt3圖4 pSilencer 3.1-Sirt3降低Sirt3的蛋白水平的表達Figure 4 The pSilencer 3.1-Sirt3 down-regulated the protein level of Sirt3
3 討論
Sirt3是唯一在遺傳學上與人的壽命相關的成員,由于其主要在線粒體定位,因此具有特殊的研究意義[9]。許多研究表明,在應激條件或細胞膜去極化條件下,Sirt3會促進線粒體有氧氧化功能,對于細胞的生存和維持能量的供應必不可缺[7,10]。Sirt3在組織器官中的表達缺陷或突變則與許多疾病的發生密切相關,如心臟功能缺陷、神經退行性病變等[11,12]。活性氧(reactive oxygen species,ROS)是導致細胞損傷的重要因素,目前認為,Sirt3主要從三個方面清除內源性ROS的水平:Sirt3可以通過去乙酰化的方式直接激活超氧化物歧化酶2(superoxide dismutase 2,SOD2),清除ROS[13,14];Sirt3通過增強電子傳遞鏈的功能,提高ATP生成效率,減少ROS生成[15,16];Sirt3通過激活轉錄因子FOXO3A活性,促進抗氧化因子的轉錄和表達[17,18]。此外,最新的研究發現Sirt3在腫瘤細胞中的作用機制也成為科學界的一個研究重點[19]。現已證實SIRT3在基因組穩定性方面可能發揮重要的作用。另外,Sirt3還可以通過破壞HIF-1α的穩定性來介導代謝重組,然后調節糖酵解基因的表達,從而抑制腫瘤的發生,證明了Sirt3在細胞代謝中的重要作用[20]。因此,本研究首先篩選了三對Sirt3干擾序列,從中篩選Sirt3干涉效果最好的一對(Sirt3-938),并將該序列成功插入干涉載體中。結果顯示pSilencer3.1-Sirt3在真核細胞中有效降低內源性Sirt3的mRNA水平和蛋白質水平,這對于進一步研究Sirt3與疾病發生的關系、解讀相關機制、探討其生物學功能均具有重要意義。
[1] Koentges C, Bode C, Bugger H. SIRT3 in cardiac physiology and disease[J]. Front Cardiovasc Med, 2016, 3: 38.
[2] Ashraf N, Zino S, Macintyre A,etal. Altered sirtuin expression is associated with node-positive breast cancer[J]. Br J Cancer, 2006, 95(8): 1056-1061.
[3] Yamamoto H, Schoonjans K, Auwerx J. Sirtuin functions in health and disease[J]. Mol Endocrinol, 2007, 21(8):1745-1755.
[4] Michan S, Sinclair D. Sirtuins in mammals: insights into their biological function[J]. Biochem J, 2007, 404(1):1-13.
[5] Kim HS, Patel K, Muldoon-Jacobs K,etal. SIRT3 is a mitochondria-localized tumor suppressor required for maintenance of mitochondrial integrity and metabolism during stress[J]. Cancer Cell, 2010, 17(1):41-52.
[6] Lu Y, Wang YD, Wang XY,etal. SIRT3 in cardiovascular diseases: Emerging roles and therapeutic implications[J]. Int J Cardiol, 2016, 220:700-705.
[7] Hirschey MD, Shimazu T, Goetzman E,etal. SIRT3 regulates mitochondrial fatty-acid oxidation by reversible enzyme deacetylation[J]. Nature, 2010, 464(7285):121-125.
[8] Hebert AS, Dittenhafer-Reed KE, Yu W,etal. Calorie restriction and SIRT3 trigger global reprogramming of the mitochondrial protein acetylome[J]. Mol Cell, 2013, 49(1):186-199.
[9] Chen J, Wang A, Chen Q. SirT3 and p53 deacetylation in aging and cancer[J]. J Cell Physiol, 2016.
[10] Yang W, Nagasawa K, Munch C,etal. Mitochondrial sirtuin network reveals dynamic SIRT3-dependent deacetylation in response to membrane depolarization[J]. Cell, 2016, 167(4): 985-1000 e21.
[11] Winnik S, Auwerx J, Sinclair DA,etal. Protective effects of sirtuins in cardiovascular diseases: from bench to bedside[J]. Eur Heart J, 2015, 36(48):3404-12.
[12] Kincaid B, Bossy-Wetzel E. Forever young: SIRT3 a shield against mitochondrial meltdown, aging, and neurodegeneration[J]. Front Aging Neurosci, 2013, 5:48.
[13] Qiu X, Brown K, Hirschey MD,etal. Calorie restriction reduces oxidative stress by SIRT3-mediated SOD2 activation[J]. Cell Metab, 2010, 12(6):662-667.
[14] Chen Y, Zhang J, Lin Y,etal. Tumour suppressor SIRT3 deacetylates and activates manganese superoxide dismutase to scavenge ROS[J]. EMBO Rep, 2011, 12(6):534-541.
[15] Ahn BH, Kim HS, Song S,etal. A role for the mitochondrial deacetylase Sirt3 in regulating energy homeostasis[J]. Proc Natl Acad Sci U S A, 2008, 105(38):14447-14452.
[16] Rahman M, Nirala NK, Singh A,etal. Drosophila Sirt2/mammalian SIRT3 deacetylates ATP synthase beta and regulates complex V activity[J]. J Cell Biol, 2014, 206(2):289-305.
[17] Sundaresan NR, Gupta M, Kim G,etal. Sirt3 blocks the cardiac hypertrophic response by augmenting Foxo3a-dependent antioxidant defense mechanisms in mice[J]. J Clin Invest, 2009, 119(9): 2758-2771.
[18] Peserico A, Chiacchiera F, Grossi V,etal. A novel AMPK-dependent FoxO3A-SIRT3 intramitochondrial complex sensing glucose levels[J]. Cell Mol Life Sci, 2013, 70(11):2015-2029.
[19] Ansari A, Rahman MS, Saha SK,etal. Function of the SIRT3 mitochondrial deacetylase in cellular physiology, cancer, and neurodegenerative disease[J]. Aging Cell, 2017, 16(1):4-16.
[20] Finley LW, Carracedo A, Lee J,etal. SIRT3 opposes reprogramming of cancer cell metabolism through HIF1alpha destabilization[J]. Cancer Cell, 2011, 19(3):416-428.
Construction and biological function identification of pSilencer 3.1-Sirt3 vector
QU Xuan*,LI Jun,MA Xiaojun,HAN Luochuan,SHI Hailong
(ShaanxiUniversityofChineseMedical,Xianyang712046,China;*Correspondingauthor,E-mail:quxuan519@163.com)
ObjectiveTo construct the Sirt3 interference vector, and verify its biological function in mammal cells.MethodsThe Sirt3 interference sequence was synthesized byinvitroDNA synthetic technology and liquid chromatogram purification assay. The fragments were inserted into pSilencer 3.1 by digestion and DNA ligation. The resulted plasmid was transformed into competentEscherichiacolicells. The positive clone was selected and sequenced with the second DNA sequencing technology. The correct plasmid was used to observe its expression in eukaryotic cells and the invention efficacy of endogenous Sirt3 by Western blot and real time PCR assays.ResultsThe sequence of the pSilencer 3.1-Sirt3 was consistent with that of the Sirt3 interference sequence. After the pSilencer 3.1-Sirt3 vector was transfected into AGS and SGC-7901 cells, the endogenous Sirt3 mRNA and protein expression was inhibited.ConclusionThe construction of pSilencer 3.1-Sirt3 vector is successfully obtained. The vector of pSilencer 3.1-Sirt3 can efficiently decrease the mRNA and protein expression of Sirt3. The results may provide a basis for the further studies on the roles of Sirt3.
Sirtuin-3(Sirt3); RNA interference; vector construction
國家自然科學基金資助項目(81502370)
曲璇,女,1983-05生,博士,講師,E-mail:quxuan519@163.com
2017-03-02
Q789
A
1007-6611(2017)07-0650-04
10.13753/j.issn.1007-6611.2017.07.003

