間質性肺炎合并侵襲性肺曲霉菌病的死亡危險因素分析
莊誼,劉寅,曹孟淑,張英為,陳露露,肖永龍,蔡后榮,代靜泓
(南京大學醫學院附屬鼓樓醫院呼吸內科,江蘇 南京 210008)
間質性肺炎合并侵襲性肺曲霉菌病的死亡危險因素分析
莊誼,劉寅,曹孟淑,張英為,陳露露,肖永龍,蔡后榮,代靜泓
(南京大學醫學院附屬鼓樓醫院呼吸內科,江蘇 南京 210008)
目的:分析間質性肺炎合并侵襲性肺曲霉病(invasive pulmonary aspergillosis,IPA)的臨床特點和死亡危險因素。方法:回顧性分析2010年12月至2016年4月本院49例間質性肺炎合并IPA患者的臨床資料,以診斷后12周為觀察終點,將患者分為存活組和死亡組,對兩組病例的臨床資料進行對比,分析間質性肺炎合并IPA的死亡危險因素。結果:單因素分析顯示,年齡>65歲、低蛋白血癥、氧合指數<300、胸部CT示彌漫性磨玻璃影和診斷時間>7 d是間質性肺炎合并IPA的死亡危險因素(P<0.05),伏立康唑治療的患者預后較好(P=0.033)。Logistic多因素回歸分析僅發現氧合指數<300是影響間質性肺炎合并IPA患者預后的死亡危險因素(P=0.016,OR=4.833,95%CI:1.669~138.659,β=2.722,SE=1.128,Wald=5.827)。結論:入院時已發生呼吸衰竭是間質性肺炎合并IPA患者死亡的獨立危險因素。
間質性肺炎;侵襲性肺曲霉菌病;死亡危險因素
侵襲性肺曲霉病(invasive pulmonary aspergillosis,IPA)多見于免疫受損患者,特別是粒缺患者,然而非粒缺患者的IPA發病卻逐漸增多。間質性肺炎患者雖然很少合并粒缺的情況,但也易合并IPA[1],且死亡率高[2]。本研究通過回顧性分析單中心的住院間質性肺炎合并IPA病例,了解該類患者的死亡危險因素,為臨床判斷該病患者預后提供參考。
1 資料與方法
1.1 研究對象
以2010年12月至2016年4月南京鼓樓醫院呼吸科住院治療的49例間質性肺炎合并IPA患者為研究對象,收集臨床資料進行回顧性分析。其中確診患者1例,臨床診斷患者48例;年齡(66.96±10.33)歲;男性28例,女性21例;特發性間質性肺炎30例,繼發于結締組織病的間質性肺炎19例(干燥綜合癥5例,類風濕性關節炎3例,類風濕性關節炎合并干燥綜合癥2例,皮肌炎2例,系統性血管炎2例,抗Jo-1抗體綜合癥1例,系統性硬化癥1例,混合性結締組織病1例,系統性紅斑狼瘡1例,系統性紅斑狼瘡合并類風濕性關節炎1例)。
入組的患者須符合2013年美國胸科協會和歐洲呼吸學會制定的間質性肺炎診斷標準[3],并同時滿足我國2007年《肺真菌病診斷和治療專家共識》中IPA確診或臨床診斷的標準[4]。排除標準:合并血液系統疾病;器官移植史;惡性腫瘤;AIDS。入組患者中未發現入院時存在嚴重粒細胞缺乏者。
1.2 觀察指標
以診斷間質性肺炎合并IPA后12周為觀察終點,將納入的間質性肺炎合并IPA患者分為死亡組和存活組,比較兩組間臨床資料的差異,對可能的死亡危險因素進行分析。
應用廣譜抗生素指入院前3個月內使用廣譜抗生素療程超過1周,使用糖皮質激素指入院前連續使用糖皮質激素(相當于潑尼松30 mg/d>14 d或<30 mg/d)1 個月以上,使用免疫抑制劑指入院前連續使用免疫抑制劑療程超過1 個月。IPA診斷時間定義為獲得第1個微生物學或病理學IPA診斷證據的時間。初始抗真菌治療指IPA病程中最初兩周內接受的抗曲霉藥物治療,且初始治療方案療程≥1周,這些方案包括伊曲康唑、伏立康唑、卡泊芬凈單藥治療及伏立康唑聯合卡泊芬凈治療。抗真菌藥物聯合治療指在治療開始兩周內同時接受兩種或兩種以上抗真菌藥物治療,且≥72 h。在治療最初兩周內分別接受兩種或兩種以上抗真菌藥物治療的患者被認為是接受單藥治療,并按最先使用的藥物歸類。
1.3 統計學分析
2 結果
單因素分析情況見表1。分析顯示,年齡>65歲、低蛋白血癥、氧合指數<300、胸部CT示彌漫性磨玻璃影和診斷時間>7 d是間質性肺炎合并IPA的12周死亡危險因素(P<0.05),而接受伏立康唑治療的患者預后較好(P=0.033)。將上述因素應用Logistic多因素回歸分析后顯示,僅發現氧合指數<300,即入院時已發生呼吸衰竭是影響間質性肺炎合并IPA患者預后的獨立死亡危險因素(P=0.016,OR=4.833,95%CI:1.669~138.659,β=2.722,SE=1.128,Wald=5.827)。
3 討論
非粒缺IPA患者的發病危險因素包括需要長期使用糖皮質激素、肝硬化失代償、實體腫瘤、COPD、HIV感染和其它造成非結構破壞在慢性肺疾病,如陳舊性肺結核、支氣管擴張等,其中也包括間質性肺炎[1,5]。然而,影響間質性肺炎合并IPF患者的死亡危險因素目前尚無報道。
IPA患者的病死率較高,在充分抗曲霉治療的情況下,病死率仍高達30%以上[6]。本研究納入的間質性肺炎合并IPA患者的12周死亡率為49%,高于IPA患者死亡率的總體平均水平,可能與疾病早期易漏診、誤診及肺部正常結構的破壞影響藥物治療效果有關,故而了解間質性肺炎合并IPA患者的預后影響因素顯得非常重要。
對于影響曲霉感染患者預后的影響因素,因研究人群及考察參數等的不同而有所差異。針對慢性壞死性肺曲霉菌病的研究顯示,高齡、并發癥的出現、糖皮質激素的使用、體質指數<18.5 kg/m2以及C反應蛋白>5 mg/dL是影響全因死亡率的獨立危險因素[7]。對于ICU中的侵襲性曲霉菌病患者,影響死亡的獨立危險因素包括高齡、有骨髓移植病史、接受機械通氣、腎臟替代治療和診斷時更高的序貫臟器衰竭評分[8]。而基線的血小板計數和肌酐清除率水平是粒缺相關性侵襲性曲霉菌病結局的預測因素[9]。腎移植前6個月內發生過IPA和診斷時雙肺累及是肺移植后IPA患者6周全因死亡率的獨立預測因子[10]。一項來自日本的單中心回顧性研究則發現COPD和KL-6水平升高是間質性肺炎合并肺部曲霉感染患者死亡的危險因素,但該研究僅納入了15例肺部曲霉感染患者,且IPA患者只有1例[1]。而本研究的單因素分析結果表明,高齡、低蛋白血癥、氧合指數<300、胸部CT表現為彌漫性磨玻璃影、診斷時間>7 d是間質性肺炎合并IPA患者預后差的預測因素,而伏立康唑治療有助于改善患者預后,但多因素分析則顯示僅氧合指數水平是影響間質性肺炎合并IPA患者預后的獨立危險因素。
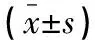
表1 間質性肺炎合并侵襲性肺曲霉菌病的12周死亡危險因素的單因素分析
a:Fisher’s精確檢驗。
暈輪征和結節內空洞影是IPA的典型CT表現,但主要見于粒缺和惡性血液系統疾病患者,并不是非粒缺患者和非血液系統腫瘤患者的主要CT表現[11],后者更多表現為沿氣道分布的多發性結節或實變。關于IPA患者CT表現與預后關系的研究很少,1項針對非HIV感染的免疫缺陷患者合并IPA的研究認為,沒有1項CT早期改變(結節、實變、支氣管周圍滲出)與預后有關[12]。然而,也有研究認為暈輪征與較好的預后有關[13],而出現大片實變影或新發胸腔積液時死亡風險更高[14]。結論不同主要考慮為納入的研究對象不同及考察樣本量較小所造成。臨床上有時可見IPA表現為廣泛磨玻璃影的CT表現,其病理實質多為彌漫性肺泡損傷(diffusealverolardamage,DAD),在間質性肺炎中多見于急性間質性肺炎和間質性肺炎的急性加重,通常會造成呼吸衰竭。目前急性間質性肺炎和特發性肺纖維化急性加重的診斷標準要求排除感染引起的病情急性加重,但在臨床實踐中排除感染十分困難。而且有觀點認為,感染可能誘發間質性肺炎患者肺內的炎癥瀑布級聯反應,導致DAD的發生[15]。因此,IPA也可能是肺組織出現DAD的重要誘因,影像學上表現為肺部彌漫性磨玻璃影的DAD造成的呼吸衰竭預示患者的預后不良[16]。
IDSA的指南中,對于IPA患者首選伏立康唑或兩性霉素B(包括脂質體)治療,其它如三唑類藥物伊曲康唑、泊沙康唑、棘白菌素類藥物卡泊芬凈等可作為備選藥物。兩性霉素B由于不良反應較多,在安全性上不如三唑類和棘白菌素類藥物。目前對于聯合用藥的療效是否優于單藥使用仍然存在爭議。一項單中心的對血液系統惡性腫瘤合并IA患者的研究表明,作為初始經驗性治療,與卡泊芬凈相比,伏立康唑能夠顯著降低患者IA相關死亡率。而伏立康唑聯合卡泊芬凈治療與單用伏立康唑相比,并不能獲得更好的治療效果,且不良反應發生率增加[17]。本研究的單因素分析提示,對于間質性肺炎合并IPA患者,可優先選用伏立康唑。
本研究也存在一些局限性:(1)為單中心回顧性研究,且樣本量有限;(2)僅驗證了有限的影響因素,可能遺漏一些未知或不易采集的影響因素,例如本院在近年才開展GM試驗檢測,未能將其納入考察。
綜上所述,在臨床工作中,應當提高對于間質性肺炎合并IPA的認識,優化診治流程,盡早明確診斷,選擇有針對性的抗曲霉藥物,避免患者病情惡化出現呼吸衰竭。
[1]KurosakiF,BandoM,NakayamaM,et al.Clinicalfeaturesofpulmonaryaspergillosisassociatedwithinterstitialpneumonia[J].InternMed,2014,53(12):1299-1306.
[2]CornilletA,CamusC,NimubonaS,et al.Comparisonofepidemiological,clinical,andbiologicalfeaturesofinvasiveaspergillosisinneutropenicandnonneutropenicpatients:a6-yearsurvey[J].ClinInfectDis,2006,43(5):577-584.
[3]TravisWD,CostabelU,HansellDM,et al.AnofficialAmericanThoracicSociety/EuropeanRespiratorySocietystatement:Updateoftheinternationalmultidisciplinaryclassificationoftheidiopathicinterstitialpneumonias[J].AmJRespirCritCareMed,2013,188(6):733-748.
[4] 中華醫學會呼吸病學分會感染學組,中華結核和呼吸雜志編輯委員會.肺真菌病診斷和治療專家共識[J].中華結核和呼吸雜志,2007,30(11):821-834.
[5]BassettiM,RighiE,DePascaleG,et al.Howtomanageaspergillosisinnon-neutropenicintensivecareunitpatients[J].CritCare,2014,18(4):458.
[6]LiD,ChenL,DingX,et al.Hospital-acquiredinvasivepulmonaryaspergillosisinpatientswithhepaticfailure[J].BMCGastroenterol,2008,8(1):32.
[7]NakamotoK,TakayanagiN,KanauchiT,et al.Prognosticfactorsin194patientswithchronicnecrotizingpulmonaryaspergillosis[J].InternMed,2013,52(7):727-734.
[8]TacconeFS,VandenAbeeleAM,BulpaP,et al.Epidemiologyofinvasiveaspergillosisincriticallyillpatients:clinicalpresentation,underlyingconditions,andoutcomes[J].CritCare,2015,19(1):7.
[9]NouerSA,NucciM,KumarNS,et al.Baselineplateletcountandcreatinineclearanceratepredicttheoutcomeofneutropenia-relatedinvasiveaspergillosis[J].ClinInfectDis,2012,54(12):e173-e183.
[10]Lopez-MedranoF,Fernandez-RuizM,SilvaJT,et al.ClinicalPresentationandDeterminantsofMortalityofInvasivePulmonaryAspergillosisinKidneyTransplantRecipients:AMultinationalCohortStudy[J].AmJTransplant,2016,16(11):3220-3234.
[11]ParkSY,KimSH,ChoiSH,et al.Clinicalandradiologicalfeaturesofinvasivepulmonaryaspergillosisintransplantrecipientsandneutropenicpatients[J].TransplInfectDis,2010,12(4):309-315.
[12]HorgerM,HebartH,EinseleH,et al.InitialCTmanifestationsofinvasivepulmonaryaspergillosisin45non-HIVimmunocompromisedpatients:associationwithpatientoutcome?[J].EurJRadiol,2005,55(3):437-444.
[13]MaromEM,KontoyiannisDP.Imagingstudiesfordiagnosinginvasivefungalpneumoniainimmunocompromisedpatients[J].CurrOpinInfectDis,2011,24(4):309-314.
[14]HuangL,HeH,DingY,et al.Valuesofradiologicalexaminationsforthediagnosisandprognosisofinvasivebronchial-pulmonaryaspergillosisincriticallyillpatientswithchronicobstructivepulmonarydiseases[J].ClinRespirJ,2016.doi:10.1111/crj.12551.
[15]CollardHR,MooreBB,FlahertyKR,et al.Acuteexacerbationsofidiopathicpulmonaryfibrosis[J].AmJRespirCritCareMed,2007,176(7):636-643.
[16]SongJW,HongSB,LimCM,et al.Acuteexacerbationofidiopathicpulmonaryfibrosis:incidence,riskfactorsandoutcome[J].EurRespirJ,2011,37(2):356-363.
[17]RaadII,ZakhemAE,HelouGE,et al.Clinicalexperienceoftheuseofvoriconazole,caspofunginorthecombinationinprimaryandsalvagetherapyofinvasiveaspergillosisinhaematologicalmalignancies[J].IntJAntimicrobAgents,2015,45(3):283-288.
(學術編輯:何清華)
本刊網址:http://www.nsmc.edu.cn
作者投稿系統:http://noth.cbpt.cnki.net
郵箱:xuebao@nsmc.edu.cn
Analysis of risk factors of mortality in interstitial pneumonia patients with invasive pulmonary aspergillosis
ZHUANG Yi,LIU Yin,CAO Meng-shu,ZHANG Ying-wei,CHEN Lu-lu,XIAO Yong-long,CAI Hou-rong,DAI Jing-hong
(DepartmentofRespiratoryMedicine,TheAffiliatedDrumTowerHospitalofNanjingUniversityMedicalSchool,Nanjing210008,Jiangsu,China)
Objective:To analyze the clinical features and risk factors of mortality in interstitial pneumonia patients with invasive pulmonary aspergillosis (IPA).Methods:The clinical data of a total of 49 cases of interstitial pneumonia patients with IPA in our hospital from December 2010 to April 2016 were collected.All the patients were followed up for 12 weeks after diagnosis and were divided into survival group and death group according to the outcome of follow-up.The clinical data was analyzed to explore the risk factors of mortality in interstitial pneumonia patients with IPA.Results:Univariate analysis showed that age >65 years old,hypoproteinemia,baseline oxygenation index <300,diffuse ground glass appearance in chest CT and diagnosis time >7 d were the risk factors of mortality in interstitial pneumonia patients with IPA (P<0.05).Patients treated with voriconazole have a better prognosis(P=0.033).After multivariate Logistic regression analysis,only oxygenation index <300 was found to be the risk factor of mortality in interstitial pneumonia patients with IPA(P=0.016,OR=4.833,95% CI:1.669~138.659,β=2.722,SE=1.128,Wald=5.827).Conclusion:Respiratory failure when being admitted to hospital is an independent factor of mortality for interstitial pneumonia patients with IPA.
Interstitial pneumonia; Invasive pulmonary aspergillosis; Risk factors of mortality
10.3969/j.issn.1005-3697.2017.03.001
國家自然科學基金(81370161);中央高校基本科研業務費專項資金(20620140732)
2017-01-05
莊誼(1978-),碩士,主治醫師。E-mail:drzy78@163.com
代靜泓,E-mail:23568@sina.com
時間:2017-6-21 18∶09 網絡出版地址:http://kns.cnki.net/kcms/detail/51.1254.R.20170621.1809.002.html
1005-3697(2017)03-0316-04
R563.4
A

