930例糖肽類和唑烷酮類抗感染藥物藥品不良反應/事件報告分析
王東曉,朱 曼,郭代紅,趙粟裕,馬 亮,陳 超,趙鵬芝,趙 靚 (中國人民解放軍總醫院藥品供應中心,北京 100853)
王東曉,朱 曼,郭代紅,趙粟裕,馬 亮,陳 超,趙鵬芝,趙 靚 (中國人民解放軍總醫院藥品供應中心,北京 100853)
目的:通過分析軍隊醫院糖肽類和唑烷酮類藥物藥品不良反應/事件(ADR/ADE)報告,了解糖肽類和唑烷酮類藥物ADR/ADE發生特點及規律,為臨床用藥提供參考。方法:采用回顧性方法,收集2009年 – 2015年軍隊ADR監測管理系統中糖肽類和烷酮類藥物ADR/ADE報告930例,對患者年齡、性別、引起ADR藥品種類、給藥途徑、藥品劑型,累及系統/器官及臨床表現、ADR/ADE報告類型、關聯性評價及轉歸情況等進行描述性統計分析。結果:930例糖肽類和烷酮類藥物ADR/ ADE中,男女比例為1.36 : 1,平均年齡(48.41 ± 24.95)歲;給藥途徑和藥品劑型以靜脈給藥和注射劑型為主。930例ADR/ADE以糖肽類藥物(768例,82.58%)為主,共涉及4個藥物品種,萬古霉素(554例,58.49%)、利奈唑胺(162例,17.42%)位居前2位。930例ADR/ADE共累及多個系統/器官,994頻次,最常見的為皮膚及其附件損害(472頻次,47.48%),以萬古霉素(340頻次,36.56%)為最;其次為血液系統損害(156頻次,15.69%),以利奈唑胺(110頻次,11.83%)為最。結論:930例糖肽類和烷酮類藥物所致的ADR/ADE涉及不同年齡段患者,累及多個系統/器官,臨床應用中應加強用藥安全風險防范,及時識別并處理ADR/ADE。
糖肽類;烷酮類;抗感染藥物;藥品不良反應;藥品不良事件
抗感染藥物是臨床使用最廣泛的一類藥物,也是藥品不良反應/事件(ADR/ADE)報告涉及最多的藥物[1-3]。近20年來,以金黃色葡萄球菌,特別是耐甲氧西林金黃色葡萄球菌(MRSA)等為代表的革蘭陽性球菌感染發生率明顯上升[4],其針對性治療藥物主要包括糖肽類抗菌藥物和以利奈唑胺為代表的烷酮類抗菌藥物。目前已有研究分別報道了萬古霉素、替考拉寧、利奈唑胺等相關不良反應,但尚無針對該二類藥物相關不良反應的綜合評價。筆者對解放軍藥品不良反應監測中心2009年– 2015年糖肽類和唑烷酮類抗感染藥物的藥品不良反應/事件(ADR/ ADE)報告進行回顧性分析,旨在了解常用MRSA針對性治療藥物,即糖肽類和烷酮類藥物的ADR/ ADE發生特點及規律,為臨床合選用糖肽類和烷酮類藥物、減少或避免ADR/ADE的發生提供安全信息參考。
1 資料與方法
1.1 數據來源
基于軍隊藥品不良反應監測管理系統,調取數據庫中2009年1月1日 – 2015年12月31日期間來自159所網點醫院的ADR/ADE報告109 554例。按照國家藥品不良反應監測中心的6級關聯性評價標準[5],納入評價為“肯定”、“很可能”和“可能”的有效報告108 938例,從中篩選第一懷疑藥品藥物類別為糖肽類和烷酮類的ADR/ADE報告930例,占同期ADR/ADE有效報告總數的0.85%。
1.2 數據整理
采用回顧性分析方法,對涉及ADR/ADE的患者年齡、性別、引起ADR/ADE的藥品種類、藥物品種、藥品劑型、給藥途徑、累及系統/器官損害以及ADR/ ADE的報告人職業分布、報告類型、關聯性評價、轉歸等運用Excel軟件進行數據匯總和分析。
ADR名稱按照《WHO藥品不良反應術語集》[6]進行整理,并對其累及的系統/器官進行分類,對同一報告累及多個系統/器官,涉及多個臨床表現的分別計算頻次。按照《中華人民共和國藥典臨床用藥須知》(2010年版)[7]和《新編藥物學》(17版)[8]對藥物類別進行分類,同一藥品不同劑型不同廠家的計為1個品種。按照藥品不良反應嚴重程度分級評分標準[9]對ADR嚴重程度進行分級。
1.3 統計學方法
采用SPSS20.0軟件進行統計分析,計量資料采用t檢驗,計數資料采用χ2檢驗,P<0.05為差異有統計學意義。
2 結果
2.1 患者性別與年齡分布
930例ADR/ADE中,男性536例(57.63%),女性394例(42.37%),男女比例為1.36 : 1。患者年齡最大101歲,最小為新生兒,平均年齡為(48.41 ± 24.95)歲,各年齡段和性別分布組間比較差異有統計學意義(χ2= 25.56,P= 0.001 2),詳見表1。
2.2 給藥途徑和藥品劑型
930例ADR/ADE報告共涉及6種給藥途徑:靜脈滴注898例(96.56%);口服22例(2.37%);靜脈注射6例(0.64%);其他給藥途徑4例(0.43%),包括泵內注射2例、鼻飼1例、鞘內注射1例;共涉及3個藥品劑型分別為:粉針劑758例(81.51%);注射液150例(16.13%);片劑22例(2.37%)。
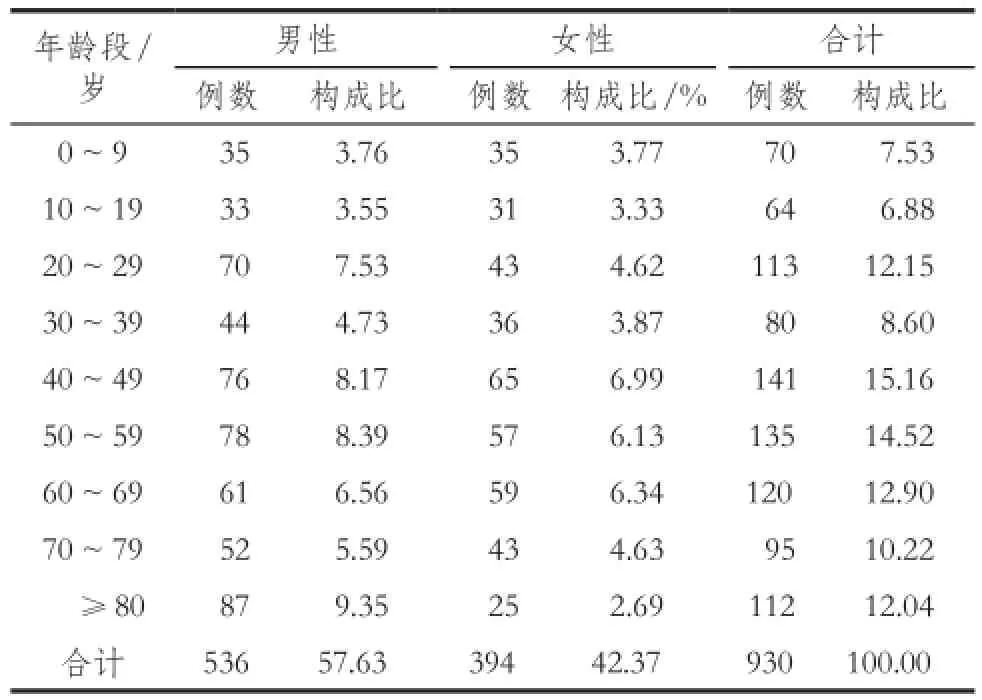
表1 患者的年齡與性別分布情況Tab 1 Distribution of age and gender in patients
2.3 藥物類別、品種及嚴重程度分布
糖肽類藥物ADR/ADE中,90.23%(693例)為一般ADR,嚴重ADR(嚴重程度≥3級)僅占9.77%(75例);烷酮類藥物(利奈唑胺)的ADR/ADE中,一般ADR為92例(56.79%),嚴重ADR則為70例(43.21%)。
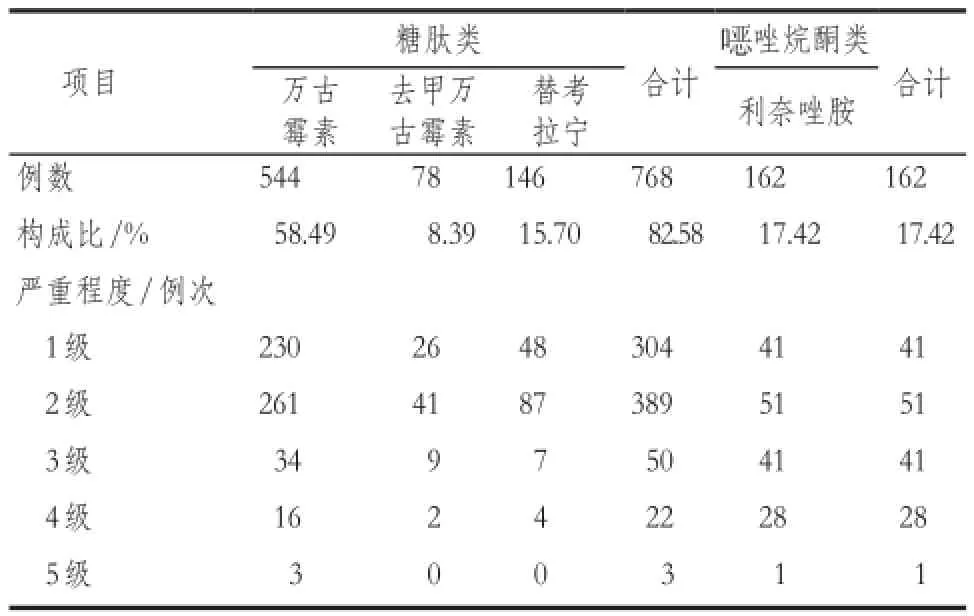
表2 930例ADR/ADE的藥物類別、品種及嚴重程度分布Tab 2 Distribution of drug category, species and ADR severity in 930 ADR/ADE
2.4 累及的系統/器官、主要臨床表現及藥物品種
表3 930例糖肽類和烷酮類ADR/ADE累及的系統/器官、主要臨床表現及藥物品種Tab 3 Systems/organs, drugs involved in 930 ADR/ADE and the clinical manifestations

表3 930例糖肽類和烷酮類ADR/ADE累及的系統/器官、主要臨床表現及藥物品種Tab 3 Systems/organs, drugs involved in 930 ADR/ADE and the clinical manifestations
累及系統/器官臨床表現頻次構成比/%藥物品種(頻次)皮膚及附件皮疹、潮紅、蕁麻疹、瘙癢、斑丘疹、剝脫性皮炎、多形性紅斑、紅人綜合征、皮膚脫落、瘀斑47247.48萬古霉素(340)、替考拉寧(78)、去甲萬古霉素(37)、利奈唑胺(17)血液系統白細胞減少、血小板減少、紅細胞減少、粒細胞減少、骨髓抑制、貧血15615.69利奈唑胺(110)、萬古霉素(33)、替考拉寧(9)、去甲萬古霉素(4)消化系統惡心、嘔吐、食欲不振、胃部燒灼感、口干、口苦、口腔金屬味、腹痛、腹瀉、肝臟轉氨酶升高、膽紅素血癥11411.47萬古霉素(56)、去甲萬古霉素(22)、利奈唑胺(21)、替考拉寧(15)全身性反應過敏樣反應、過敏性休克、發熱、寒戰、畏寒 98 9.86萬古霉素(57)、替考拉寧(30)、去甲萬古霉素(7)、利奈唑胺(4)泌尿系統腎功能異常、血尿、肌酐清除率降低 565.63萬古霉素(44)、替考拉寧(7)、去甲萬古霉素(4)、利奈唑胺(1)呼吸及心血管系統454.53萬古霉素(27)、替考拉寧(8)、利奈唑胺(7)、去甲萬古霉素(3)中樞及外周神經系統心悸、胸悶、氣促、喘息、呼吸困難、高血壓、低血壓、262.62萬古霉素(16)、替考拉寧(5)、利奈唑胺(4)、去甲萬古霉素(1)用藥部位損害靜脈炎、脈管炎、注射部位疼痛 101.01萬古霉素(8)、利奈唑胺(2)耳毒性耳鳴、聽力降低、耳聾、耳部不適、耳痛 80.80萬古霉素(6)、去甲萬古霉素(2)視覺損害視物模糊、眼部不適、眼痛、眼瞼炎 50.50萬古霉素(2)、利奈唑胺(2)、去甲萬古霉素(1)其他口腔黏膜白斑、手術部位疼痛、腿部疼痛、脫發 40.40萬古霉素(2)、去甲萬古霉素(1)、替考拉寧(1)頭痛、頭暈、震顫、多汗、癲癇大發作、嗜睡、局部麻木
2.5 報告類型及報告人職業分布
依據《藥品不良反應報告和監測管理辦法》[5-6],可將ADR分為一般的、新的一般的、新的嚴重的和嚴重的4種報告類型,其中新的一般的、新的嚴重的和嚴重的報告類型統稱為新的和嚴重的ADR。本次調研中,一般的共766例(82.37%);新的和嚴重為164例(17.63%),包括新的一般的13例,新的嚴重的3例、嚴重的148例。
從報告人的職業分布看,醫生424例(45.59%)為報告主體,其次為護士和藥師。其中,醫生(8.60%)和藥師(6.56%)是新的和嚴重的ADR/ADE的報告主體。報告人職業、報告類型組間比較,有統計學差異(χ2= 25.35,P= 0.0000),詳見表4。
2.6 關聯性評價和轉歸
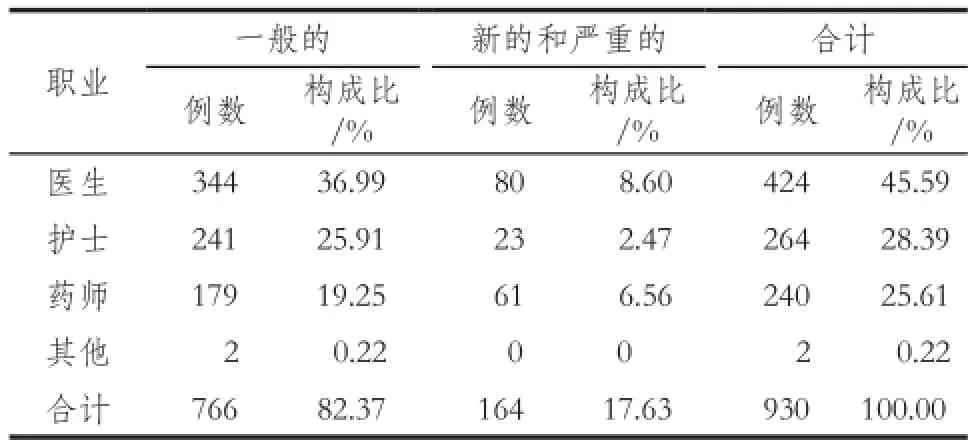
表4 930例ADR/ADE的報告類型及報告人職業分布Tab 4 Report type and reporter occupation of 930 ADR/ADE
930例ADR/ADE報告中肯定22例(2.37%);很可能558例(60.00%);可能350例(37.63%)。從轉歸情況看:痊愈484例(52.04%);好轉352例(37.85%);持續72例(7.74%);22例(2.37%)自動出院、轉院或結局不詳,無死亡病例。
3 討論
3.1 患者的性別和年齡
老年人具有肝腎功能減退、血漿蛋白低等特點,易導致藥物蓄積、藥效過強而發生不良反應[11-12]。本次調研也發現,930例ADR/ADE中,年齡≥60歲的老年患者所占比重最大,共計327例(35.16%),提示老年人是糖肽類和烷酮類藥物ADR/ADE的高發人群。在使用糖肽類及烷酮類藥物時,應在考慮其高齡、重癥、基礎疾病多、機體免疫力及器官功能減退、耐藥菌感染等特點基礎上,結合藥物特點,如萬古霉素、利奈唑胺血清蛋白結合率為34.3%、31%,而替考拉寧的蛋白結合率高達90 ~ 95%,合理選擇藥物、給藥劑量及給藥間隔,做到個體化用藥[12-13],以減少和避免ADR發生。
3.2 ADR/ADE給藥途徑及藥品劑型
930例ADR/ADE報告中,粉針劑、注射液共908例(97.63%)、片劑22例(2.37%);與此相對應的給藥方式以靜脈給藥(包括靜脈滴注、靜脈注射)904例(97.20%)為主,其次為口服22例(2.37%),這與糖肽類和烷酮類藥物的市場供應劑型相關,除利奈唑胺有口服和注射液兩種劑型外,糖肽類藥物均為注射劑型。但仍需注意:靜脈給藥引起的ADR/ADE顯著高于其他給藥途徑和劑型[10-11,14]。因此,從患者安全用藥的角度考慮,建議在使用糖肽類和烷酮類藥物時,應規范用法用量、溶媒、滴注速度等[12];選用利奈唑胺時,考慮其口服絕對生物利用度可達100%,建議在保證臨床藥物治療方案的需求下優選口服給藥。
3.3 引起ADR/ADE的藥物類別、品種及嚴重程度
萬古霉素是治療革蘭陽性菌感染的首選藥物,利奈唑胺與之比較,對多重耐藥革蘭陽性球菌,包括耐萬古霉素腸球菌(VRE)均有較好抗菌活性。本研究中,930例ADR/ADE以糖肽類藥物768例(82.58%)為主,萬古霉素544例(58.49%)、利奈唑胺162例(17.42%)在4個藥物品種中位居前2位,提示與藥物特點及其臨床應用廣泛程度相關。林敏等[15]對利奈唑胺與糖肽類藥物對HAP治療效果及安全性的Meta分析發現,利奈唑胺的病死率及不良反應總發生率略優于糖肽類,但本研究中,糖肽類藥物和烷酮類藥物亞組分析結果發現,利奈唑胺嚴重ADR(嚴重程度≥3級)的發生率(43.21%)明顯高于糖肽類藥物(9.77%),提示在臨床用藥中應重點關注。
3.4 ADR/ADE累及的系統/器官
文獻研究表明,糖肽類藥物ADR以皮疹、紅人綜合征等最為多見,其次為泌尿系統損害[16-17];利奈唑胺腎功能異常發生率(0.25%)顯著低于糖肽類抗生素(0.80%)[OR = 0.41,95% CI(0.06,2.77),P= 0.36][15]。本研究中,930例ADR/ADE主要累及皮膚及其附件(47.48%),其中以萬古霉素(340頻次,36.56%)為首的糖肽類藥物為455頻次(48.92%),利奈唑胺僅為17頻次(1.83%)。泌尿系統損害除1例涉及利奈唑胺外,其余均由糖肽類藥物引起,與文獻報道結果相符。提示在糖肽類藥物的用藥過程中,應合理控制給藥濃度及給藥速度,嚴密關注患者反應,密切監測腎功能。
國外文獻報道,利奈唑胺致血小板減少發生率為1% ~ 13%[18];療程超過2周,血小板減少癥發生率可達15.1% ~ 29.5%[19]。本研究中,930例ADR/ADE中血液系統損害(156頻次,15.69%)占據第二位,其中利奈唑胺110頻次(11.83%)為最,提示應重視利奈唑胺的血液系統損害,給藥前應檢測血常規,血小板基礎值低者應盡量避免與其他引起血小板減少的藥物聯用。治療時間一般不宜超過2周,治療期間及治療后應密切監測血常規,一旦發現血小板降低應立即停藥[19]。
3.5 ADR/ADE報告類型、報告人職業分布
WHO推薦成熟ADR監測系統中新的和嚴重的報告比例應達到30%以上,但930例報告中新的和嚴重的ADR/ADE報告占17.63%(164例),推測可能與醫務人員對新的和嚴重的ADR認識不夠、對上報嚴重ADR存在一定的思想顧慮、部分醫療機構片面追求報告數量或報告比例達標等因素有關[1]。
作為患者的直接接觸者或第一信息接收人,醫生、護士通常為ADR/ADE的報告主體[20]。930例ADR/ADE中,醫生(45.59%)仍為報告主體,其次為護士(25.91%)和藥師(19.25%),報告人職業、報告類型組間有統計學差異。但應注意的是,藥師與護士的差距正在縮減,且在新的和嚴重ADR/ADE報告中,除醫生群體外,藥師(6.56%)已躍升為第二位報告群體,明顯高于護士(2.47%),提示隨著國家臨床藥學服務的深入,藥師在用藥安全,特別是新的和嚴重ADR/ADE的識別和報告中的作用已逐漸凸顯。
總之,自2011年7月1日新修訂的《藥品不良反應報告和監測管理辦法》正式實施以來,我國在ADR監測的各個領域已取得了長足發展[21]。本文基于2009年 – 2015年解放軍藥品不良反應中心的930例糖肽類和烷酮類抗感染藥物ADR/ADE報告,對其相關信息進行了描述性解析,為其臨床應用提供了一定的安全用藥參考。
[1] 朱曼,郭代紅,凡超,等.軍隊醫院22 605例抗感染藥物藥品不良反應/事件報告分析[J].中國藥物應用與監測,2015,12(5):284-288.
[2] 朱昆,李忻,劉玉梅.278例藥品不良反應分析[J].中國藥物應用與監測,2015,12(5):288-291.
[3] 國家食品藥品監督管理總局.國家藥品不良反應監測年度報告(2014年)[J].中國藥物評價,2015,32(4):252-256.
[4] 陸菲婕,徐志豪.抗革蘭陽性細菌藥物研究進展[J].中國新藥與臨床雜志,2008,27(7):543-548.
[5] 國家食品藥品監督管理局.藥品不良反應報告和監測管理辦法[S].2011.
[6] 郭代紅,張曉東,劉皈陽.醫療機構藥物安全性監測[M].第1版.北京:人民軍醫出版社,2010:86-88.
[7] 國家藥典委員會.中華人民共和國藥典臨床用藥須知[M].2010年版.北京:中國醫藥科技出版社,2011:622-852.
[8] 陳新謙,金有豫,湯光.新編藥物學[M].17版.北京:人民衛生出版社,2011:34-134.
[9] 李利軍,胡晉紅,王卓,等.藥品不良反應嚴重程度分級評分標準的制定及藥品不良反應嚴重度指數的應用[J].藥學服務與研究,2008,8(1):9-13.
[10] 曹軍華,韓勇,陳東生.1596例藥品不良反應報告分析[J].藥物流行病學雜志,2012,21(9):431-433.
[11] 孫言才,劉斌,蘇丹,等.12 249例藥品不良反應報告中年齡分布的分析評價[J].藥物流行病學雜志,2014,23(1):29-34.
[12] 秦慶芳,陸衛英,譚柳英,等.2010 – 2012年1237例中成藥致不良反應報告分析[J].中國醫院用藥評價與分析,2014,14(3):262-264.
[13] 劉曉東,菅凌燕,王法.利奈唑胺不良反應的文獻分析[J].醫藥導報,2012,31(6):811-813.
[14] 任淑娟,吉金燕,解娟,等.我院304例藥品不良反應報告分析[J].西北藥學雜志,2014,29(1):93-96.
[15] 林敏,卓儀,鄭莉莉,等.利奈唑胺與糖肽類對HAP治療效果及安全性的Meta分析[J].今日藥學,2014,24(12):897-902.
[16] 伍俊.替考拉寧致不良反應14例文獻分析[J].藥學與臨床研究,2013,21(3):291-292.
[17] 劉曉東,原思佳.萬古霉素與去甲萬古霉素不良反應文獻分析[J].藥物流行病學雜志,2010,19(9):531-533.
[18] Garazzino S, De Rosa FG, Bargiacchi O,et al. Haematological safety of long-term therapy with linezolid[J]. Int J Antimicrob Agents, 2007, 29(4): 480-483.
[19] 白艷,王羽凝,李其,等.利奈唑胺不良反應的文獻計量分析[J].中國臨床藥理學雜志,2015,31(24):2459-2461.
[20] 郭代紅,陳超,馬亮,等.2009 – 2013年軍隊醫院67 826例藥品不良反應報告分析[J].中國藥物應用與監測,2014,11(5):300-304.
[21] 田春華,杜曉曦.論我國藥品不良反應監測工作幾點進展[J].藥物流行病學雜志,2014,23(1):1-4.
Analysis on 930 cases of ADR/ADE associated with glycopeptides and oxazolidinone antibacterials from military hospitals
WANG Dong-xiao, ZHU Man, GUO Dai-hong, ZHAO Su-yu, MA Liang, CHEN Chao, ZHAO Peng-zhi, ZHAO Liang
(Department of Pharmaceutical Care, PLA General Hospital, Beijing 100853, China)
Objective: To investigate the characteristics and regular patterns of adverse drug reaction reports and events (ADR/ ADE associated with glycopeptides and oxazolidinone based on the analysis of glycopeptides and oxazolidinone antibacterials ADR/ ADE from military hospitals, and to provide references for the clinical rational drug use. Methods: A total of 930 ADRs/ADEs of glycopeptides and oxazolidinone antibacterials from 2009 to 2015 were collected from the database of PLA ADR monitoring center. The age and gender of patients, categories of suspected anti-infective drugs, route of administration, systems/organs involved, clinical manifestations, report type, relevance evaluation and prognosis were retrospectively analyzed. Results: Among 930 ADRs/ADEs, the male to female ratio was 1.36 : 1. The average age of the patients was (48.41 ± 24.95) years. Intravenous infusion and injection type were the main administration route and pharmaceutical form, respectively. The ADRs/ADEs were mainly related to glycopeptides antibacterials (768 cases, 82.58%). Four drugs were involved in 930 ADRs/ADEs, and the top 2 drugs in terms of frequency of occurrence were vancomycin (554 cases, 58.49%) and linezolid (162 cases, 17.42%). 930 cases of the ADR/ADE involved multiple systems/organs (994 frequencies). The most common ADRs were the skin and its appendages damage (472 cases, 47.48%), most of which were associated with vancomycin (340 cases, 36.56%). The second was the hematological system damage (156 cases, 15.69%), most of which were associated with linezolid (110 cases, 11.83%). Conclusion: The ADR/ADE induced by glycopeptides and oxazolidinone antibacterials involved different ages of patients and multiple systems/organs. In order to recognize and treat the ADR/ADE in time, risk prevention of drug safety should be strengthened in the application of anti-infective agents.
R969.3
A
1672 – 8157(2017)01 – 0037 –05
2016-07-27
2016-10-25)
2014全軍后勤科研重點項目(BWS14R039)
郭代紅,女,主任藥師,碩士生導師,主要從事藥事管理及臨床藥學工作。E-mail:guodh301@163.com
王東曉,女,副研究員,主要從事臨床藥學工作。E-mail:baixiao301@163.com

