三唑類抗真菌藥物的藥源性肝損傷主動監測研究
朱 曼,郭茂文,2,郭代紅,吳 旭,3,馬 亮,趙鵬芝,趙 靚(.解放軍總醫院藥學部臨床藥學中心,北京 00853;
2.首都兒科研究所附屬兒童醫院,北京 100020;3.重慶醫科大學藥學院,重慶 401331)
三唑類抗真菌藥物的藥源性肝損傷主動監測研究
朱 曼1,郭茂文1,2,郭代紅1,吳 旭1,3,馬 亮1,趙鵬芝1,趙 靚1(1.解放軍總醫院藥學部臨床藥學中心,北京 100853;
2.首都兒科研究所附屬兒童醫院,北京 100020;3.重慶醫科大學藥學院,重慶 401331)
目的:研究應用計算機輔助系統主動監測住院患者3種三唑類抗真菌藥物致藥源性肝損傷的可行性和關鍵要素。方法:利用住院患者藥品不良事件主動監測與評估警示系統,通過團隊論證的方式優化住院患者三唑類抗真菌藥物致藥源性肝損傷主動監測的事件配置器。回顧性調取2015年1月1日– 2015年11月30日我院經靜脈途徑應用氟康唑氯化鈉注射液、注射用伏立康唑、伊曲康唑注射液的住院患者,對系統提示的陽性預警病例進行人工再評價。結果:計劃3參數為最優的事件配置器參數,分別篩查氟康唑組、注射用伏立康唑組和伊曲康唑組病例840例、211例和81例。其中氟康唑組系統陽性預警病例377例,人工再評價實際陽性病例為42例,人工陽性預警率為5.00%;注射用伏立康唑組系統陽性預警病例94例,人工再評價實際陽性病例為15例,人工陽性預警率為7.11%;伊曲康唑注射液組系統陽性預警病例28例,人工再評價實際陽性病例為4例,人工陽性預警率為4.94%。結論:本研究中設置的肝損傷事件配置器結合了多種標準參數,可操作性好,彈性空間大,陽性病例丟失率低。采用該系統進行主動監測研究時,事件配置器的參數設置為關鍵要素,應基于不同目標藥物和藥品不良事件特點進行個體化設置。
三唑類抗真菌藥物;藥源性肝損傷;主動監測;氟康唑;伏立康唑;伊曲康唑
藥源性肝損傷(drug-induced liver injury,DILI)是一類較為嚴重的藥品不良反應(adverse drug reaction,ADR),發生率僅次于皮膚黏膜損害和藥物熱,約占ADR的10% ~ 15%[1],占急性肝損傷的50%以上[2],據世界衛生組織調查顯示,以每年5%的速度上漲[3]。據報道,有1000種以上的藥物可能引起肝損傷[4],其中抗感染藥物為引起DILI的常見藥物類別之一。三唑類抗真菌藥物[5-6]是臨床上應用廣泛的抗真菌藥物,因該類藥物可與體內的P-450蛋白血紅素輔基Fe原子配位結合,普遍具有一定的肝、腎毒性[7]。住院患者藥品不良事件(ADE)主動監測與評估警示系統是我院依托軍衛1號醫院信息系統,采用觸發器技術原理設計開發,對接軍隊ADR監測管理系統,完成了藥物相關性血小板減少、貧血、肝損傷、腎損傷4個事件的自動識別規則設計,建立了集自動監測、用藥審查、輔助評估、特征分析、風險警示、高危篩選為一體的監測構架[8]。本研究開展住院患者因三唑類抗真菌藥物致藥源性肝損傷的主動監測研究,旨為藥品安全風險防范重點監測工作提供參考。
1 資料與方法
1.1 三唑類抗真菌藥致藥源性肝損傷的事件配置器參數
事件配置器設定包括4個模塊:①病例排除模塊,子條件包括排除病區、排除診斷、排除合并用藥、排除基值異常、排除臨時醫囑、排除指標缺失、檢驗指標取值時間范圍等;②肝功能異常觸發器模塊,參列指標有:ALT、AST、TB、DB高于2倍正常值上限或連續2次高于正常值上限或較基值增幅等;ALP高于2倍正常值上限或連續2次高于正常值上限且ALT、AST、TB、DB一項高于正常值上限;③肝功能嚴重程度分級標準模塊,含美國國立、中國抗癌協會、國家ADR中心、DELIN2012等官方標準及自定義嚴重程度標準可供研究者選擇;④輔助提示模塊,含其他懷疑藥品、解救藥品目錄。研究者可根據不同的研究目的和需求,靈活組合設定主動監測事件配置器各項參數,詳見圖1。
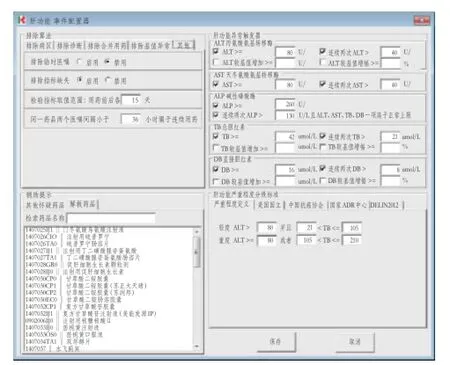
圖1 藥源性肝損傷主動監測的事件配置器Fig 1 The event configurator of drug-induced liver injury
1.2 病例入選標準
回顧性調取解放軍總醫院2015年1月1日– 2015年11月30日期間經靜脈途徑應用氟康唑氯化鈉注射液、注射用伏立康唑、伊曲康唑注射液的住院患者。年齡不限;臨床資料及用藥醫囑完整、準確、可靠。
1.3 病例排除及肝功能異常觸發器參數
基于國內外文獻對于藥源性肝損傷的定義、臨床特點、診斷標準、因果關系評價[9-14]、臨床實踐指南[15]、三唑類藥物說明書等資料,由臨床藥師與藥品不良反應監測專職人員共同設定本次研究的藥源性肝損傷主動監測的事件配置器參數。研究中對事件配置器參數設置先后做了3次調整優化,分別命名為計劃1、2、3,(○表示“無”;●表示“有”),詳見表1。
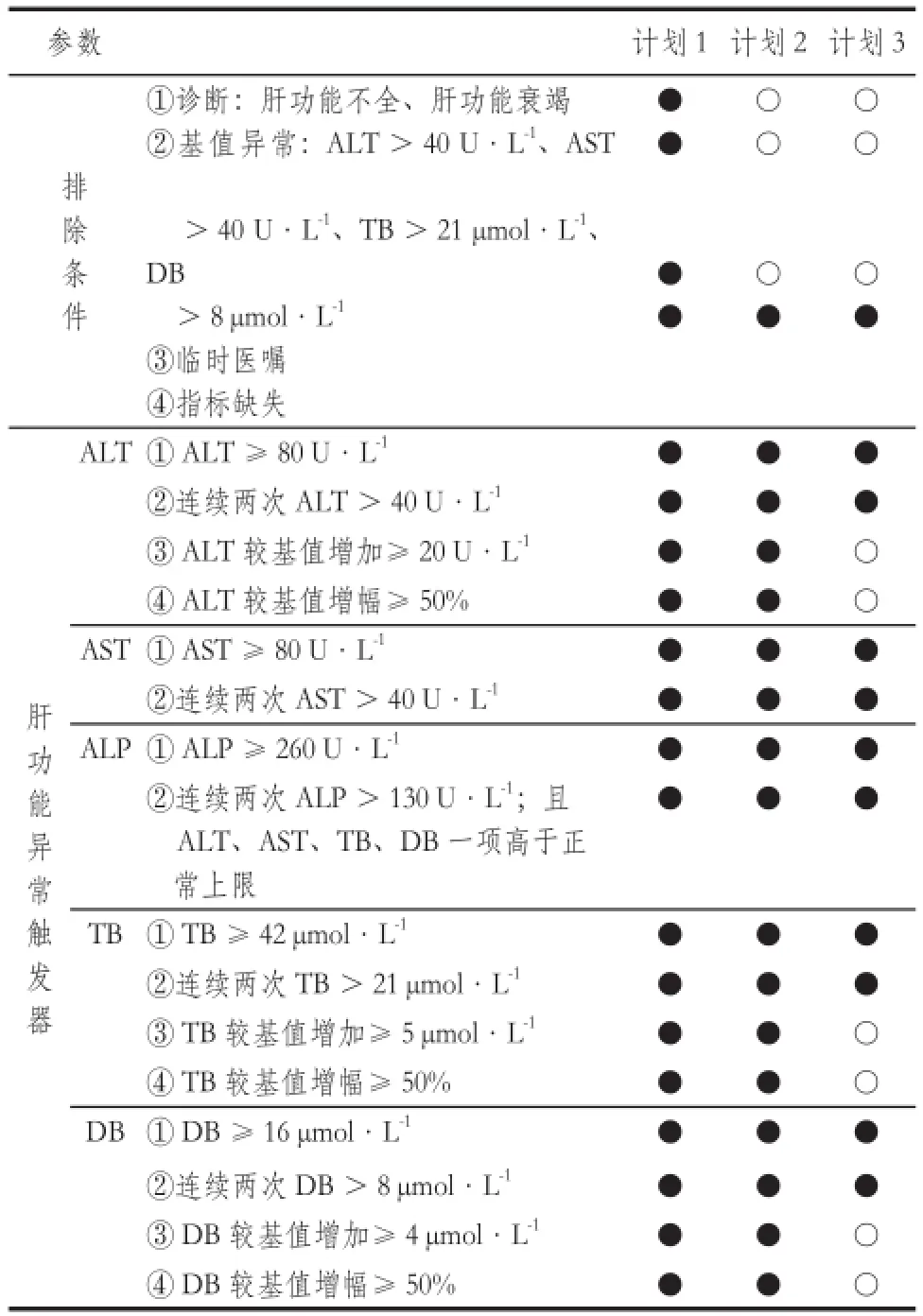
表1 病例排除及肝功能異常觸發器參數Tab 1 The exclusion criteria of cases and trigger parameters of liver dysfunction
2 結果
2.1 事件配置器參數的優化設置
對回顧性抽取的研究對象,依托住院患者藥品不良事件主動監測與評估警示系統分別用事件配置器計劃1、2、3進行主動監測,其中患者的年齡和性別分布詳見表2。不同事件配置器主動監測的排除病例情況、實際篩查病例以及系統陽性預警結果詳見表3。
2.2 人工再評價結果
臨床藥師和專職藥品不良反應監測人員依托住院患者藥品不良事件主動監測與評估警示系統自動提取的用藥醫囑、合并用藥、檢驗指標變化情況結合臨床藥學工作站綜合評價患者的個體化情況,對事件配置器計劃3的系統陽性預警涉及的可疑ADE進行人工關聯性評價,結果詳見表4,其中氟康唑、伏立康唑和伊曲康唑組的人工陽性預警率分別為5.00%、7.11%和4.94%。
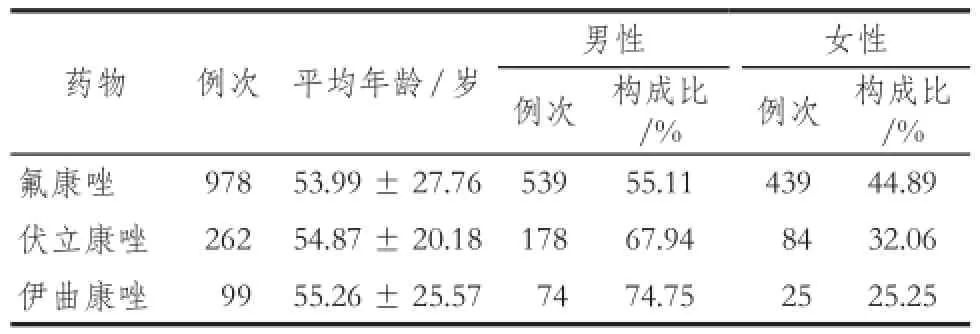
表2 患者年齡和性別分布Tab 2 The patients' age and gender distribution
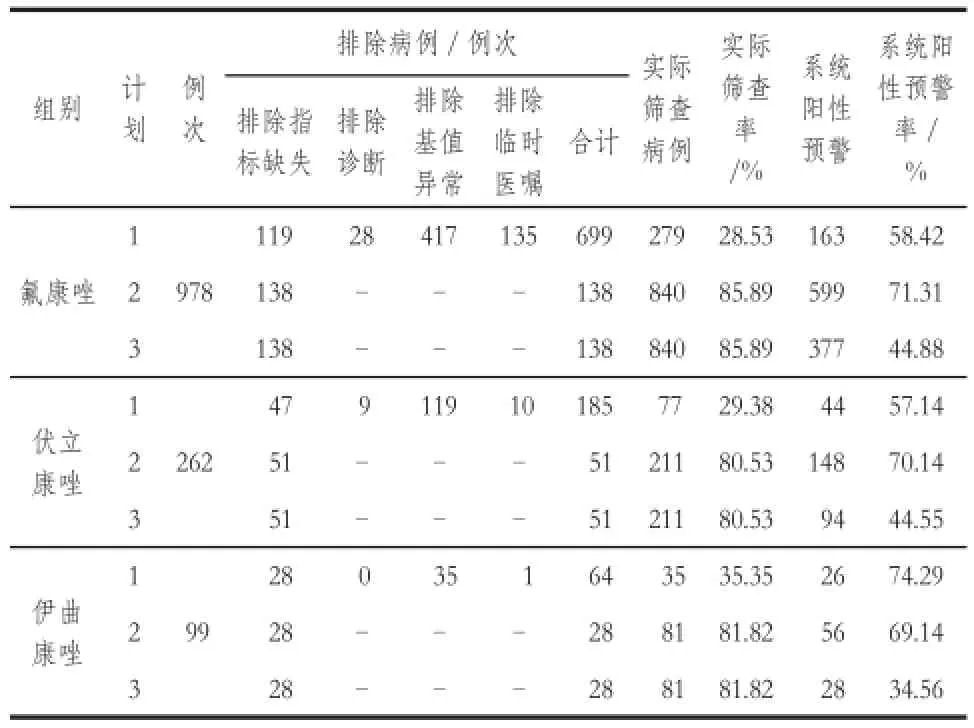
表3 住院患者三唑類抗真菌藥物致肝損傷主動監測結果Tab 3 The active surveillance of inpatients' drug-induced liver injury of triazoles
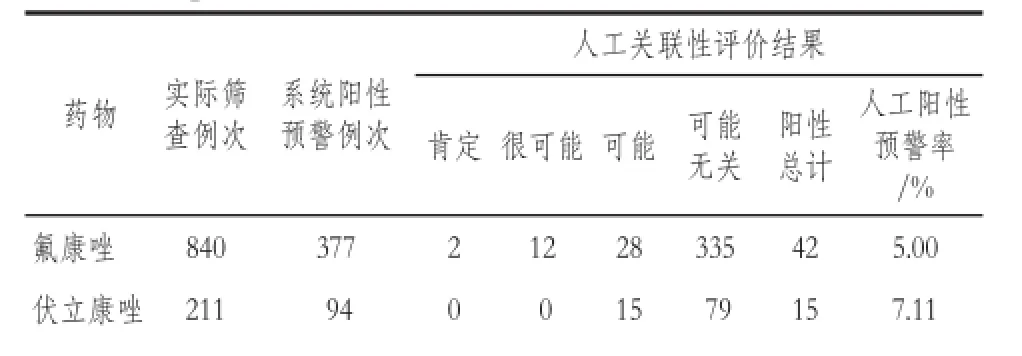
表4 計劃3系統陽性預警病例的人工關聯性評價結果Tab 4 The manual relevance re-evaluation of system warning cases of the third plan
3 討論
3.1 事件配置器參數優化為主動監測研究的關鍵要素
從表3可見:計劃1中氟康唑組、伏立康唑組和伊曲康唑組的實際篩查率僅為28.53%、29.38%和35.35%,提示排除病例過多,導致實際篩查病例過少。通過對計劃1病例排除標準4個子條件的細化分析,考慮到“基礎疾病、基值異常”等因素分析起來復雜多變,有的異常表現也是對個體化評價有參考意義的,需要依靠臨床藥師和ADR監測人員結合具體病例進行人工評價,并且在臨床實際中,存在以“臨時醫囑”的形式長期用藥的情況,只有“指標缺失”會導致無法對照評價患者用藥前后藥源性肝損傷情況,最終計劃2和計劃3均調整為只保留排除指標缺失的子條件,以規避后續關聯性評價中因患者指標不完全,而對ADE關聯性判定結果的干擾,調整后計劃2和3的實際篩查率在80%以上。
此外,計劃2中三組藥物的系統陽性預警率分別為71.31%、70.14%和69.14%,提示系統陽性預警比例偏高,可能造成需進行后續人工再評價的病例過多,預警特異性不足。經對計劃2的事件配置器參數分析發現:“較基值增加≥0.5 ULN”和“較基值增幅≥50%”兩個觸發條件使預警特異性不足,以伊曲康唑組中人工評價結果為“可能無關”的原因為例,“較基值增加≥0.5 ULN”和“較基值增幅≥50%”兩個條件觸發報警器的病例數為19例,占“可能無關”病例數的37.25%,因此計劃3的事件配置器參數在計劃2的基礎上,刪除了“較基值增加≥0.5 ULN”和“較基值增幅≥50%”兩個觸發報警器的條件。最終計劃3的氟康唑、伏立康唑和伊曲康唑組的系統陽性預警率分別為44.88%、44.55%和34.56%。
研究結果提示在肝損傷事件配置器參數的優化設置中,過于嚴苛的排除條件可能導致部分陽性預警病例漏報,但排除條件的放寬,又必然使陽性預警率降低,需要研究人員結合臨床對肝功能相關指標的監測頻率和數量不能完全達到評價標準理想需求的實際情況,在運用中針對不同目標藥物和ADE,設置個體化的事件配置器參數。
3.2 系統陽性預警病例的人工再評價結果分析
本研究中三組藥物的人工陽性預警率分別為5.00%、7.11%和4.94%,而氟康唑注射液、注射用伏立康唑和伊曲康唑注射液藥品說明書中提及的肝損傷相關數據分別為常見(≥1/100 ~ <1/10)、2.7%和2% ~ 6%,兩者差異的可能原因分析為藥品說明書中ADR數據主要源于上市前Ⅰ~Ⅲ期藥物臨床試驗,而上市前藥物臨床試驗是對較小范圍、特殊群體的病人進行藥品評價,病人是經過嚴格篩選和控制的。而上市后臨床試驗需要達到上市前試驗例數的5 – 8倍,通常在3000例以上,并且是用于更多不同類型的病人,包括兒童、老年及合并多系統疾病的人群。本研究中納入的這些臨床住院患者病情及實際聯合用藥情況極其復雜,分析為本研究人工陽性預警率高于藥品說明書所給數據的可能原因。
此外,本研究中受臨床藥物實際使用情況、醫院信息管理系統數據調取時限等條件限制,不同藥物的入組例數差異較大,有的組別樣本量不足,也給研究結果帶來一定局限性,我們將在后期的工作中加以完善。
[1] Stickel F, Patsenker E, Schuppan D. Herbal Hepatotoxicity[J]. J Hepatol, 2005, 43(43): 901-910.
[2] Ostapowicz G, Fontana RJ, Schi?dt FV,et al. Results of a prospective study of acute liver failure at 17 tertiary care centers in the United States[J]. Ann Intern Med, 2002, 137(12): 947-954.
[3] Bj?rnsson E, Olsson R. Suspected drug-induced liver fatalities reported to the WHO database[J]. Dig Liver Dis, 2006, 38(1): 33-38.
[4] Grant LM, Rockey DC. Drug-induced liver injury[J]. Curr Opin Gastroenterol, 2012, 28(3): 198-202.
[5] Pfaller MA,Diekema DJ,Messer SA,et al.In vitroactivities of voriconazole,posaconazole, and four licensed systemic antifungal agents against canadida species infrequently isolated from blood[J]. J Clin Microbiol, 2003, 41(1): 78-83.
[6] 曹江,白艷,王冬,等.抗真菌藥物的TDM文獻計量分析[J].中國藥物應用與監測,2015,12(3):184-187.
[7] 謝海偉,楊賢松,呂超田,等.抗真菌藥物及其作用機制研究[J].中國微生態學雜志,2015,27(12):1477-1479.
[8] 陳超,郭代紅,薛萬國,等.住院患者藥品不良事件主動監測與評估警示系統的研發[J].中國藥物警戒,2013,10(7):411-414.
[9] Danan G. Causality assessment of drug-induced liver injury. Hepatology Working Group[J]. J Hepatol, 1988, 7(1): 132-136.
[10] Danan G,Benichou C. Causality assessment of adverse reactions to drugs-I.A novel method based on the conclusions of international consensus meetings: application to drug-induced liver injuries[J]. J Clin Epidemiol, 1933, 46(11): 1323-1330.
[11] Maria VA, Victorino RM. Development and validation of a clinical scale for the diagnosis of drug-induced hepatitis[J]. Hepatology, 1997, 26(3): 664-669.
[12] 滝川一,朱麗影,谷仁燁.診斷標準的變遷經緯概要[J].日本醫學介紹,2006,27(6):243.
[13] 熊木天児,朱麗影,谷仁燁.新版診斷標準的實用性及貽留問題[J].日本醫學介紹,2006, 27(6): 244-247.
[14] 中華醫學會消化病學分會肝膽疾病協作組.急性藥物性肝損傷診治建議(草案)[J].中華消化雜志,2007,27(11):765-767.
[15] Chalasani NP, Hayashi PH, Bonkovsky HL,et al. ACG clinical guideline: the diagnosis and management of idiosyncratic drug-induced liver injury[J]. Am J Gastroenterol, 2014, 109(7): 950-966.
The active surveillance of triazole antifungal agents-induced liver injury
ZHU Man1, GUO Mao-wen1,2, GUO Dai-hong1, WU Xu1,3, MA Liang1, ZHAO Peng-zhi1, ZHAO Liang1(1. Department of Clinical Pharmacy, PLA General Hospital, Beijing 100853, China; 2. Capital Institute of Pediatrics, Beijing 100020, China; 3. College of Pharmacy, Chongqing Medical University, Chongqing 401331, China)
Objective: To study the feasibility and key elements of active surveillance of inpatient's drug-induced liver injury on three kinds of triazole antifungal agents based on computer-aided system. Methods: Based on inpatient's active monitor and assessment system of adverse drug events and team work, the event configurator of drug-induced liver injury on triazole antifungal agents was optimized. Retrospective method was used for evaluating the inpatients in PLA general hospital from January 1, 2015 to November 30, 2015 who intravenously used the fl uconazole and sodium chloride injection, voriconazole for injection and itraconazole injection. The positive warning cases were re-evaluated manually. Results: The event monitor con fi gurator parameters of plan three were the most reasonable. The screening cases about fl uconazole, voriconazole and itraconazole were 840, 211 and 81 cases, respectively. A total of 377 warning cases of f l uconazole were screened by the system, and after the manual re-evaluation, the actual positive cases and warning rate were 42 cases and 5.00%. 94 warning cases about voriconazole were screened by the system, while the actual positive cases and warning rate were 15 cases and 7.11%. 28 warning cases about itraconazole were screened by the system, and the actual positive cases and warning rate were 4 cases and 4.94%. Conclusion: In this study, we considered diverse criteria to set the parameters of hypohepatia event configurator, which was proved excellent maneuverability and elasticity. The loss rate of positive cases was low. Setting parameters of adverse drug events configurator was the key point and should be based on different target drugs as well as the characteristics of different adverse drug events.
Triazole antifungal agents; Drug-induced liver injury; Active surveillance; Fluconazole; Voriconazole; Itraconazole
R969.3
A
1672 – 8157(2017)01 – 0045 – 04
2014全軍后勤科研重點項目(BWS14R039)
郭代紅,女,主任藥師,碩士生導師,主要從事藥事管理及臨床藥學工作。E-mail:guodh301@163.com
朱曼,女,副主任藥師,主要從事臨床藥學工作。E-mail:zhucindy301@189.cn

