米諾環素體外抑制弓形蟲增殖作用的研究
趙瑩,楊曉燕,陳順儀,廖利銀
(廣州市番禺區中心醫院檢驗科,廣東廣州511400)
米諾環素體外抑制弓形蟲增殖作用的研究
趙瑩,楊曉燕,陳順儀,廖利銀
(廣州市番禺區中心醫院檢驗科,廣東廣州511400)
目的評價米諾環素(MNC)體外抑制弓形蟲速殖子的增殖作用。方法體外在96孔板中用Hela細胞培養弓形蟲速殖子,設置SMX給藥組、MNC給藥組和未給藥組。觀察各組弓形蟲速殖子的增殖情況、形態變化,并對各組進行活蟲計數。結果給藥后72 h,與未給藥組比較,SMX給藥組活蟲計數顯著減少[(2.08±0.40)vs (15.17±2.07),P<0.01],MNC給藥組活蟲數亦顯著減少[(1.42±0.20)vs(15.17±2.07),P<0.01];給藥后96 h,與未給藥組相比,SMX給藥組活蟲計數顯著減少[(1.42±0.20)vs(10.92±0.47),P<0.01],MNC給藥組活蟲數亦顯著減少[(1.92±0.33)vs(10.92±0.47),P<0.01],差異均有統計學意義;給藥后120 h,各組活蟲計數比較差異無統計學意義(P>0.05)。結論MNC在體外能夠明顯抑制弓形蟲速殖子的增殖。
體外;弓形蟲;米諾環素;速殖子
剛地弓形蟲(Toxoplasma gondii)是一種專性細胞內寄生、呈世界性分布的機會性致病原蟲,可引起廣泛人畜共患感染。免疫正常人群感染后多表現為隱性癥狀,但免疫低下或免疫缺陷者感染后,可引起全身廣泛弓形蟲病。孕婦等特殊人群感染弓形蟲可能導致嚴重后果,如早產、流產、死胎等[1]。宿主感染弓形蟲后,寄生蟲刺激機體產生特異性和非特異性免疫應答,巨噬細胞、T淋巴細胞、NK細胞及各細胞因子如白介素、γ-干擾素(IFN-γ)等發揮重要抗感染作用[2]。在弓形蟲病治療方面,經典藥物如磺胺嘧啶、乙胺嘧啶等長期為臨床使用,效果顯著,但存在一定副作用,且不適用于孕婦。米諾環素(minocycline,MNC)是第二代半合成四環素類藥物的衍生物。研究表明,MNC具有良好的抗炎、抗菌等作用,同時具有強大的神經保護作用,并且其相對分子量小,口服易吸收,可通過血—腦屏障[3]。本實驗初步證實,體外米諾環素能顯著抑制弓形蟲速殖子增殖。
1 材料與方法
1.1 材料弓形蟲RH株速殖子(中山大學呂芳麗教授惠贈)由昆明鼠傳代保種。昆明鼠(Kunming, KM,6~8周)購自中山大學實驗動物中心。小牛血清、RPMI 1640培養基購自美國HyClone公司,96孔細胞培養板、細胞培養瓶購自美國Corning公司。臺盼藍染液、雙抗(青霉素、鏈霉素抗生素)購自美國Sigma公司。
1.2 細胞培養將Hela細胞培養于含5%CO2、37℃的CO2培養箱中,相對濕度為95%。培養液中加入10%小牛血清和雙抗。在細胞生長旺盛時,消化收集并轉入細胞培養板,每孔加入100 μL細胞培養液,其中含104個Hela細胞,培養24 h后,鏡下觀察細胞生長情況。各實驗組均重復設置6孔,實驗重復做一次。
1.3 藥物米諾環素購自美國Sigma公司。磺胺甲噁唑片(SMX)為中國廣州白云山藥物有限公司產品。
1.4 體外實驗96孔細胞培養板中,每孔加入1× 104個Hela細胞,體積為100 μL,培養24 h待細胞貼壁生長達90%以上,每孔加入5×104個弓形蟲速殖子,體積為100 μL。兩者共同培養2 h后吸去各孔培養液,再用細胞培養液沖洗兩次以除去Hela細胞外的速殖子。加入制備好的MNC和SMX,設置MNC給藥組、SMX給藥組及未給藥組。參照陳莉等[4]的實驗方法,選取MNC的終濃度為100 μmol/L;參照趙瑩等[5]的實驗方法,選取SMX的終濃度為1 mg/mL。鏡下觀察給藥后72 h、96 h、120 h 3個時間點弓形蟲速殖子的增殖情況及其形態變化,并酚酞藍染色以計數活蟲數,分析減蟲率[5]。
1.5 統計學方法應用SPSS19.0統計學軟件進行數據分析,計量資料以均數±標準差()表示,多組間均值比較采用方差分析,組間兩兩比較采用t檢驗,以P<0.05表示差異有統計學意義。
2 結果
2.1 體外觀察各組弓形蟲速殖子增殖情況給藥72 h、96 h、120 h后,倒置熒光顯微鏡觀察弓形蟲速殖子增殖情況及形態變化(圖1)。72 h,弓形蟲速殖子在Hela細胞內大量增殖,形態大致正常。未給藥組弓形蟲速殖子增殖活躍,表現為高密度影,與之相比,MNC及SMX兩給藥組弓形蟲速殖子密度強度顯著減弱;鏡下,各組均可見部分弓形蟲速殖子從Hela細胞中釋放出,形態正常,活力較好。96 h,所有實驗組弓形蟲速殖子密度強度均有所降低,未給藥組弓形蟲速殖子密度強度仍然高于兩給藥組;各組均可見部分弓形蟲蟲體腫脹、出現無活力的死蟲。120 h,各實驗組弓形蟲速殖子密度強度均進一步減弱,這可能是由于藥物的持續作用以及營養物質消耗,出現大量無活力死亡蟲體。
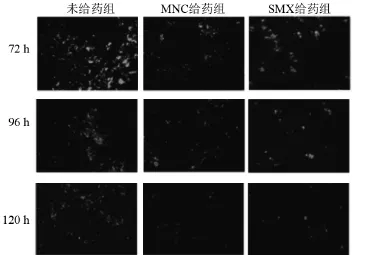
圖1 各實驗組不同時間點弓形蟲速殖子增殖情況(×40)
2.2 各組各時間點活蟲計數酚酞藍染色,計數各時間點各實驗組活蟲數見表1。72 h,與未給藥組比較,MNC給藥組和SMX給藥組活蟲數均顯著降低(P<0.01)。其中,SMX給藥組活蟲數進一步低于MNC給藥組,但兩組差異無統計學意義(P=0.493)。96 h,與未給藥組比較,兩給藥組活蟲數亦顯著降低(P<0.01)。120 h,各實驗組活蟲數均明顯減少,出現大量死蟲,各組間活蟲數對比差異無統計學意義。與未給藥組比較,SMX給藥組在72 h、96 h、120 h減蟲率分別為88.5%、86.9%、50.2%;MNC給藥組在72 h、96 h、120 h減蟲率分別為86.3%、82.4%、30.9%。說明SMX、MNC體外均能較好抑制弓形蟲速殖子增殖,其中SMX作用效果更好。
表1 各實驗組不同時間點活蟲計數()
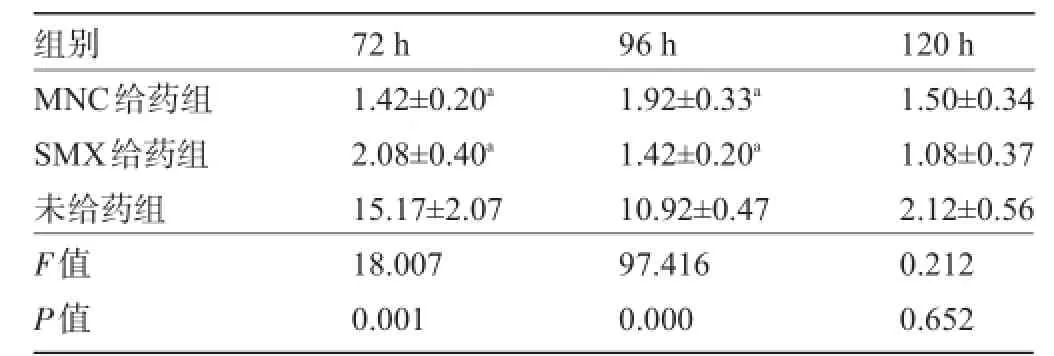
表1 各實驗組不同時間點活蟲計數()
注:每一組12個副孔;與未給藥組比較,aP<0.01。
組別120 h 72 h 96 h MNC給藥組SMX給藥組未給藥組F值P值1.50±0.34 1.08±0.37 2.12±0.56 0.212 0.652 1.42±0.20a2.08±0.40a15.17±2.07 18.007 0.001 1.92±0.33a1.42±0.20a10.92±0.47 97.416 0.000
3 討論
弓形蟲寄生于除成熟紅細胞之外的所有有核細胞,能侵入多種臟器甚至免疫豁免區引起嚴重弓形蟲病[6]。作為機會致病性原蟲,免疫低下人群罹患弓形蟲病往往是致死性的。弓形蟲感染引起T細胞介導的強烈的免疫反應,釋放大量Th1型細胞因子如γ-干擾素(IFN-γ)、腫瘤壞死因子-α(TNF-α)等。IFN-γ既可抑制弓形蟲的繁殖,也是重要的巨噬細胞活化因子,在抗弓形蟲感染中發揮重要作用[7]。同時研究證實,宿主感染弓形蟲RH強毒株后,刺激IFN-γ、TNF-α等細胞因子的釋放,這些細胞因子一方面發揮積極的抗感染作用,一方面由于其大量釋放導致肝、脾等器官損傷,故在感染后期,機體Th2免疫應答增強以拮抗過度的Th1型免疫應答,使機體度過急性期并存活[8-9]。
治療弓形蟲病的經典藥物為磺胺類藥物,如磺胺嘧啶、乙胺嘧啶等,其作用機制為通過阻礙二氫葉酸的形成、影響核酸和蛋白質的合成,從而抑制弓形蟲的生長與繁殖。但此類藥物存在一定副作用,如產生骨髓抑制等,孕婦使用可能導致胎兒流產[10]。米諾環素為半合成四環素,在四環素類藥物中抗菌作用最強,具有抗菌、抗支原體、衣原體等作用。研究顯示,米諾環素能抑制多種炎癥介質和細胞因子的產生,在抗炎、抗菌等免疫調節的同時亦具有強大的神經保護作用[3,11]。本實驗旨在評價米諾環素體外抑制弓形蟲速殖子增殖作用。
本研究顯示:體外Hela細胞內,MNC和SMX均能較好的抑制弓形蟲速殖子的增殖。72 h,與未給藥組比較,MNC和SMX給藥組活蟲數均顯著減少,表現為弓形蟲密度影的顯著降低,但兩給藥組之間活蟲數差異無統計學意義;96 h,隨著培養時間的延長和藥物的作用,速殖子的增殖受到進一步抑制,并呈現異常形態,如蟲體膨脹、活性減弱等,與未給藥組比較,MNC和SMX兩給藥活蟲計數顯著減少,兩給藥組之間活蟲計數差異無統計學意義;120 h,各實驗組弓形蟲密度均進一步減弱,各組間活蟲計數差異無統計學意義,可能是由于藥物的持續作用、營養物質消耗、代謝產物大量堆積,細胞環境不利于弓形蟲生長,故出現大量死蟲。
綜上所述,米諾環素體外能較好地抑制弓形蟲速殖子增殖。由于MNC在抗菌的同時可下調免疫應答,降低過度免疫反應對機體造成的傷害[12],因此具有高效和長效性,在四環素類中,其抗菌作用最強。不僅如此,MNC還有一定的抗支原體、衣原體、真菌感染作用。本實驗證實米諾環素體外具有一定抗弓形蟲感染作用,為弓形蟲病的治療提供一個新思路。若生物體在感染弓形蟲的同時感染對米諾環素敏感的細菌,使用MNC治療或許能起到更好的效果。
[1]楊慧,武一娜,苑文英,等.弓形蟲感染與慢性疾病的關系[J].中國老年學雜志,2013,33(10):2468-2469.
[2]苑文英,趙清,張平,等.白細胞介素家族在弓形蟲感染中的作用[J].中國血吸蟲病防治雜志,2010,22(1):96-99.
[3]Yong VW,Wells J,Giuliani F,et al.The promise of minocycline in neurology[J].Lancet Neurol,2004,3(12):744-751.
[4]陳莉,朱乃軍,袁媛.米諾環素對人臍靜脈內皮細胞-單核細胞黏附的抑制作用及其機制研究[J].中國藥房,2015,26(31):4381-4384.
[5]趙瑩,呂芳麗.匹多莫德體外抑制弓形蟲增殖作用的研究[J].熱帶醫學雜志,2013,13(5):531-534.
[6]Tardiuex I,Menard R.Migration of apicomplexa across biological barriers:the Toxoplasma and Plasmodium rides[J].Traffic,2008,9 (5):627-635.
[7]Suzuki Y,Orellana MA,Schreiber RD,et al.Interferon-gamma:the major mediator of resistance against Toxoplasma gondii[J].Science, 1988,240(4851):516-518.
[8]Mordue DG,Monroy F,La RM,et al.Acute toxoplasmosis lead to lethal overproduction of Th1 cytokines[J].J Immunol,2001,167(8): 4574-4584.
[9]Gavrilescu LC,Denkers EY.IFN-gamma overproduction and high level apoptosis are associated with high but not low virulence toxoplasma gondii infection[J].J Immunol,2001,167(2):902-909.
[10]王大為,郭曉改,司海洋,等.弓形蟲感染治療方法的研究進展[J].黑龍江畜牧獸醫,2016,3:54-57.
[11]Wang J,Wei Q,Wang CY,et al.Minocycline up-regulates Bcl-2 and protects against cell death in mitochondria[J].J Biol Chem,2004, 279(19):19948-19954.
[12]姚滿林,曾耀英,黃秀艷,等.米諾環素對小鼠T淋巴細胞體外活化和增殖的影響[J].現代免疫學,2008,28(2):136-141.
In vitro effects of Minocycline on the proliferation of Toxoplasma gondii.
ZHAO Ying,YANG Xiao-yan,CHEN Shun-yi,LIAO Li-yin.Department of Clinical Laboratory,Guangzhou Panyu District Central Hospital,Guangzhou 511400, Guangdong,CHINA
ObjectiveTo evaluate the in vitro effect of Minocycline on the proliferation of Toxoplasma gondii. MethodsThe T.gondii tachyzoites were cultured in Hela cells.The cells were divided into the SMX-treated group,Minocycline-treated group and untreated control group.Proliferation of the tachyzoites and morphological changes were observed,and the numbers of live tachyzoites at 72 h,96 h and 120 h were recorded after using drugs.ResultsAt 72 hours after treatment,compared with the untreated control group,the the numbers of live tachyzoites in SMX-treated group and Minocycline-treated group were significantly decreased[(2.08±0.40)vs(15.17±2.07),P<0.01;(1.42±0.20)vs (15.17±2.07),P<0.01].At 96 hours after treatment,compared with the untreated control group,the the numbers of live tachyzoites in SMX-treated group and Minocycline-treated group were significantly decreased[(1.42±0.20)vs(10.92± 0.47),P<0.01;(1.92±0.33)vs(10.92±0.47),P<0.01].At 120 hours after treatment,there were no significant difference in the the number of live tachyzoites among the three groups(P>0.05).ConclusionMinocycline can inhibit T.tachyzoite proliferation in vitro.
In vitro;Toxoplasma gondii;Minocycline;Tachyzoites
R531.8
A
1003—6350(2017)07—1036—03
10.3969/j.issn.1003-6350.2017.07.002
2016-10-11)
廣東省廣州市番禺區科技計劃項目(編號:2015-Z03-18)
陳順儀。E-mail:1277063279@qq.com

