必要時T支架術邊支開口優化治療冠狀動脈分叉病變的初步臨床研究
蔡 煒, 鄭行春, 羅育坤, 彭亞飛, 林朝貴, 陳良龍
目前,冠狀動脈分叉病變(coronary bifurcation lesion, CBL)仍然是經皮冠狀動脈介入治療(percutanous coronary intervention, PCI)領域極富挑戰性的難題之一,約占冠心病介入治療的15%~20%[1-2]。已有研究顯示,多數CBL應用單支架治療具有良好的臨床療效且技術簡單,雙支架治療效果總體上并不優于單支架。因此,現行的專家共識及指南傾向于采用簡單的處理策略(必要時T支架術)[3-5]。
必要時T支架術作為分叉病變介入治療的初始策略時,主支植入支架后,若邊支不需要植入支架,是否需要以及如何優化邊支開口尚無定論[6-9]。現有資料顯示,主支支架植入后有無對吻擴張對分叉病變介入治療的主要心血管不良事件(major adverse cardiovascular events, MACE)無顯著影響[7-8,10]。陳良龍等提出的邊支開口優化技術(ostial optimization technique, OOT)有別于經典的同步對吻擴張技術,在利用OOT優化邊支開口時,通常選擇較小的非順應球囊及特殊的依偎球囊序貫對吻擴張技術[11]。體外模擬研究證實,OOT可有效推開/外翻覆蓋于邊支開口的主支支架,并使其充分覆蓋邊支開口上緣斑塊負荷較高的區域,減少邊支開口殘余狹窄,降低分叉部支架貼壁不良發生率,避免新生血管嵴殘留,可實現“單支架植入-雙支架開口覆蓋”的實際效果,有望進一步降低支架內再狹窄的發生率及支架內血栓的風險。然而,在臨床處理分叉病變時,OOT的實際臨床應用效果尚待進一步驗證。
本研究擬通過單醫學中心回顧性觀察隊列研究的方法,以冠狀動脈真性分叉病變患者為研究對象,比較必要時T支架術中主支支架植入后有無OOT治療冠狀動脈真性分叉病變的臨床結果,以期為OOT技術的應用提供臨床證據。
1 對象與方法
1.1對象 收集2014年1月-2016年12月于筆者科室接受冠狀動脈造影并采用必要時T支架術治療的冠狀動脈真性分叉病變患者45例,男性40例,女性5例;年齡(62.33±11.71)歲(38~92歲)。45例均未植入補救性邊支支架,同時完成1年臨床或電話隨訪。入選標準:(1)穩定型心絞痛、不穩定型心絞痛或急性非ST段抬高型心肌梗死患者;(2)De novo冠狀動脈真性分叉病變(Medina分型為0,1,1;1,1,1;1,0,1);(3)病變適合PCI治療(若左主干分叉病變,SYNTAX評分≤32),且必要時病變適合雙支架植入者。排除標準:(1)急性ST段抬高型心肌梗死患者;(2)病變不適合PCI治療,如SYNTAX評分>32者;(3)孕婦或計劃妊娠者;(4)造血系統明顯異常者,如血小板<100×109L-1或>700×109L-1、白細胞<3×109L-1;(5)預期壽命<12月;(6)合并肝腎功能不全。45例按有無OOT分為2組,其中OOT組22例,男性20例,女性2例,年齡(63.14±11.57)歲(38~81歲);無OOT組23例,男性20例,女性3例,年齡(61.57±12.05)歲(45~92歲)。2組患者的年齡、性別及高血壓病、糖尿病、高脂血癥、吸煙史等危險因素及空腹血糖、甘油三酯、膽固醇、低密度脂蛋白膽固醇、心率、既往心肌梗死及PCI病史等比較,差別均無統計學意義(P>0.05,表1),具有可比性。
表12組患者基線特征比較
Tab1Comparison of baseline characteristics between the two groups

變 量 OOT組 無OOT組n 22 23年齡/歲63.14±11.5761.57±12.05n男性(%)20(90.9)20(87.0)n高血壓病(%)12(54.5)13(56.5)收縮壓/mmHg127.91±20.34131.22±17.76舒張壓/mmHg78.55±9.7775.87±11.13心率/min-169.82±10.3673.17±14.79n糖尿病(%)8(36.4)5(21.7)c空腹血糖/(mmol·L-1)6.42±1.876.22±1.86c同型半胱氨酸/(mmol·L-1)13.01±9.0412.15±8.08n高脂血癥(%)7(31.8)8(34.8)cTG/(mmol·L-1)1.63±0.781.71±1.09cTC/(mmol·L-1)4.00±0.894.26±1.11cLDL-C/(mmol·L-1)2.61±0.822.74±0.99n吸煙(%)11(50.0)16(69.6)n既往心肌梗死(%)1(4.5)5(21.7)n既往PCI(%)3(13.6)8(34.8)冠心病類型 n穩定型心絞痛(%)3(13.60)3(13.0) n不穩定型心絞痛(%)13(59.1)15(65.2) n急性心肌梗死(%)6(27.3)5(21.7)
1 mmHg=133.3 Pa. OOT:邊支開口優化技術;TG:甘油三酯;TC:膽固醇;LDL-C:低密度脂蛋白膽固醇.
1.2方法
1.2.1藥物治療 所有患者術前12 h均給予負荷量的阿司匹林(300 mg,拜耳醫藥保健有限公司)、氯吡格雷(300 mg,杭州賽諾菲安萬特制藥有限公司)或替格瑞洛(180 mg,阿斯利康制藥有限公司)。術中根據冠狀動脈情況酌情使用血小板糖蛋白GPⅡb/Ⅲa受體拮抗劑。術后如無出血等特殊情況,終身服用阿司匹林100 mg/d,氯吡格雷75 mg/d或替格瑞洛180 mg/d,至少12月。
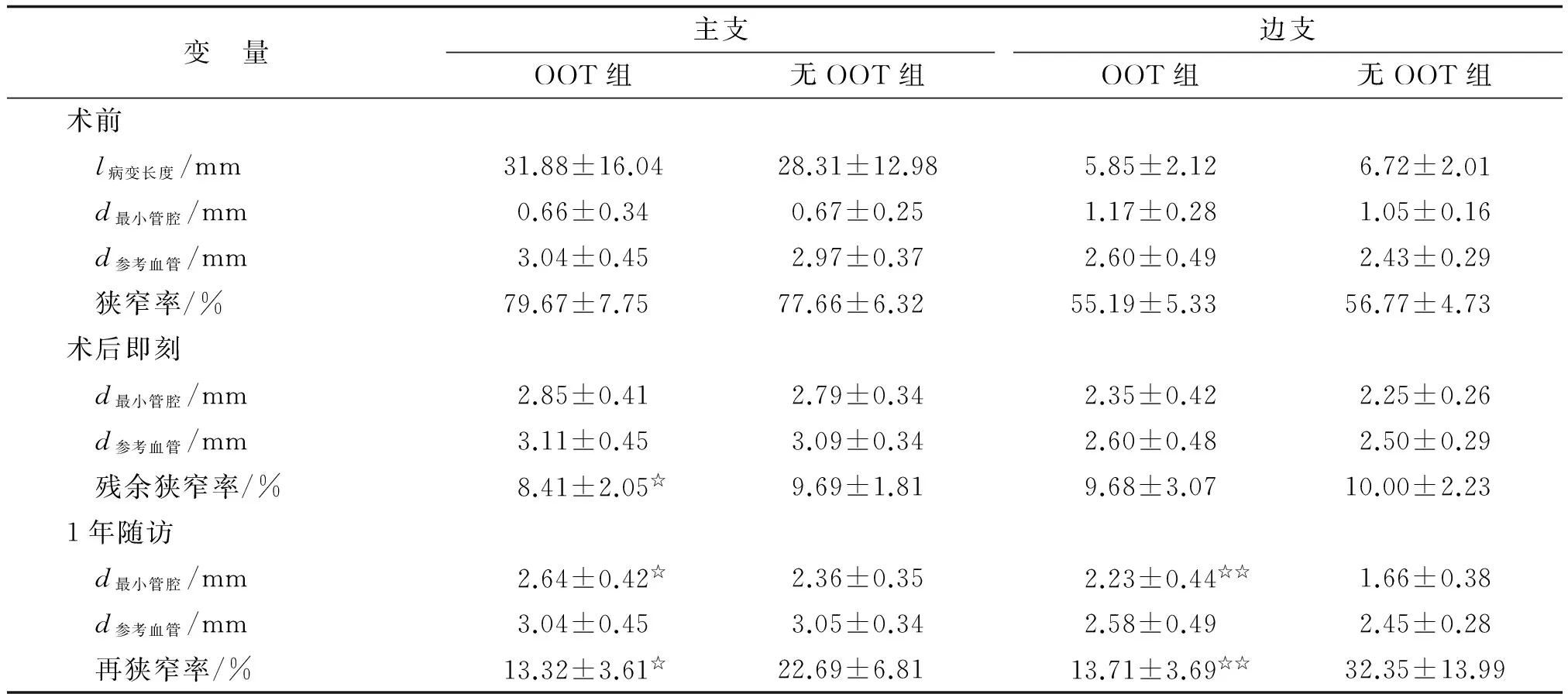
1.2.2PCI治療 所有患者均由具有心臟介入資質的專科醫師完成冠狀動脈造影檢查,采用定量冠狀動脈造影分析(quantitative coronary angiography, QCA)及SYNTAX評分評估患者冠狀動脈病變情況。血管內超聲(intravascular ultrasound, IVUS)的使用及支架品牌的選擇均由術者自行判斷。OOT組患者在主支植入支架后,選用與近端參考血管直徑相匹配或略大的、足夠短的非順應性球囊進行近端優化擴張(proximal optimisation technique, POT),確保靠近分叉嵴部交換邊支導絲,隨后沿主支及邊支導絲分別送入與參考血管直徑匹配的非順應性球囊完成OOT擴張,即依偎球囊序貫對吻擴張技術,邊支球囊微突入主支管腔(與主支球囊呈依偎對位),先擴張邊支,緊接著對吻擴張主支(無間斷地、邊支球囊不減壓),對吻擴張結束,雙球囊同步減壓,如此可使位于邊支開口的主支支架有效“唇樣”外翻,進入并覆蓋邊支血管開口的上緣部分,最后沿主支導絲送入非順應性球囊行再次近端優化擴張(re-POT)并結束手術。無OOT組患者在主支植入支架后,常規交換邊支導絲并行POT擴張,冠狀動脈內給予200 μg硝酸甘油充分擴張,交叉投照體位造影評估分叉部病變情況,若邊支開口狹窄<75%或邊支血流無明顯受限,則不行邊支球囊擴張,若邊支開口狹窄>75%或血流 1.3研究終點及定義 1.3.1研究終點 研究的首要終點是隨訪1年時的MACE,包括心源性死亡、心肌梗死和靶血管/病變血運重建(target vessel/lesion revascularization, TVR/TLR),僅將患者第1次發生的MACE納入統計分析。次級終點為造影隨訪的最小管腔直徑及直徑再狹窄程度。 1.3.2終點定義 (1)心源性死亡:根據美國學術研究協會(Academic Research Consortium, ARC)的定義[12],心源性死亡定義為由心臟原因如心肌梗死、心衰、致命性心律失常等導致的死亡,或支架手術引發的死亡。此外,難以解釋的不明原因死亡亦計入心源性死亡。(2)心肌梗死:參照第3版心肌梗死全球定義[13]。(3)TVR:包括左主干、前降支、回旋支及右冠狀動脈。無論靶病變部位,還是靶病變的上游或下游,任何血運重建,包括PCI或冠狀動脈旁路移植術(coronary artery bypass grafting, CABG)治療,均視作為TVR。 2.1手術情況比較 冠狀動脈造影顯示患者分叉病變部位,OOT組中,左主干前三叉2例(9.1%),前降支-對角支19例(86.4%),回旋支-鈍緣支1例(4.5%),無右冠狀動脈后三叉病例;無OOT組中,左主干前三叉3例(13.0%),前降支-對角支18例(78.3%),回旋支-鈍緣支1例(4.3%),右冠狀動脈后三叉1例(4.3%)。2組比較,差別無統計學意義(P>0.05,表2)。2組病變Medina分型及SYNTAX評分、置入平均支架長度及直徑、平均手術時間、總透視時間以及造影劑用量比較,差別均無統計學意義(P>0.05,表2)。 表22組患者病變特征及手術風險評分比較 Tab2Comparison of baseline lesion characteristics and procedural detail between the two groups 變 量OOT組無OOT組n2223病變部位 左主干前三叉2(9.1)3(13.0) 前降支-對角支19(86.4)18(78.3) 回旋支-鈍緣支1(4.5)1(4.3) 右冠狀動脈01(4.3)Medina分型 0,1,16(27.3)4(17.4) 1,1,18(36.4)12(52.2) 1,0,18(36.4)7(30.4)SYNTAX評分22.20±10.0320.02±7.81d平均支架直徑/mm3.00±0.383.04±0.33l平均支架長度/mm24.59±5.3126.13±4.63t手術/min31.12±2.1130.48±2.23t總透視/min20.32±2.6020.35±2.55V造影劑用量/mL128.95±6.91127.87±8.94 病變部位及Medina分型數據為n(%). OOT:邊支開口優化技術. 2.2復查冠狀動脈造影情況 所有患者于PCI術后9~12月復查冠狀動脈造影。2組患者術前主支及邊支血管病變長度、最小管腔直徑、參考血管直徑、狹窄率差別均無統計學意義(均為P>0.05)。PCI術后即刻,2組患者主支及邊支血管最小管腔直徑、參考血管直徑、殘余狹窄率差別無統計學意義(均為P>0.05)。術后1年,隨訪復查冠狀動脈造影時,OOT組主支血管最小管腔直徑、再狹窄率均顯著優于無OOT組,差別有統計學意義。2組術后1年最小管腔直徑分別為(2.64±0.42)及(2.36±0.35)mm(P=0.024),主支血管再狹窄率分別為(13.32±3.61)%及(22.69±6.81)%(P<0.01)。OOT組邊支血管最小管腔直徑、再狹窄率均顯著優于無OOT組,差別有統計學意義。2組術后1年邊支血管最小管腔直徑分別為(2.23±0.44)mm及(1.66±0.38)mm(P<0.01),邊支血管再狹窄率分別為(13.71±3.69)%及(32.35±13.99)%(P<0.01,表3)。 2.3住院期間及臨床隨訪結果 2組患者住院期間造影及手術成功率均為100%。1年隨訪結束時,OOT組共計1例發生MACE,為主支血管再狹窄,行TVR。無OOT組共計3例發生MACE,其中1例為分支血管閉塞致急性心肌梗死,2例為主支血管再狹窄,均行TVR。2組比較,終點事件發生率差別無統計學意義(P>0.05)。 冠狀動脈分叉由于其解剖形態的特殊性,心臟搏動、分叉角度的變化以及分叉部壁面剪切應力變化等,均使冠狀動脈分叉部的血液流動較非分叉部位更為復雜,更容易導致動脈粥樣硬化斑塊的形成和進展。Alamri及Tsuchida等研究顯示,分叉病變約占PCI的15%~20%[2,14]。目前,多數指南及專家共識傾向于推薦采用簡單的策略治療CBL,如“單支架術”或“必要時T支架術”。然而,主支支架植入后發生的斑塊移位“鏟雪現象”、血管嵴偏移等,均導致主支支架植入后邊支血管血流受限或開口狹窄加重,從而需要對邊支血管進行進一步的介入干預(球囊擴張或植入補救性支架)。因此,主支支架植入后合理的邊支開口優化處理策略不可或缺。最終球囊對吻擴張(final kissing balloon dilatation, FKBD)技術最早用于減輕分叉部主支球囊擴張時的“斑塊鏟雪”現象[15-16]。在復雜的雙支架術中,FKBD可以糾正PCI術后分叉部支架的幾何形態及血管嵴偏移,降低多邊形匯合區(polygon of confluence, POC)區域支架貼壁不良率,因此可減少分叉部支架晚期管徑丟失,并降低支架內再狹窄率。多個研究證實,高質量的FKBD可明顯降低分叉病變雙支架術后MACE事件的發生率[3,17-19]。然而,目前FKBD多應用于雙支架術式,在簡單策略(必要時T支架術)中,單支架植入后FKBD能否獲得更多的臨床獲益仍存在爭議。 盡管單支架置入后同步球囊對吻擴張(kissing balloon dilatation, KBD)的遠期有效性存在很大的爭議,但當邊支血流受限(部分專家共識建議TIMI血流<3級)時,仍是臨床邊支開口處理策略的不二選擇。同步雙球囊對吻擴張的核心是:將主支球囊和邊支球囊分別送到目標位置,兩球囊近端標記在母血管段(proximal main vessel, PMV)或POC對齊,同步充盈主支和邊支球囊,完成對吻擴張后同步減壓,避免血管嵴移位。KBD的技術優勢在于:開放邊支開口的同時維持主支血管開口形態的完整性,降低主支支架的變形及貼壁不良的發生率。然而Gwon等研究證實,單支架植入術后的KBD不但沒有改善臨床預后反而增加TLR的發生率[20]。體外模擬研究進一步證實,KBD可使兩球囊重疊段支架呈橢圓形,而主支近端支架形態的改變又是導致支架內再狹窄及TLR發生的主要原因之一[10,21-24]。 表3 2組患者靶病變QCA測量結果 OOT:邊支開口優化技術;QCA:定量冠狀動脈造影. 與無OOT組比較,☆:P<0.05;☆☆:P<0.01. OOT技術由陳良龍首次提出,技術核心為依偎球囊序貫對吻擴張,是針對雙球囊同步對吻擴張技術缺陷的重大改良創新,其主要技術細節為:(1)靠近分叉嵴部交換導絲[必要時可在IVUS或光學相干斷層成像(Optical coherence tomography,OCT)指導下完成],避免金屬支架梁殘留形成金屬血管嵴;(2)采用依偎對位的球囊定位方式,確保主支球囊與邊支球囊的最少重疊,在有效開放邊支開口的基礎上,避免了主支支架內過多球囊重疊導致的支架變形;(2)序貫球囊擴張方式即微突入主支的邊支球囊以一定壓力優先膨脹,固定外翻支架梁長度;隨后主支球囊膨脹,產生垂直于邊支血管軸向的推力推擠邊支球囊,使支架梁充分外翻并覆蓋邊支開口上緣;(3)雙球囊同步減壓,避免血管嵴偏移;(4)再次近端優化擴張技術確保主支近端支架形態及良好的支架貼壁。上述技術處理使得序貫對吻擴張技術在確保支架梁充分外翻覆蓋邊支開口上緣的同時不破壞主支支架形態,實現了“單支架植入-雙支架開口覆蓋”的效果。 本研究為回顧性隊列觀察研究,評價OOT技術在治療冠狀動脈真性分叉病變的安全性及有效性。研究結果顯示:(1)OOT成功率以及手術成功率均達到100%。(2)盡管OOT技術要求術者盡量靠近分叉嵴部交換邊支導絲,但借助于POT,可大大降低邊支導絲交換及球囊定位的難度,相比經典的同步對吻擴張,其平均手術時間、總透視時間以及造影劑用量均無明顯差異。(3)1年造影隨訪顯示,相比無OOT組,OOT組主支支架內及邊支血管近段的再狹窄明顯降低,主支支架內及邊支血管近段的最小管腔直徑明顯增加,差別具有統計學意義,證明了OOT技術的安全性及有效性。(4)1年臨床隨訪結束時,OOT組發生MACE僅1例,無OOT組3例,2組間差別未達到統計學意義,考慮其主要原因為樣本量較小所致。 綜上所述,OOT技術可有效降低主支支架和邊支血管的再狹窄率及MACE的發生率,是一種安全、有效的邊支開口優化處理技術,值得臨床推廣應用。本研究為回顧性研究,且樣本量較小,其結論具有一定局限性,OOT技術治療真性分叉病變的長期臨床療效仍需大規模前瞻性多中心RCT試驗的證實。 [1] Martin D M, Murphy E A, Boyle F J. Computational fluid dynamics analysis of balloon-expandable coronary stents: influence of stent and vessel deformation[J].MedEng&Phys, 2014,36(8):1047-1056. [2] Alamri H S, Alotaiby M, Almoghairi A,etal. Lessons from the SYNTAX trial[J].JSaudiHeartAssoc, 2010,22(2):35-41. [3] Lassen J F, Holm N R, Banning A,etal. Percutaneous coronary intervention for coronary bifurcation disease: 11th consensus document from the European Bifurcation Club[J].EuroIntervention, 2016,12(1):38-46. [4] Hildick-Smith D, de Belder A J, Cooter N,etal. Randomized trial of simple versus complex drug-eluting stenting for bifurcation lesions: the British Bifurcation Coronary Study: old, new, and evolving strategies[J].Circulation, 2010,121(10):1235-1243. [5] Hildick-Smith D, Behan M W, Lassen J F,etal. The EBC two study (European Bifurcation Coronary TWO): a randomized comparison of provisional t-stenting versus a systematic 2 stent culotte strategy in large caliber true bifurcations[J].CircCardiovascInterv, 2016,9(9):e003643. [6] Hariki H, Shinke T, Otake H,etal. Potential benefit of final kissing balloon inflation after single stenting for the treatment of bifurcation lesions--insights from optical coherence tomography observations[J].CircJ, 2013,77(5):1193-1201. [7] Niemel? M, Kervinen K, Erglis A,etal. Randomized comparison of final kissing balloon dilatation versus no final kissing balloon dilatation in patients with coronary bifurcation lesions treated with main vessel stenting: the Nordic-Baltic Bifurcation Study Ⅲ[J].Circulation, 2011,123(1):79-86. [8] Biondi-Zoccai G, Sheiban I, De Servi S,etal. To kiss or not to kiss? Impact of final kissing-balloon inflation on early and long-term results of percutaneous coronary intervention for bifurcation lesions[J].Heart&Vessels, 2014,29(6):732-42. [9] Yamawaki M, Muramatsu T, Kozuma K,etal. Long-term clinical outcome of a single stent approach with and without a final kissing balloon technique for coronary bifurcation[J].CircJ, 2014,78(1):110-121. [10] Rahman S, Leesar T, Cilingiroglu M,etal. Impact of kissing balloon inflation on the main vessel stent volume, area, and symmetry after side-branch dilation in patients with coronary bifurcation lesions: a serial volumetric intravascular ultrasound study[J].JACCCardiovascInterv, 2013,6(9):923-931. [11] 陳良龍, 蔡 煒. 冠狀動脈分叉病變介入治療精要[M]. 北京:人民衛生出版社, 2013:90-99. [12] Cutlip D E, Windecker S, Mehran R,etal. Clinical end points in coronary stent trials: a case for standardized definitions[J].Circulation, 2007,115(17):2344-2351. [13] Thygesen K, Alpert J S, Jaffe A S,etal. Third universal definition of myocardial infarction[J].EurHeartJ, 2012,33(20):2551-2567. [14] Tsuchida K, Colombo A, Lefevre T,etal. The clinical outcome of percutaneous treatment of bifurcation lesions in multivessel coronary artery disease with the sirolimus-eluting stent: insights from the Arterial Revascularization Therapies Study part Ⅱ(ARTS Ⅱ)[J].EurHeartJ, 2007,28(4):433-442. [15] Fischman D L, Savage M P, Leon M B,etal. Fate of lesion-related side branches after coronary artery stenting[J].JAmCollCardiol, 1993,22(6):1641-1646. [16] Aliabadi D, Tilli F V, Bowers T R,etal. Incidence and angiographic predictors of side branch occlusion following high-pressure intracoronary stenting[J].AmJCardiol, 1997,80(8):994-997. [17] Gwon H C, Song Y, Hahn J Y. TCT-13: Side branch ballooning after main vessel stenting may increase the long-term risk of target lesion revascularization rate in the coronary bifurcation lesion[J].JAmCollCardiol, 2010, 56(suppl):B3. [18] Ge L, Airoldi F, Iakovou I,etal. Clinical and angiographic outcome after implantation of drug-eluting stents in bifurcation lesions with the crush stent technique: importance of final kissing balloon post-dilation[J].JAmCollCardiol, 2005,46(4):613-620. [19] Chen S L, Mintz G, Kan J,etal. Serial intravascular ultrasound analysis comparing double kissing and classical crush stenting for coronary bifurcation lesions[J].CatheterCardiovascInterv, 2011,78(5):729-736. [20] Gwon H C, Hahn J Y, Koo B K,etal. Final kissing ballooning and long-term clinical outcomes in coronary bifurcation lesions treated with 1-stent technique: results from the COBIS registry[J].Heart, 2012,98(3):225-231. [21] Finet G, Derimay F, Motreff P,etal. Comparative analysis of sequential proximal optimizing technique versus kissing balloon inflation technique in provisional bifurcation stenting: fractal coronary bifurcation bench test[J].JACCCardiovascInterv, 2015, 8(10):1308-1317. [22] Mortier P, Hikichi Y, Foin N,etal. Provisional stenting of coronary bifurcations: insights into final kissing balloon post-dilation and stent design by computational modeling[J].JACCCardiovascInterv, 2014,7(3):325-333. [23] Foin N, Torii R, Mortier P,etal. Kissing balloon or sequential dilation of the side branch and main vessel for provisional stenting of bifurcations: lessons from micro-computed tomography and computational simulations[J].JACCCardiovascInterv, 2012,5(1):47-56. [24] Mortier P, de Beule M, Dubini G,etal. Coronary bifurcation stenting: insights frominvitroand virtual bench testing[J].EuroIntervention, 2010, 6(Suppl):53-60.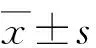
2 結 果
3 討 論