高中化學建模解題方法及其應用
姜文敬
【摘要】文章首先介紹了高中化學建模解題方式的含義及使用步驟,進而分析了幾種常見高中化學題目建模法解題的途徑。
【關鍵詞】高中化學;建模解題;方法;應用
高中化學是我們每一位高中生都必須認真學習的學科,但是高中化學又是一門極其抽象的學科,我們在學習的過程中往往會覺得很多題目的反應過程過于復雜,知識解題思緒混亂。而面對這些問題的最佳解題方式便是建模法,通過建模法將復雜繁瑣的化學反應簡易化和清晰化,進而達到易于解題的效果。
一、高中化學建模解題方式的含義及使用步驟
(一)建模解題方法的含義
高中化學建模解題法指的是使用建構模式的方式,解決實際問題的一種高中化學解題方式。根據布魯姆教育目標的分類原理觀察,可以將實際問題通過概括和抽象處理之后,將其轉化為模型給以表達出來;然后再利用所掌握的化學題目解題的方法和知識對建立的模型進行進一步分析;最后再將模型給以推廣,通過類比的方式實現一類問題的解答[1]。
(二)建模解題方法的解題步驟
在高中化學建模法的應用解題步驟上分為以下幾個部分。對實際問題進行審題—抽象、概括—建立模型—模型解讀—分析模型—解答模型問題—解決實際問題[2]。
二、常見高中化學題目建模法解題分析
(一)建構等效化學式模型
例一:已知現有KCl和NaCl的混合物,在該混合物中a%為Cl元素質量,求該混合物中K、Na的質量占比各為多少?
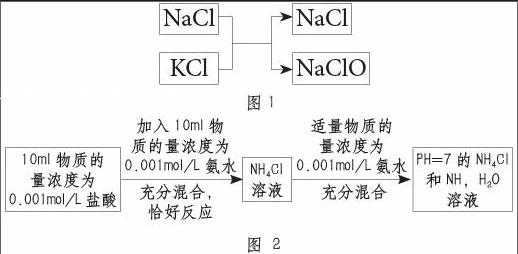
首先對題目進行觀察,混合溶液中求兩個陽離子的質量比,其陰離子為一種元素,對陽離子的質量進行觀察K為39,Na為23,可知K比Na大16,而16剛好是O的分子量,所以可以將K使用Na和O進行代替,即將KCl,建模等效為NaClO,如圖1所示。
然后在建立的模型內進行題目的解答。去100g作為研究的對象,將NaCl視為一個整體,故此可以在混合溶液中的各個元素含量有n(K)=n(O),n(NaCl)=n(Cl)。
因此K的含量比K%=(100-58.5a/35.5)/16,Na的含量等于1減去K的含量比和Cl的含量比,為Na%=1-a%-K%。
這類混合溶液的問題,在高中化學中是十分常見的一類問題,文章所舉的例題是較為簡單的一道題,是實際的題目中可能溶液中含有的元素成分更為復雜,甚至還可能會在混合后發生一些反應。我們在解決這類問題時,需要重點找到溶液中固定不變的元素含量,并且找到其他元素含量之間的系數關系,建模法是解決該類問題的有效解題方式之一,其可以很大程度上將一些復雜的計算步驟給以避免,出現錯誤的可能性更低。但是建模法也并不是唯一的解題方式,也不一定是最佳的解題方式,還需要我們面對實際題目時,根據題目的具體情況選擇最佳的解題方式[3]。
(二)建構等效化學反應過程模型
例二:已知有10毫升的鹽酸溶液,其摩爾濃度為0.001mol/L,此時向該鹽酸溶液中倒入相同濃度的氨水,直至溶液的濃度達到pH=7,請問以下關系式正確的有()
A c(Cl-)﹥C(OH-)>c(NH4+)>C(H+)
B c(NH4+)=c(Cl-)>c(H+)=c(OH-)
C V(總)<20毫升
D V(總)>20毫升
面對該類題型我們在解答時也可以首先考慮使用建模法的方式進行解題。我們可以清楚10毫升的鹽酸溶液,其摩爾濃度為0.001mol/L,如果加入10毫升的氨水溶液,其摩爾濃度也為0.001mol/L,那么兩者會出現完全的反應,所以最后生成的NH4Cl,故此溶液呈現酸性,因此需要達到pH=7,就需要繼續向溶液中加入氨水溶液,因此必然氨水溶液的體積大于鹽酸溶液,因此兩者混合的總體積必然大于二倍鹽酸溶液體積,大于20毫升,因此D選項正確,C錯誤。然后我們就可以將整個反應過程進行等效的建模,具體反應模型過程見圖2.
然后對剩余的兩項選項進行觀察,其中A選項c(Cl-)﹥C(OH-)>c(NH4+)>C(H+),溶液中陰離子總數不可能大于陽離子總數,因此為錯誤選項。然后對建模構成進行觀察,可知在溶液中必有c(Cl-)+C(OH-)=c(NH4+)+C(H+)。而最后溶液又呈中性,所以C(OH-)=C(H+),c(Cl-)=c(NH4+),而顯然最后生成溶液為NH4Cl,所以c(Cl-和c(NH4+)必然會大于C(OH-)和C(H+),因此B選項c(NH4+)=c(Cl-)>c(H+)=c(OH-)正確,最后正確答案為B、D。
這類元素單質及化合物在高中化學知識體系中,也是考察很多的一個知識點,并且該類題型的難度一般較大,在高考的選擇題中屬于中上難度的題目。而這類題型最大的特點便是反應十分復雜,并且元素之間的關系也多,而這也是建模法應用其中的原因,可以通過使用建模清晰將反映過程表示出來,進而對化學反應的過程進行直觀的表達,對我們解決該類問題很有效果。
結束語:
高中化學建模解題法指的是使用建構模式的方式實現實際問題解答的一種高中化學解題方式。文章以自己在化學學習中的感觸為背景,簡易闡述了建構等效化學式模型、建構等效化學反應過程模型兩種建模法的應用途徑,希望可以給更多的同學以感觸和啟迪。
參考文獻:
[1]楊鎰濤,周鑫.幾種建模思想在高中化學解題中的應用[J].理科考試研究(高中版),2016,23(2):88.
[2]劉宗華.初探在高中化學學習中運用建模思想[J].中學課程輔導(教學研究),2014,20(26):99-100.
[3]鄭大江.建模思想在高中化學選擇題中的應用[J].理科考試研究(高中版),2013,20(6):57-58.

