TNF-α+489位點多態(tài)性與慢性阻塞性肺疾病易感性關(guān)系的Meta分析
梁歡 何杰 李小燕 李萬成 方恩容
?
TNF-α+489位點多態(tài)性與慢性阻塞性肺疾病易感性關(guān)系的Meta分析
梁歡1何杰2李小燕2李萬成2方恩容2
610041 成都,四川大學(xué)華西醫(yī)院感染科1
【摘要】目的探討TNF-α+489位點多態(tài)性與慢性阻塞性肺疾病(COPD)發(fā)病風(fēng)險的相關(guān)性。方法計算機檢索PubMed、EMbase、WanFang、CNKI文獻數(shù)據(jù)庫,查找國內(nèi)外關(guān)于TNF-α+489多態(tài)性與慢性阻塞性肺疾病易感性關(guān)系的病例對照研究,檢索時限為建庫至2015年7月20日。由2名評價者根據(jù)納入和排除標(biāo)準(zhǔn)篩選文獻,提取并評價資料后,采用RevMan 5.2軟件及Stata 10.0軟件進行Mete分析。結(jié)果在這項薈萃分析中,共納入13個研究,有病例組患者2 459例、對照組患者2 823例;Meta分析結(jié)果顯示,對于總體人群而言TNF-α+489位點基因多態(tài)性與慢性阻塞性肺疾病的患病風(fēng)險不相關(guān)(OR=1.20,95% CI: 0.96~1.50,P=0.11 )。在研究人群種族的基礎(chǔ)上進行亞組分析,結(jié)果顯示:在高加索人群及亞組人群中,TNF-α+489與慢性阻塞性肺疾病(COPD)易感性關(guān)聯(lián)均無統(tǒng)計學(xué)意義。吸煙是慢性阻塞性肺疾病最重要的危險因素之一,本研究對吸煙人群進行亞組分析,結(jié)果表明在這類人群中TNF-α+489與COPD易感性關(guān)聯(lián)也無統(tǒng)計學(xué)意義(OR=1.24,95% CI: 0.96~1.59,P=0.09)。結(jié)論TNF-α+489基因多態(tài)性與COPD的發(fā)病風(fēng)險可能不存在相關(guān)性。
【關(guān)鍵詞】肺疾病,慢性阻塞性;腫瘤壞死因子-α;Meta分析;多態(tài)性
慢性阻塞性肺疾病(chronic obstructive pulmonary disease, COPD)是全球最主要的慢性疾病之一,對患者的健康、生活質(zhì)量以及病死率有重要影響,其特點是不完全可逆的氣流受限和持續(xù)性氣道炎癥[1-3]。據(jù)世界衛(wèi)生組織的估計,在2014大約有6千萬人罹患COPD,三百多萬人死于該病[4]。COPD的發(fā)生和進展過程復(fù)雜,有各種危險因素參與,包括環(huán)境因素、遺傳因素和吸煙狀況等[5]。雖然吸煙是COPD發(fā)展的主要危險因素,但只有不到20%的吸煙者發(fā)展成為COPD[6];COPD患者中非吸煙者占了相當(dāng)比例[7];這一結(jié)果表明環(huán)境和遺傳因素可能在COPD的發(fā)病機制中有著重要作用[8-10]。
腫瘤壞死因子-α(tumor necrosis factor-α, TNF-α)是由巨噬細胞β單核細胞活化產(chǎn)生的一種具有多種生物學(xué)效應(yīng)的細胞因子,在COPD患者的痰液、支氣管肺泡灌洗液、肺活檢標(biāo)本中均可發(fā)現(xiàn)[11-13]。TNF-α在COPD患者早期氣道炎癥開始時即發(fā)揮著重要作用[14-15]。已有研究表明在COPD患者的急性加重期和穩(wěn)定期均能檢測到高濃度的TNF-α[12]。TNF-α的表達受相關(guān)基因多態(tài)性的調(diào)控,TNF +489基因多態(tài)性是最近研究熱點之一。+489G/A是TNF-α基因第一內(nèi)含子,參與TNF-α轉(zhuǎn)錄水平調(diào)節(jié),控制TNF-α的轉(zhuǎn)錄活性[16-18]。在過去的十年中,有大量的文獻研究關(guān)于TNF-α+489多態(tài)性與COPD發(fā)病風(fēng)險的相關(guān)性,但是TNF-α基因與COPD的關(guān)系在不同人群種族、性別、年齡等因素下得到的結(jié)論不盡一致。Teramoto等[19]研究顯示,TNF-α+ 489多態(tài)性與COPD發(fā)病風(fēng)險無顯著相關(guān)性。同樣,Gingo等[20]對美國人群的研究中也證實了這一結(jié)論。然而,Kücükaycan等[21]發(fā)現(xiàn)TNF-α+489位點可能是增加COPD患病風(fēng)險的危險因素。為了進一步探討TNFα+ 489位點多態(tài)性與COPD易感性的關(guān)系,本研究采用Meta分析方法,綜合評價TNF-α+489位點是否與COPD發(fā)病風(fēng)險相關(guān)。
資料與方法
一、 檢索策略
計算機全面檢索PubMed,EMBASE,CNKI,CBM,Wanfang data,VIP數(shù)據(jù)庫中有關(guān)TNF-α+489多態(tài)性和COPD發(fā)病風(fēng)險的病例-對照研究(檢索時限:均從建庫至2015年7月)。文獻檢索策略采用主題詞和自由詞結(jié)合的原則,中文檢索詞包括:慢性阻塞性肺疾病、腫瘤壞死因子TNF-α、多態(tài)性等,英文檢索詞包括:chronic obstructive pulmonary disease、COPD、tumor necrosis factor-alpha、TNF-α、polymorphism等。
二、納入與排除標(biāo)準(zhǔn)
所有的研究都符合以下的納入標(biāo)準(zhǔn):①研究內(nèi)容為詳細描述TNF-α+489多態(tài)性與COPD發(fā)病風(fēng)險的相關(guān)性的文獻;②研究設(shè)計類型:病例-對照研究;③病例-對照組基因型分布適中;④對照組基因型分布必須符合Hardy-Weinberg(HWE)遺傳定律;⑤ 研究對象 根據(jù)相關(guān)指南明確診斷為COPD患者。排除標(biāo)準(zhǔn):①以家系為基礎(chǔ)研究;②研究方法不是以病例-對照研究,不能提供確切基本信息;③文摘、會議、重復(fù)文獻;④對照組基因型分布不符合Hardy-Weinberg(HWE)遺傳定律。
三、文獻篩選、數(shù)據(jù)提取與質(zhì)量評價
兩名獨立的研究員按照納入排除標(biāo)準(zhǔn)對文獻質(zhì)量進行逐一篩選,并提取數(shù)據(jù)。對于符合標(biāo)準(zhǔn)的文獻均提取以下內(nèi)容:第一作者、出版時間、國家( 地區(qū)) 、種族、 樣本大小、病例組-對照組數(shù)量,病例組和對照組基因型分布數(shù)量等。當(dāng)意見不同時,由第三名研究人員協(xié)助評估解決。對每個納入研究按照STERGA原則進行質(zhì)量評分。評價內(nèi)容如下:①樣本量是否充分;②診斷標(biāo)準(zhǔn)是否清楚;③對照組是否與病例組具有可比性,對照組基因分布是否符合遺傳平衡定律;④分組匹配情況;⑤基因檢測方法合理性;⑥數(shù)據(jù)是否充分。以上6條,每滿足1條計1分,總分大于3分視為質(zhì)量可靠性好。
四、統(tǒng)計學(xué)方法
采用Cochrane 協(xié)助網(wǎng)RevMan 5.2版本軟件對研究數(shù)據(jù)進行統(tǒng)計學(xué)分析,采用OR值與95%CI為效應(yīng)量評價TNF-α+489多態(tài)性與COPD易感性的關(guān)系。首先對納入研究的對照組基因型進行Hardy-Weinberg遺傳定律檢驗,若不符合HWE,予以排除。對符合HWE的研究分別計算其在5種遺傳模型(AA+AGvs. GG、AAvs. GA+GG、AAvs. GG、AGvs. GG、Avs. G)下的基因型分布,并采取Q檢驗進行異質(zhì)性分析,若P>0.1且I2<50%,采用固定效應(yīng)模型進行Meta分析;反之,采用隨機效應(yīng)模型進行Meta分析。發(fā)表偏倚的檢驗采用Stata10.0軟件進行分析。
結(jié) 果
一、 文獻檢索結(jié)果
從PubMed、CNKI、萬方數(shù)據(jù)庫初步收索出242篇文獻,見圖1。經(jīng)過逐步篩選,最終納入12篇符合納入排除標(biāo)準(zhǔn)文獻,共13項病例對照研究[18,20-30]。有7項研究在亞洲人群中進行,有6項在高加索人群中進行。所有研究中COPD患者2 459例、健康對照組2 823例。有11項病例對照研究包含了吸煙者。依據(jù)STERGA原則對所有納入文獻質(zhì)量進行評價,所有文獻質(zhì)量總分均大于3分,質(zhì)量可靠性好,各研究文獻的基本情況特征,見表1。各納入研究的基因型和等位基因分布情況,見表2。

表1 納入研究的基本特征
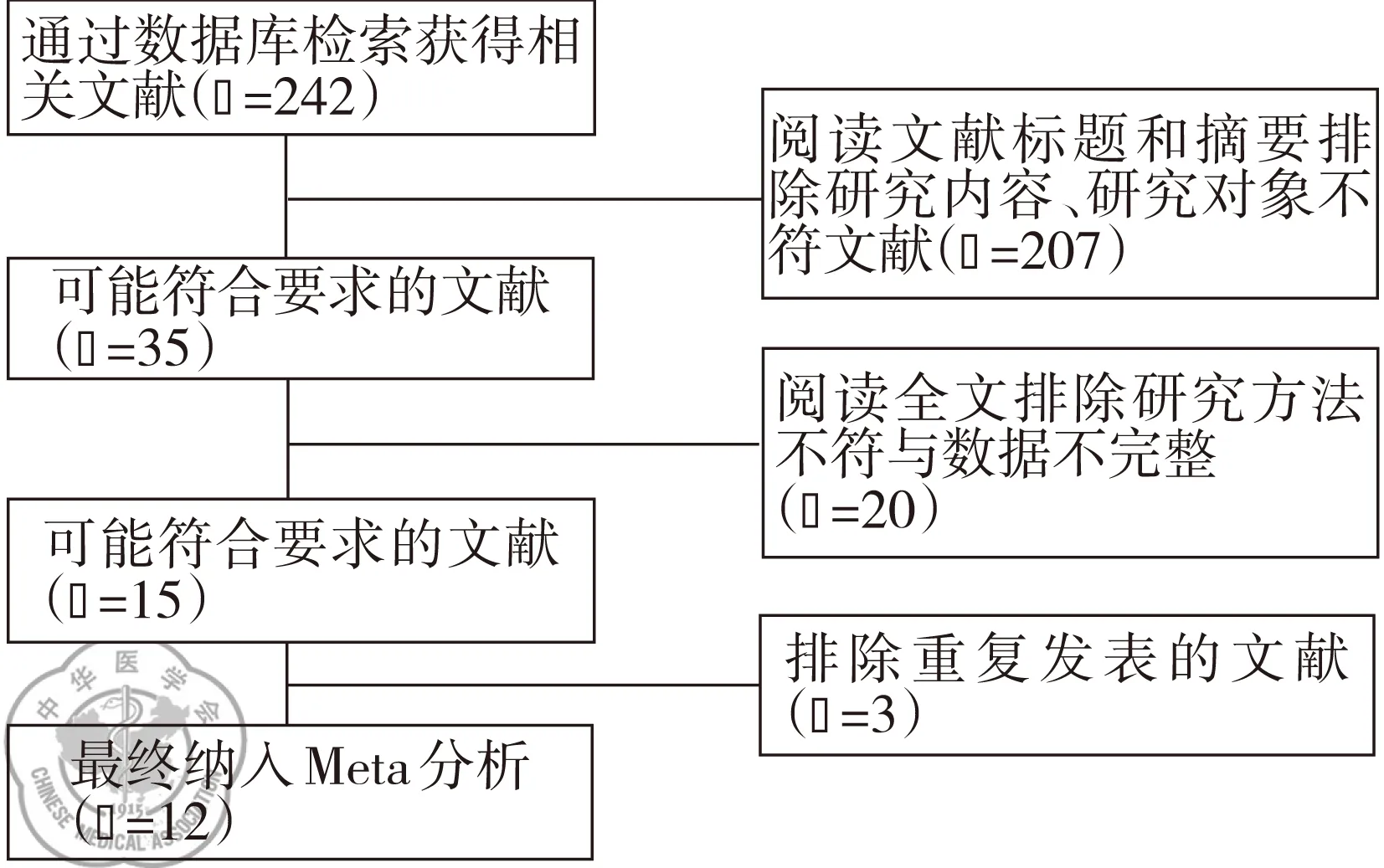
圖1文獻篩選流程及結(jié)果
二、Meta分析結(jié)果
1. 總體人群中的TNF-α+489多態(tài)性與COPD易感性的關(guān)系的Meta分析:本組研究納入的13項研究中,經(jīng)異質(zhì)性檢驗,各研究間存在統(tǒng)計學(xué)異質(zhì)性(χ2=28.29,P=0.005)。因此,采用隨機效應(yīng)模型來分析數(shù)據(jù),結(jié)果顯示:對總體人群而言,TNF-α+489G/A基因多態(tài)性與慢性阻塞性肺疾病易感性關(guān)聯(lián)無統(tǒng)計學(xué)意義 (Avs. G:OR=1.20,95%CI: 0.96~1.50,P=0.11),攜帶等位基因A的個體可能與COPD發(fā)病風(fēng)險無相關(guān)性,見圖2。各個基因組比較,見表3。

圖2TNF-α-489位點多態(tài)性與COPD易感性關(guān)系的總體及亞組分析結(jié)果(Avs. G)
2. 吸煙人群中的TNF-α+489多態(tài)性與COPD易感性的關(guān)系的Meta分析:由于吸煙是慢性阻塞性肺病的主要危險因素之一,本研究對吸煙者進行了Meta分析,發(fā)現(xiàn)TNFα+489多態(tài)性與COPD發(fā)病風(fēng)險之間存無顯著相關(guān)性(Avs. G:OR=1.24,95%CI:
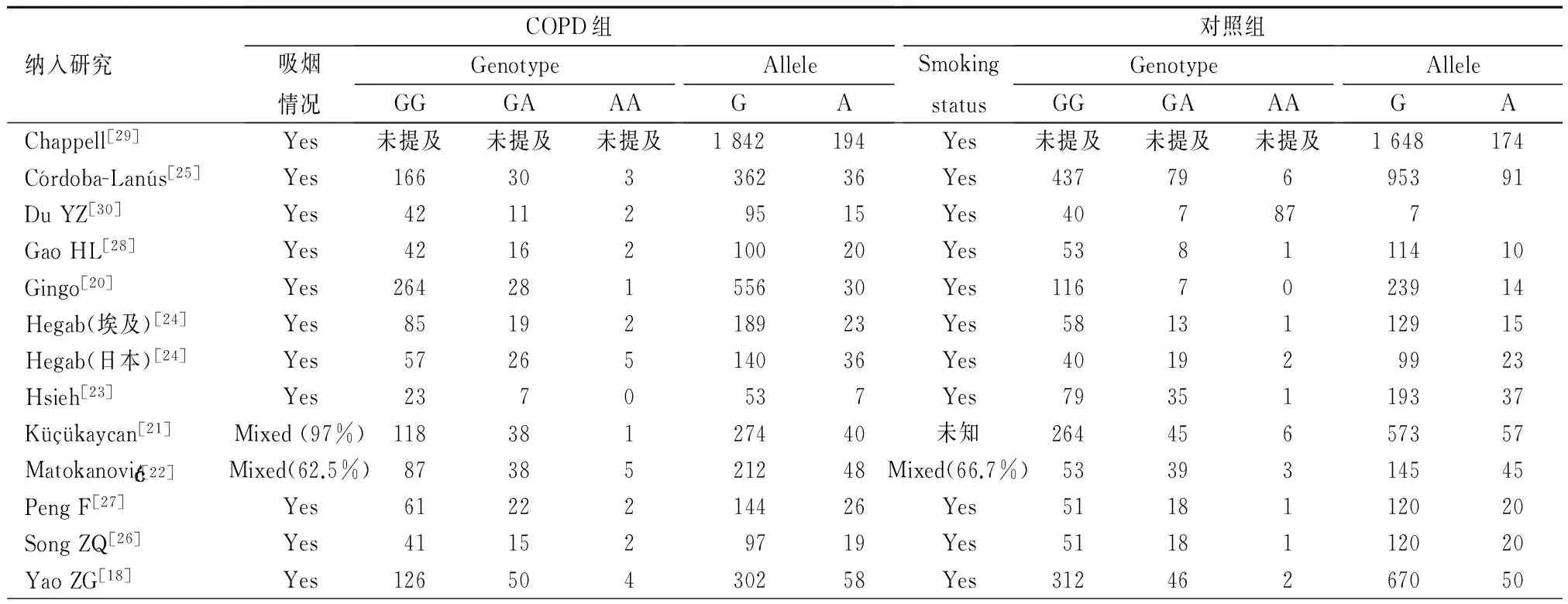
表2 納入研究基因型頻率分布
注:Genotype:基固類型;Allele:等位基因;GG、GA、AA、A:基因型
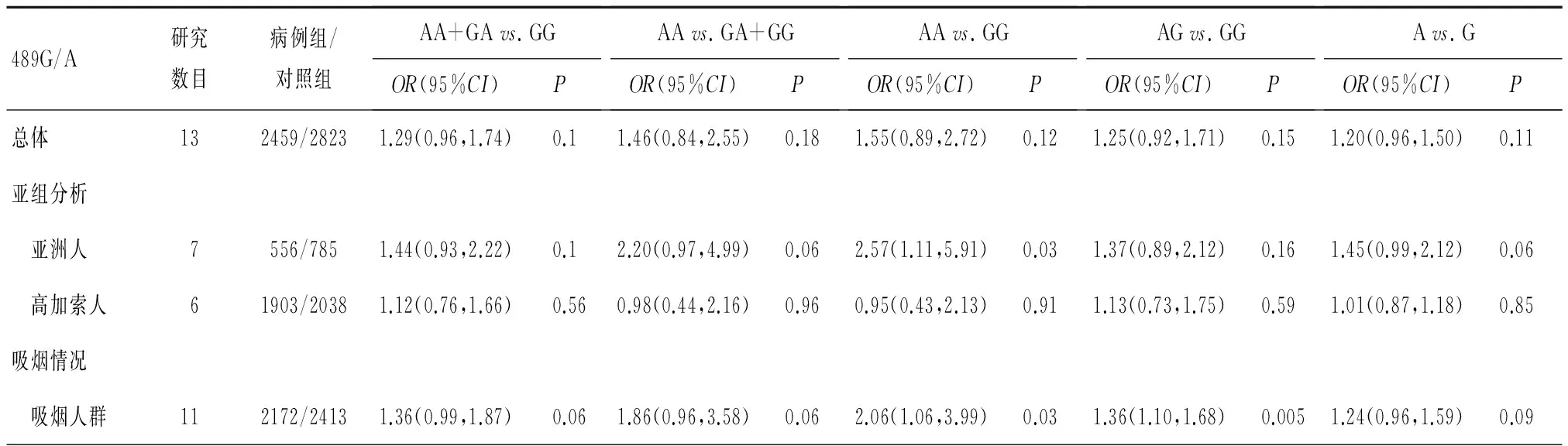
表3 各種遺傳模型的Meta分析結(jié)果
注:GG、GA、AA、A:基因型
0.96~1.59,P=0.09),見圖3,其他比較結(jié)果,見表3。

圖3TNF-α-489位點多態(tài)性與COPD易感性關(guān)系在吸煙人群中的分析結(jié)果(Avs. G)
3. TNF-α+489多態(tài)性與不同人群COPD關(guān)系的Meta分析結(jié)果:13項研究分為亞洲人群、高加索人群,使用等位基因模型進行Meta分析發(fā)現(xiàn),在亞洲人群中,TNF-α+489基因多態(tài)性與COPD發(fā)病風(fēng)險不相關(guān)(Avs. G:OR=1.45, 95%CI: 0.99~2.12,P=0.06),同時,在高加索人群中,TNF-α+489基因多態(tài)性與COPD發(fā)病風(fēng)險也不存在相關(guān)性(Avs. G:OR=1.02, 95%CI: 0.87~1.18,P=0.84),見圖2,其余基因型比較結(jié)果,見表3。
三、發(fā)表偏倚分析及敏感性分析
本研究采用Begg檢驗法、Egger回歸法檢驗發(fā)表偏倚。Begg′s漏斗圖的形狀對稱,見圖4。同時采用Egger線性回歸法檢驗漏斗圖數(shù)據(jù)有無統(tǒng)計學(xué)意義(t=0.10,P=0.920)。以上數(shù)據(jù)表明,在本次Meta分析中納入文獻無發(fā)表偏倚。依次剔除每一病例對照研究,統(tǒng)計學(xué)結(jié)果未發(fā)生明顯改變,其結(jié)果表明納入的每個研究權(quán)重均對分析結(jié)果無明顯影響。
討 論
TNF-α基因位于人染色體的6p21.3區(qū)域,其編碼的蛋白在免疫及炎癥反應(yīng)中發(fā)揮著重要作用[14]。在COPD患者血液和痰中檢測到高濃度TNF-α表明,TNF-α參與了COPD局部和全身炎癥反應(yīng)[21]。由于TNF-α的表達受其基因多態(tài)性的調(diào)控,近年來,越來越多研究者均在研究TNF-α基因多態(tài)性對COPD易感性的影響。已有研究報道,TNF-α+489基因含等位基因A的可以促進TNF-α產(chǎn)生,并參與介導(dǎo)COPD患病易感性[30-31]。然而,目前TNF-α+ 489基因突變導(dǎo)致COPD發(fā)病風(fēng)險增高的機制仍未明確。Castaldi等[32]對TNF-α+489多態(tài)性與COPD易感性進行了系統(tǒng)評價,認(rèn)為攜帶等位基因A的個體可能增加COPD的患病風(fēng)險,但在過去幾年中,有較多研究發(fā)表了關(guān)于不同人群中TNF-α+489多態(tài)性與COPD易感性的文章,其結(jié)論不盡相同,這些新的數(shù)據(jù)資料應(yīng)該被納入。因此,TNF-α+489多態(tài)性與COPD易感性值得我們將所有符合條件的研究納入進行分析,以便于我們準(zhǔn)確的得到兩者間的關(guān)系。

圖4納入文獻的發(fā)表偏倚分析
本研究系統(tǒng)評價了TNF-α+489多態(tài)性與COPD易感性的相關(guān)病例對照研究。共納入13項研究,包括2 459例COPD患者和2 823例健康正常人,采用等位基因模型進行Meta分析,對于總體人群而言,TNF-α+489多態(tài)性和COPD易感性關(guān)聯(lián)無統(tǒng)計學(xué)意義;本研究結(jié)果表明,攜帶A基因及其等位基因的人可能不會增加或降低COPD發(fā)病風(fēng)險。因納入研究人群的遺傳背景不同,本研究又按種族不同進行了亞組分析:亞洲人群和高加索人群。和以前的研究結(jié)論不同,TNF-α+489多態(tài)性在亞洲人群及高加索人群中與COPD發(fā)病風(fēng)險不存在相關(guān)性。造成這種結(jié)果的原因可能為:①TNF-α其他位點共同參與編碼TNF-α蛋白,可能只有部分TNF-α基因位點多態(tài)性涉及COPD疾病的發(fā)生;②不同位點的TNF-α基因多態(tài)性可能與不同疾病相關(guān)聯(lián),TNF-α基因?qū)NF-α水平的調(diào)控可能存在細胞、組織以及器官的特異性,并與外界不同刺激因素相關(guān)聯(lián);③與臨床異質(zhì)性,如:年齡、生存環(huán)境、吸煙情況、性別、基礎(chǔ)肺功能等因素相關(guān)。根據(jù)吸煙情況進行分層分析時,發(fā)現(xiàn)吸煙人群的TNF-α基因多態(tài)性與COPD發(fā)病風(fēng)險無顯著相關(guān)性,表明吸煙狀況可能不會影響TNF-α+489多態(tài)性對COPD易感性。在本研究中,納入的各個研究間存在一定異質(zhì)性,其原因可能是:納入研究的人群和種族不同;各納入研究的具體診斷標(biāo)準(zhǔn)、基因檢測的方法不盡相同;吸煙人群的研究樣本量相對較少,尤其是亞洲人群。據(jù)此,繼續(xù)研究其他位點的單核苷酸特性,分析多個位點多態(tài)性與環(huán)境因素在COPD中的協(xié)同作用,以及在內(nèi)環(huán)境中多個單核苷酸多態(tài)性對TNF-α表達的影響,將有可能進一步明確TNF-α基因多態(tài)性在COPD中的作用。
本研究也存在一定局限性,首先,本次研究納入的數(shù)據(jù)局限于中文文獻、英文文獻,可能會導(dǎo)致部分潛在研究缺失;其次,由于缺乏原始數(shù)據(jù),不能對納入研究的其他臨床資料,如年齡、性別、肺功能分級以及地區(qū)進行分析;再次,部分研究局限于亞洲人和白種人,缺乏對其他人群的研究,因此本研究結(jié)論只適用亞洲及高加索人群的分析。盡管存在以上局限性,本研究通過制定詳細的研究計劃將偏倚控制在最小范圍內(nèi),如數(shù)據(jù)提取、統(tǒng)計分析等,保證了本研究結(jié)果的可信度。
綜上所述,TNF-α+489多態(tài)性與COPD發(fā)病風(fēng)險可能不存在相關(guān)性。為了進一步探索基因-基因、基因-環(huán)境的交互作用對TNF-α基因多態(tài)性與COPD發(fā)病風(fēng)險的影響,仍需要開展大樣本量、多中心、多基因以及同質(zhì)性較好的病例對照研究。
參考文獻
1任成山, 錢桂生. 慢性阻塞性肺疾病發(fā)病機制研究現(xiàn)狀與展望[J/CD]. 中華肺部疾病雜志:電子版, 2009, 2(2): 104-115.
2van Dijk WD, Gupta N, Tan WC, et al. Clinical relevance of diagnosing COPD by fixed ratio or lower limit of normal: a systematic review[J]. COPD, 2014, 11(1): 113-120.
3Wang W, Li P, Chen Y, et al. Association between beta2-adrenergic receptor-16Arg/Gly gene polymorphism and chronic obstructive pulmonary disease risk: systematic review and meta-analysis[J]. Iran J Public Health, 2014, 43(7): 877-888.
4Park H, Jung SY, Lee K, et al. Prevalence of chronic obstructive lung disease in Korea using data from the fifth Korea national health and nutrition examination survey[J]. Korean J Fam Med, 2015, 36(3): 128-134.
5Bagdonas E, Raudoniute J, Bruzauskaite I, et al. Novel aspects of pathogenesis and regeneration mechanisms in COPD[J]. Int J Chron Obstruct Pulmon Dis, 2015, 10: 995-1013.
6Zhang S, Wang C, Xi B, et al. Association between the tumour necrosis factor-alpha-308G/A polymorphism and chronic obstructive pulmonary disease: an update[J]. Respirology, 2011, 16(1): 107-115.
7Lamprecht B, McBurnie MA, Vollmer WM, et al. COPD in never smokers: results from the population-based burden of obstructive lung disease study[J]. Chest, 2011, 139(4): 752-763.
8Marciniak SJ, Lomas DA. What can naturally occurring mutations tell us about the pathogenesis of COPD?[J]. Thorax, 2009, 64(4): 359-364.
9Wei L, Xu D, Qian Y, et al. Comprehensive analysis of gene-expression profile in chronic obstructive pulmonary disease[J]. Int J Chron Obstruct Pulmon Dis, 2015, 10: 1103-1109.
10Hobbs BD, Hersh CP. Integrative genomics of chronic obstructive pulmonary disease[J]. Biochem Biophys Res Commun, 2014, 452(2): 276-286.
11Ji J, von Scheele I, Bergstrom J, et al. Comsect1ment differences of inflammatory activity in chronic obstructive pulmonary disease[J]. Respir Res, 2014, 15: 104.
12Keatings VM, Collins PD, Scott DM, et al. Differences in interleukin-8 and tumor necrosis factor-alpha in induced sputum from patients with chronic obstructive pulmonary disease or asthma[J]. Am J Respir Crit Care Med, 1996, 153(2): 530-534.
13Takabatake N, Arao T, Sata M, et al. Circulating levels of soluble Fas ligand in cachexic patients with COPD are higher than those in non-cachexic patients with COPD[J]. Intern Med, 2005, 44(11): 1137-1143.
14Li YF, Gauderman WJ, Avol E,et al. Associations of tumor necrosis factor G-308A with childhood asthma and wheezing[J]. Am J Respir Crit Care Med, 2006, 173(9): 970-976.
15Mukhopadhyay S, Hoidal JR, Mukherjee TK. Role of TNFalpha in pulmonary pathophysiology[J]. Respir Res, 2006, 7: 125.
16Noguchi E, Yokouchi Y, Shibasaki M, et al. Association between TNFA polymorphism and the development of asthma in the Japanese population[J]. Am J Respir Crit Care Med, 2002, 166(1): 43-46.
17Lucey EC, Keane J, Kuang PP, et al. Severity of elastase-induced emphysema is decreased in tumor necrosis factor-alpha and interleukin-1beta receptor-deficient mice[J]. Lab Invest, 2002, 82(1): 79-85.
18姚志剛, 王浩彥, 賈楠. TNF-α+308、TNF-α+489基因態(tài)性與慢性阻塞性肺疾病的相關(guān)性研究[J]. 現(xiàn)代中西醫(yī)結(jié)合雜志, 2012, 21(22): 2400-2402.
19Teramoto S, Ishii T, Ishii M, et al. Variation in the tumour necrosis factor-alpha gene is not associated with susceptibility to Asian COPD[J]. Eur Respir J, 2008, 31(3): 682-683.
20Gingo MR, Silveira LJ, Miller YE, et al. Tumour necrosis factor gene polymorphisms are associated with COPD[J]. Eur Respir J, 2008, 31(5): 1005-1012.
21Kücükaycan M, Van Krugten M, Pennings HJ, et al. Tumor necrosis factor-alpha+489G/A gene polymorphism is associated with chronic obstructive pulmonary disease[J]. Respir Res, 2002, 3: 29.
22Matokanovic M, Rumora L, Popovic-Grle S, et al. Association of hsp70-2 (+1267A/G), hsp70-hom (+2437T/C), HMOX-1 (number of GT repeats) and TNF-alpha (+489G/A) polymorphisms with COPD in Croatian population[J]. Clin Biochem, 2012, 45(10-11): 770-774.
23Hsieh MH, Chong IW, Hwang JJ, et al. Lack of associations between several polymorphisms in cytokine genes and the risk of chronic obstructive pulmonary diseases in Taiwan[J]. Kaohsiung J Med Sci, 2008, 24(3): 126-137.
24Hegab AE, Sakamoto T, Saitoh W, et al. Polymorphisms of TNFalpha,IL1beta, and IL1RN genes in chronic obstructive pulmonary disease[J]. Biochem Biophys Res Commun, 2005, 329(4): 1246-1252.
25Córdoba-Lanús E, Baz-Dvila R, de-Torres JP, et al. TNFA-863 polymorphism is associated with a reduced risk of chronic obstructive pulmonary disease: a replication study[J]. BMC Med Genet, 2011, 12: 132.
26宋澤慶, 彭峰, 陳敏. TNF-α位基因多態(tài)性與慢性阻塞性肺疾病的易感性研究[J]. 中國現(xiàn)代醫(yī)學(xué)雜志, 2008, 18(19): 2775-2778.
27彭峰. TNF-α+489位基因多態(tài)性與慢性阻塞性肺疾病的易感性研究[C]. 廣東醫(yī)學(xué)院, 2008: 982-984.
28高歡玲. TNF-α和IL-6基因基因多態(tài)性與COPD易感性的關(guān)系研究[C]. 山西醫(yī)科大學(xué), 2010: 39-42.
29Chappell S, Daly L, Morgan K et al. Variation in the tumour necrosis factor gene is not associated with susceptibility to COPD[J]. Eur Respir J, 2007, 30(4): 810-812.
30杜昀澤, 劉林林, 紀(jì)鳳祥, 等. 腫瘤壞死因子α+489G/A基因多態(tài)性與慢性阻塞性肺疾病的相關(guān)性研究[J]. 國際呼吸雜志, 2008, 28(12): 729-732.
31Murugan V, Peck MJ. Signal transduction pathways linking the activation of alveolar macrophages with the recruitment of neutrophils to lungs in chronic obstructive pulmonary disease[J]. Exp Lung Res, 2009, 35(6): 439-485.
32Castaldi PJ, Cho MH, Cohn M, et al. The COPD genetic association compendium: a comprehensive online database of COPD genetic associations[J]. Hum Mol Genet, 2010, 19(3): 526-534.
(本文編輯:黃紅稷)
梁歡,何杰,李小燕,等. TNF-α+489位點多態(tài)性與慢性阻塞性肺疾病易感性關(guān)系的Meta分析[J/CD]. 中華肺部疾病雜志: 電子版, 2016, 9(3): 286-291.
DOI:10.3877/cma.j.issn.1674-6902.2016.03.012
基金項目:四川省科技廳基金資助項目(2014JY0176)
通訊作者:何杰,Email: hejieli1987@sina.com
中圖法分類號:R563
文獻標(biāo)識碼:A
Corresponding author:He Jie, E-mail: hejieli1987@sina.com
(收稿日期:2015-08-18)
Tumor necrosis factor-α+489 polymorphism and risk of chronic obstructive pulmonary disease: A Meta-analysis
LiangHuan1,HeJie2,LiXiaoyan2,LiWancheng2,FangEnrong2.1Desect1mentofInfectiousDisease,WestChinaHospital,SichunUniversity,Chengdu610041,China,2Desect1mentofRespiratoryMedicine,TheFirstAffiliatedHospitalofChengduMedicalCollege,Chengdu, 610500,China
【Abstract】ObjectiveTo investigate the association between tumor necrosis factor-α+48(TNF-α+489) and the risk of chronic obstructive pulmonary disease(COPD) by Meta-analysis. MethodsThe Embase, PubMed, CNKI, Wanfang databases were searched to identify domestic and foreign case-control studies involving the association between TNF-α+489 polymorphism and risk of COPD (last updated to June 20th 2015). Two independent reviewers collected the data and reached an agreement on all items according to the inclusion and exclusion criteria and extracted data. Statistical analysis was performed by Revman 5.2 software and Stata10.0 software. ResultsA total of 2 459 cases and 2 823 controls in thirteen case-control studies were included in this Meta-analysis. The results suggested that the +489 G/A polymorphism in TNF-α gene might not be associated with risk of COPD (OR=1.20, 95% CI: 0.96-1.50, P=0.11 for A vs. G). In the subgroup by ethnicity, no significant associations were found in Asians (OR=1.45, 95% CI: 0.99-2.12, P=0.06) and in Caucasians (OR=1.02, 95% CI: 0.87-1.18, P=0.84) for the comparison of A vs. G. As smoking is one of the most crucial risk factors for COPD, a Meta-analysis that included only smokers was carried out. The results indicated that significant associations were not found in this population (OR=1.24, 95% CI: 0.96-1.59, P=0.09 for A vs. G). ConclusionResults from the current Meta-analysis indicate that the TNF-α+489 G/A polymorphism might not contribute to susceptibility to COPD.
【Key words】Chronic obstructive pulmonary disease;Tumor necrosis factor-α;Meta-analysis;Polymorphism
610500 成都,成都醫(yī)學(xué)院第一附屬醫(yī)院呼吸內(nèi)科2

