硫酸卡那霉素注射液含量測定的不確定度分析
于麗娜,徐嫄,韓寧寧,趙暉,郝利華
(中國獸醫藥品監察所,北京100081)
硫酸卡那霉素注射液含量測定的不確定度分析
于麗娜,徐嫄,韓寧寧,趙暉,郝利華
(中國獸醫藥品監察所,北京100081)
為研究微生物檢定法(管碟法)測定硫酸卡那霉素注射液生物效價試驗中各因素對結果的影響,采用不確定度分析,將影響因素歸納為稱量、稀釋、加樣、測定、平行試驗,量化各不確定度分量,評估各因素的影響因子。結果表明,牛津杯加樣體積對測定結果影響最大,提示試驗中應盡可能精確控制加樣體積。
微生物檢定法;硫酸卡那霉素注射液;效價;不確定度
目前,國際上通用的抗生素微生物檢定法包括管碟法和濁度法。管碟法,又稱杯碟法,是各國(獸)藥典收載的經典抗生素微生物檢定通用方法。管碟法操作步驟繁多,如何評估各操作步驟對測定結果的影響,從而提高管碟法的準確度是目前抗生素分析工作者所關心的問題之一。不確定度分析[1]通過對實驗過程各個環節引入的不確定度進行評估,可分析各因素對測定結果的影響。目前廣泛通用的不確定度評定模型是來自由ISO、IEC等七個國際組織聯合發布的《測量不確定度評估指南》[2]中的模型,也是國際上第一個取得一致認同的模型。根據《JJF1059.1-2012測量不確定度評定與表示》[3],本文對微生物檢定法(管碟法)測定硫酸卡那霉素注射液生物效價的不確定度進行了分析和評估。
1 儀器與試藥
CHB-1抗生素效價測量儀(北京潮聲技術開發公司);AX-205分析天平(瑞士Sartorius公司);恒溫培養室;硫酸卡那霉素標準品(USP標準品,775單位/mg,批號:35500J)與硫酸卡那霉素注射液供試品(某市售產品,規格10 mL∶1.0 g(100萬單位);Ⅰ號培養基(批號131105);枯草芽孢桿菌〔CMCC(B)63501〕(中國獸醫藥品監察所);磷酸二氫鉀與磷酸氫二鉀等試劑均為分析純。
2 方法與結果
2.1 供試品溶液的制備 取供試品3支,混合均勻,精密量取5mL,置50mL量瓶中,用滅菌水稀釋至刻度,精密量取該溶液5mL,置50mL量瓶中,用滅菌水稀釋至刻度,搖勻,制成每1mL中約含1000單位的溶液。精密量取該溶液(1000單位/mL)5 mL,置50 mL量瓶中,用磷酸鹽緩沖液(pH 7.8)稀釋至刻度,搖勻,制成每1 mL中約含100單位的溶液;再分別吸取該溶液(100單位/mL)2.00 mL,分置50 mL、100 mL量瓶中,分別用磷酸鹽緩沖液(pH 7.8)稀釋至刻度,搖勻,得到濃度分別為4單位/mL和2單位/mL的溶液,作為供試品溶液的高、低劑量。
2.2 標準品溶液的制備 精密稱取硫酸卡那霉素標準品32.26 mg,置25 mL量瓶中,加滅菌水溶解并稀釋至刻度,制成每1 mL中約含1000單位的溶液,稀釋同供試品溶液制備項下,自“精密量取該溶液(1000單位/mL)……”起,同法操作。
2.3 雙碟的制備與培養 取平底雙碟約7套(n),分別加入加熱融化的培養基20 mL,放置水平臺上使凝固,作為底層。另取加熱融化后的培養基適量,放冷至60℃,加入枯草芽孢桿菌的菌懸液適量,搖勻,在每一雙碟中分別加入5 mL,攤布均勻,作為菌層。冷卻后,在每一雙碟中以等距離安置不銹鋼小管4(k)個,待用。將上述稀釋好的標準品溶液與供試品溶液分別滴加于不銹鋼小管內,在35~37℃恒溫培養室中培養14~16 h。
2.4 抑菌圈直徑的測定與效價計算 取出培養好的雙碟,用抑菌圈測量儀測量各個抑菌圈的直徑,照生物檢定統計法[4]進行可靠性檢驗與效價計算。當可靠性檢驗結果為回歸非常顯著(P<0.01)與偏離平行不顯著(P>0.05)時,實驗結果才成立。測定結果見表1。
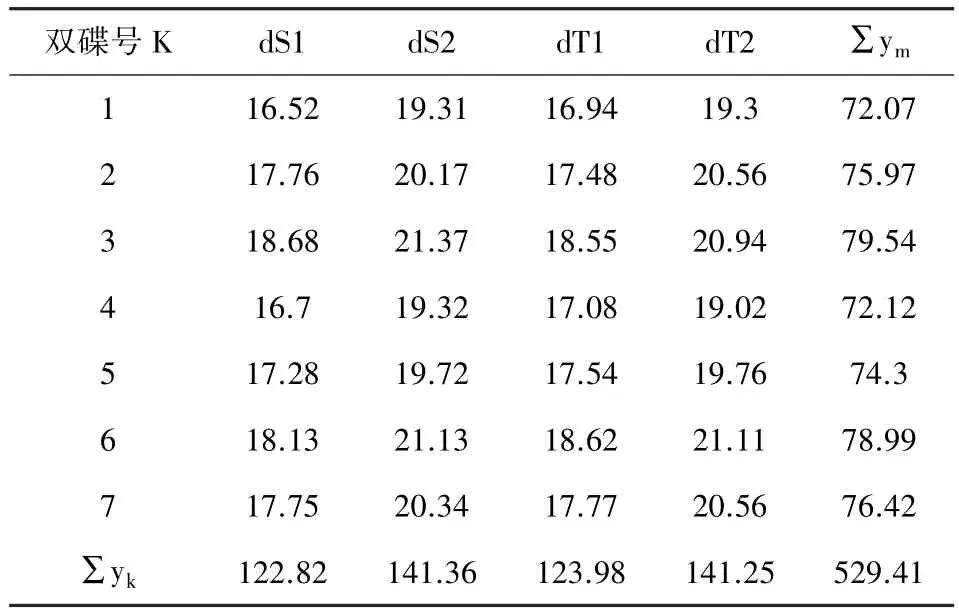
表1 抑菌圈直徑測量結果
3 測量不確定度評估
3.1 數學模型 效價由下式給出:

式中,P為供試品效價(相當于標示量或估計效價的百分含量),S2為標準品高濃度溶液所致的各抑菌圈直徑(面積)的總和,S1為標準品低濃度溶液所致的各抑菌圈直徑(面積)的總和,T2為供試品高濃度溶液所致的各抑菌圈直徑(面積)的總和,T1為供試品低濃度溶液所致的各抑菌圈直徑(面積)的總和,I為高、低劑量之比的對數,當劑量比為2∶1時,I=log2/1=0.3010,與所用碟數無關。
3.2 不確定度來源分析 對抗生素微生物檢定法(管碟法)二劑量法的不確定度來源進行分析,主要分為可直接估算的不確定度和不可直接估算的不確定度。可直接估算的不確定度有:稱量、稀釋、加樣、測定、平行試驗。不可直接估算的不確定度有:標準品純度、加樣時間、培養溫度。
3.3 可直接估算的標準不確定度
3.3.1 測量過程引入的不確定度
3.3.1.1 抑菌圈直徑重復測量引入的不確定度分量u測量(1) 在二劑量法中,由于每份測定報告都是由N個培養皿組成,抑菌圈直徑重復測量引入的不確定度分量為實際測量中供試品重復測量的標準偏差。對抑菌圈直徑的測量結果進行統計分析,計算效價(y)為101.54單位/mg,同時統計分析得自由度f=(k-1)(n-1)=18,其合并樣本標準差即標準不確定度為:

3.3.1.2 抑菌圈測量儀的不確定度分量u測量(2)自檢報告顯示,抑菌圈測量儀的最大允許誤差為±0.03 mm,則區間半寬度αP=0.03 mm,測量值落在該區間的概率分布為均勻分布,標準不確定度為0.03/3=0.017 mm;抑菌圈測量儀的標準圈直徑為19 mm,則相對標準不確定度為:

3.3.2 加樣過程引入的不確定度 在本實驗中,采用定量移液器向牛津杯中滴加抗生素溶液,加樣體積的不確定度來自于:①定量移液器的系統允差;②定量移液器重復量取偏差;③溫度校正引入的不確定度。
由廠商提供的信息可知,1 mL定量移液器的系統允差為±3.0%,則使用定量移液器量取0.27 mL液體的系統允差為±0.0081 mL,按矩形分布估計,標準偏差為:0.0081/3=0.00468mL;使用定量移液器重復量取10次,標準偏差為0.00372 mL;定量移液器應在23℃校準,量取抗生素溶液時溫度為25℃,與校準溫度有2℃的溫差,在95%的置信區間下,按均勻分布計,則標準偏差為
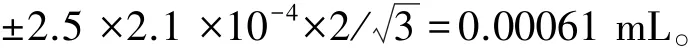
因此,使用定量移液器滴加抗生素溶液時,由加樣體積引入的合成不確定度為:
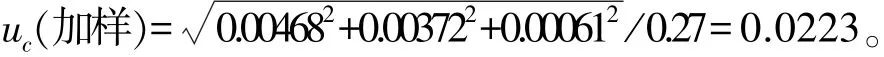
3.3.3 溶液配制引入的不確定度
3.3.3.1 量瓶、移液管的相對標準不確定度 根據《常用玻璃儀器檢定規程》[5]查得,A級100 mL、50 mL、25 mL單標線容量瓶的允許誤差分別為:±0.10 mL、±0.05 mL、±0.03 mL,以B類不確定度計算,按三角分布估計,則標準偏差分別為:0.10/6=0.0408mL,0.05/6=0.0204mL,0.03/6=0.0122mL;A級5mL和2 mL移液管最大允差分別為0.015 mL和0.010 mL,按B類不確定度評定,假定為三角形分布,則標準偏差分別為:0.015/6=0.006 mL,0.010/6=0.004 mL;配制溶液時,實驗室溫度接近15℃,容量器皿校準溫度為23℃,在95%的置信區間下,按均勻分布計,則標準偏差為±2.5×2.1× 10-4×8/3=0.0024 mL;因此,100 mL量瓶的相對標準偏差為:3.3.3.2 溶液配制的不確定度us(稀釋) 標準品溶液配制過程中分別使用100 mL(V?1)、50 mL(V?2)、25 mL(V?1)量瓶,5 mL移液管(V?1)、2 mL移液管(V?1),則如公式(1)。

供試品溶液配制過程中分別使用100mL(V?1)、50 mL(V?4)量瓶,5 mL移液管(V?1)、2 mL移液管(V?1),則如公式(2)。

3.3.4 稱量/取樣引入的不確定度
3.3.4.1 標準品取樣引入的不確定度 標準品為固體,采用稱量取樣,不確定度主要來自于:①稱量偏差;②天平校正偏差。
(1)稱量偏差:使用天平對同一質量恒定的物體(1 g,標準砝碼)反復稱量10次,其標準偏差為0.0099 mg。
(2)天平校正偏差:天平(AX205,d=0.01 mg)檢定證書標明其最大允差為0.10 mg,按矩形分布估計,校準不確定度為0.10=0.0577mg,上述分量必須計3
算2次,一次作為空盤,一次作為毛重,因為每次稱量均為獨立的觀測結果,兩者的線性影響不相關,因此

則標準品取樣的合成不確定度為:3.3.4.2 供試品取樣引入的不確定度 供試品為注射劑,采用5 mL移液管取樣,如前述,不確定度uT(取樣)為0.0013。
3.3.5 平行試驗引入的不確定度uc(平行) 根據《獸藥檢驗操作規程》“HYZY081-2011化學原料藥和制劑的含量測定法”規定,含量(效價)測定至少平行測定兩份。因此,平行量取供試品2份,同時操作,測定結果見表2,取兩次測定的平均值作為硫酸卡那霉素效價的測定結果,采用極差法對平行測定引入的不確定度進行評估。

表2 注射用硫酸卡那霉素平行測定結果

式中,A為1號供試品測得的效價比值;B為2號供試品測得的效價比值。
3.4 總合成標準不確定度u(x)rel

3.5 擴展不確定度U 將合成標準不確定度乘以一個給定概率的包含因子(k),得到擴展不確定度[6]。本文采用置信概率為95%的包含因子(k95),根據t分布表,取k=2,則擴展不確定度為:u(x)/x=0.024,x=10.09萬單位/mL,u(x)=0.024× 10.09萬單位/mL=0.24萬單位/mL。取k=2,則擴展不確定度為U=2u(x)=2×0.24萬單位/mL=0.48萬單位/mL。
硫酸卡那霉素效價測定的結果可表示為:(10.09±0.48)萬單位/mL(95%置信限)。
4 討論與小結
按照《中國藥品檢驗標準操作規范》[7],二劑量法加樣順序為:高濃度標準品溶液→高濃度供試品溶液→低濃度標準品溶液→低濃度供試品溶液,每次滴加的溶液應為同一濃度,雙碟數不超過5個,如樣品溶液滴加雙碟數目多,可分組滴加。對于不同的操作者而言,加樣方法略有不同。由加樣時間引入的不確定度對測定結果的影響為系統誤差,在試驗中,應盡量減少加樣時間,以將該因素的影響控制在最小,在不確定度分析中做零項處理[8]。恒溫培養室大小約為3m×1.5m,房間密閉,同時布有溫度檢測探頭,溫度區間為35~37℃,通過長期觀察記錄,溫度可穩定在35~37℃,因此,培養溫度對測定結果的影響可忽略不計。
綜上所述,各因素對測定結果影響如下:加樣體積>平行試驗>供試品/標準品溶液的配制>標準品稱量>抑菌圈重復測量>抑菌圈測量儀>供試品取樣。由此可見,當供試品為液體時,采用移液管取樣,供試品取樣引入的不確定度最小,儀器引入的不確定度次之,而牛津杯中的加樣體積,則是影響測定結果的關鍵因素。本文為分析微生物檢定法(管碟法)測定抗生素生物效價不確定度提供了可靠的方法,并為如何提高抗生素效價測定結果的準確度提供了參考依據。
[1] 劉建坤,朱家平,鄭榮.測量不確定度評定研究現狀及進展[J].現代科學儀器,2013,10(5):12-17.
[2] ISO 1993(E).Guide to the Expression of Uncertainty in Measurement[S].
[3] JJF1059.1-2012.測量不確定度評定與表示[S].
[4] 中國獸藥典委員會.中華人民共和國獸藥典一部[S].2010年版.
[5] JJF1059.1-2012.玻璃儀器檢定規程[S].
[6] 粟曉黎,李冠民,金少鴻.藥品檢驗一般檢測項目不確定度評定研究-1.B類評定[J].藥物分析雜志,2005,25(6):699-705.
[7] 中國藥品生物制品檢定所.中國藥品檢驗標準操作規范[M].北京:中國醫藥科技出版社,2010.
[8] 常艷.抗生素標準品的定值及其不確定度評定[D].北京:北京協和醫學院研究生院,2011.
(編輯:李文平)
Evaluation of Uncertainty of Determ ination of Kanam ycin M onosulfate for Injection by the M icrobiological M ethod
YU Li-na,XU Yuan,HAN Ning-ning,ZHAO Hui,HAO Li-hua
(China Institute of Veterinary Drug Control,Beijing 100081,China)
To evaluate the uncertainty of determination of kanamycin monosulfate for injection by the microbiological method in Chinese Veterinary Pharmacopoeia(edition 2010),a mathematied model was established to evaluate the factors affecting sample determination.Each componentof uncertainty was calculated by analyzing the various variable parameters among the procedures.The combined uncertainty was finally obtained by synthesizing the uncertainties of various component variables.The volume of sample added into Oxford Cup effects resultmost.As a result,the added volume should be controlled accurately in the test.
microbiologicalmethod;kanamycin monosulfate for injection;biological value;uncertainty evaluation
2014-11-24
A
1002-1280(2015)02-0040-04
S859.79
于麗娜,碩士,從事藥物分析及檢驗工作。E-mail:yulinachina@163.com

