疊氮基HNC(N3)2合成設計與穩定性研究
張國華,張影,李晶,劉芳
哈爾濱理工大學應用科學學院
疊氮基HNC(N3)2合成設計與穩定性研究
張國華,張影,李晶,劉芳
哈爾濱理工大學應用科學學院
利用密度泛函(DFT-B3LYP)系統研究HNC(N3)2體系的幾何結構和振動頻率,設計合成反應的路徑,通過對分解反應勢能曲面的研究得出其具有較高的動力學穩定性,該雙疊氮基化合物是極有可能在試驗中合成的物。
該項目是由黑龍江省教育廳科技項目(No.12541172)資助
1 、簡介
高能量的含氮分子因其具有較多的N-N單鍵和雙鍵,從而具有較高的能量儲備,因此,在實驗中合成由較大數量的氮原子組成的多氮分子成為實驗化學家關注的熱點之一。于是人們將目光投到其他能夠使多氮分子穩定的方法上。疊氮基化合物就是其中的一種。通過對含氟或含氯分子進行N3取代,就能夠形成疊氮基化合物。
2 、計算方法
本章利用密度泛函(DFT-B3LYP)對HNC(N3)2分子結構優化和振動頻率的計算。諧振頻率的計算用來確定穩定結構(全正頻)以及過渡結構(有一個負頻),并且提供零點振動能修正(0.9806修正)。對勢能面的分子內稟反應路徑(IRC)計算能夠確定合成與分解反應的反應路徑和反應產物。所有計算結果都是利用Gaussian 03軟件包得到的。
3 、結果與討論
(1)、HNC(N3)2的合成
HNC(N3)2的合成是通過用HN3中的N3基團取代HNCCl2中的Cl原子來實現的,我們對該合成路徑所涉及的物質進行結構優化,各物質的對稱性、能量以及相對能列于表1,幾何結構列于圖1。
HNCCl2是Cs對稱性分子,與HN3反應時N3基團與H原子分離,N3基團取代其中一個Cl原子,生成一個HNCClN3分子,同時產生一個氣態的HCl分子。HNCClN3分子中疊氮基N3基團的N-N鍵長為1.178和1.244?,介于雙鍵和三鍵之間,當期N-N鍵斷裂釋放氮氣過程中將會放出巨大能量。HNCClN3分子與HN3進一步反應,另一個Cl原子也將被取代,生成一個HNC(N3)2分子和一個氣態HCl分子。
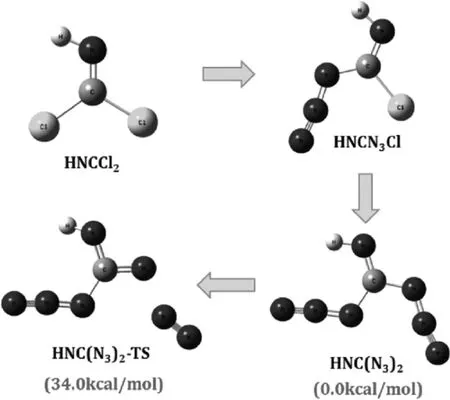
圖1 .HNC(N3)2分子路徑上所涉及物質的幾何結構及相對能
(2)、HNC(N3)2的穩定性分析
為了確定HNC(N3)2分子的動力學穩定性,我們對其勢能曲面進行系統計算,確定其分解路徑,找到其分解過渡態結構,如圖1。HNC(N3)2中的一個N3基團的一個N-N鍵長由1.243?增加到1.928?(如圖1中的HNC(N3)2-TS過渡結構),接下來將會釋放一個N2分子。該分解反應勢壘為34.0kcal∕mol,說明HNC(N3)2具有較高的動力學穩定性,在試驗中一旦合成,將不易分解。
HNCN3N分子的N3基團將進一步釋放氮氣,N-N鍵長由1.245?增加到2.065?釋放一個N2分子后的HNCN3N分子將變成HNCN2分子。HNCN3N分子的分解勢壘為34.0 kcal∕mol,說明HNCN3N的動力學穩定性也很高,不易放生分解反應。
結論
1、HNC(N3)2分子可以由HNCCl2分子和2個HN3分子的取代反應來合成。
2、HNC(N3)2分子可以通過增加N-N鍵長來釋放氮氣從而放出巨大能量,分解勢壘分別為31.8 kcal∕mol和34.0 kcal∕mol,說明該疊氮基分子具有較高的動力學穩定性,在實驗室中合成穩定性較高,不易分解,具有較高的應用價值。
[1]王廣厚.物理學的新進展[M].物理學進展,1994,14(2):121~172
[2]馮端,金國鈞.凝聚態物理學新論.上海科學技術出版社. 1992:286~292
[3]S.Herler,P.Mayer,H.N?th,A.Schulz,M.Suter,M.Vogt. S2N3+:An Aromatic SN Cation with an N3 Unit.Angew.Chem.Int. Ed.2001,40:3173~3175
[4]【美】J.A.波普爾,D.L.貝弗里奇,江元生譯《分子軌道近似方法理論》.科學出版社.1978

