體外膜肺氧合并發血流感染病原菌及耐藥性分析
李茜 孫仁華 洪軍 胡秀平 呼邦傳 公方曉
[摘要] 目的 了解重癥醫學科(ICU)中體外膜肺氧合(ECMO)治療過程中并發血流感染病原菌的分布、耐藥性特點以及可能的發病危險因素。 方法 選擇2006年9月~2015年6月接受ECMO治療并確診發生血流感染的患者,對血培養分離到的病原菌進行鑒定和藥敏學分析,并分析評價感染發生可能的危險因素。 結果 ECMO患者發生血流感染的血培養共分離出7株病原菌,其中革蘭陰性(G-)桿菌5株,占71.4%,革蘭陽性(G+)球菌2株,占28.6%;G-桿菌如肺炎克雷伯菌肺炎亞種、乙酸鈣鮑氏復合不動桿菌、銅綠假單胞菌及大腸埃希菌對各種常用抗菌藥物耐藥嚴重,2株G+球菌分別為表皮葡萄球菌和頭狀葡萄球菌,對苯唑西林均耐藥,但對萬古霉素均敏感。ECMO時間≥7 d、置管部位出血等有可能是ECMO并發血流感染的危險因素。 結論 G-桿菌是ECMO治療中并發血流感染的主要病原菌,且對多種抗菌藥物耐藥,G+球菌敏感性尚可,應根據病原學及藥敏結果合理用藥,ECMO治療期間應對發生血流感染的可能危險因素應實行重點監控并積極避免。
[關鍵詞] 體外膜氧合作用;血流感染;病原;抗生素耐受性;危險因素
[中圖分類號] R563.8 [文獻標識碼] A [文章編號] 1673-9701(2015)30-0018-04
Analysis of pathogens and antibiotics resistance of bloodstream infection in patients undergoing extracorporeal membrane oxygenation
LI Qian SUN Renhua HONG Jun HU Xiuping HU Bangchuan GONG Fangxiao
Department of ICU, Zhejiang Provincial People's Hospital, Hangzhou 310014, China
[Abstract] Objective To investigate pathogens,antibiotics resistance and the probable risk factors of bloodstream infection in patients undergoing extracorporeal membrane oxygenation(ECMO) in our intensive care unit(ICU). Methods Blood samples collected from patients undergoing ECMO from September 2006 to June 2015 in ICU received bacterial culture and antibiotics sensitive test. The risk factors related to bloodstream infection in ECMO were identified and evaluated. Results 7 strains of pathogens had been isolated by culture and 5 of which were Gram negative bacilli (71.4%). 2 strains are Gram positive cocci (28.6%). Gram negative bacilli include Klebsiella pneumoniae, Acinetobacter calcoaceticus-baumannii, Escherichia coli and Pseudomonas aeruginosa. Most of the Gram negative bacilli were highly resistant to many kind of antibiotics. 2 strains Gram positive cocci were Staphylococcus epidermidis and Staphy- lococcus capitis. They were both Meticillin-resistant and all sensitive to Vancomycin. The duration of ECMO≥7 days, bleeding at the catheter site et al were probably the risk factors for bloodstream infection during ECMO. Conclusion Gram negative bacilli are the main pathogen of bloodstream infection during ECMO, and they are highly resistant to the most antibiotics agents. There are still some antibiotics sensitive to Gram positive cocci separated. The choice of antibiotics should be according to the pathogens antibiotics sensitivity test. The probable risk factors of bloodstream infection should be key-monitored and actively avoided.
[Key words] Extracorporeal membrane oxygenation; Blood stream infection; Pathogens; Antibiotics resistance; Risk factors
體外膜肺氧合療法(extrcorporeal memberane orygenation,ECMO)是將血液從體內引到體外,經膜肺氧合再用泵將血液注入體內,針對一些呼吸或循環衰竭及休克的患者進行有效支持,使心肺得以充分的休息。ECMO在急性呼吸窘迫綜合征(ARDS)、嚴重心源性休克、心肺復蘇、冠狀動脈嚴重病變行經皮冠狀動脈介入治療患者的輔助支持,以及心臟移植術前、術后過渡等疾病的救治中的應用日益增多,已成為醫療機構危重病治療水平的體現[1,2]。然而,由于ECMO體內置管管徑較粗、置管時損傷較大,體外管路長、連接膜肺及泵的接口較多等原因,導致ECMO治療中并發血流感染的機會增多,并直接影響ECMO治療患者的預后。本文對本中心ECMO治療患者發生血流感染的病原菌及可能的危險因素進行總結,現報道如下。
1 資料與方法
1.1 一般資料
回顧分析我院重癥醫學科2006年9月~2015年6月接受ECMO治療的患者共34例,其中男21例,女13例,年齡15~88歲,平均45歲。ECMO應用指征包括重癥心肌炎合并心源性休克12例,冠心病嚴重主干合并心功能不全PCI術中支持6例,重度急性呼吸窘迫綜合征(acute respiratory distress syndrome,ARDS)6例,重癥肺炎4例,心肌梗死合并心源性休克3例,骨折后脂肪栓塞綜合征2例,急性肺梗死1例。建立ECMO地點,在重癥醫學科內21例,在心導管室6例,急診室4例,外院轉來3例。
1.2 ECMO建立方法和參數
15例患者使用日本泰爾茂公司的離心式EQL002-PCPS系統管道系統,19例患者使用瑞典MAQUET公司的ROTAFLOW離心泵及管道系統。V-A模式ECMO有23例,置管部位為股動脈和股靜脈,V-V模式有11例,置管部位為頸內靜脈和股靜脈;置管方式切開+穿刺置管10例,經超聲引導下穿刺置管24例;ECMO運轉時間1~45 d。
1.3 血流感染診斷
ECMO并發血流感染屬于院內感染范疇。ECMO支持過程中院內感染定義采用美國密西根大學醫學院定義[3],即發生于ECMO開始24 h后與ECMO停機48 h內的院內感染。血流感染的定義參照衛生部2001年發布的《醫院感染診斷標準(試行)》[4]。
1.4 血流感染的監測和病原菌分析
ECMO運轉過程中常規監測患者體溫、白細胞計數和分類、C反應蛋白、降鈣素原等。隔日進行血細菌真菌培養及藥敏試驗。如患者出現疑似血流感染征象,即時加送血培養,更換或拔除介入性插管,如中心靜脈導管等常規送檢。血標本置于BacT/Alert120全自動血培養儀中培養,采用ViteK-32全自動細菌分析鑒定系統進行菌種鑒定及藥敏分析,操作及結果判讀嚴格按照臨床實驗室標準化協會(Clinical and Laboratory Standards Institute,CLSI)的微生物抗生素敏感標準,以2014年版[5]為最新標準。
2 結果
2.1 ECMO并發血流感染的發生率
34例納入研究患者有7例發生血流感染,發生率為20.59%。
2.2 病原菌分析
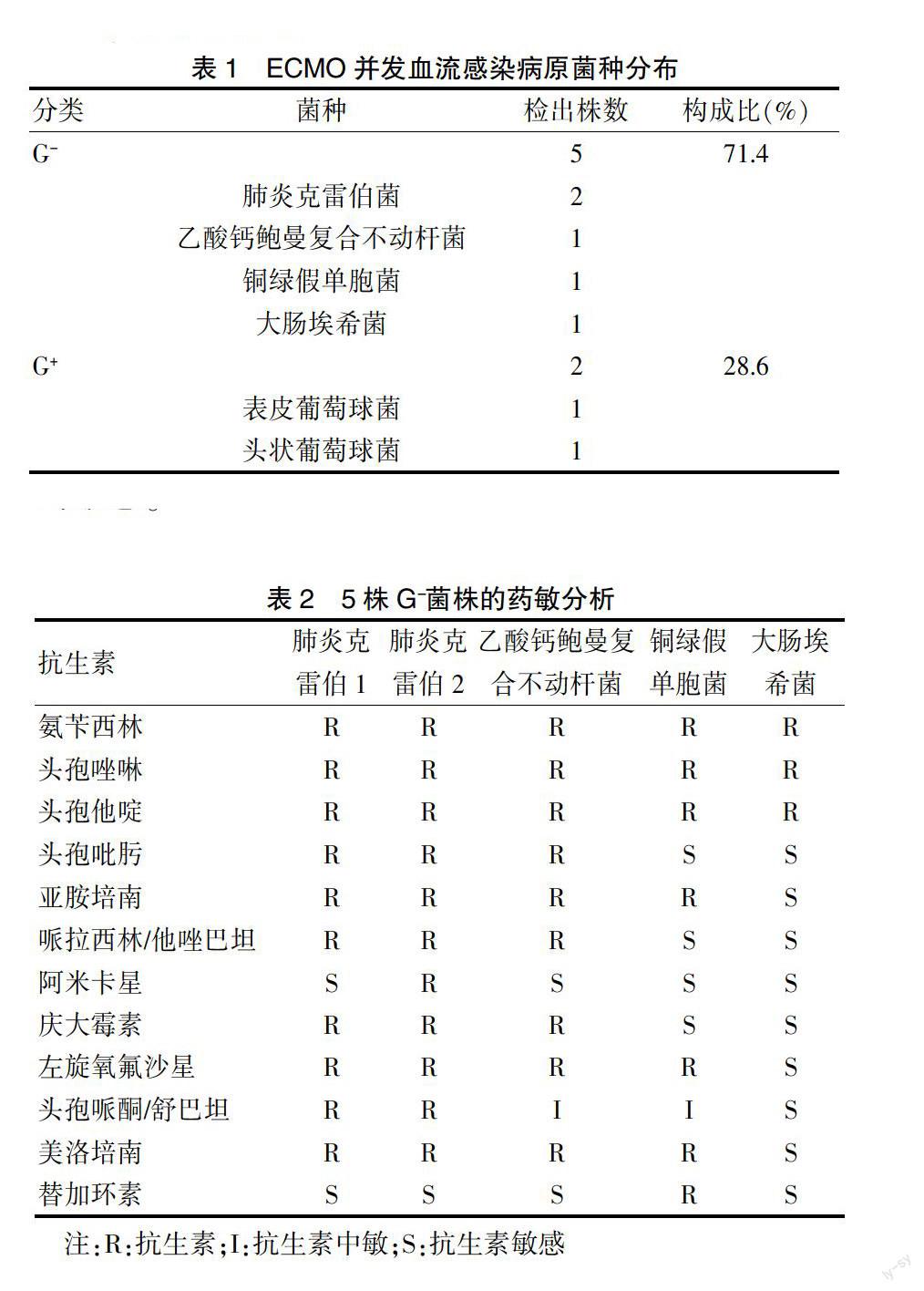
所有7例血流感染患者共分離到菌株7株(同一患者多次培養結果為同一種病原菌算作一株),其中G- 5株,占71.4%,G+ 2株,占28.6%,未分離出真菌菌株,病原學分類見表1。
表1 ECMO并發血流感染病原菌種分布
2.3 藥敏試驗結果
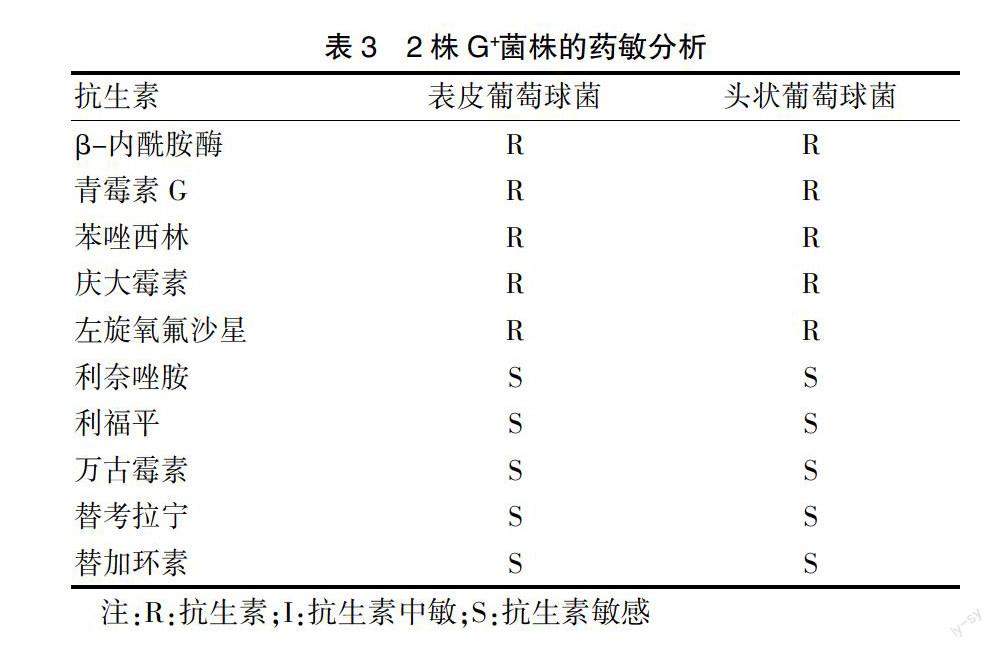
7株致病菌的藥敏結果見表2、表3。5株G-菌株對頭孢菌素(包括第二、三、四代頭孢菌素)均耐藥,2株肺炎克雷伯菌肺炎亞種、乙酸鈣鮑曼復合不動桿菌對β-內酰胺酶抑制劑的復合制劑也耐藥,對碳青霉烯酶類也呈現耐藥。除銅綠假單胞菌外,其余6株G-菌株對替加環素均敏感。2株G+菌株對苯唑西林均耐藥,而對萬古霉素、替考拉寧、利奈唑胺及替加環素均敏感。
表2 5株G-菌株的藥敏分析
注:R:抗生素;I:抗生素中敏;S:抗生素敏感
2.4 可能危險因素分析
34例接受ECMO治療患者中,按可能的危險因素分組,依據血流感染診斷標準對血流感染發生率進行分析。結果顯示,ECMO治療時間≥7 d血流感染發生率為37.5%(6/16),ECMO治療時間<7 d組的發生率5.6%(1/18);V-A模式血流感染發生率為21.7%(5/23),V-V模式的發生率18.2%(2/11);置管方式為切開加穿刺的血流感染發生率為30.0%(3/10),置管方式為穿刺的發生率16.7%(4/24);置管部位出血時血流感染發生率44.4%(4/9),無出血時發生率12.0%(3/25);治療過程中更換管路的血流感染發生率50.0%(1/2),未更換管路的感染發生率18.8%(6/32)。其中ECMO時間≥7 d、置管部位出血兩種情況下血流感染發生率的差異較大,很有可能是ECMO治療中血流感染發生的危險因素,但由于病例數量少,無法行統計學分析。
3 討論
在ICU中,血流感染是重要的院內感染類型。EPIC II研究對全球ICU感染的橫斷面調查顯示ICU患者血流感染發生率為7.76%[6]。ECMO相關血行感染是ECMO治療期間最常見的醫院感染類型,發生率為新生兒3.5%~30.0%[7],成人為16.4%[8]。本組資料結果顯示ICU內接受ECOM治療的患者血流感染發生率20.59%,高于前述ICU所有患者的發病率,而與其他資料中ECMO患者的數據相近,分析其原因包括:接受ECOM治療的患者病情重、抵抗力差,置管手術創傷過大及置管時間過長,同時ECOM進行過程中的操作以及并發癥如出血等也增加了感染的機會。
本組資料顯示,ICU中ECMO治療并發血流感染的病原菌以G-桿菌為主,占71.4%,G+占28.6%,病原菌分布與我科以往血流感染病原菌的構成比有較大差異[9],這可能與本組病例數較少,病情較為危重且住院時間相對較長而更易感染G-桿菌可能有關。分離到的G-桿菌包括2例肺炎克雷伯菌及乙酸鈣鮑曼復合不動桿菌、銅綠假單胞菌、大腸埃希氏菌各1例,與我國院內感染G-桿菌菌種分布的前四位相符[10]。其中,2株肺炎克雷伯菌對碳青霉烯類均耐藥,顯示出嚴峻的耐藥形勢。碳青霉烯類抗生素長期以來被認為是治療包括產超廣譜β內酰胺酶(ESBLs)的肺炎克雷伯菌感染最可靠的藥物,但近年來耐碳青霉烯類的肺炎克雷伯菌日益增多,導致感染治療成功率下降。肺炎克雷伯菌對碳青霉烯類抗生素耐藥的主要機制為產肺炎克雷伯碳青霉烯水解酶(Klebsiella pnermoniae carbapenemase, KPC)。KPC存在于質粒中,易于傳播,且同時攜帶有多種耐藥基因,造成流行及極度耐藥或泛耐藥[11]。本資料中2株肺炎克雷伯菌對替加環素均顯示良好的敏感性,與本地區的藥敏研究結果相符[12],并且此2例患者經使用替加環素聯合其他抗生素抗感染治療后,病原菌均清除,血流感染均得到控制。
2株G+菌血流感染的菌株分別為表皮葡萄球菌和頭狀葡萄球菌,均屬于凝固酶陰性的葡萄球菌屬,與國外報道的凝固酶陰性葡萄菌屬是血流感染中主要的G+菌的報道一致[13]。2株葡萄球菌對苯唑西林均耐藥,但對萬古霉素、利奈唑胺及替加環素等均敏感,說明葡萄球菌的甲氧西林耐藥仍然占優勢,針對醫院G+菌血流感染,仍可以選擇萬古霉素、利奈唑胺及替加環素等作為治療藥物。
ECMO治療中可能有多種并發癥,而血流感染是嚴重的并發癥,可能導致病死率的升高[14],需要加強監測并予以控制。ECMO治療中并發血流感染與多種危險因素相關,研究發現[15,16],導致ECMO患者繼發感染的最大風險因素是長時間ECMO血管插管,患者ECMO輔助時間超過7~10 d,發生ECMO相關感染,特別是血行感染的可能大大增加,患者死亡率相應明顯增高。本組資料也表明7例血流感染患者中有6例ECMO時間≥7 d,是發生血流感染可能的危險因素,ECMO治療時間長意味著患者病情更加危重。血管通路操作機會大,因此有更高的血流感染發生率。ECMO治療期間應每日評估撤機條件,爭取盡早撤機。同時,我們的資料還顯示,ECMO置管部位出血也是發生血流感染的可能危險因素,由于局部出血使皮膚消毒難度增加,置管周圍出血成為病原菌生長的培養基,有利于外界病原菌沿血管通路遷徙進入血管。ECMO實施時應讓有經驗的醫生置管,置管前盡量避免使用抗凝藥物,妥善縫合切口并固定管路,避免出血。對于ECMO治療期間有危險因素的患者,應盡量減少對治療ECMO管路的操作,尤其是接頭部位,嚴格消毒隔離制度,加強醫護人員的洗手制度,防止交叉感染等。
綜上所述,ECMO治療中血流感染是常見且危重的感染并發癥,病原菌以多重耐藥的G-桿菌為主,治療難度大,預后差。多種因素影響ECMO血流感染的發生,本組資料顯示ECMO時間≥7 d、置管部位出血可能與感染發生相關。由于ECMO治療技術要求高,費用昂貴,單中心資料病例數偏少,所得數據有限,亟需進一步積累病例或開展多中心合作以進一步了解ECMO并發感染的特點,為預防治療尋找最佳對策。
[參考文獻]
[1] Ventetuolo CE,Muratore CS. Extracorporeal life support in critically ill adults[J]. Am J Respir Crit Care Med,2014, 190(5):497-508.
[2] Paden ML,Rycus PT,Thiagarajan RR. Update and outcomes in extracorporea1 life support[J]. Semin Perinato,2014,38(2):65-70.
[3] Burket JS,Bartlett RH,Vander Hyde K,et al. Nosocomial infections in adult patients undergoing extracorporeal membrane oxygenation[J]. Clin Infect Dis,1999,28(4):828-833.
[4] 中華人民共和國衛生部.醫院感染診斷標準(試行)[J].中華醫學雜志,2001,81:314-320.
[5] Clinical and Laboratory Standards Institute. Performance standards for antimicrobial susceptibility testing:Twenty-fourth informational supplement[S]. CLSI document M-100 S24. Wayne,PA:CLSI,2014.
[6] Vincent JL,Rello J,Marshall J,et al. EPIC II Group of Investigators. International study of the prevalence and outcomes of infection in intensive care units[J]. JAMA,2009, 302(21):2323-2329.
[7] Coffin SE,Bell LM,Manning M,et al. Nosocomial infections in neonates receiving extracorporeal membrane oxygenation[J]. Infect Control Hosp Epidemiol,1997,18(2):93-96.
[8] 高國棟,黑飛龍,吉冰洋,等. 128例成人體外膜肺氧合支持治療患者相關并發癥回顧分析[J]. 中國分子心臟病學雜志,2015,15(1):1197-1201.
[9] 呼邦傳,孫仁華,徐云祥,等. ICU血流感染的病原菌分布及耐藥性分析[J]. 中華醫院感染學雜志,2012,22(4):860-863.
[10] 胡付品,朱德妹,汪復,等. 2013年中國CHINET細菌耐藥性監測[J]. 中國感染與化療雜志,2014,14(5):369-378.
[11] 胡慶豐,呂火祥,張玉霞,等. 耐碳青霉烯類肺炎克雷伯菌同源性分析[J]. 中華醫院感染學雜志,2009,19(12):1482-1485.
[12] 李茜,胡慶豐,孫仁華. 重癥監護病房肺炎克雷伯菌的分布及耐藥性變遷[J]. 健康研究,2013,3(2):116-119.
[13] Cavalcanti SM,Franca ER,Cabral C,et al. Prevalence of staphylococcus aureus introduced into intensive care units of a university hospital[J]. Braz J Infect Dis,2005,9(1):56-63.
[14] Cheng R. Hachamovitch R. Kittleson M. Complications of extracorporeal membrane oxygenation for treatment of cardiogenic shock and cardiac arrest:A meta-analysis of 1,866 adult patients[J]. Ann Thorac Surg, 2014,97(2): 610-616.
[15] ONeil JM,Schutze GE,Heulitt MJ,et al. Nosocomial infections during extracorporeal membrane oxygenation[J].Intensive Care Med,2001,27(8):1247-1253.
[16] Steiner CK,Stewart DL,Bond SJ,et al. Predictors of acquiring a nosocomial bloodstream infection on exacorporeal membrane oxygenation[J]. J Pediatr Surg,2001,36(3):487-492.
(收稿日期:2015-07-13)

