微波輔助PEG提取金銀花葉中綠原酸的工藝優化
黃 榮,向 福,2 *,馬文靜,吳 偉,項 俊,2
(1.黃岡師范學院生命科學學院,湖北 黃州 438000;2.大別山特色資源開發湖北省協同創新中心,湖北 黃州 438000;3.湖北理工學院醫學院,湖北 黃石 435003)
金銀花(Lonicerae japonicaThunb)又名忍冬,是我國一種傳統的中草藥植物。綠原酸是金銀花中主要的活性成分,具有抗菌、抗腫瘤、抗病毒、降血脂、降血壓、保肝利膽以及清除自由基等功能[1],被譽為“植物黃金”,廣泛用于食品、保健、醫藥、衛生和化工等領域。金銀花葉中含有豐富的綠原酸,山東、河南等地金銀花葉中的綠原酸含量均超過了同一時期的金銀花[2],而黃岡地標產品—羅田金銀花,其葉中綠原酸含量達7%左右[3]。另外,金銀花葉的產量是同期花產量的10倍左右[4]。因此,金銀花葉中的綠原酸比金銀花中的更豐富且采集更容易、成本更低廉,科學利用金銀花資源,對促進大別山地區金銀花產業的發展具有重要的應用價值和現實意義。
以金銀花為原料提取綠原酸的工藝主要有醇提法、水提法、半仿生法等[5-8]。但這些提取方法存在耗時長、成本高、提取率低、有機溶劑消耗量大、雜質多等問題。研究一種成本低、產率高、簡單快速、環境友好的綠原酸提取工藝對大別山金銀花產業的發展意義重大。
微波法提取具有選擇性好、穿透力強、溶劑用量少、提取時間短、提取效率高等優點[9-12],且能有效克服中藥材細粉煎煮提取過程中的堵塞、糊化等問題,適合工業化生產[13]。聚乙二醇(polyethylene glycol,PEG)具有良好的生物相容性和低免疫原性,不易燃、耐酸堿、耐高溫、成本低、溶解性好、可生物降解、環境友好、低分子質量的PEG(如PEG-200)不揮發等諸多優良性質,且美國食品藥物管理局(food and drug administration,FDA)已證實其安全無毒[14]。因此,將PEG用于藥用植物中活性成分的提取具有廣闊的應用前景。
本研究以金銀花葉為原料,采用微波輔助PEG-200提取金銀花葉中綠原酸。以綠原酸的提取率為響應值,在單因素試驗基礎上對提取溫度、PEG-200體積分數、提取時間等關鍵影響因素,根據Box-Behnken原理設計響應面優化試驗,探討微波輔助PEG-200提取金銀花葉中綠原酸的優化工藝,對科學利用金銀花資源、促進大別山地區金銀花產業的發展具有重要的應用價值和現實意義。
1 材料與方法
1.1 材料與試劑
金銀花葉:采于湖北楚天舒藥業有限公司金銀花基地,陰干,粉碎備用;綠原酸標準品(純度≥98%),批號20120117:上海源葉生物科技有限公司;PEG-200(分析純):上海山浦化工有限公司。
1.2 儀器與設備
Varian Cary 100 Scan型紫外可見分光光度計:美國Varian公司;MM721NH1-PW型微波爐:廣東美的微波電器制造有限公司;Ax-205 METTLER TOLEDO型電子天平:瑞士梅特勒-托利多集團;DZKW-D-2型電熱恒溫水浴鍋:北京西城區醫療器械廠。
1.3 試驗方法
1.3.1 綠原酸的提取分離
微波輔助PEG-200提取金銀花葉中綠原酸提取液,通過大孔樹脂吸附,乙醇溶液洗脫,濃縮干燥,可分離制得綠原酸提取物。
1.3.2 綠原酸標準曲線及提取率測定
精確稱取10.8 mg綠原酸標準品置于100 mL容量瓶,用體積分數30%的PEG-200定容,搖勻即可得質量濃度為108 μg/mL的綠原酸參照液。取2 mL參照液于10 mL容量瓶,用體積分數30%的PEG-200定容至刻度,搖勻,以體積分數30%的PEG-200為空白,在波長200~800 nm范圍掃描,確定檢測波長為327 nm。
綠原酸標準曲線制備:吸取綠原酸參照液1.0 mL、2.0 mL、3.0 mL、4.0 mL、5.0 mL、6.0 mL分別置于6個10 mL的容量瓶中,用體積分數30%的PEG-200定容,搖勻,以體積分數30%的PEG-200為空白,在波長327 nm處測定吸光度值,繪制標準曲線。
以綠原酸質量濃度(C)為橫坐標,吸光度值A為縱坐標,得標準曲線回歸方程為A=0.056 4C+0.004 3,相關系數R2=0.999 8,綠原酸在10.8~54.0 μg/mL質量濃度范圍內與吸光度值線性關系良好。
綠原酸提取率計算公式:
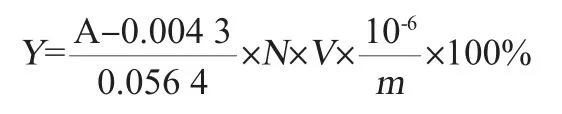
式中:Y為綠原酸提取率,%;V為綠原酸提取液體積,mL;m為金銀花葉的質量,g;A為吸光度值;N為稀釋倍數。
1.3.3 單因素試驗
稱取5份陰干、粉碎后的金銀花葉粉末5 g置于圓底燒瓶,按照一定的料液比加入不同體積分數的PEG-200,在不同的微波功率條件下處理不同時間,然后在一定溫度條件下回流一定時間提取金銀花葉中綠原酸。通過單因素試驗分別考察微波功率、微波時間、PEG-200體積分數、料液比、提取溫度和提取時間等因素對金銀花葉中綠原酸提取率的影響。
1.3.4 響應面優化試驗
根據單因素試驗結果,選取提取溫度(X1)、PEG-200體積分數(X2)、提取時間(X3)3個對金銀花葉中綠原酸提取率影響較為顯著的因素,以綠原酸提取率(Y)為響應值,利用Box-Behnken中心組合試驗設計原理設計3因素3水平的響應面優化試驗,響應面分析因素和水平如表1所示。
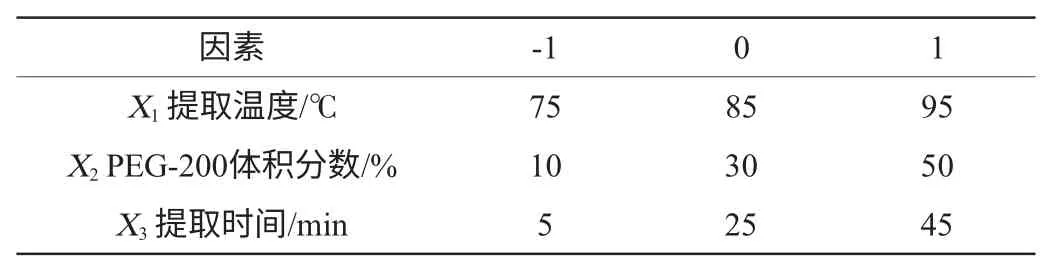
表1 綠原酸提取響應面分析因素及水平Table 1 Variables and levels of response surface design for chlorogenic acid extraction
2 結果與分析
2.1 單因素試驗結果
2.1.1 微波功率對綠原酸提取率的影響
稱取5份金銀花葉粉末5 g置于圓底燒瓶,按料液比1∶20(g∶mL)加入體積分數30%的PEG-200,在70 W、210 W、350 W、490 W、630W功率條件下,微波處理60 s,然后80 ℃回流15 min提取金銀花葉中綠原酸,考察微波功率對綠原酸提取率的影響。結果如圖1所示。

圖1 微波功率對綠原酸提取率的影響Fig.1 Effect of microwave power on the extraction rate of chlorogenic acid
由圖1可知,微波功率為70~350 W時,隨著微波功率的增加,綠原酸提取率增大;在微波功率達到350 W時,綠原酸提取率達到峰值,為4.93%;繼續增大微波功率(>350 W),綠原酸提取率則急劇降低。這是因為分子運動速度隨著微波功率增加而加快,綠原酸的提取率增加;但微波功率太高,所產生的高溫不僅導致綠原酸分解,還會導致蛋白質凝固,綠原酸難以溶出細胞壁[15]。因此,選擇微波功率350 W為宜。
2.1.2 微波時間對綠原酸提取率的影響
稱取5份金銀花葉粉末5 g置于圓底燒瓶,按料液比1∶20(g∶mL)加入體積分數30%的PEG-200,在350 W功率下,微波處理50 s、60 s、70 s、80 s、90 s,然后80 ℃回流15 min提取金銀花葉中綠原酸,考察微波時間對綠原酸提取率的影響。結果如圖2所示。

圖2 微波時間對綠原酸提取率的影響Fig.2 Effect of microwave time on the extraction rate of chlorogenic acid
由圖2可知,在試驗條件內,綠原酸提取率呈波浪形變化,當微波時間為70 s時,金銀花葉中綠原酸的提取率最高,為5.43%。微波輻射一定時間內對金銀花葉細胞破碎作用較大,使細胞內的有效成分快速溶出[15-16],綠原酸提取率達到最高,但超過70 s后,微波產生的強熱效應導致綠原酸結構破壞,提取率降低。因此,選擇微波時間70 s為宜。
2.1.3 PEG-200體積分數對綠原酸提取率的影響
稱取5份金銀花葉粉末5 g置于圓底燒瓶,按料液比1∶20(g∶mL)分別加入體積分數10%、20%、30%、40%、50%的PEG-200,在350 W功率下,微波處理70 s,80 ℃回流15 min提取金銀花葉中綠原酸,考察PEG-200體積分數對綠原酸提取率的影響。結果如圖3所示。
由圖3可知,PEG-200體積分數為10%~30%時,隨著PEG-200體積分數的增加,綠原酸提取率逐漸增加;在PEG-200體積分數為30%時,綠原酸提取率達到峰值,為5.37%,提取效果最好;PEG-200體積分數>30%以后,綠原酸提取率有所下降。原因可能是PEG能增加了綠原酸的溶解度,同時也改變了溶液的耗散因素和微波能量傳遞[14],從而加快能量傳遞速度和提取效率,導致綠原酸提取率隨著PEG-200體積分數的增加而增加,但PEG-200體積分數的增大會增加溶液的黏度,從而影響傳質,綠原酸提取率降低。因此,選擇PEG-200體積分數30%為宜。

圖3 PEG-200體積分數對綠原酸提取率的影響Fig.3 Effect of PEG-200 concentration on the extraction rate of chlorogenic acid
2.1.4 料液比對綠原酸提取率的影響
稱取5份金銀花葉粉末5 g置于圓底燒瓶,分別按料液比1∶5、1∶10、1∶15、1∶20、1∶25(g∶mL)加入體積分數30%的PEG-200,在350 W功率下,微波70 s,80 ℃回流15 min提取金銀花葉中綠原酸,考察料液比對綠原酸提取率的影響。結果如圖4所示。

圖4 料液比對綠原酸提取率的影響Fig.4 Effect of the solid liquid ratio on the extraction rate of chlorogenic acid
由圖4可知,隨料液比的增加,綠原酸提取率先不斷上升,后趨于平緩,當料液比為1∶20(g∶mL)時綠原酸得提取達最高,為5.24%;料液比>1∶20(g∶mL)后綠原酸提取率趨于穩定。考慮綠原酸提取后的去除提取溶劑的經濟成本,因此,選擇料液比1∶20(g∶mL)為宜。
2.1.5 提取溫度對綠原酸提取的影響
稱取5份金銀花葉粉末5 g置于圓底燒瓶,按液料體積質量比1∶20(g∶mL)加入體積分數30%的PEG-200,在350 W功率下,微波70 s,分別在75 ℃、80 ℃、85 ℃、90 ℃、95 ℃條件下回流15 min提取金銀花葉中綠原酸,考察提取溫度對綠原酸提取率的影響。結果如圖5所示。
由圖5可知,在70~85 ℃時,隨著提取溫度的增長,綠原酸的提取率不斷上升,在85 ℃時提取率達到最大值,為5.33%。提取溫度>85 ℃,綠原酸提取率逐漸下降。隨著提取溫度的升高,綠原酸提取率增加,但提取溫度太高會導致綠原酸分解。因此,選擇85 ℃回流的提取溫度為宜。

圖5 提取溫度對綠原酸提取率的影響Fig.5 Effect of extraction temperature on the extraction rate of chlorogenic acid
2.1.6 提取時間對綠原酸提取率的影響
稱取5份金銀花葉粉末5 g置于圓底燒瓶,按液料體積質量比1∶20(g∶mL)加入體積分數30%的PEG-200,在350 W功率下,微波70 s,在85 ℃分別回流5 min、15 min、25 min、35 min、45 min,提取金銀花葉中綠原酸,考察提取時間對綠原酸提取率的影響,結果如圖6所示。

圖6 提取時間對綠原酸提取率的影響Fig.6 Effect of extraction time on the extraction rate of chlorogenic acid
由圖6可知,在5~25 min時,隨著提取時間的延長,綠原酸的提取率不斷上升,在25 min時綠原酸提取率達到最大值,為5.88%。提取時間>25 min之后綠原酸提取率開始下降。這是由于在85 ℃溫度下,提取時間過長會導致綠原酸的分解所致。因此,提取時間以25 min為宜。
2.2 響應面試驗結果
在單因素試驗的基礎上,固定微波功率、時間及料液比分別為350 W、70 s和1∶20(g∶mL),采用Box-Behnken中心組合試驗設計,以提取溫度(X1)、PEG-200體積分數(X2)和提取時間(X3)為自變量,以綠原酸提取率(Y)為響應值,對金銀花葉中綠原酸提取工藝進行優化,響應面試驗設計及結果見表2,回歸模型方差分析見表3。

表2 響應面試驗設計及結果Table 2 Design and results of response surface methodology

表3 響應面回歸模型方差分析Table 3 ANOVA for response surface quadratic model
表2試驗數據利用Design Expert 8.0.5b軟件進行多元回歸擬合,得到綠原酸提取率(Y)對提取溫度(X1)、PEG-200體積分數(X2)和提取時間(X3)的二次多項回歸模型方程如下:

由表3方差分析可知,各因子F值反映了對響應值的重要性,F值越大,則P值越小,該因素對響應值作用越大。F(X2)=848.28>F(X3)=9.17>F(X1)=0.017,表明各因子對綠原酸提取率影響程度大小為:PEG-200體積分數>提取時間>提取溫度。就顯著性而言,X2、X22對響應值Y有極顯著影響(P<0.000 1),X3、X1X2、和X32等因素對響應值Y有顯著影響(P<0.05)。因此,盡管提取溫度、提取時間、PEG-200體積分數等3個因素的交互作用對綠原酸的綠的影響較小,但各因素與響應值Y之間不存在簡單的線性關系,綠原酸提取率同時也受到二次項的影響。模型分析結果表明,模型的P<0.000 1,表明模型極其顯著;失擬項P值為0.623 2>0.05,即模型失擬項不顯著,表明模型對試驗數據擬合度較好,試驗誤差小;變異系數較小,為0.57%,表明操作可信;模型信噪比值很高,為32.498,遠>4,表明模型可信度高,有意義,可用于預測,且預測擬合度0.961 8和校正擬合度0.988 7比較一致,說明該模型較為合適。相關系數R2=0.996 0表明回歸方程中99.60%的因變量變化可以由其自變量的變化進行解釋,也就是說在該工藝中,未計入回歸方程的變量對金銀花葉中綠原酸的提取效果影響較小。因此,可用該模型代替真實試驗點對金銀花葉中綠原酸提取過程進行分析和預測。
由多元擬合模型產生的響應面及其等高線,結果見圖7。表示用于響應面分析的提取溫度、提取時間、PEG-200體積分數等3個因素中,某個因子為零水平時,另外兩個因子對綠原酸提取率的影響,直觀地反映各因子及其相互間的交互作用。由圖7可知,提取時間和PEG-200體積分數間不存在交互作用,表現為等高線中心區域呈明顯圓形;提取時間和提取溫度間的交互作用明顯,表現為等高線中心區域呈明顯的橢圓形;提取溫度和PEG-200體積分數間的交互作用不明顯,表現為等高線中心區域不構成橢圓。此外,響應面均為開口向下的凸面,提取溫度、提取時間、PEG-200體積分數等3個因素與綠原酸提取率基本呈拋物線關系,說明在試驗區域內存在最佳值。多元回歸模型預測的最佳提取工藝條件為溫度81.53 ℃,PEG-200體積分數41.50%,提取時間23.58 min,該條件下綠原酸提取率預測值為5.86%。

圖7 提取溫度、PEG-200體積分數和提取時間交互作用對綠原酸提取率的響應面及等高線Fig.7 Response surfaces plots and contour line of effects of interactions between extraction temperature,PEG-200 concentration and extraction time on extraction rate of chlorogenic acid
2.3 響應面驗證試驗
驗證時考慮實際操作問題,將最佳條件修正為:微波功率350 W,微波時間70 s,料液比1∶20(g∶mL),提取溫度82 ℃,PEG-200體積分數40%,提取時間24 min。在修正后的最佳條件下,利用微波輔助PEG從金銀花葉中提取綠原酸,進行了5次平行驗證試驗,綠原酸實測平均提取率為5.87%,相對誤差為0.17%,與理論預測值5.86%吻合度較高,說明響應面優化回歸模型對實際工藝操作具有一定的指導意義。
3 結論
本研究采用單因素試驗和響應面試驗對金銀花葉中綠原酸提取條件進行了優化,建立了微波輔助PEG提取金銀花葉中綠原酸的最佳工藝為微波功率350 W,微波時間70 s,料液比1∶20(g∶mL),提取溫度82 ℃,PEG-200體積分數40%,提取時間24 min。在最佳條件下綠原酸提取率為5.87%。該工藝簡單可行、快速有效、綠色環保,適合于提取金銀花葉中綠原酸工業化生產。
[1]王 輝,田呈瑞,馬守磊,等.綠原酸的研究進展[J].食品工業科技,2009,30(5):341-345.
[2]林慧彬,彭廣芳,鐘方曉,等.山東金銀花葉的質量研究[J].時珍國醫國藥,1997,8(2):125.
[3]向 福,郭文韜,袁 婷,等.羅田縣兩種金銀花中綠原酸含量的比較[J].黃岡師范學院學報,2013,33(3):36-37.
[4]熊建華,湯凱潔,羅秋水,等.大孔吸附樹脂純化金銀花葉總多酚的工藝優化[J].食品與機械,2011,27(3):52-55.
[5]趙鐘興,韋藤幼,郝瑞然,等.從金銀花中提取綠原酸生產工藝的改進[J].時珍國醫國藥,2004,15(12):829-830.
[6]李玉山.綠原酸在天然植物中的分布和提取純化工藝研究進展[J].解放軍藥學學報,2012,28(4):355-359.
[7]肖懷秋,李玉珍,蘭立新,等.半仿生法萃取金銀花中綠原酸的研究[J].中國釀造,2009,28(3):129-131.
[8]向 福,劉 亮,秦 婷,等.羅田金銀花葉中綠原酸的提取工藝改進[J].食品與機械,2013,29(6):150-152.
[9]曾 里,夏之寧.超聲波和微波對中藥提取的促進和影響[J].化學研究與應用,2002,14(3):245-249.
[10]翟碩莉.超聲波法和微波法提取馬齒莧中總黃酮的比較研究[J].中國釀造,2012,31(8):120-122.
[11]李燕婷,周文富.金銀花中綠原酸的微波輔助提取工藝研究[J].化學與生物工程,2011,28(10):65-69.
[12]李 克,吳龍琴,湯 溟,等.正交實驗優化微波輔助提取忍冬藤中綠原酸和咖啡酸工藝研究[J].中成藥,2014,36(4):864-867.
[13]歐陽麗娜,李蘭林,吳 雪,等.正交設計優選竹節參總皂苷微波提取工藝的研究[J].中草藥,2010,41(10):1639-1642.
[14]ZHOU T,XIAO X,LI G,et al.Study of polyethylene glycol as a green solvent in the microwave-assisted extraction of flavone and coumarin compounds from medicinal plants[J].J Chromatogr A,2011,1218(23):3608-3615.
[15]王 端,周鴻翔,田婭玲,等.微波輔助提取葛根黃酮的工藝研究[J].中國釀造,2014,33(3):81-86.
[16]王青豪,方 芳,張熊祿.微波輔助提取絞股藍黃酮工藝研究[J].食品科學,2010,31(22):149-152.

