右美托咪定輔助全麻對患者心腦缺血再灌注損傷的保護作用Δ
黃厚剛,羅紅霞(重慶醫科大學附屬永川醫院麻醉科,重慶 402160)
術中的不良刺激如組織損傷和病原體侵入術中創傷,會引發外周炎癥反應,從而導致機體應激。這些應激反應會導致組織代謝急劇改變,進而引起組織器官損傷[1]。麻醉管理是調節術中及術后應激反應、減少手術對組織器官損傷作用的關鍵[2]。右美托咪定是一種α2腎上腺素能受體激動藥,主要作用于腦和脊髓的α2腎上腺素能受體,曾被用作臨床降壓藥。近年來研究顯示,它在輔助麻醉過程中能降低麻醉劑用量,改善術中血流動力學波動,具有明顯的抗交感、鎮痛作用[3-4]。
心肌肌鈣蛋白Ⅰ(cTn Ⅰ)是傳統心血管損傷的重要指標之一,對心肌有高度特異性,能敏感地反映應激導致的心肌缺血再灌注損傷[5]。兒茶酚胺是機體應激反應的重要指標。在手術過程中,全身應激狀態會導致兒茶酚胺水平升高,過多的兒茶酚胺會加重腦組織缺血缺氧程度,從而加重腦損傷[6-7]。研究表明,在腦缺血再灌注損傷模型中,血漿中兒茶酚胺濃度與神經細胞功能具有明確相關性[6]。鑒于此,本研究通過比較應用右美托咪定輔助全麻患者與生理鹽水對照患者的cTn Ⅰ和兒茶酚胺水平,評價常規應用右美托咪定輔助全麻是否對心、腦缺血再灌注損傷具有保護作用。
1 資料與方法
1.1 研究對象
選擇美國麻醉師協會(ASA)分級Ⅰ~Ⅱ級、擬行氣管插管全麻下行擇期手術的18~60歲患者共50例,按隨機數字表法分為右美托咪定組(D組)和對照組(C組),各25例。兩組患者性別、年齡、身高、體質量、手術時間和麻醉時間等一般資料比較,差異無統計學意義(P>0.05),具有可比性,詳見表1。本研究方案經醫院醫學倫理委員會批準,患者或其家屬均知情同意并簽署知情同意書。
表1 兩組患者一般資料比較(,n=25)Tab 1 Comparison of general information between 2 groups(,n=25)
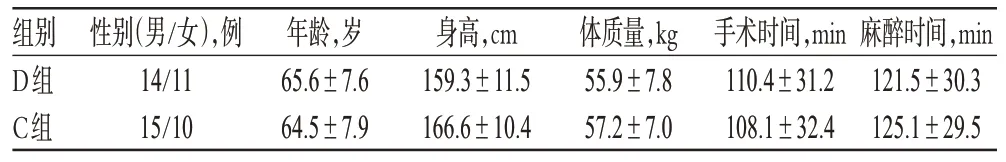
表1 兩組患者一般資料比較(,n=25)Tab 1 Comparison of general information between 2 groups(,n=25)
1.2 納入與排除標準
納入標準:①ASA分級Ⅰ~Ⅱ級;心功能Ⅰ~Ⅱ級。②無糖尿病、血液病及其他代謝障礙性疾病史;無高血壓,無長期使用糖皮質激素、三環類抗抑郁藥、抗菌藥物史。③未服用維生素類藥。④無嚴重感染性疾病,肺功能及實驗室檢查基本正常,血常規檢查中性粒細胞計數及分類數值均在正常范圍。⑤術前未行放療和化療。⑥預計手術時間≥1 h且≤4 h。
排除標準:①ASA分級Ⅲ~Ⅴ級者;②患有嚴重的呼吸、循環和內分泌疾病者;③肝腎功能不全者;④神經系統疾病者。
1.3 麻醉方法
麻醉前開放上肢靜脈通路,進行無創血壓監測,指測血氧飽和度,進行心電監護等,以10 ml/(kg·h)靜脈滴注乳酸鈉林格注射液。D組患者于全麻前開始靜脈泵注右美托咪定1 μg/kg負荷劑量,持續泵入10 min,隨后給予0.5 μg/(kg·h)維持劑量至手術結束。C組患者給予生理鹽水,其余處理相同。兩組患者麻醉誘導均采用丙泊酚2 mg/kg、芬太尼2 μg/kg、咪達唑侖0.02 mg/kg、維庫溴銨0.1 mg/kg,肌肉松弛后氣管插管,接麻醉機,機控呼吸,持續監測維持呼氣末二氧化碳分壓(PETCO2)在35~45 mm Hg(1 mm Hg=0.133 kPa),維持血壓波動在基礎值±20%范圍內。術中靜脈滴注丙泊酚3~6 mg/(kg·h)、瑞芬太尼7~9 μg/(kg·h)維持麻醉,縫皮時停用丙泊酚和瑞芬太尼。兩組患者麻醉深度盡量控制在同一水平。
1.4 觀察指標
監測兩組患者在手術開始時和切皮后10、30 min 以及手術結束時的心率(HR)、收縮壓(SBP)、舒張壓(DBP)。全麻誘導前(T0)、手術結束時(T1)、術后6 h(T2)、術后12 h(T3)、術后24 h(T4)、術后48 h(T5)采集患者頸內靜脈血檢測cTn Ⅰ、腎上腺素和去甲腎上腺素水平。
1.5 統計學方法
采用Prism 6.0軟件對數據進行統計學分析。組間比較采用兩獨立樣本t檢驗。P<0.05為差異有統計學意義。
2 結果
2.1 兩組患者手術過程各時點血流動力學變化
兩組患者手術開始時的HR、SBP、DBP 比較,差異均無統計學意義(P>0.05)。C 組患者在手術切皮后10、30 min 的HR、SBP、DBP 較手術開始時顯著升高,差異有統計學意義(P<0.05),且顯著高于D 組患者相應時點的HR、SBP、DBP值,差異有統計學意義(P<0.05)。兩組患者手術過程各時點血流動力學變化見表2。
表2 兩組患者手術過程各時點血流動力學變化(,n=25)Tab 2 Haemodynamics change of 2 groups at each time point during operation(,n=25)
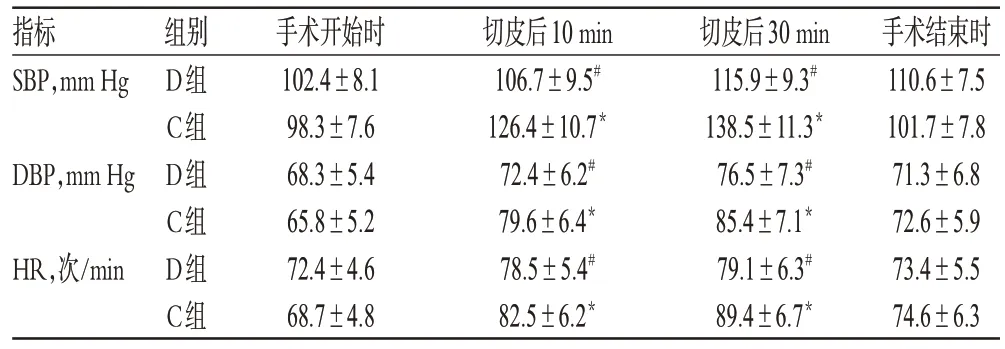
表2 兩組患者手術過程各時點血流動力學變化(,n=25)Tab 2 Haemodynamics change of 2 groups at each time point during operation(,n=25)
注:與手術開始時比較,*P<0.05;與C組比較,#P<0.05Note:vs.at the beginning of operation,*P<0.05;vs.group C,#P<0.05
2.2 兩組患者手術過程各時點cTn Ⅰ水平比較
與T0時比較,兩組患者的cTn Ⅰ水平從T1時即升高;在T2、T3、T4、T5時點,C 組患者的cTn Ⅰ水平較D 組升高明顯,差異有統計學意義(P<0.05)。兩組患者手術過程各時點cTn Ⅰ水平比較見表3。
表3 兩組患者手術過程各時點cTn Ⅰ水平比較(,n=25)Tab 3 Comparison of cTn Ⅰ concentration between 2 groups at each time point during operation(,n=25)

表3 兩組患者手術過程各時點cTn Ⅰ水平比較(,n=25)Tab 3 Comparison of cTn Ⅰ concentration between 2 groups at each time point during operation(,n=25)
注:與T0時比較,*P<0.05;與C組比較,#P<0.05Note:vs.T0,*P<0.05;vs.group C,#P<0.05
2.3 兩組患者各時點腎上腺素和去甲腎上腺素水平比較
與T0時比較,兩組患者的腎上腺素和去甲腎上腺素水平從T1時即升高;在T1、T2、T3、T4、T5時點,C組患者的腎上腺素和去甲腎上腺素水平較D 組升高明顯,差異有統計學意義(P<0.05)。兩組患者各時點腎上腺素和去甲腎上腺素水平比較見表4。
表4 兩組患者各時點腎上腺素和去甲腎上腺素水平比較(,n=25)Tab 4 Comparison of adrenaline and norepinephrine between 2 groups at each time point during operation(,n=25)
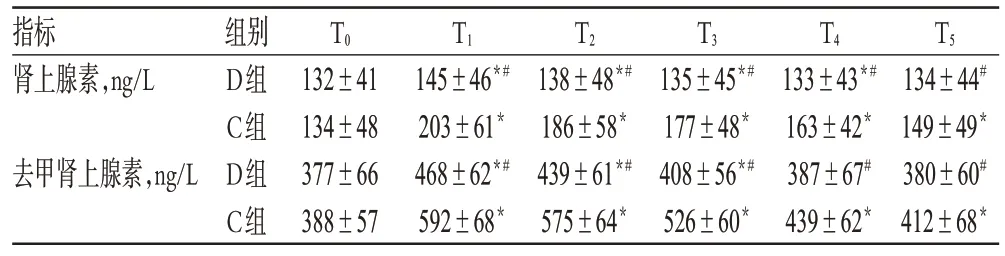
表4 兩組患者各時點腎上腺素和去甲腎上腺素水平比較(,n=25)Tab 4 Comparison of adrenaline and norepinephrine between 2 groups at each time point during operation(,n=25)
注:與T0時比較,*P<0.05;與C組比較,#P<0.05Note:vs.T0,*P<0.05;vs.group C,#P<0.05
3 討論
在全麻手術中,患者通常會因為手術刺激而產生全身應激反應,過度的應激反應會打破患者體內的內穩態平衡,產生血壓波動、心率升高、微循環代謝障礙等血流動力學異常現象,從而引發心、腦等重要臟器的并發癥[8]。因此,在臨床全麻手術中維持組織穩定的血流灌注、保護內穩態平衡是手術能否順利進行、術后能否良好恢復的關鍵[9-10]。
右美托咪定是一種高選擇性的α2受體激動藥,具有很強的鎮靜、鎮痛、抗焦慮及交感阻滯作用。它可以通過以下途徑對中樞神經、循環系統產生影響:(1)阻滯蛋白激酶A 及其磷酸化;(2)活化鉀通道和超極化細胞膜;(3)阻滯磺胺酸環化酶活化;(4)減少神經元活化和阻滯鈣離子通道[11-12]。
本研究中,兩組患者的cTn Ⅰ水平在術后均有一定程度升高,提示在圍術期均發生了心肌損傷;但D組患者cTn Ⅰ水平在T2、T3、T4、T5時點顯著低于C 組,提示右美托咪定對心臟有一定保護作用;兩組患者在T1時點的cTn Ⅰ水平比較雖然無明顯差異,但D 組較C 組有降低的趨勢(P=0.084),這可能與cTn Ⅰ于心肌損傷6 h 后達峰值有關。此外,D 組患者的HR、SBP、DBP在手術過程中各時點無顯著改變,且低于C組,據此推測右美托咪定可能在手術過程中通過穩定患者血流動力學、維持心肌組織灌流,一定程度上改善或預防了心腦缺血再灌注損傷,從而發揮了心臟保護作用。
右美托咪定還能通過調節機體外周循環腎上腺素和去甲腎上腺素濃度、抑制谷氨酸鹽釋放、抗凋亡等途徑實現對腦缺血再灌注損傷的保護作用[13-14]。本研究中,D組患者腎上腺素和去甲腎上腺素的水平在T1、T2、T3、T4、T5時點均較C組降低,差異有統計學意義(P<0.05),提示右美托咪定能有效控制術中和術后應激反應程度,避免高濃度腎上腺素和去甲腎上腺素對神經功能的毒性作用,從而發揮腦缺血再灌注損傷的保護效應。但是,右美托咪啶降低cTn Ⅰ、腎上腺素及去甲腎上腺素水平的具體作用機制有待進一步研究,這是本研究的不足所在。
[1]徐華.手術應激反應引發機制與調控[J].人民軍醫,2008,51(2):120.
[2]Bekker A,Haile M,Kline R,et al.The effect of intraoperative infusion of dexmedetomidine on the quality of recovery after major spinal surgery[J].J Neurosurg Anesthesiol,2013,25(1):16.
[3]劉玲,紀風濤,劉付寧,等.右美托咪定對老年患者腰-硬聯合麻醉的鎮靜效應[J].臨床麻醉學雜志,2011,27(1):49.
[4]萬永靈,陳學鈞,林濤,等.右美托咪定聯合地佐辛對剖胸手術后拔管期血流動力學及鎮痛鎮靜的影響[J].中國藥房,2013,24(38):3 616.
[5]Donnelly R,Millar-Craig MW.Cardiac troponins:IT upgrade for the heart[J].Lancet,1998,351(9 102):537.
[6]Eser O,Fidan H,Sahin O,et al.The influence of dexmedetomidine on ischemic rat hippocampus[J].Brain Res,2008,1 218:250.
[7]李煜,張永福,賴國忠,等.右美托咪定對腹腔鏡手術圍術期血兒茶酚胺及血流動力學的影響[J].中國微創外科雜志,2011,11(2):119.
[8]Chrousos GP,Gold PW.The concepts of stress and stress system disorders;overview of physical and behavioral homeostasis[J].Jama,1992,267(9):1 244.
[9]張瑜.麻醉深度對體外循環腦損傷的影響[D].大連:大連醫科大學,2011.
[10]郭榮,程芮.右美托咪定對腦缺血性損傷的保護作用[J].中國新藥與臨床雜志,2012,31(4):197.
[11]Afonso J,Reis F.Dexmedetomidine:current role in anesthesia and intensive care[J].Rev Bras Anestesiol,2012,62(1):118.
[12]Khan ZP,Ferguson CN,Jones RM.Alpha-2 and imidazoline receptor agonists.Their pharmacology and therapeutic role[J].Anaesthesia,1999,54(2):146.
[13]Kan MC,Wang WP,Yao GD,et al.Anticonvulsant effect of dexmedetomidine in a rat model of self-sustaining status epilepticus with prolonged amygdala stimulation[J].Neurosci Lett,2013,543:17.
[14]Dahmani S,Rouelle D,Gressens P,et al.Characterization of the postconditioning effect of dexmedetomidine in mouse organotypic hippocampal slice cultures exposed to oxygen and glucose deprivation[J].Anesthesiology,2010,112(2):373.

