培美曲塞或吉西他濱聯合順鉑治療晚期肺腺癌的對照研究
鄧 穎 胡洪林 楊 蘭 潘海霞 朱學強
國際多中心臨床研究證明了培美曲塞在晚期非小細胞肺癌(NSCLC)非鱗癌一線治療中的優勢后[1-2],非小細胞肺癌的治療進入到個體化治療時代[3]。我科采用培美曲塞聯合順鉑和吉西他濱聯合順鉑一線治療晚期肺腺癌患者,并進行隨機臨床對照實驗,現報告如下。
1 資料與方法
1.1 一般資料
將2009年2月至2012年12月收治的60例EGFR基因無突變晚期肺腺癌患者,隨機分為2組。實驗組30例,其中男性25例,女性5例,年齡30~69歲,平均51歲;ⅢB 期3例,Ⅳ期27例;對照組30例,其中男性20例,女性10例,年齡34~69歲,平均50.3歲;ⅢB期5例,Ⅳ期25例。2組性別、年齡、分期及病理類型比較差異無顯著性意義(P>0.05)。60例患者均無心、肝、腎及造血功能障礙,血常規正常,卡氏評分≥80分。
1.2 治療方案
實驗組(PP組)30例,培美曲塞500 mg/m2靜脈滴注,第1天;順鉑25 mg/m2靜脈滴注,第1~3天,每3周為1個化療周期。對照組(GP組)30例,采用吉西他濱1 000 mg/m2靜脈滴注第1天+順鉑25 mg/m2靜脈滴注第1~3天,每3周為1個化療周期。
1.3 療效評價標準
2組均化療2個周期后評價療效。以CT檢查結果評價目標病灶近期療效。采用RECIST實體瘤療效評價標準:完全緩解(CR),部分緩解(PR),穩定(SD),進展(PD)。不良反應評價采用不良反應常規標準(Common Terminoloy Criteria for Adverse Events v3.0,CTCAE 3.0)。
1.4 統計學方法
采用χ2檢驗比較2組患者治療后的近期療效和不良反應,所有統計處理采用SPSS 13.0軟件完成,P<0.05認為差異具有統計學意義。
2 結果
2.1 2組患者接受治療情況
每組患者共完成60個療程的化療,每例患者平均接受2個療程化療,提示初治的2個周期化療,患者耐受性均不錯。
2.2 近期療效
2組患者化療2個周期后評價療效。目標病灶的有效率實驗組和對照組分別是30.0%和26.7%,差異無統計學意義(χ2=0.08,P>0.05);疾病控制率(CR+PR+SD)實驗組和對照組分別是66.7%和70.0%,差異無統計學意義(χ2=0.08,P>0.05)。見表1。

表1 化療2個周期后的近期療效/例
2.3 不良反應
實驗組和對照組Ⅲ-Ⅳ度白細胞減少發生率分別為 13.3%和40.0%,差異有統計學意義(χ2=5.45,P<0.05);實驗組和對照組Ⅲ-Ⅳ度貧血發生率分別為3.3%、6.7%,差異無統計學意義(χ2=0.00,P>0.05);實驗組和對照組Ⅲ-Ⅳ度血小板下降發生率分別為6.7%、36.7%,差異有統計學意義(χ2=7.95,P<0.01)。肝功損害發生率2組比較,差異無統計學意義(χ2=0.27,P>0.05);2組腎毒性發生率都很低,差異無統計學意義;惡心嘔吐發生率實驗組與對照組相近,差異無統計學意義(χ2=0.07,P>0.05);脫發發生率實驗組和對照組分別為10.0%、33.3%,差異有統計學意義(χ2=4.81,P<0.05)。見表2。
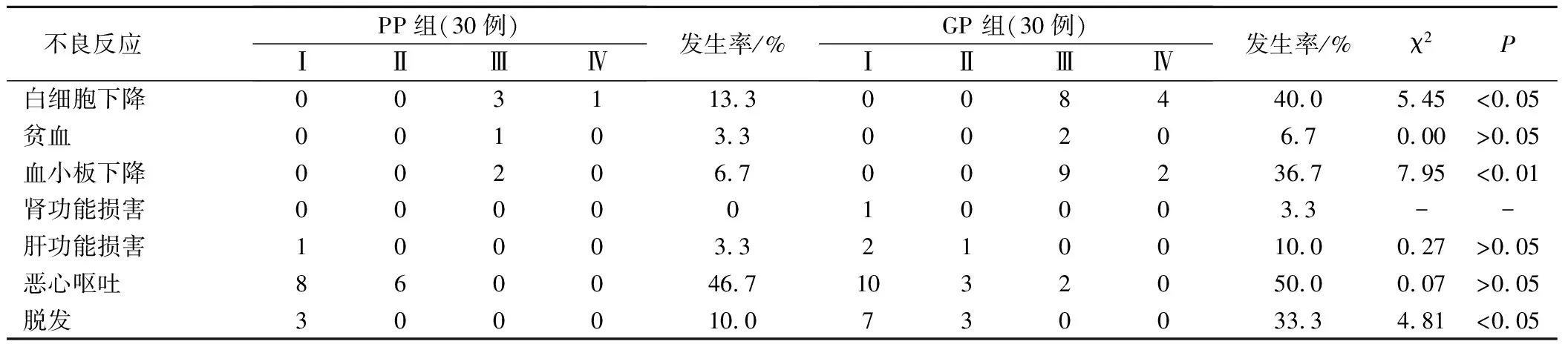
表2 2組患者化療后不良反應/例
3 討論
培美曲塞(pemetrexed,Alimta,力比泰)是種多靶點抗代謝的細胞毒藥物[4],與吉西他濱等藥物相比不良反應更輕[5]。培美曲塞通過破壞細胞內葉酸依賴性的正常代謝過程,抑制細胞復制,從而抑制腫瘤的生長。培美曲塞通過運載葉酸的載體和細胞膜上的葉酸結合蛋白運輸系統進入細胞膜內。一旦培美曲塞進入細胞內,它就在葉酸多谷氨酸合成酶的作用下轉化為多谷氨酸的形式。多谷氨酸存留于細胞內成為胸苷酸合成酶(TS)、二氫葉酸還原酶(DHFR)和甘氨酰胺核苷酸甲酰基轉移酶(GARFT)抑制劑,通過干擾胸腺嘧啶核苷和嘌呤核苷的生物合成,從而達到抗腫瘤的目的[6]。
一項非劣效性研究在1 745例晚期NSCLC患者(ⅢB期或Ⅳ期,多數為Ⅳ期)中比較了順鉑加吉西他濱與順鉑加培美曲塞的療效[1],非鱗狀細胞癌患者使用順鉑加培美曲塞方案生存期獲改善(12.6個月 vs 10.9個月);鱗狀細胞癌患者使用順鉑加吉西他濱方案生存期獲改善(10.8個月 vs 9.4個月)。基于這個實驗2011版的美國國立綜合癌癥網絡(NCCN)指南明確將晚期NSCLC的組織學分型作為指導臨床治療方案的第一選擇。
本研究中用培美曲塞或吉西他濱聯合順鉑一線治療晚期肺腺癌,2組有效率相近,但培美曲塞組卻大大降低了3/4級血液學毒性,脫發,增強了患者的耐受性。本觀察將有效和穩定的患者繼續原方案化療4~6個周期,若仍然腫瘤緩解或穩定,則2組均用培美曲塞維持化療,繼續觀察1年生存率,中位生存期,無疾病進展時間等遠期指標。
[1] Scagliotti GV,Parikh P,von Pawel J,et al.Phase Ⅲ study comparing cisplatin plus gemcitabinewith cisplatin plus pemetrexed in chemotherapy-na?ve patiens with advanced-stage NSCLC 〔J〕.Clin Oncol,2008,26(3):3543-3551.
[2] Wu LJ.Pemetrexed is approved for the treatment of non-sm-all cell lung canceras the first-line drugs〔J〕.Foreign Pharm Antibiot,2008,29(6):285-286.
[3] Wu SG,Yang CH,Yu CJ,et al.Good response to pemetrexed in patients of lung adenocarcinoma with epidemal growth factor receptor(EGFR)mutations〔J〕.Lung Cancer,2011,72(3):333-339.
[4] Kulkarni PM,Chen R,Anand T,et al.Efficacy and safety of Pemetrexed in elderly cancer patients:results of an integrated analysis 〔J〕.Crit Rev Oncol Hemato,2008,67(1):64-70.
[5] 姜 金,李 倫,王小晶,等.培美曲塞聯合鉑類對比吉西他濱聯合鉑類治療晚期非小細胞肺癌的meta分析〔J〕.中國肺癌雜志,2011,1(14):43-49.
[6] 黃漢生,楊蘭平.培美曲塞聯合順鉑治療晚期非小細胞肺癌的療效觀察〔J〕.實用癌癥雜志,2012,27(5):497-499.

