急性早幼粒細胞白血病緩解過程風險控制的臨床療效觀察
張軍 李東書 曹德文
急性早幼粒細胞白血病緩解過程風險控制的臨床療效觀察
張軍 李東書 曹德文
目的 探討全返式維A酸(ATRA)、三氧化二砷(ATO)聯合小劑量細胞毒藥物(常規劑量的1/4~1/5)在早幼粒細胞白血病(acute promyelocytic leukemia, APL)誘導緩解過程風險控制的臨床療效觀察。方法 22例APL患者(低、中危險組)隨機分成治療組和對照組。治療組患者12例, 對APL應用常規劑量ATRA 、ATO 聯合小劑量細胞毒藥物(常規劑量的1/4~1/5)。對照組患者10例, ATRA、ATO同治療組, 聯合常規劑量細胞毒藥物(按照2011版APL治療指南)。結果 兩組患者的完全緩解率90%以上, 差異無統計學意義(P>0.05);治療組患者無臟器出血, 感染發生率(4/12)33%, 對照組患者臟器出血(3/10)30%。感染率(10/10)100%, 其中肺炎發生率(2/10)20%, 高白細胞發生率8.3%, 差異有統計學意義(χ2=5.632, P<0.05);治療組較對照組明顯節約血液制品, 血小板輸注量減少81.6%, 紅細胞輸注量減少50%, 血漿輸注量減少79.1%。療效顯著, 差異有統計學意義(χ2=2.354, P<0.05)。結論 小劑量細胞毒藥物在APL誘導緩解中能有效的降低臨床風險、節約血液制品輸注。
急性早幼粒細胞白血病;全返式維A酸;砷劑;小劑量細胞毒藥物;風險控制;血制品
急性早幼粒細胞白血病(APL)占急性髓系白血病5%~8%, 以往治療死亡率高, 大部分死于出血、感染。自從全返式維A酸、砷劑問世以來, 開辟了急性白血病新的治療理念, 改變了以往的治療模式, 預后轉好。但在臨床治療過程中仍有一些問題存在, 有待解決。例如誘導緩解過程嚴重出血、感染等。本院選擇低、中危組APL患者, 分別應用小劑量細胞毒藥物(1/4~1/5量)和按照2011版血液病治療指南應用常規劑量細胞毒藥物, 兩組進行比較, 獲得了較滿意效果, 不影響臨床緩解率, 且有效的控制了臨床風險, 減少了血液制品的輸注。
1 資料與方法
1.1 一般資料 2010年1月~2012年1月經臨床確診為急性早幼粒細胞白血病患者22例, 采取隨機數字表法隨機分組為治療組和對照組。治療組患者12例, 男5例, 女7例,年齡13~55歲, 中位年齡39歲。對照組:10例患者, 男5例,女5例, 年齡15~50歲, 中位年齡36歲。治療前獲得患者及家屬的同意并簽署知情同意。
1.2 治療方法 治療組:誘導緩解方案:口服全反式維甲酸(ATRA)20 mg/(m2·d), 靜脈滴注三氧化二砷(ATO )0.16 mg/(kg·d),小劑量細胞毒藥物[ 靜脈滴注DNR 10~12 mg/(m2·d), 或米托蒽醌1~2 mg/(m2·d) , 靜脈滴注Ara-C 20~30 mg/(m2·d)]。細胞毒藥物應用原則:根據誘導緩解治療后白細胞數目變化情況應用, 一般不超過5 d, 這樣可以恰當、有效的控制白細胞綜合征發生, 又可最大限度的降低臨床風險。用藥時間:治療前白細胞總數低于10×109/L, 治療后翻倍或超過10×109/L時開始應用細胞毒藥物。
對照組:口服全返式維甲酸(ATRA)20 mg/(m2·d),靜脈滴注三氧化二砷(ATO ) 0.16 mg/(kg·d);靜脈滴注DNR 45~90 mg/(m2·d), 第2、4、6或第8天;靜脈滴注米托蒽醌12 mg/(m2·d), 第2、4、6或第8天; 靜脈滴注Ara-C 150 mg/(m2·d), 第1~7天。
1.3 選擇標準 臨床病史、實驗室及影像學依據均符合國際急性白血病MICM分型的診斷標準, 診斷急性早幼粒細胞白血病(低、中危組)。Karnofsky功能評分標準(KPS)評分≥60分;治療前心、肝、腎功能基本正常, 無化療禁忌證及過敏史;獲得家屬及患者同意。
1.4 療效評價標準 按張之南主編的《血液病診療和療效標準》中的急性早幼粒細胞白血病診療標準選擇患者與判定療效。完全緩解(CR)標準:①臨床無白血病細胞浸潤所致的癥狀和體征, 生活正常或接近正常。②血象:HB≥100 g/L(男), 或≥90 g/L (女及兒童), 中性粒細胞絕對值≥1.5×109/L, 血小板≥100×109/L。外周血白細胞分類中無白血病細胞。③骨髓象:原粒細胞+早幼粒細胞≤5%。部分緩解(PR)標準:骨髓原粒細胞+早幼粒細胞>5%而≤20%;臨床、血象中有一項未達完全緩解標準者。未緩解(NR)標準:骨髓象、血象、臨床均未達到緩解標準。
1.5 統計學方法 采用SPSS17.0統計學軟件對數據進行統計學分析。計量資料以均數±標準差( x-±s)表示, 采用t檢驗;計數資料采用χ2檢驗, P<0.05為差異具有統計學意義。
2 結果
急性早幼粒細胞白血病治療臨床緩解率均在90%以上,已經成為臨床共識。風險控制、節約血液制品是研究的課題。治療組輸注血制品機會明顯較少, 減輕患者負擔, 節約血源。治療組與對照組比較臨床緩解率差異無統計學意義(P>0.05)。風險控制方面:治療組無臟器出血, 感染發生率(4/12)33.3%,無高白細胞綜合征、維A酸綜合征發生;對照組臟器出血(3/10)30%, 感染發生率(10/10)100%, 其中肺炎發生率20%, 高白細胞發生率8.3%;血小板輸注量較少81.6%, 紅細胞輸注量較少50%, 血漿輸注量減少79.1%。療效顯著, 差異有統計學意義(χ2=2.354, P<0.05)。見表1, 表2。

表1 治療組與對照組并發癥對比
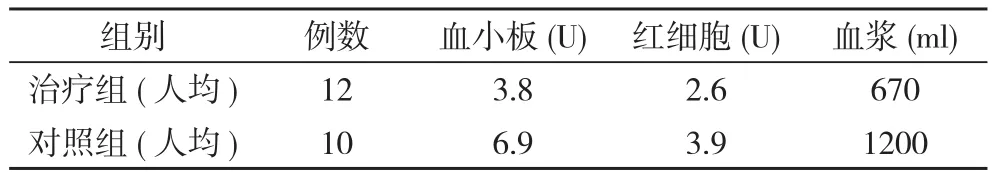
表2 治療組與對照組輸注血液制品情況
不良反應:治療組:毒副反應輕微, 胃腸反應Ⅰ度;骨髓輕度抑制Ⅱ度。對照組:胃腸反應Ⅱ~Ⅲ度;骨髓輕度抑制Ⅲ~Ⅳ度。
3 討論
個體化治療已成為惡性腫瘤治療的新理念。作者根據APL的自身特點, 一改以往應用常規劑量細胞毒藥物而改用小劑量(常規劑量的1/4~1/5)細胞毒藥物, 而且在給藥時機、用藥療程、給藥劑量上均因人而異, 不但不影響緩解率, 大大降低臨床風險, 而且無一例發生高白細胞綜合征和維A酸綜合征。作者采取小劑量細胞毒藥物有切實的理論依據:①充分利用急性早幼粒細胞白血病本身特點, 盡可能不造成異常早幼粒細胞的大量破壞導致促凝顆粒大量釋放引發嚴重出血。②上海瑞金醫院血液科李軍民教授在醫學論壇發表《急性早幼粒細胞治療有革新有爭議》文章中指出中國人群研究發現:ATRA和ATO分別作為單藥或結合再聯合蒽環類化療誘導初發APL患者, 結果完全緩解在三組均超過90%。③根據2011版中華醫學會血液學分會及美國NCCN制定APL的治療指南中應用足劑量細胞毒藥物誘導緩解率[1,2]與李軍民教授研究結果相當, 說明細胞毒藥物劑量越大所帶來的治療風險越大, 不會提高緩解率。④北京人民醫院血液科黃曉軍[3]教授編著的《血液病學》中APL誘導緩解治療篇指出要應用小劑量細胞毒藥物, 特別重用蒽環類細胞毒藥物。⑤APL經誘導治療使大量的病理早幼粒細胞轉化為中、晚幼粒細胞,而控制大量中、晚幼粒細胞的辦法恰是慢性粒細胞白血病(慢性期)的治療辦法[4]。張之南[5]主編《血液病學》關于慢性粒細胞白血病(慢性期)治療一篇中指出細胞毒藥物要小劑量應用。由于本樣研究為小樣本研究, 存在一定的不足,尚有待于進一步開展臨床大樣本、前瞻性、對照、雙盲研究驗證。
[1] 中華醫學會血液學分會.成人急性髓系白血病(非急性早幼粒細胞白血病)中國診療指南(2011年版).中華血液學雜志, 2011, 32(11): 804-807.
[2] 美國國立綜合癌癥網絡.《美國國立綜合癌癥網絡(NCCN)非小細胞肺癌(NSCLC)臨床實踐指南》.2011版.
[3] 黃曉軍.血液病學.北京:人民衛生出版社.2010:50.
[4] 張之南, 沈悌.血液病診斷及療效標準.北京:科技出版社, 2007:72.
[5] 張之南, 楊天楹, 郝玉書.血液病學.第2版.北京:人民衛生出版社, 2011:85.
2014-04-28]
136200 遼源市中心醫院血液科

