米卡芬凈治療兒童肺侵襲性真菌感染75例臨床研究
蘇庸春,管賢敏,溫賢浩,于 潔,憲 瑩,肖劍文,徐紅珍
(重慶醫(yī)科大學附屬兒童醫(yī)院血液科 400014)
隨著針對兒童白血病各種化療方案的持續(xù)改進及干細胞移植的廣泛開展,兒童惡性血液病尤其白血病的治療效果有了明顯的提高,但伴隨著強烈化療的開展及免疫抑制治療在干細胞移植后的長期應用,在治療過程中或治療后粒細胞缺乏階段,繼發(fā)侵襲性真菌感染的患兒卻明顯上升[1],并成為導致最終治療失敗的重要原因之一。在對深部真菌感染時抗真菌藥物的選擇上,有效性、安全性及盡可能小的交叉耐藥性與藥物相互作用是應首先考慮的因素。米卡芬凈是新近上市的一種棘白菌素類抗真菌藥,已經在歐洲及美國被推薦用于兒童抗真菌感染的治療[2]。本文作者以米卡芬凈經驗性治療75例兒童惡性血液病、原發(fā)性免疫缺陷病及干細胞移植患兒繼發(fā)肺部真菌感染,總結米卡芬凈治療兒童肺侵襲性真菌感染的療效與不良反應,現報道如下。
1 資料與方法
1.1 一般資料 75例患兒中,男30例(40%),女45例(60%);中位年齡34個月(11~160個月),平均體質量16.5 kg(8~50kg)。75例患兒中,急性淋巴細胞白血病37例(49.3%),急性髓細胞白血病21例(28.0%),再生障礙性貧血6例(8.0%),原發(fā)性免疫缺陷病6例(8.0%),噬血淋巴組織細胞增生癥5例(6.7%)。63例(84.0%)患者接受了持續(xù)化療,10例(13.3%)患者行干細胞移植(其中,臍血干細胞移植9例,同胞異基因骨髓干細胞移植1例),2例(2.7%)行免疫調節(jié)治療。
1.2 病例選擇標準 所有病例均在化療或干細胞移植后免疫抑制劑使用過程中并發(fā)較重的肺侵襲性真菌感染,或前期應用口服抗真菌藥防治過程中出現肺部病變加重,達到侵襲性深部真菌感染不同程度診斷標準[3]。其中,7例患兒正在口服伊曲康唑,9例患兒正在口服伏立康唑,12例患兒在正應用靜脈脂質體二性霉素B治療中,共計28例患兒由于肺部感染加重換用米卡芬凈靜脈治療。
1.3 方法 開始應用米卡芬凈時即停用其他抗真菌或預防真菌藥;米卡芬凈劑量2.5~5mg·kg-1·d-1,靜脈滴注,持續(xù)1h以上,每天1次,14d為1個療程,根據臨床癥狀體征及肺部影像學情況換用其他抗真菌藥;未采用聯合抗真菌治療策略。
1.4 臨床療效及安全性評價 治療前后行血、尿常規(guī),肝腎功能及胸部高分辨率CT檢查,治療前行痰培養(yǎng)、G試驗、GM試驗尋找病原學依據;治療期間詳細觀察癥狀、體征及有關實驗室檢查,并記錄有無不良反應及對癥處理。根據衛(wèi)生部1993年頒發(fā)的抗菌藥物臨床研究指導原則,按痊愈、顯效、進步、無效4級進行臨床療效判斷,前2級合計為有效并計算有效率。
1.5 統計學處理 采用χ2檢驗對米卡芬凈在不同危險因素及基礎疾病,以及基礎治療方法間的療效進行比較,以P<0.05為差異有統計學意義。
2 結 果
2.1 米卡芬凈應用情況 75例應用米卡芬凈治療的兒童肺侵襲性真菌感染病例中,均有咳嗽至少1周以上常規(guī)抗感染治療無效,經胸部高分辨率CT檢查有斑片影、廣泛滲出性病變或毛玻璃樣改變;有55例同時符合粒細胞缺乏伴發(fā)熱診斷,用米卡芬凈治療前粒細胞缺乏時間平均11.3d(中位數12d)。其中,達到確診標準的6例(8.0%);達到臨床診斷標準的47例(62.7%);達到擬診診斷標準的22例(29.3%)。米卡芬凈平均使用劑量為3.8mg·kg-1·d-1,治療時間平均18d(14~28d);初始治療及治療過程中至治療結束均未調整劑量,見表1。
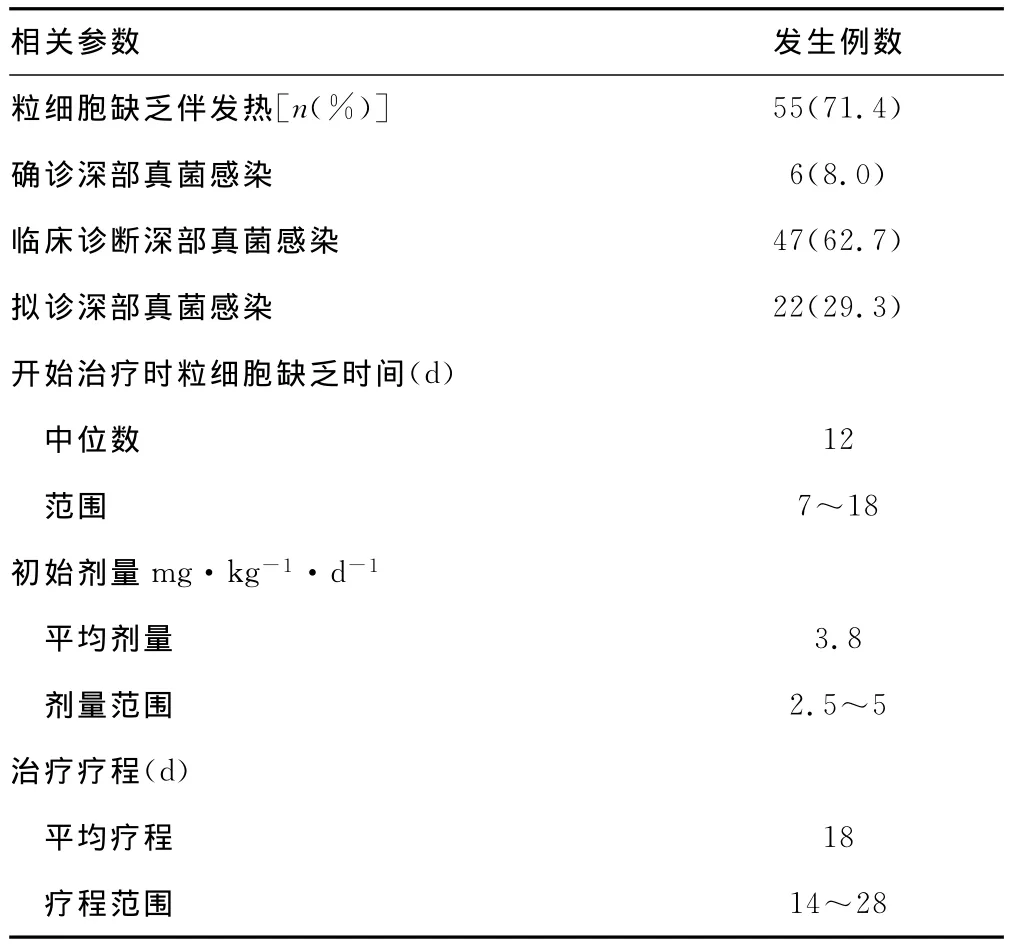
表1 米卡芬凈治療相關資料
2.2 米卡芬凈對兒童肺侵襲性真菌感染療效 米卡芬凈治療75例兒童擬診或臨床診斷深部真菌感染療效見表2。75例患兒均表現為肺侵襲性真菌感染;經治療后痊愈5例,顯效62例,進步4例,無效4例;總有效率為89.3% ;死亡2例,病死率為2.7%。不同基礎疾病應用米卡芬凈治療效果存在差異,但無統計學意義(急性白血病總有效率93.1%,原發(fā)性免疫缺陷病66.7%,噬血淋巴組織細胞增生癥80.0%,再生障礙性貧血83.3%);米卡芬凈在治療化療患兒與干細胞移植患兒合并肺部深部真菌感染療效差異無統計學意義(P>0.05);應用米卡芬凈前是否已經應用其他抗真菌藥的療效差異無統計學意義(P>0.05)。
2.3 米卡芬凈治療兒童肺真菌感染安全性評價 所有應用米卡芬凈的兒童均未觀察到與藥物相關或可能相關的過敏及精神癥狀,治療前、后轉氨酶指標、腎功能指標、電解質檢查、心肌酶譜指標差異無統計學意義,見表3。無因藥物不良反應而停藥病例。75例患兒中,有9例在用藥過程中出現了藥物相關不良反應,其中,4例為轉氨酶輕度升高,3例為隱性黃疸(血清總膽紅素小于或等于34.2mmol/L),出現皮疹及腹瀉各1例(表4)。

表2 米卡芬凈對侵襲性兒童肺真菌感染療效[n(%)]
表3 米卡芬凈用藥前后臟器功能指標監(jiān)測()

表3 米卡芬凈用藥前后臟器功能指標監(jiān)測()
項目 用藥前 用藥后P膽紅素(μmol/L) 13.71±5.7413.43±5.21 >0.05谷丙轉氨酶(U/L) 32.28±11.8235.44±14.59>0.05谷草轉氨酶(U/L) 49.74±5.9244.30±8.95 >0.05肌鈣蛋白(μg/L) 2.11±0.912.35±0.71 >0.05磷酸肌酸激酶(U/L) 158.28±20.98168.47±18.41>0.05磷酸肌酸激酶同工酶(U/L) 20.14±10.2519.45±11.53>0.05尿素氮(mmol/L) 6.19±1.415.84±1.68 >0.05血鈉(mmol/L) 138.55±11.32134.26±10.12>0.05血鉀(mmol/L) 4.14±1.233.65±1.58 >0.05血鎂(mmol/L) 0.91±0.120.87±0.13 >0.05血磷(mmol/L) 1.81±0.211.92±0.15 >0.05血鈣(mmol/L) 2.01±0.162.11±0.11 >0.05

表4 藥物相關不良反應
3 討 論
近年來隨著大劑量聯合化療、免疫抑制劑、廣譜抗菌藥物及造血干細胞移植的廣泛應用,惡性血液病患者包括合并肺侵襲性真菌感染的發(fā)病率逐年升高;且由于惡性血液病患者合并肺侵襲性真菌感染時癥狀常不典型,明確診斷困難,因此,預后較差、病死率較高[4]。中華醫(yī)學會兒科分會呼吸學組新近發(fā)布的“兒童侵襲性肺真菌感染診治指南(2009版)”涵蓋了兒童血液病治療過程中必將發(fā)生的宿主危險因素,如原發(fā)疾病所致的免疫功能低下、強烈化療、長期皮質激素和其他免疫抑制劑應用、造血干細胞移植、為控制繼發(fā)感染采用強效廣譜抗菌藥物及深靜脈置管等[5]。因此,兒童血液病及原發(fā)性免疫缺陷癥患者必然是肺侵襲性真菌感染高危患者,在治療原發(fā)病的過程中隨時應對肺侵襲性真菌感染保持高度警惕,合理控制肺侵襲性真菌感染的危險因素;及時診斷、早期經驗性治療,對改善兒童血液病患者預后具有重要意義。本組病例達到確診及臨床診斷水平的僅53例,22例均為擬診階段根據病情及時加用或換用米卡芬凈,這是取得較好治療效果的一個重要原因。
目前,治療肺侵襲性真菌感染的常用藥物有:兩性霉素B、唑類(如氟康唑、伊曲康唑、伏立康唑等)及棘白菌素類。雖然兩性霉素B是廣譜的抗真菌藥并具有很強的抗真菌活性,但對兒童患者,其腎功能損害、頑固性低鉀血癥等嚴重的不良反應使其應用受到限制;唑類抗真菌藥物毒性較兩性霉素B低,但近年來耐藥率顯著增加[6]。米卡芬凈是美國食品藥品管理局批準的另一種棘白菌素類抗真菌藥物,其抗菌譜廣,對唑類抗真菌藥耐藥的念珠菌屬和曲霉菌屬具有廣譜的抗菌活性,而且米卡芬凈與三唑類抗真菌藥及二性霉素B不存在交叉耐藥[7],因此,該藥一上市即很快被臨床醫(yī)師所接受。此外,由于米卡芬凈對肝腎功能影響小,對輕中度肝腎功能損害的患者無需調整劑量,在多個真菌防治指南中已將其列入血液腫瘤患者預防性或經驗性治療深部真菌感染的推薦用藥。本組資料有28例患者均為前期使用其他抗真菌藥的情況下,因藥物相關不良反應或病情進展換用米卡芬凈治療,并且均取得較好的療效,且臨床證實米卡芬凈與其他抗真菌藥之間不存在交叉耐藥性。
由于目前絕大部分抗真菌藥均缺乏兒童用藥依據,對于兒童肺侵襲性真菌感染的治療常常是臨床醫(yī)師面臨的棘手問題。臨床研究證實,米卡芬凈對兒童肺侵襲性真菌感染患者具有抗菌效力強、安全性高、抗菌譜廣的特點[8],藥物經濟學研究還證實以米卡芬凈預防性應用于干細胞移植具有成本-效益優(yōu)勢,顯示其高性價比的特點[9]。
本文作者應用米卡芬凈經驗性治療兒童肺侵襲性真菌感染75例,取得了滿意的臨床效果,總體有效率89.3%。取得如此臨床效果,除米卡芬凈廣譜的抗真菌效力外,與本研究中多數病例是在獲得病原學依據之前經驗性用藥有關。因此,盡早的合理選用抗真菌藥物對患兒最終治療效果尤為重要。本研究還發(fā)現對兒童化療以及干細胞移植期間合并肺侵襲性真菌感染治療效果差異無統計學意義(P>0.05),兒童白血病、噬血淋巴組織細胞增生癥及原發(fā)性免疫缺陷癥合并肺侵襲性真菌感染應用米卡芬凈治療療效差異無統計學意義(P>0.05)。因此,米卡芬凈對于各種危險因素條件下繼發(fā)的肺侵襲性真菌感染均有良好的治療效果。
經過對米卡芬凈在兒童深部真菌感染治療中的臨床觀察及相關臟器功能隨訪,本研究中未發(fā)現與米卡芬凈密切相關的嚴重不良反應,所有患兒均能良好的耐受靜脈給藥,除4例轉氨酶輕度升高,2例出現輕度膽紅素升高、腹瀉及皮疹各1例外,未觀察到心肌酶譜、肝腎功能、電解質指標的異常,隨訪各項指標用藥前后差異無統計學意義,提示其安全性良好。
[1]Mor M,Gilad G,Kornreich L,et al.Invasive fungal infections in pediatric oncology[J].Pediatr Blood Cancer,2011,56(7):1092-1097.
[2]Hicheri Y,Toma A,Maury S,et al.Updated guidelines for managing fungal diseases in hematology patients[J].Expert Rev Anti Infect Ther,2010,8(9):1049-1060.
[3]謝曉恬.兒童血液病深部真菌感染的防治研究[J].臨床兒科雜志,2010,28(4):396-400.
[4]Bhatt VR,Viola GM,Ferrajoli A.Invasive fungal infections in acute leukemia[J].Ther Adv Hematol,2011,2(4):231-247.
[5]中華醫(yī)學會兒科學分會呼吸學組,中華兒科雜志編輯委員會.兒童侵襲性肺部真菌感染診治指南[J].中華兒科雜志,2009,47(2):96-98.
[6]Lass-Florl C.Triazole antifungal agents in invasive fungal infections:a comparative review[J].Drugs,2011,71(18):2405-2419.
[7]喬建軍,劉偉,萬喆,等.米卡芬凈對分離自中國的念珠菌和曲霉臨床株體外抑菌活性的研究[J].中國真菌學雜志,2007,2(1):5-9,13.
[8]Antonio CA.Philip maddison and andreas H.groll.safety of micafungin in pediatric clinical trials[J].Pediatr Infect Dis J,2011,30(6):97-102.
[9]Schonfeld W,Wang Cheng J,Tong KB,et al.Cost-effectiveness analysis of antifungal prophylaxis in patients undergoing hematopoietic stem cell transplantation[J].Clin Ther,2008,30(5):964-973.

