索拉非尼治療中晚期肝細胞癌安全性和預后因素分析
鄭家平,邵國良,羅君,陳玉堂,姚征,曾暉,郝偉遠
·腫瘤介入Tumor intervention·
索拉非尼治療中晚期肝細胞癌安全性和預后因素分析
鄭家平,邵國良,羅君,陳玉堂,姚征,曾暉,郝偉遠
目的探討索拉非尼治療中晚期肝細胞癌(HCC)的安全性及影響預后的因素。方法2006年2月—2012年12月,89例中晚期HCC患者接受索拉非尼靶向治療。采用單因素和多因素分析患者各項臨床病理學參數與其預后的關系,并觀察索拉非尼相關不良反應。結果74例患者可作療效評價,死亡45例,存活27例,失訪2例。疾病控制率(DCR)85.14%。中位腫瘤進展時間(mTTP)6.53個月(95%CI: 4.79~8.26個月),中位總生存時間(mOS)9.93個月(95%CI:8.13~11.74個月)。單因素分析發現,PS評分、Child-Pugh分級、BCLC分期、腫瘤血管侵犯及不同的治療模式對預后的影響有統計學意義。進一步多因素分析發現,Child-Pugh分級和治療模式是患者預后的獨立影響因素(P<0.05)。服用索拉非尼主要不良反應為手足皮膚反應、消化道不良反應、乏力、骨髓抑制等。結論肝功能良好的HCC患者采用TACE術后序貫索拉非尼治療可獲得較長的生存時間和疾病穩定狀態。口服索拉非尼不良反應大多可以耐受。
癌,肝細胞;索拉非尼;治療
肝細胞肝癌(HCC)是常見的惡性腫瘤。索拉非尼具有抑制腫瘤新生血管形成和抑制腫瘤細胞增殖的雙重作用[1]。在HCC藥物治療中是唯一被臨床證實能夠延長晚期HCC患者總生存期(overall survival,OS),且安全性較好的藥物[2-3]。中位OS和中位腫瘤進展時間(to tumor progress,TTP)可延長1~3個月。最近亞太多中心亞組研究顯示,無論患者基線如何,索拉非尼治療晚期HCC均安全有效,能顯著延長OS和TTP[4]。本研究旨在進一步探索索拉非尼治療中晚期HCC患者的安全性及影響預后的因素。
1 材料與方法
1.1 臨床資料
1.1.1 入選條件①年齡≥18歲;②組織學或臨床診斷為HCC[5];③PS評分0~2;④未接受全身化療;⑤預計生存期≥12周;⑥實驗室檢查,白細胞計數≥3×109/L,血小板計數≥60×109/ L,血紅蛋白≥85 g/L;總膽紅素≤1.5倍正常上限,丙氨酸轉氨酶(ALT)和天冬氨酸轉氨酶(AST)≤5倍正常上限;血清肌酐水平≤1.5倍正常上限;凝血酶原時間較正常延長≤6 s(表1)。
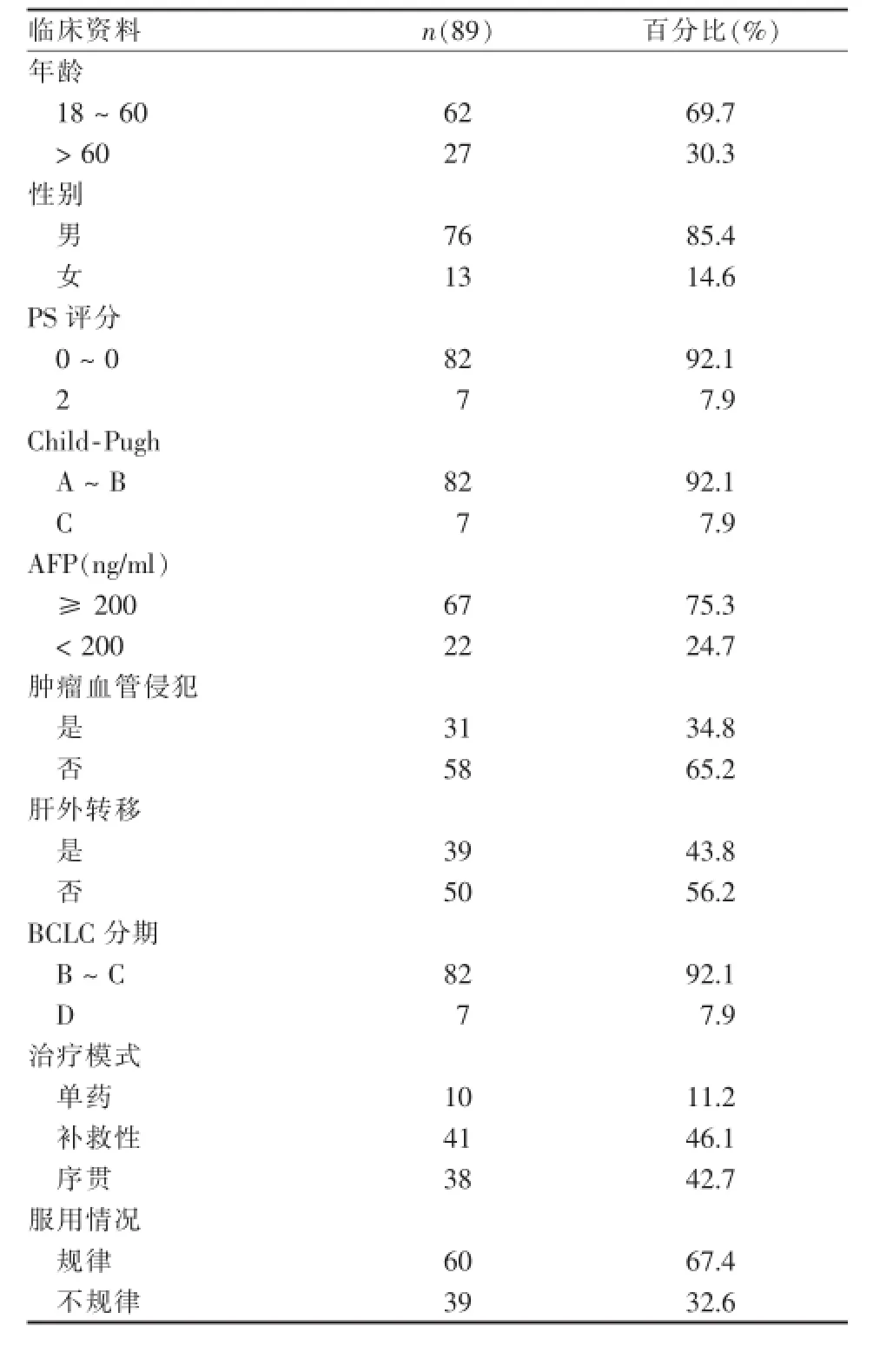
表1 入組患者臨床資料
1.1.2 排除標準①中樞神經系統轉移;②嚴重的基礎疾病,包括心臟病、感染及腎功能不全等;③難以控制的高血壓;④30 d內有大手術或消化道出血史。
1.2 方法
1.2.1 治療方法2006年2月—2012年12月,共有89例中晚期HCC患者入組,其中男76例,女13例。我們的研究按照患者意愿分為3組,①單藥組(n=10):患者只接受索拉非尼單藥治療,未接受其他系統和(或)介入治療。②序貫組(n=39):TACE術后,病灶穩定(stable disease,SD),序貫接受索拉非尼,口服索拉非尼時間為TACE術后3~7 d。TACE方法[6]:均采用Seldinger技術,經皮股動脈穿刺置入4~5 F肝管(RH導管,美國Cook公司或日本Terumo公司),必要時使用3 F微導管(日本ASAHI公司或美國Cook公司)技術超選擇至腫瘤供血動脈,注入化療藥物(鉑類、吡喃阿霉素、羥基喜樹堿等)和超液態碘油(5~20 ml,視病灶大小、數目等情況進行相應調整)的混懸液。TACE次數視病情可重復多次進行,間隔時間4~6周。③補救組(n=40):TACE術后,疾病進展(progress disease,PD)后聯合索拉非尼。
索拉非尼的初始劑量為400 mg/次,2次/d。出現不良反應時,應根據藥品說明書進行劑量調整。停藥指征為患者出現不能耐受的不良反應或死亡,或患者要求停止治療。在治療期間,患者每4~6周回訪,記錄用藥情況及不良反應。
1.2.2 療效評價完成2個周期治療后采用mRECIST[7]對療效進行評估,分為完全緩解(CR)、部分緩解(PR)、SD和PD。以CR+PR計算有效率(RR),以CR+PR+SD計算疾病控制率(disease control rate,DCR)。TTP定義為自索拉非尼口服開始至疾病進展的時間。不良反應按CTCAE 3.0標準判定[8]。
1.3 統計學方法
采用SPSS16.0軟件進行統計學分析。選取10個可能影響預后的臨床病理學參數進行單因素和多因素分析(Cox比例風險模型)。生存率采用Kaplan-Meier Log-rank test進行分析,以P<0.05為差異有統計學意義。
2 結果
2.1 腫瘤近期療效和生存隨訪
截止到2013年3月,74例患者可作療效評價,死亡45例,存活27例,失訪2例。DCR(CR+PR+ SD)(0+8+55)85.14%。15例未能獲得療效評估,其中4例口服索拉非尼2周后放棄治療;1例失訪;10例出現無法耐受不良反應,放棄治療。mTTP 6.53個月(95%CI:4.79~8.26個月),mOS 9.93個月(95%CI:8.13~11.74個月)。
2.2 生存分析
將表1中影響OS的10個因素分別行單因素分析,以P<0.05為檢驗水準,篩選出與OS顯著相關的6個因素,PS評分(P=0.000)、Child-Pugh分級(P=0.000)、BCLC分期(P=0.000)、腫瘤血管侵犯(P=0.024)、治療模式(P=0.032),余變量差異無統計學意義(P>0.05)。多因素回歸模型分析,得到2個獨立影響因子:Child-Pugh分級(P=0.021)、治療模式(P=0.045)(表2)。最后對2個獨立因子進行生存率分析,結果顯示:良好的肝功能分級和TACE序貫索拉非尼顯著延長mOS(圖1、2,表3、4)。
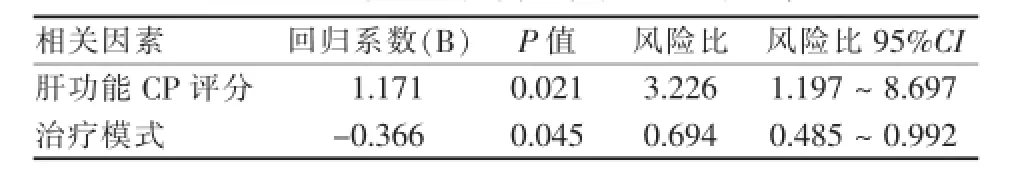
表2 影響OS的有統計學意義的因素
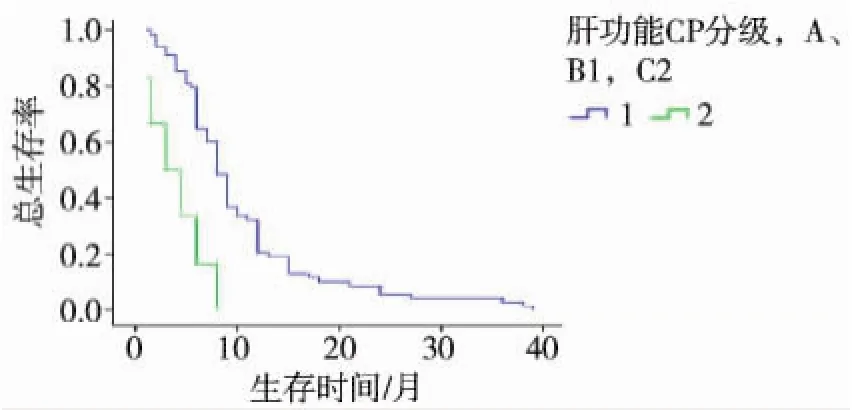
圖1 不同肝功能CP分級患者生存曲線
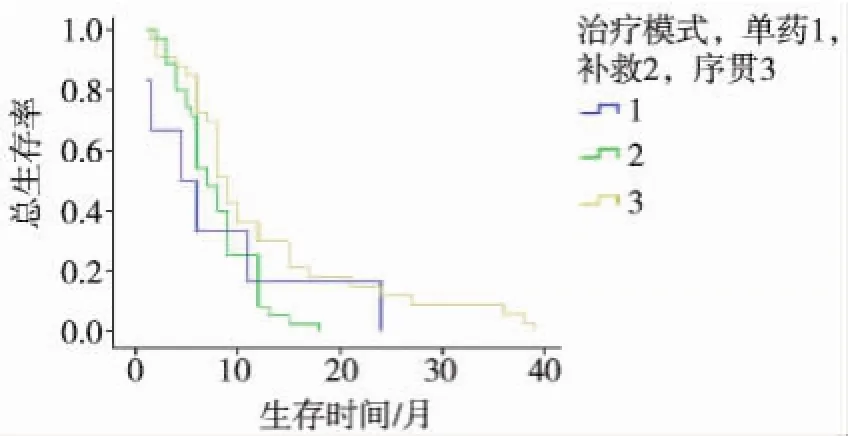
圖2 不同治療模式患者的生存曲線

表3 不同肝功能分級患者生存率
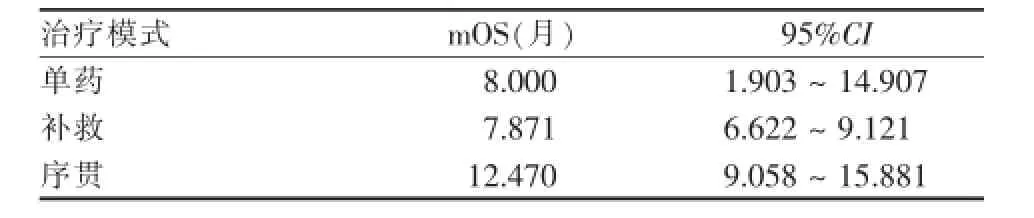
表4 不同治療模式患者的生存率
2.3 不良反應
服用索拉非尼主要不良反應為手、足和皮膚反應,消化道不良反應,乏力和骨髓抑制等(表5)。
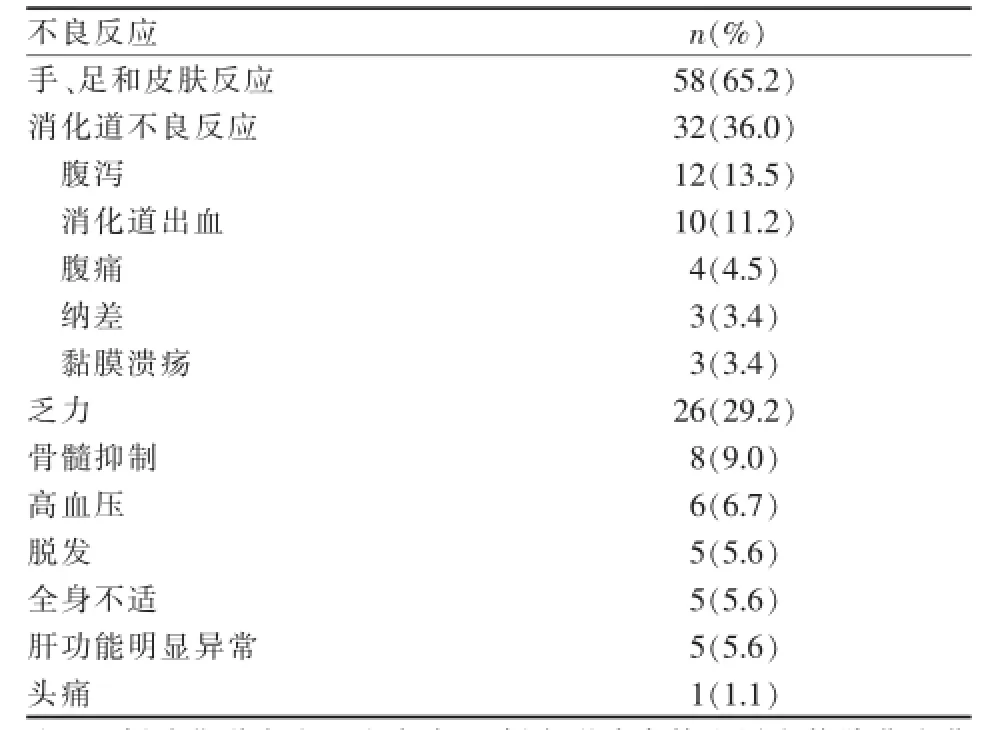
表5 索拉非尼治療89例中晚期HCC患者的不良反應
3 討論
本研究表明良好的肝功能、采用TACE術后序貫聯合索拉非尼的治療模式是提高中晚期HCC患者OS的關鍵。
索拉非尼具有抑制腫瘤新生血管形成和抑制腫瘤細胞增殖的雙重作用,一方面通過抑制Raf/ MEK/ERK信號傳導通路直接抑制腫瘤生長;另一方面通過抑制數種與新生血管生成有關受體的活性,包括血管內皮生長因子受體1(VEGFR1),VEGFR2,VEGFR3,和血小板衍生的生長因子受體β(PDGFR-β),阻斷腫瘤新生血管生成[2]。索拉非尼無論單藥還是聯合TACE均能延長HCC患者OS[1-2,6,8-9]。但需探索,預測索拉非尼療效的血清學和基于組織學的分子生物學標志物[10]。
多項研究認為,良好的肝功能或低PS評分或無血管侵犯可能是預測索拉非尼療效的影響因子[10-13]。本研究結論基本符合上述觀點。我們的研究顯示CP評分A/B與C比較,mOS得到明顯延長(10.456個月比4.0個月),一般認為,良好的肝功能儲備無疑有助于提高患者對索拉非尼的耐受性及增加同步接受其他抗腫瘤治療的機會。本研究觀察到的現象與Tsukui等[12]和Pinter等[13]報道一致:CP評分對患者OS具有獨立影響作用。另外,我們發現,單因素分析無血管侵犯可明顯延長患者OS(P= 0.024),但多因素分析未能顯示具有統計學差異,這與Iavarone等[11]及Tsukui等[12]的研究不一致。因此需要進一步擴大樣本量加以驗證。此外,Sansonno等[10]認為序貫治療模式相對比安慰劑而言,明顯延長HCC患者TTP。我們的研究表明序貫治療明顯優于單藥模式和補救模式,能明顯延長mOS(P<0.05),提示TACE仍是中晚期HCC首選微創治療,序貫聯合索拉非尼可能是目前最佳治療方案,而不是待TACE術后患者PD后采用索拉非尼進行補救,因此有理由相信,對于中晚期HCC,TACE聯合索拉非尼的時間越早越好。
口服索拉非尼不良事件發生率高,最常見仍是手、足和皮膚反應和消化道不良反應。本組有10例患者出現不能耐受嚴重不良反應,致使治療中斷。瑞士研究顯示,50例HCC患者接受TACE聯合索拉非尼序貫治療,其中出現3級以上嚴重不良事件32起,直接導致9例住院治療,死亡4例,臨床試驗隨之被迫中止[14]。臨床上一旦出現3級以上不良反應,一般采取調整藥物劑量或暫停服藥,結果可能影響療效[14-15],因此必須提高索拉非尼相關不良事件的處理能力。
本研究亦有許多不足之處:①作為回顧性的臨床隨訪研究,可信度降低;②總體變量較多,病例數仍偏少;③我們的研究將PS評分0~1和2之間進行分層分析,由于PS評分2的患者均為2009年之前納入研究的患者,樣本量少(n=7),造成了統計學的偏移,降低了研究結果的可信度。后續我們將擬對PS評分0與1之間進行分層分析。
[1]Cheng AL,Kang YK,Chen Z,et al.Efficacy and safety of sorafenib in patients in the Asia-Pacific region with advanced hepatocellular carcinoma:a phaseⅢrandomised,doubleblind,placebo-controlled trial[J].LancetOncol,2009,10:25-34.
[2]Lovet JM,Ricci S,Mazzaferro V,et al.Sorafenib in advanced hepatocellular carcinoma[J].N Engl JMed,2008,359:378-390.
[3]Zhu AX.Development of sorafenib and othermolecularly targeted agents in hepatocellular carcinoma[J].Cancer,2008,112:250-259.
[4]Cheng AL,Guan Z,Chen Z,et al.Efficacy and safety of sorafenib in patients with advanced hepatocellular carcinoma according to baseline status:subset analyses of the phaseⅢSorafenib Asia-Pacific trial[J].Eur JCancer,2012,48:1452-1465.
[5]中華人民共和國衛生部.原發性肝癌診療規范(2011年版)[J].臨床腫瘤學雜志,2011,16:929-946.
[6]Llovet JM,Bruix J.Systematic review of randomized trials for unresectable hepatocellular carcinoma:Chemoembolization improves survival[J].Hepatology,2003,37:429-442.
[7]Eisenhauer EA,Therasse P,Bogaerts J,et al.New response evaluation criteria in solid tumours:revised RECIST guideline(version 1.1)[J].Eur JCancer,2009,45:228-247.
[8]Sergio A,Cristofori C,Cardin R,et al.Transcatheter arterial chemoembolization(TACE)in hepatocellular carcinoma(HCC): the role of angiogenesis and invasiveness[J].Am JGastroenterol,2008,103:914-921.
[9]魏照光,陸驪工,邵培堅,等.肝動脈化療栓塞聯合索拉非尼治療中晚期肝細胞癌的臨床療效觀察[J].中華放射學雜志,2012,46:252-256.
[10]Sansonno D,Lauletta G,Russi S,et al.Transarterial chemoembolization plus sorafenib:a sequential therapeutic scheme for HCV-related intermediate-stage hepatocellular carcinoma:a randomized clinical trial[J].Oncologist,2012,17:359-366.
[11]Iavarone M,Cabibbo G,Piscaglia F,et al.Field-practice study of sorafenib therapy for hepatocellular carcinoma:a prospective multicenter study in Italy[J].Hepatology,2011,54:2055-2063.
[12]Tsukui Y,Mochizuki H,Hoshino Y,et al.Factors contributing to the overall survival in patients with hepatocellular carcinoma treated by sorafenib[J].Hepatogastroenterology,2012,59: 2536-2539.
[13]Pinter M,Sieghart W,Hucke F,et al.Prognostic factors in patients with advanced hepatocellular carcinoma treated with sorafenib[J].Aliment Pharmacol Ther,2011,34:949-959.
[14]Sieghart W,Pinter M,Reisegger M,et al.Conventional transarterial chemoembolisation in combination with sorafenib for patients with hepatocellular carcinoma:a pilot study[J].Eur Radiol,2012,22:1214-1223.
[15]Kudo M,Imanaka K,Chida N,et al.PhaseⅢstudy of sorafenib after transarterial chemoembolisation in Japanese and Korean patients with unresectable hepatocellular carcinoma[J]. Eur JCancer,2011,47:2117-2127.
Sorafenib f or the treatment of intermediate-advanced hepatocellular carcinomas:its safety and prognostic factors
ZHENG Jia-ping,SHAO Guo-liang,LUO Jun,CHEN Yu-tang,YAO Zheng,ZENG Hui,HAO Wei-yuan.Department of Interventional Radiology,Zhejiang Provincial Cancer Hospital,Hangzhou,Zhejiang Province 310022,China
SHAOGuo-liang,E-mail:1438238471@qq.com
ObjectiveTo discuss the safety and prognostic factorsof sorafenib in treating intermediateadvanced hepatocellular carcinoma(HCC).M ethods From February 2006 to December 2012,eighty-nine patients with pathologically-or clinically-confirmed HCC were treated with sorafenib targeted therapy.Ten factors,including gender,age,PS score,Child-Pugh,BCLC stage,AFP,vascular invasion,metastasis,therapy model,and regular oral sorafenib,were evaluated by using univariate analysis and multivariate analysis.The adverse events thatwere related to sorafenib targeted therapy were recorded.Resu lts Followup made in March 2013 showed that 27 patients survived,45 patients died,and 2 patients were lost in touch.The disease control rate(DCR)was 85.14%,mTTP 6.53months(95%CI:4.79-8.26),mOS 9.93 months(95%CI:8.13-11.74).Univariate analysis indicated that low PSscore,low Child-Pugh(CP)score,early BCLC stage,non-vascular invasion,and sequential therapy model were significantly associated with longer overall survival(OS)(P<0.05).Multivariate analysis showed that CP score and therapy model were the independent prognostic factors(P<0.05).The adverse events related to oral sorafenib included mainly hand-foot skin reaction,adverse effect of gastrointestinal tract,fatigue,marrow suppression,etc.ConclusionThe sufficient liver function and TACE with postoperative sequential oral sorafenib can prolong survival time aswell as disease-stable duration.The sorafenib-related adverse events can be well tolerated by the patients.(J Intervent Radiol,2014,23:222-225)
carcinoma,hepatocellular;sorafenib;therapy
R735.7
A
1008-794X(2014)-03-0222-04
2013-05-08)
(本文編輯:俞瑞綱)
10.3969/j.issn.1008-794X.2014.03.010
浙江省衛生高層次創新人才培養工程基金
310022杭州浙江省腫瘤醫院介入科
邵國良E-mail:1438238471@qq.com

