開發一個簡易可行的化學動力學實驗
葛蕓輝 萬鴻博 郭景德
(西交利物浦大學化學系 江蘇蘇州 215123)
開發一個簡易可行的化學動力學實驗
葛蕓輝 萬鴻博 郭景德
(西交利物浦大學化學系 江蘇蘇州 215123)
介紹如何用實驗探究亞硝酸鈉和氯化銨在弱酸催化條件下的化學反應級數、反應速率常數、活化能等化學動力學參數,并討論了該反應作為普通化學和物理化學動力學教學實驗的操作條件。
化學動力學實驗 反應速率 反應級數 反應活化能
化學動力學是普通化學和物理化學課程的重要章節,對完善學生的知識結構和培養學生分析、解決實際問題的能力有重要意義。要幫助學生學好化學動力學,除了課堂教學和作業以外,化學動力學實驗及動力學數據分析是非常重要的環節。目前,國內各高校出版的物理化學實驗教科書中,成熟的化學動力學實驗為數較少,且往往涉及較昂貴的光譜或色譜儀器,令部分普通化學和物理化學教師望而卻步。所以,開發簡而不陋、切實可行的化學動力學實驗是普通化學和物理化學師生共同面對的課題和挑戰。
本文介紹的是一個簡便的化學動力學實驗。實驗的開發者主要是在讀的大學化學本科生。我們選擇的化學反應是亞硝酸鹽和銨鹽在弱酸催化條件下反應生成氮氣、水及氯化鈉。其化學反應方程式如下:
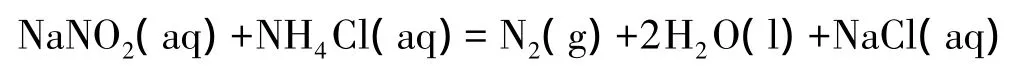
這個實驗涵蓋的化學動力學概念較為全面,簡而易行,不需任何光譜或色譜儀器,動力學數據的采集和處理也很方便,反應產物無毒性且重復性好。然而這個看似簡單的化學反應也存在著難點和可能的誤區。如果在反應物濃度、反應溫度和催化物濃度等方面處理不當,副反應會造成干擾,導致實驗失敗。本文著重討論我們在實驗開發中摸索到的較佳的操作條件,希冀能為化學動力學教學提供一種思路和方法。
1 實驗原理
從亞硝酸鹽和銨鹽制取氮氣是經典的無機化學反應,在中學化學教科書和大學普通化學中都有介紹。該反應被應用于石油管道脫蠟工藝,有實用價值。我們選擇這個反應作為化學動力學實驗的基本模型,是因為它所涉及的化學用品相對簡單,在適當的反應條件下,反應時間較短,產物收集簡便,在普通化學實驗室即可進行。這個實驗在20世紀50年代后不斷有文獻報導,但結論往往不一致,故仍值得進行探討。本實驗討論了該反應的幾個化學動力學基本參數的測定,包括反應級數、反應速率、反應速率常數以及反應活化能。其中反應速率由收集產物氮氣所需的時間來測定。在測定反應級數的過程中,為了排除因反應物濃度變化而引起的反應速率變化,我們只測量反應初速率,即反應物濃度減少不超過5%的條件下的反應速率。
從化學反應方程式看,整個反應并不涉及酸堿條件。但是在中性或堿性條件下,當反應物濃度為0.5mol/L左右,反應在室溫下幾乎不進行;當體系溫度達到50℃左右,才開始緩慢地產生氮氣。因此,在中性或堿性條件下,該反應不適合作為學生實驗。與此相反,在酸性條件下,該反應在室溫就可發生;在pH較低時反應速率更快。顯然,在反應機理中有H+參與。但由于反應過程并不消耗H+,故可以將H+作為催化劑處理。
在簡單的化學反應速率方程中,各反應物濃度的指數稱為該反應物的反應級數。反應級數反映了反應物對速率的貢獻。如依次變化反應物濃度以測量反應初始速率,即可判斷每個反應物的反應級數。具體到這個實驗,文獻中有稱其為二級反應,亦有稱其為三級反應[1];但如果計入酸濃度對反應速率的影響,反應的總級數可稱為四級。因此該反應的反應級數仍是有待探討的問題。
反應速率常數k主要決定于反應溫度。在給定溫度以及反應物濃度條件下,測定反應體系的初始速率,就可以確定反應的速率常數k。如果在兩個以上不同的溫度條件下測得不同的速率常數,在一定溫度范圍內的反應活化能Ea可視為常數,可利用阿倫尼烏斯(Arrhenius)方程獲得。
2 實驗用品
NaNO2固體(化學純),NH4Cl固體(化學純),冰醋酸,試管,橡膠塞,膠皮管,鐵架臺,量筒,厚壁斜兩口瓶,容量瓶,藥匙,燒杯,電子天平,溫度計,氣壓計,蒸餾水,油浴鍋,針頭,塑料注射器,磁力攪拌儀與攪拌子,秒表。
3 實驗步驟
3.1 溶液制備
稱量69.00g NaNO2,放入500mL容量瓶中,加蒸餾水至刻度線,搖勻,NaNO2濃度為2.00mol/L;稱量53.49g NH4Cl,放入500mL容量瓶中,加蒸餾水至刻度線,搖勻,NH4Cl濃度為2.00mol/L;稱量30.03g冰醋酸溶液,移至500mL容量瓶,加蒸餾水至刻度線,搖勻,冰醋酸濃度為1.00mol/L,放入通風櫥保存。
3.2 反應測定級數和反應速率常數測定
按照圖1方式組裝儀器,測量室溫以及大氣壓強pair。按表1在反應體系中加入NaNO2溶液、NH4Cl溶液以及攪拌子,充分攪拌溶液。由于此時尚未加入酸液,在接近室溫的條件下可以認為反應尚未發生。
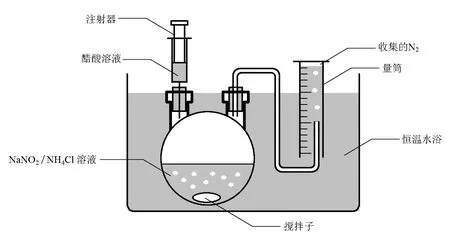
圖1 反應裝置
用注射器量取醋酸溶液,注入反應系統。當氣泡均勻穩定地生成時(建議等候約30秒鐘),開始用排水法收集氣體。測量收集1.0mL N2所需要的時間,重復一次取平均值,完成總計4×2=8組實驗。根據收集到的數據判斷NaNO2、NH4Cl的反應級數以及反應常數k。
在反應過程中,酸濃度直接與反應速率有關。但作為學生實驗,如果要求學生測定NaNO2、NH4Cl和H+三者各自的反應級數,耗時可能會超過通常的實驗課時。我們建議在實際操作時向學生說明H+的反應級數為一級,并嚴格地保持H+濃度在各組實驗中恒定,將反應級數測定的重點放在NaNO2和NH4Cl兩個化合物上。
從表面上看,反應速率方程式dV(N2)/dt=k'[NaNO2]m[NH4Cl]n[H+]中的反應速率常數k'可以通過初始速率和對應的反應物濃度求出。但在實際操作中,必須注意到方程左邊的速率單位是mL/s。要將這個單位轉換成每秒收集得到的氣體的物質的量(mol/s),需用理想氣體定律:n=,并對理想氣體方程兩邊對時間求導,得:同時,由于氮氣是在水面上方收集,真實的氮氣氣壓p(N2)等于外界大氣壓p(air)減去反應溫度條件下的水蒸氣氣壓p(H2O),即p(N2)=pair-p(H2O)。所以,在計算反應速率常數時,應為:
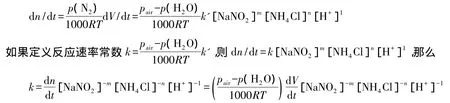
其中,k的單位是Lm+n+1mol-m-ns-1,p的單位是Pa,R的取值為8314.5Pa·L·mol-1·K-1。
3.3 反應活化能測定
在兩個以上不同溫度條件下測得反應速率常數k(T),即可根據阿倫尼烏斯方程計算反應活化能Ea。由于反應的起始時間以酸液的加入計起,所以在酸液加入之前,酸液和反應物的溫度應該用水浴控制到預定設置的溫度。
我們在實驗中發現,如果溫度高于50℃,副反應的干擾較大,測得的Ea重復性較差。如果溫度低于10℃,反應速率較慢,氣體收集時間過長。比較適宜的溫度區間為10~35℃。根據阿倫尼烏斯公式計算出該反應在醋酸催化條件下的活化能Ea,將在下節(實例)討論。
4 實例
表1列出了一個實際的實驗記錄,包括原始數據和數據處理步驟。在重復這個實驗的過程中,由于室溫、大氣壓、溶液濃度的差異,各個實驗室也許會觀察到不完全一致的結果,故表1數據僅供參考。
N2的生成速率可以表達為:
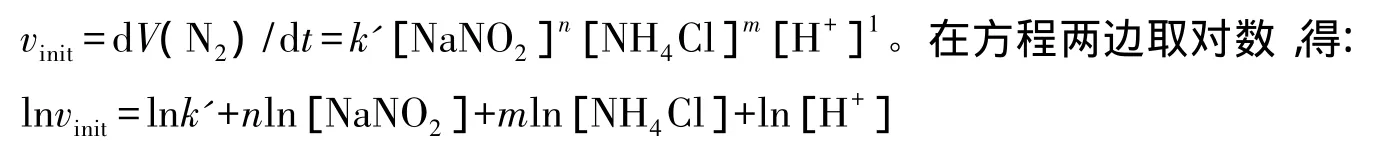
在整個實驗中,變化的參數主要是NaNO2的起始濃度(0.4~1.2mol/L)。以lnvinit對ln[NaNO2]作圖,得到的直線斜率即NaNO2的反應級數(圖2)。因為只記錄最初采集的幾毫升氣體的時間,反應物的濃度維持在初始濃度的98%以上,可以視為常數。
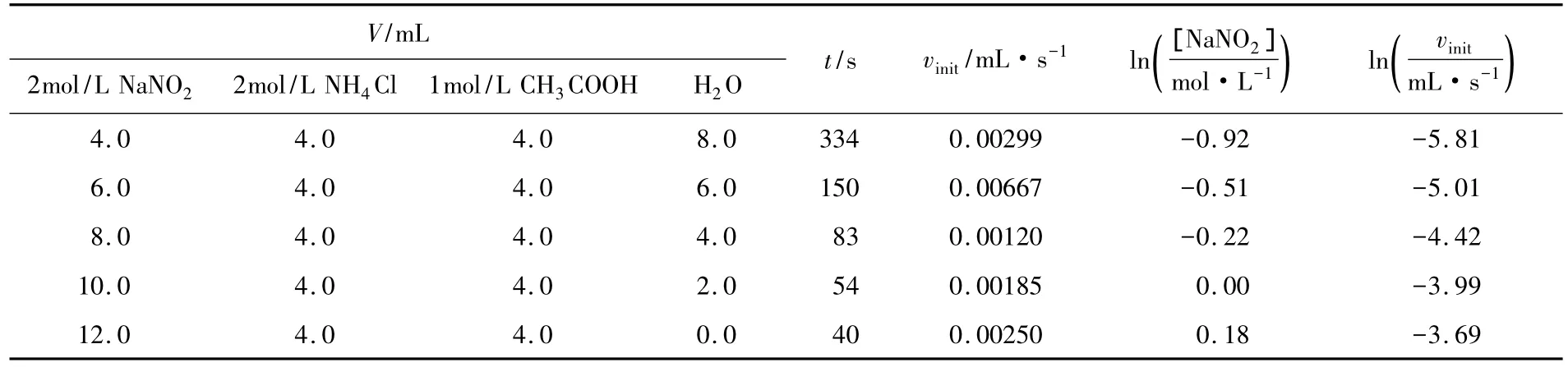
表1 測定NaNO2反應級數的實驗安排與數據
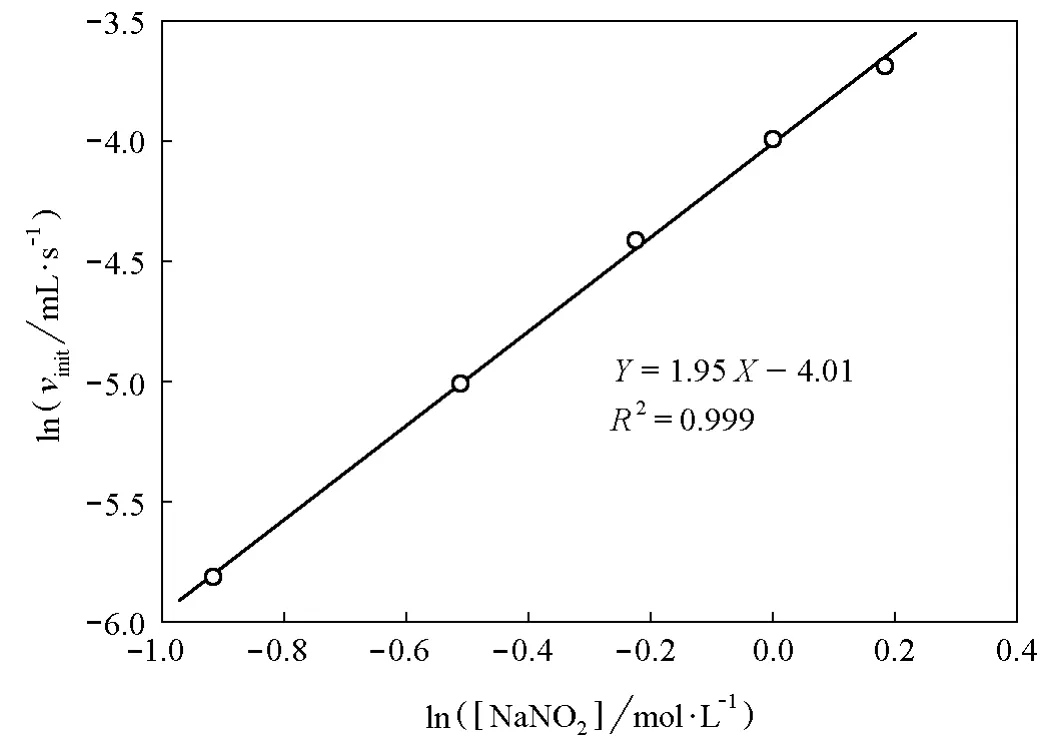
圖2 測定NaNO2的反應級數
在給出的實例中,直線斜率為1.95,據此可以判定NaNO2的反應級數為2。這個數值與文獻報導的結果吻合。用類似的方法,也可求出NH4Cl的反應級數。我們的實驗數據表明,NH4Cl的反應級數應為1,與文獻報導吻合[1]。
實際測得的反應溫度為293K,室內氣壓為pair=100120Pa,查表得水蒸氣壓力為p(H2O)=2338Pa,化學反應常數k(注意,不是k')可以表達為:
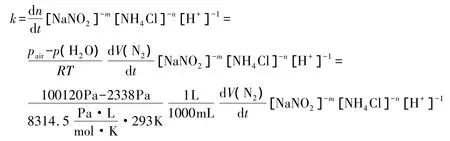
根據上述測定NaNO2反應級數的實驗數據,可以得出k的取值約為9.7×10-4L4·mol-3·s-1,與文獻值接近。需要指出的是,這里的[H+]不是醋酸的濃度,而是醋酸解離后的氫離子濃度。在計算中,0.20mol/L醋酸解離給出的氫離子濃度為0.0019mol/L。
為了測定化學反應的活化能,需要測定兩個以上不同溫度的反應常數k(T)。以下給出的實例包括了6個溫度點,從10℃到36℃。非常有趣的是,在這個相對狹窄的溫度區域內,氣體的生成速率變化了近11倍。實驗測定反應活化能的數據見表2。
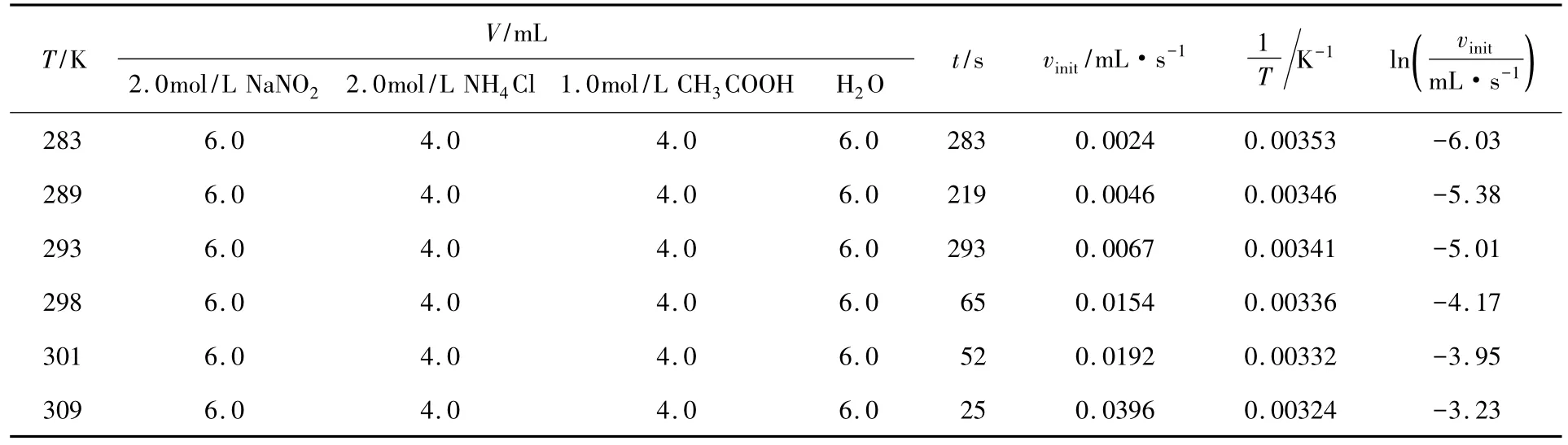
表2 測定反應活化能的實驗安排與數據
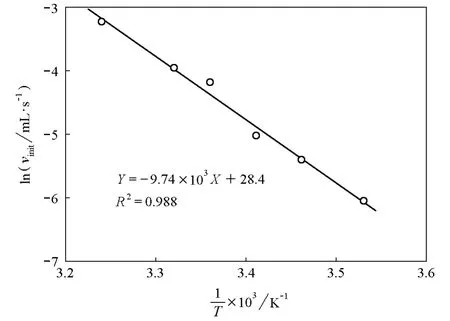
圖3 反應活化能測定數據與活化能計算
5 討論
用亞硝酸鹽-銨鹽生成氮氣的反應作為動力學模型,有如下幾個較為突出的優點:由于反應必須在酸性條件下才能發生,因此,在反應體系中加入醋酸溶液的步驟,可作為反應時間的控制開關,這就為時間控制與初始反應速率的測定提供了便利;由于反應產物是幾乎不溶于水的氮氣,可以用排除水體積法收集產物,在不具備光譜或色譜儀器的普通化學實驗室也能進行;在適當的濃度條件下,測定一個反應的初始速率,大約可在幾十秒至幾分鐘內完成,整個實驗可安排在近3小時的普化或物化實驗課內完成,這就保證了學生實驗的可行性。然而,這個看似簡單的化學反應,也存在著誤區和難點。其中最為突出的是反應的溫度控制,反應體系的密封,反應的酸性條件,生成NO等非N2氣體的副反應。
如上所述,從化學反應方程式上看,整個反應并不涉及酸堿條件。中學課本在介紹這個化學反應時,反應條件僅僅是加熱,沒有涉及加入酸液。在開發這個實驗的過程中,我們也曾嘗試在中性條件下,以加熱為反應條件生成氮氣。但在實驗中發現,當反應物濃度控制在0.5mol/L時,反應在50℃左右才會產生氣泡,且速率極其緩慢,氣體收集時間很長,因而不適合作為學生實驗。我們建議采用室溫條件,以較低濃度的弱酸作為催化劑,以縮短氣體收集時間,簡化實驗條件,并保證實驗的可重復性。
在實際操作時,如反應體系的接口處漏氣,會導致實驗失敗。因此,在反應前務必仔細檢查容器接口處是否密封,毛玻璃接口處要用真空硅膏密封。
很多文獻在報道亞硝酸鹽與氯化銨反應時,都提及用鹽酸作催化劑,反應速率與質子濃度成正比。然而,許多文獻避而未談作為強酸的鹽酸,會與反應物NaNO2反應生成一氧化氮(NO)以及其他非N2氣體,而且NO會與體系中殘存的氧氣反應生成紅棕色的NO2。同時,由于NO2溶于水,會造成反應體系的負壓,從而導致水的回流和實驗失敗,這一現象是在實驗設計中必須避免的。為了減少副反應的干擾,避免NO的生成,我們建議用醋酸取代鹽酸,并控制醋酸濃度在0.2mol/L以下;避免使用濃度過高的NaNO2;控制溫度接近室溫(10~35℃)。我們發現,在接近室溫條件下,控制體系醋酸濃度低于0.20mol/L,反應物濃度在0.4~1.2mol/L之間,形成NO等非N2氣體的副反應的干擾可以忽略。
另外,在測定反應活化能時,需在兩個以上溫度進行。我們發現在酸催化下,反應對溫度的改變非常敏感:如果溫度過高(如40℃),氣體的生成將會非常迅速,不利于氣體的收集和初速率的測定,并且有副反應發生,易導致實驗失敗。但若溫度過低(如0℃),反應則幾乎停止。用阿倫尼烏斯方程測定活化能時,為確保反應在較為穩定的條件下進行,我們建議取10~35℃,在這個溫度區間測得的反應速率有高達11倍的明顯差異,而且副反應的干擾可以忽略,測得的Ea重復性較好。
總之,我們在開發這個實驗時摸索到的較佳實驗參數是:反應溫度為25±10℃;體系醋酸濃度為0.2mol/L左右;體系NaNO2和NH4Cl的濃度為0.4~1.2mol/L。
值得指出的是,該反應看似簡單,但反應機理卻相當復雜,且目前尚無定論。Harrison等人在1996年報告中指出該反應是三級反應[1],而Dusenbury和Powell在1951年報告中指出該反應是二級反應[2]。我們認為,這些不一致的結論很可能是由于反應條件的差異引起的。由于我們的重點是開發簡易可行的動力學實驗,所以并不涉及對反應機理的研究。對機理有興趣的教師和學生可參閱文獻[3],其中有對該反應較為詳細的反應機理推測。
西交利物浦大學化學系王瑞瑤教授和陳曉翠研究生對本文提出了寶貴意見,特此致謝。
[1]Harrison C,Malati M,Smetham N.J Solution Chem,1996,25(5):505
[2]Dusenbury J,Powell R.J Am Chem Soc,1951,73(7):3266
[3]Nguyen D,Iwaniw M,Fogler S.Chem Eng Sci,2003,58(19):4351

