宮頸微偏腺癌16例臨床、影像與病理分析
吳建磊,孫寒雪,常爽,接智慧,王敏
(中國醫科大學附屬盛京醫院1.婦產科;2.病理科,沈陽 110004)
宮頸微偏腺癌(minimal deviation adenocarcinoma of cervix,MDA)是一種罕見的宮頸腺癌,由于其臨床表現缺乏特異性,病理組織學改變輕微,常易漏診及誤診,使大多數患者錯過最佳治療時機,預后不佳。因此,本研究收集了我院自2006年1月至2012年6月間16例MDA患者的臨床病理資料,現結合文獻總結分析如下:
1 材料與方法
1.1 一般資料
2006年1月至2012年6月我院共收治16例MDA患者,發病年齡37~64歲,平均45.1歲。主訴:白帶增多明顯,呈稀黏液狀12例,其中伴不規則陰道流血5例,病程1個月~5年;接觸性陰道流血3例,下腹疼痛1例。婦科檢查:宮頸顯著增大11例,直徑4~8 cm,其中5例宮頸表面光滑,6例伴宮頸表面輕至中度糜爛,3例伴乳頭狀或息肉狀增生,1例宮頸呈潰瘍狀改變;4例有接觸性出血,宮旁組織增厚5例,其中盆側壁累及1例。血清腫瘤標記物:2例癌胚抗原(CEA)升高(12.7 ng/mL,8.2 ng/mL);4例癌抗原(CA125)升高(45.6 U/mL,231.4 U/mL,85.7 U/mL,136.4 U/mL);1 例甲胎蛋白(AFP)升高(196 μg/L);鱗狀細胞癌抗原(SCC)均在正常范圍內(0.4~1.1 ng/mL)。宮頸細胞學檢查:僅有7例行液基薄層細胞學檢查(TCT),其中4例輕度炎癥,2例見未明確診斷意義的不典型鱗狀上皮細胞,1例見非典型細胞,不除外腺細胞來源。依據國際婦產科聯盟(FIGO,2000年)宮頸癌臨床分期標準,16例患者臨床分期:ⅠB 期 18.8%(3/16),ⅡA 期 25%(4/16),ⅡB期56.3%(9/16)。所有宮頸活檢標本及手術切除標本均經HE染色,光鏡觀察;免疫組化采用SP法,分別有9例應用CEA,7例應用p53,6例應用Ki-67、CAl25及ER染色。16例患者術前均行盆腔超聲檢查,10例術前行盆腔增強CT檢查,7例術前行盆腔增強MRI檢查,5例同時行CT和MRI檢查。
1.2 治療及隨訪
11例行廣泛性全子宮切除術及淋巴結切除術,其中1例手術后加局部放療1個周期后化療(FIP方案),其余10例手術后行化療(PVB方案5例,TC方案3例,TP方案2例);2例行宮頸錐切術后加化療(TC方案);2例門診陰道鏡活檢確診后行新輔助化療(TC方案);另1例拒絕治療自行出院。隨訪2.5~32個月,中位隨訪時間15個月,隨訪截止至2012年6月30日。
2 結果
2.1 病理診斷
13例術前行l~2次活檢,確診7例,首次活檢確診5例,首診確診率 38.5%(5/13),活檢陽性率 53.8%(7/13);另 9例術后病理檢查確診為MDA。術后病理檢查結果:16例病變部位可見深層浸潤的大量黏液腺體,腺體浸潤深部血管及神經組織,達100%(16/16),其中7例浸潤宮頸間質全層,占43.8%(7/16);盆腔淋巴結轉移者6例,占37.5%(6/16);其他:2例宮旁組織轉移,l例右側卵巢轉移。免疫組化:本組病例CEA染色陽性率為55.6%(5/9),p53染色陽性率為28.6%(2/7),Ki-67染色陽性率為 33.3%(2/6),CA125及 ER 均為陰性。見圖1。
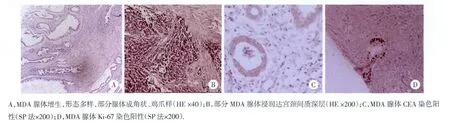
圖1 宮頸MDAHE及免疫組化染色圖片
2.2 影像學檢查
6例患者術前超聲檢查提示宮頸肥大,2例提示宮頸肥大伴血流豐富,8例提示宮頸囊性改變。8例患者術前行盆腔增強CT檢查,提示為宮頸管增大,其中5例呈多囊蜂窩樣改變,伴低密度區,增強后可見強化;4例提示宮頸癌可能性大。7例患者術前行盆腔增強MRI檢查均見子宮頸增大,其中6例見子宮頸間質多發、不規則的囊性病灶,T1WI低信號,T2WI高信號,靜脈注射釓(Gd)后囊腫明顯強化。
2.3 治療及隨訪
7例患者獲隨訪2.5~32個月。2例健在,其中1例于我院行根治術后加用局部放療1周期,后行FIP方案化療5周期,后改用FP方案化療3周期,于2012年5月復查出現肺轉移病灶,現應用斑蝥酸鈉+DP方案化療中。4例分別因局部復發和其他疾病死亡。另9例患者術后未至我院隨診,遂失訪。
3 討論
MDA組織學形態溫和,貌似良性,極易誤診。MDA的命名現已擴展應用于具有相應形態特征的子宮內膜樣、透明細胞和中腎腺癌[1]。MDA發病率低,所見文獻多為個案報道,尚缺乏大樣本的流行病學研究結果,國外報道其發病率約占宮頸腺癌的1%~3%[2],國內報道的發病率從1%~7.6%不等[3,4]。本研究中,MDA 占同期收治宮頸腺癌的 1.37%(16/1 168),與國內外文獻報道類似。
3.1 臨床表現
本組MDA患者平均年齡為45.1歲,與文獻報道接近[5]。MDA最常見的臨床癥狀為大量黏液性白帶,不規則陰道流血,部分患者間歇性下腹痛及性交后出血。婦科檢查宮頸呈不同程度的糜爛、增生,或宮頸部腫瘤,部分形態可正常,后期宮頸可桶狀或橡皮球狀,光滑,表面呈環形或結節狀,質硬。另外,MDA有時還伴有Peutz-Jeghers綜合征[6]。由于這些臨床表現缺乏特異性,常造成漏診及誤診,因此,我們認為在臨床工作中如遇到這樣的病例須注意MDA的可能,采取適當的檢查手段,以避免延誤診斷及治療時機。
3.2 診斷
MDA的診斷以宮頸活檢或術后病理診斷為準,其組織學特點:(1)腺體類似卵圓形,核質比正常,核染色質不粗,細胞核有異型性,核分裂少見;(2)腺體扭曲,或并有尖角狀、雞爪樣或樹枝樣突出;(3)腺上皮細胞呈高柱狀,細胞質內含黏液,異型性不明顯;(4)腫瘤性腺體分布不均勻,但一般無背靠背現象。另外,免疫組織化學在MDA的診斷中有重要的作用:CEA、Ki-67、p53、PCNA 在 MDA 中均呈陽性或強陽性反應,而正常宮頸腺體或良性增生的腺上皮中均呈陰性或微弱反應[7],本組16例MDA的確診由我院2位病理專家閱片確定,均符合上述組織學特點,同時16例MDA免疫組化染色均出現至少1項以上的指標陽性。
3.3 治療及預后
由于MDA病例數量較少,目前無循證醫學的研究,治療方式的選擇尚無統一標準。關于MDA的預后,文獻報道差異很大。Gilks等[8]報道26例MDA患者中,2年的無瘤生存率僅為50%,國內李華等[9]報道15例MDA患者的5年生存率達85.7%。本組獲隨訪的7例MDA患者5年生存率為28.6%,遠低于文獻報道,我們認為與獲隨訪的患者例數較少、分期較晚,且有2例患者術后未接受規范療程的化療有關。
MDA病例少見,臨床表現不典型,早期診斷困難。臨床醫生對MDA的臨床表現應該提高警惕,檢查中應結合超聲及增強MRI,如術前影像學檢查發現病灶呈多囊性改變并有明顯強化,應高度懷疑MDA的可能。總之,如何提高MDA的診治水平、改善預后仍值得廣大臨床醫生進一步探討研究。
[1]張建民,黃受方.女性生殖道病理學[M].北京:人民軍醫出版社,2009:243-246.
[2]Li G,Jiang W,Gui S,et al.Minimal deviation adenocarcinoma of the uterine cervix[J].Int J Gynecol and Obstet,2010,110(2):89-92.
[3]常沽,張莘,周暉,等.5例宮頸微偏腺癌的臨床分析[J].癌癥,2008,27(12):1310-13l4.
[4]徐珍,彭芝蘭,楊開選,等.宮頸微偏腺癌16例臨床與病理分析[J].實用婦產科雜志,2011,27(7):519-521.
[5]王袢晨,羊正炎.宮頸微偏腺癌201例分析[J].現代實用醫學,2012,24(3):321-322.
[6]伊喜苓,林蓓,朱連成,等.269例子宮頸微偏腺癌的meta分析[J].中國醫科大學學報,2009,38(5):369-372.
[7]魏萍,盛修貴,鄒衛青.宮頸微偏腺癌14例臨床病理分析[J].腫瘤學雜志,2009,15(3):200-201.
[8]Gilks CB,Young RH,Aguirre P,et a1.Adenoma malignum(minimal deviation adenocarcinoma)of the uterine cervix:a clinicopathologic and immunohistochemical analysis of 26 case[J].Am J Clin Pato,1989,13(9):717-729.
[9]李華,郭紅燕,韓勁松,等.宮頸微小偏離性腺癌的診治分析[J].中華腫瘤雜志,2008,30(10):772-774.

