一測(cè)多評(píng)法測(cè)定金銀花復(fù)方制劑中新綠原酸、綠原酸和隱綠原酸
朱粉霞,張亞麗,汪 晶,賈曉斌*
(1.江蘇省中醫(yī)藥研究院國(guó)家中醫(yī)藥管理局中藥口服制劑釋藥系統(tǒng)重點(diǎn)研究室,江蘇南京 210028;2.中國(guó)藥科大學(xué)中藥學(xué)院,江蘇南京 210009)
中藥復(fù)方制劑所含成分的復(fù)雜性使得單一成分或指標(biāo)性成分難以整體表達(dá)復(fù)方制劑的質(zhì)量,由此提出多指標(biāo)的質(zhì)量控制模式。在多指標(biāo)的質(zhì)量控制模式中,需要用足夠的化學(xué)對(duì)照品,而現(xiàn)實(shí)中對(duì)照品的供需矛盾和多指標(biāo)質(zhì)控高昂的檢測(cè)成本反過來又限制了多指標(biāo)質(zhì)量控制模式在實(shí)際生產(chǎn)、科研、監(jiān)督中的應(yīng)用。“一測(cè)多評(píng)”法(QAMS)是一種用于多指標(biāo)質(zhì)量控制的研究思路,目前已用于解決中藥質(zhì)量控制中缺乏對(duì)照品這一瓶頸問題,黃連的一測(cè)多評(píng)標(biāo)準(zhǔn)被2010年版《中國(guó)藥典》采納[1],其他化合物的一測(cè)多評(píng)研究也被報(bào)道[2-5]。超高效液相色譜(UPLC)具有超高壓、超高靈敏度、超高分離度等特點(diǎn),在中藥等復(fù)雜體系的分離分析上具有明顯優(yōu)勢(shì),目前正被越來越廣泛地應(yīng)用于中藥復(fù)雜體系的研究[6-12]。
金銀花復(fù)方制劑脈絡(luò)寧注射液、雙黃連口服液和銀黃顆粒中新綠原酸、綠原酸和隱綠原酸的含有量較高,為其藥理活性成分。綠原酸供應(yīng)量大,價(jià)格便宜,且新綠原酸、綠原酸和隱綠原酸分別為5-咖啡酰、3-咖啡酰和4-咖啡酰奎尼酸類物質(zhì),其結(jié)構(gòu)類似,紫外響應(yīng)接近,然而新綠原酸和隱綠原酸價(jià)格昂貴且供應(yīng)不足,因此考慮用一測(cè)多評(píng)法進(jìn)行測(cè)定。本實(shí)驗(yàn)以綠原酸為內(nèi)標(biāo)物,采用UPLC和HPLC兩種色譜系統(tǒng),建立脈絡(luò)寧注射液、雙黃連口服液和銀黃顆粒三種金銀花復(fù)方制劑中綠原酸與新綠原酸和隱綠原酸的相對(duì)校正因子,用校正因子計(jì)算新綠原酸和隱綠原酸的量,同時(shí)對(duì)一測(cè)多評(píng)的計(jì)算值與外標(biāo)法實(shí)測(cè)值進(jìn)行比較,評(píng)價(jià)一測(cè)多評(píng)法在金銀花復(fù)方制劑脈絡(luò)寧注射液、雙黃連口服液和銀黃顆粒中多指標(biāo)質(zhì)量控制中應(yīng)用的準(zhǔn)確性和可行性。
1 儀器與材料
1.1 儀器 Waters Acquity超高效液相色譜系統(tǒng),Empower工作站(美國(guó)Waters公司);Agilent 1100高效液相色譜系統(tǒng),Agilent chemstation工作站(美國(guó)Agilent公司)。Waters Acquity UPLC BEH C18色譜柱(2.1 mm×100 mm,1.7μm);Agilent Poroshell 120 EC-C18(3.0 mm×100 mm,2.7μm);Waters SunFire C18(4.6 mm× 250 mm,5μm),Agilent SB C18(4.6 mm× 250 mm,5μm)。MT5百萬分之一分析天平(瑞士Mettler Toledo公司)。Milli-Q超純水機(jī)(美國(guó)Millipore公司)。
1.2 材料 脈絡(luò)寧注射液(金陵藥業(yè)股份有限公司,批號(hào)20111209、20111213),雙黃連口服液(哈藥集團(tuán)三精制藥股份有限公司,批號(hào)10082627、11031624),銀黃顆粒(江西濟(jì)民可信藥業(yè)有限公司,批號(hào)111008、110503)。
1.3 試劑 綠原酸(批號(hào)110753-200413)購自中國(guó)藥品生物制品檢定所,新綠原酸和隱綠原酸購自成都普瑞科技開發(fā)有限公司,純度按HPLC面積歸一化法測(cè)定均≥98%。甲醇(色譜純,德國(guó)Merck公司),乙酸和磷酸(色譜純,美國(guó)Tedia公司)。其他試劑均為分析純。
2 方法與結(jié)果
2.1 方法學(xué)考察
2.1.1 色譜條件
2.1.1.1 HPLC色譜條件 Waters SunFire C18色譜柱(4.6 mm×250 mm,5μm)和Agilent SB C18色譜柱(4.6 mm×250 mm,5μm);流動(dòng)相為甲醇(A)-0.1%磷酸水(B),梯度洗脫(0~10 min,10% ~20%A;10~20 min,20% ~40%A;20~25 min,40% ~50%A);柱溫30℃;體積流量1 mL/min;檢測(cè)波長(zhǎng) 327 nm;進(jìn)樣量 10μL。見圖1。
2.1.1.2 UPLC色譜條件1 Waters Acquity UPLC BEH C18色譜柱(2.1 mm×100 mm,1.7μm),流動(dòng)相為甲醇(A) -0.1%乙酸水(B),梯度洗脫(0~2 min,8% ~16%A;2~8 min,16%A);柱溫28℃;體積流量0.3 mL/min;檢測(cè)波長(zhǎng)327 nm;進(jìn)樣量2μL。見圖2。
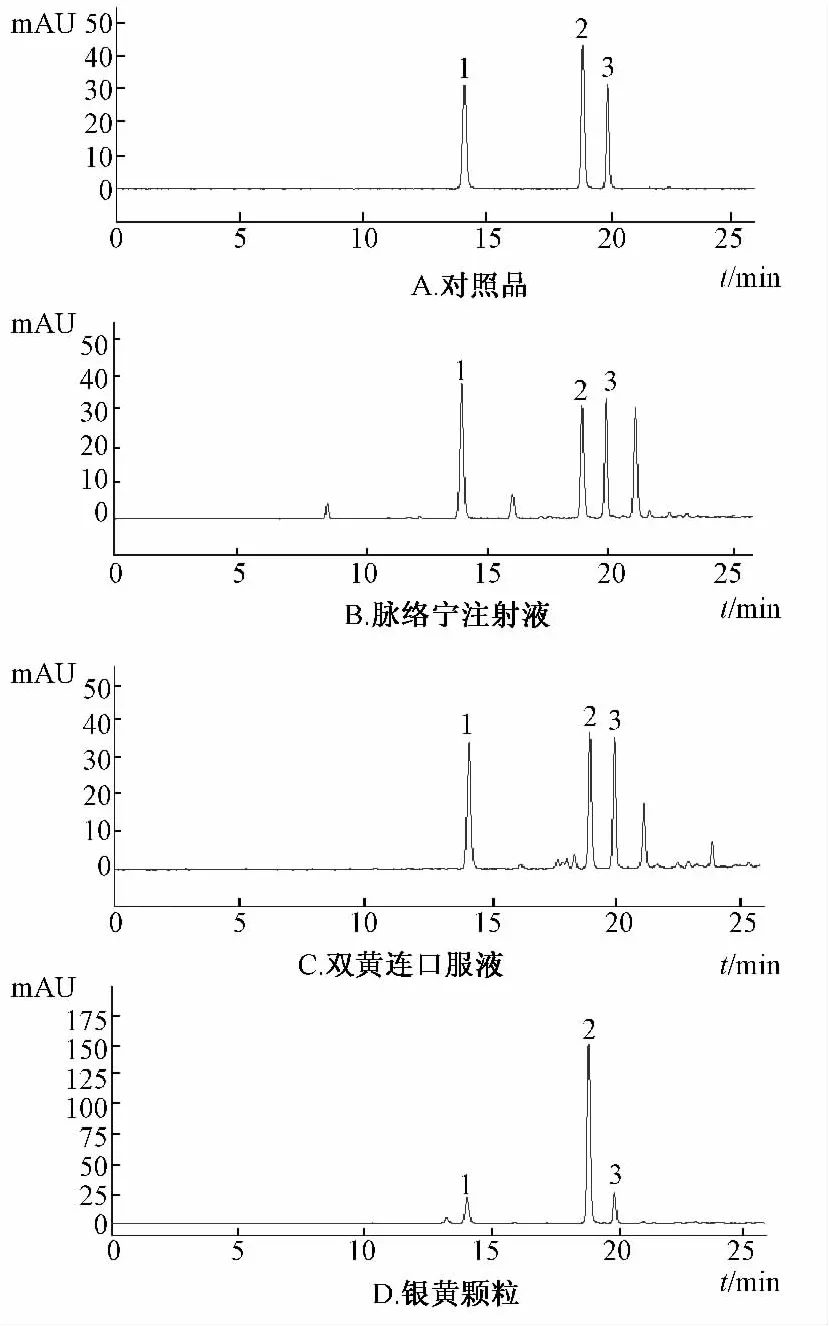
圖1 對(duì)照品和樣品的HPLC圖譜Fig.1 HPLC chromatograms of reference substances and samples
2.1.1.3 UPLC色譜條件2 Agilent Poroshell 120 EC-C18色譜柱(3.0 mm×100 mm,2.7μm),流動(dòng)相為甲醇(A) -0.1%乙酸水(B),梯度洗脫(0~2 min,8% ~16%A;2~10 min,16% ~25%A);柱溫28℃;體積流量0.3 mL/min,檢測(cè)波長(zhǎng)327 nm,進(jìn)樣量2μL。
2.1.2 對(duì)照品溶液的制備 精密稱取新綠原酸、綠原酸、隱綠原酸對(duì)照品適量,分別置25 mL棕色量瓶中,適量甲醇溶解后,以50%甲醇定容至刻度,其質(zhì)量濃度分別為 1018、1216和 808μg/mL。
2.1.3 供試品溶液的制備
2.1.3.1 脈絡(luò)寧注射液供試品溶液 精密移取0.5 mL脈絡(luò)寧注射液,置25 mL棕色量瓶中,以超純水定容至刻度,過0.22μm微孔濾膜,置棕色進(jìn)樣小瓶中,待用。
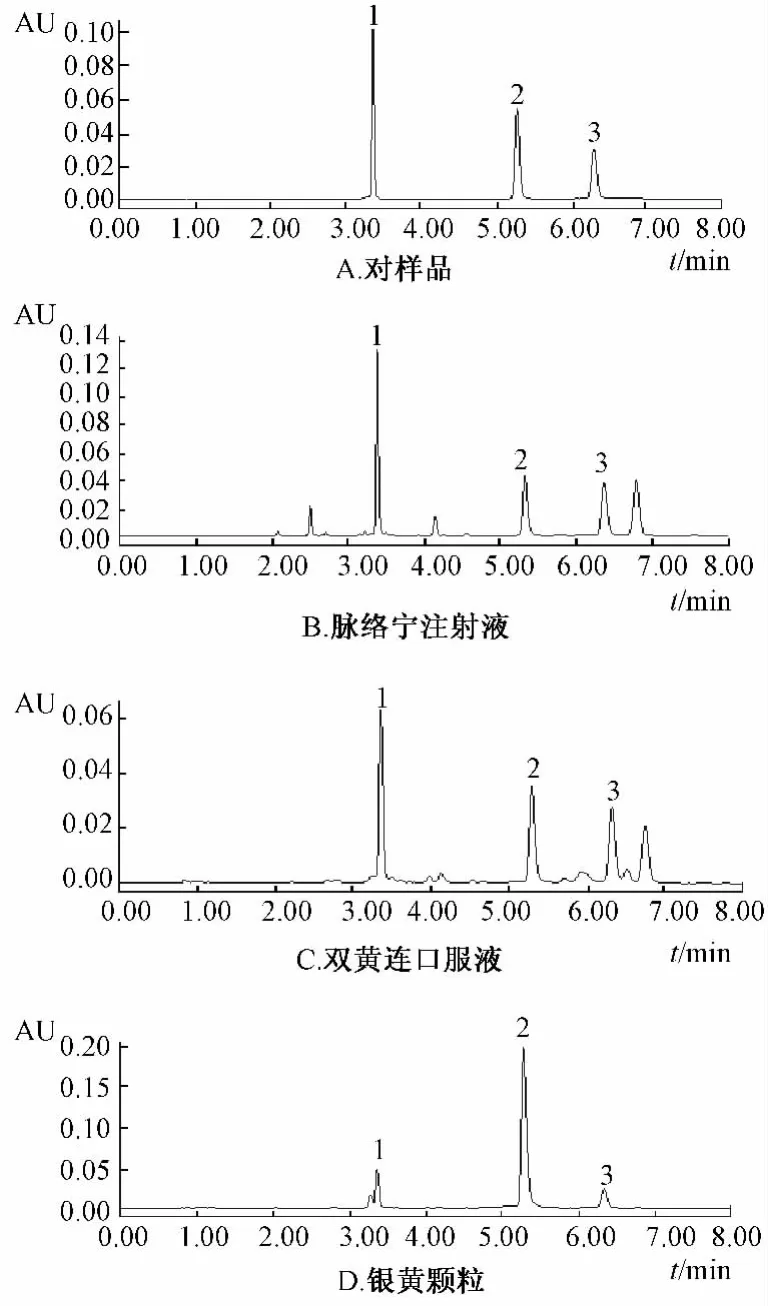
圖2 對(duì)照品和樣品的UPLC圖Fig.2 UPLC chromatograms of reference substances and samples
2.1.3.2 雙黃連口服液供試品溶液 精密移取0.5 mL雙黃連口服液,置25 mL棕色量瓶中,加入50%甲醇定容,稱定,超聲處理30 min,放至室溫,以50%甲醇補(bǔ)定失質(zhì)量,過0.22μm微孔濾膜,置棕色進(jìn)樣小瓶中,待用。
2.1.3.3 銀黃顆粒供試品溶液 稱取銀黃顆粒約0.1 g,置10 mL棕色量瓶中,加入50%甲醇定容,稱定,超聲處理30 min,放至室溫,以50%甲醇補(bǔ)定失質(zhì)量,過0.22μm微孔濾膜,置棕色進(jìn)樣小瓶中,待用。
2.1.4 線性關(guān)系、定量限(LOQ)及檢測(cè)限(LOD) 分別精密移取上述各對(duì)照品溶液2.0 mL,置10 mL棕色量瓶中,以50%甲醇定容,制得混合對(duì)照品溶液。取混合對(duì)照品溶液,以50%甲醇稀釋,稀釋倍數(shù)分別為2倍、10倍、20倍、40倍,得到系列對(duì)照品溶液,過0.22μm微孔濾膜后,置棕色進(jìn)樣小瓶中,依上述色譜條件進(jìn)樣,HPLC色譜柱為Waters SunFire C18(4.6 mm×250 mm,5μm),UPLC 色譜 柱為 Waters BEH C18(2.1 mm×100 mm,1.7μm),測(cè)定峰面積值,以峰面積值(Y)對(duì)質(zhì)量濃度(X)進(jìn)行線性回歸,得到新綠原酸、綠原酸和隱綠原酸的回歸方程、相關(guān)系數(shù)和線性范圍;將混合對(duì)照品以50%甲醇不斷稀釋后分析,分別得到3個(gè)成分的LOD(S/N≈3~4)和LOQ(S/N≈10~12),HPLC的結(jié)果見表1,UPLC的結(jié)果見表2。
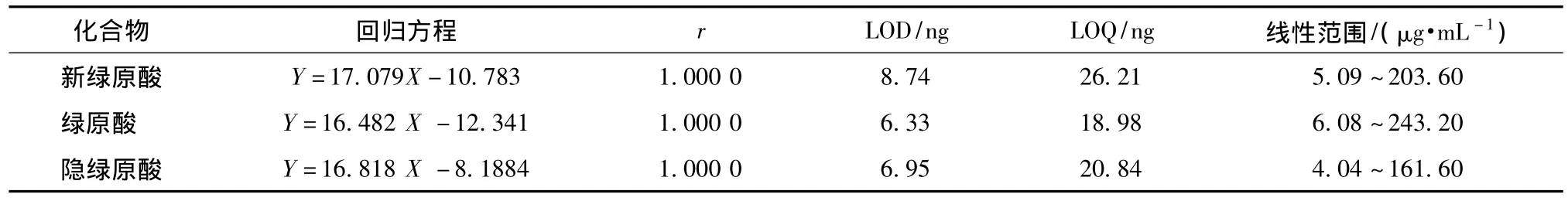
表1 新綠原酸、綠原酸和隱綠原酸的HPLC線性回歸方程及LOD、LOQ的測(cè)定結(jié)果Tab.1 Linear regression equation,LOD,and LOQ of 3 phenolic acids by HPLC
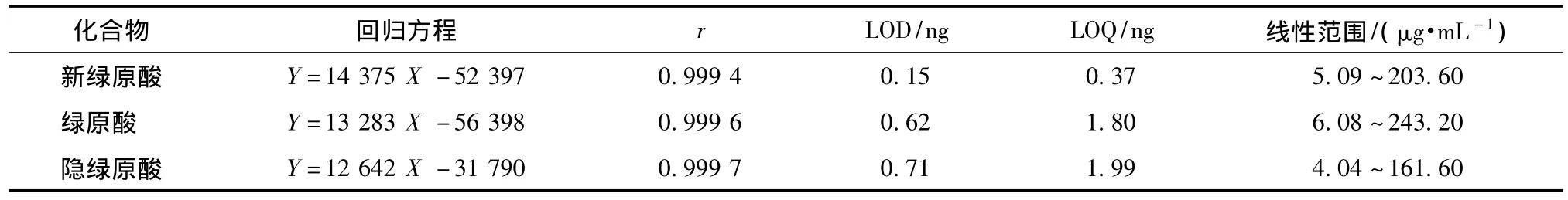
表2 新綠原酸、綠原酸和隱綠原酸的UPLC線性回歸方程及LOD、LOQ的測(cè)定結(jié)果Tab.2 Linear regression equation,LOD,and LOQ of 3 phenolic acids by UPLC
2.1.5 精密度試驗(yàn) 取中濃度混合對(duì)照品溶液,在上述色譜條件下連續(xù)進(jìn)樣6次,測(cè)定新綠原酸、綠原酸和隱綠原酸的峰面積值,計(jì)算峰面積的RSD,新綠原酸、綠原酸和隱綠原酸在HPLC儀器上峰面積RSD分別為0.86%、1.52%、1.23%,在UPLC儀器上峰面積RSD分別為1.13%、1.35%、1.22%,表明兩種儀器精密度良好。
2.1.6 穩(wěn)定性試驗(yàn) 取脈絡(luò)寧供試品溶液(批號(hào)20111209),0.22μm微孔濾膜過濾后,置棕色進(jìn)樣小瓶中,分別于0、2、4、8、12、24 h進(jìn)HPLC分析,測(cè)定各成分的峰面積值,計(jì)算,新綠原酸、綠原酸和隱綠原酸的RSD分別為0.78%、1.15%、0.94%,表明樣品溶液在24 h內(nèi)穩(wěn)定。
2.1.7 重復(fù)性試驗(yàn) 分別取脈絡(luò)寧注射液(批號(hào)20111209)、雙黃連口服液(批號(hào)10082627)和銀黃顆粒(批號(hào)111008)6份,按2.1.3項(xiàng)下制備供試品溶液,以UPLC和HPLC測(cè)定各成分的峰面積值,計(jì)算,結(jié)果見表3。
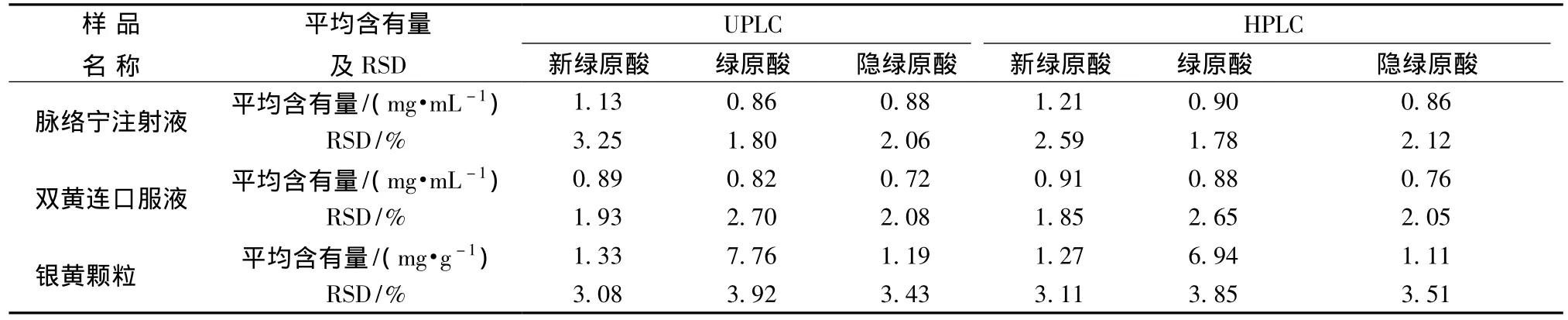
表3 重復(fù)性數(shù)據(jù)Tab.3 Reproducibility of the three components
2.1.8 加樣回收率試驗(yàn) 分別制備脈絡(luò)寧注射液(批號(hào)20111209)、雙黃連口服液(批號(hào)10082627)和銀黃顆粒(批號(hào)111008)各6份,分別精密加入相當(dāng)于樣品含有量的新綠原酸、綠原酸和隱綠原酸對(duì)照品溶液,按2.1.3項(xiàng)下制備供試品溶液,以UPLC測(cè)定各成分峰面積值,計(jì)算結(jié)果見表4。
2.2 校正因子的重現(xiàn)性考察 取系列混和對(duì)照品溶液,混合對(duì)照品溶液為1號(hào),稀釋倍數(shù)為2倍、10倍、20倍、40倍的分別為2號(hào)、3號(hào)、4號(hào)和5號(hào),本實(shí)驗(yàn)在UPLC上考察Waters Acquity UPLC BEH C18(2.1 mm×100 mm,1.7μm)和Agilent Poroshell 120 EC-C18(3.0 mm×100 mm,2.7μm)兩種色譜柱,在HPLC上考察Waters SunFire C18(4.6 mm×250 mm,5μm)和 Agilent SB C18(4.6 mm×250 mm,5μm)兩種色譜柱。所得的相對(duì)校正因子及其相對(duì)標(biāo)準(zhǔn)差見表5,由表可知,不同的儀器及不同型號(hào)色譜柱所得的相對(duì)校正因子差異并不顯著。
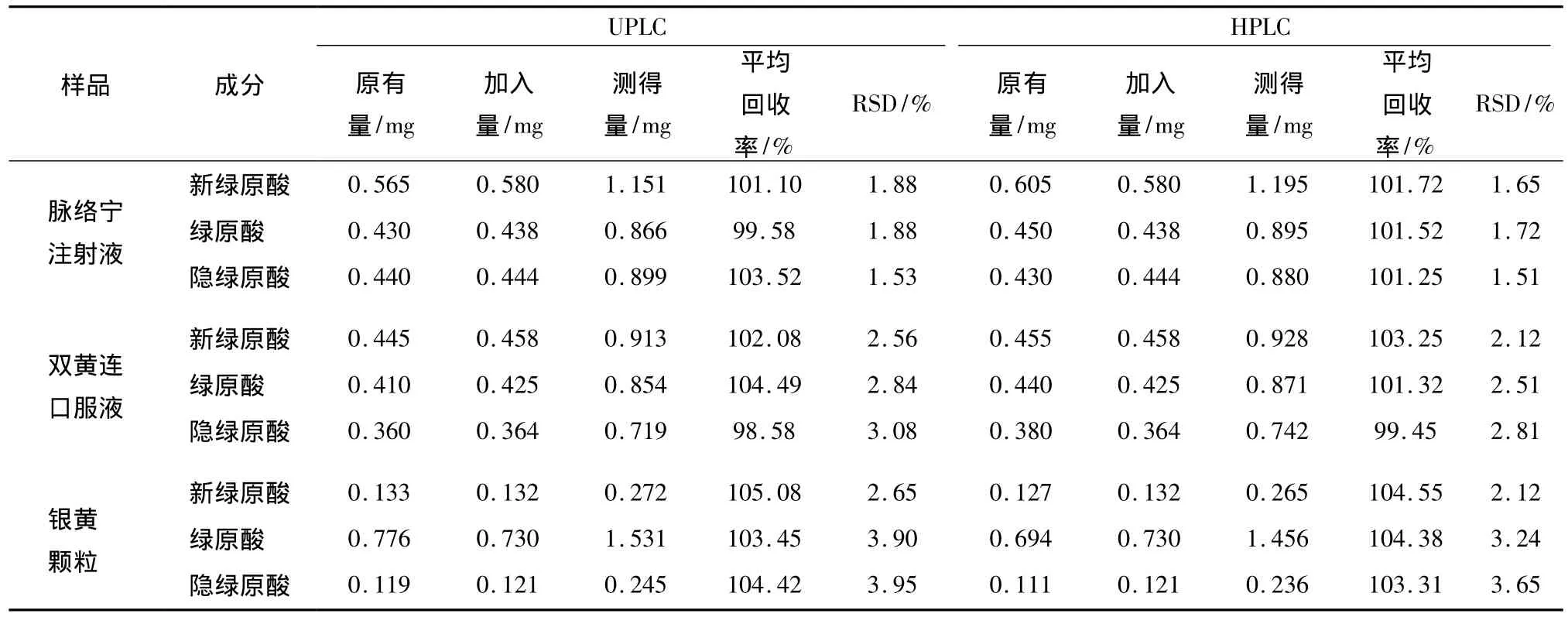
表4 回收率數(shù)據(jù)Tab.4 Recovery tests of the three components
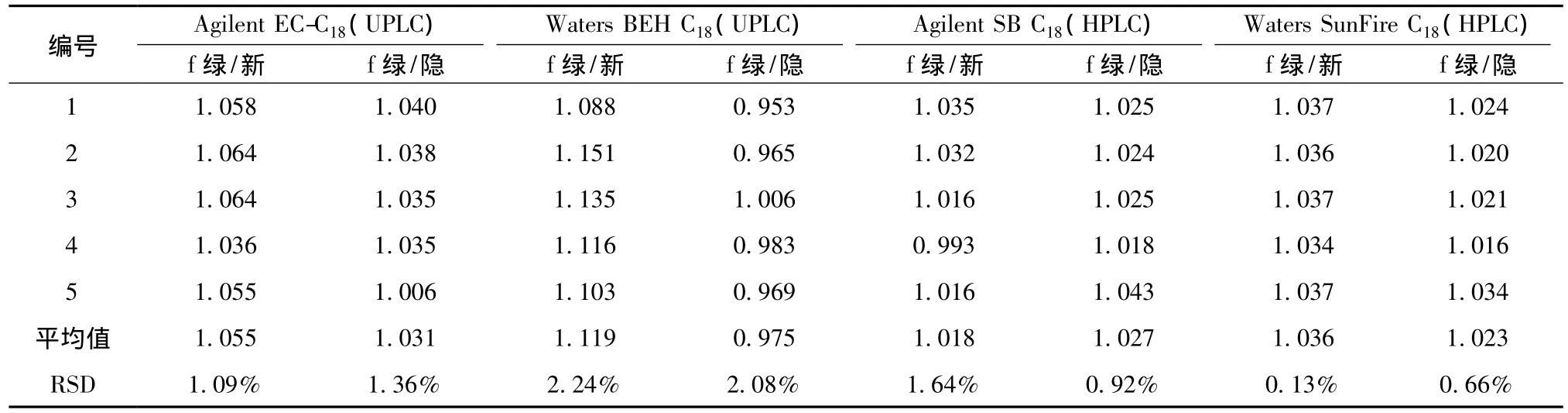
表5 測(cè)得相對(duì)校正因子Tab.5 RCFs of phenolic acid
2.3 一測(cè)多評(píng)法與常規(guī)外標(biāo)法比較 分別取脈絡(luò)寧注射液,雙黃連口服液和銀黃顆粒,按2.1.3項(xiàng)下制備供試品溶液,以UPLC和HPLC及以上4種不同品牌和型號(hào)的色譜柱測(cè)定,并用外標(biāo)法及一測(cè)多評(píng)法分別計(jì)算新綠原酸及隱綠原酸量,將兩種方法的計(jì)算結(jié)果進(jìn)行比較,以驗(yàn)證QAMS法用于復(fù)方金銀花制劑中新綠原酸、綠原酸和隱綠原酸質(zhì)量評(píng)價(jià)的準(zhǔn)確性,見表6。結(jié)果表明,常規(guī)的外標(biāo)法實(shí)測(cè)含量值與一測(cè)多評(píng)計(jì)算的含量值經(jīng)t檢驗(yàn)比較,P>0.05,表明兩種方法測(cè)得量沒有顯著性差異,證明所建立的一測(cè)多評(píng)法具有較好的可信度。
3 討論
3.1 關(guān)于流動(dòng)相的考察,在UPLC中,流動(dòng)相水相中加入0.1%的乙酸即可改善峰型,3種成分達(dá)基線分離;在HPLC中,流動(dòng)相水相中加入0.1%的乙酸時(shí),三種成分未達(dá)到基線分離,加入0.1%的磷酸,分離效果明顯改善,峰型較好,所以,在UPLC和HPLC中,流動(dòng)相水相中分別加入0.1%的乙酸和0.1%的磷酸。
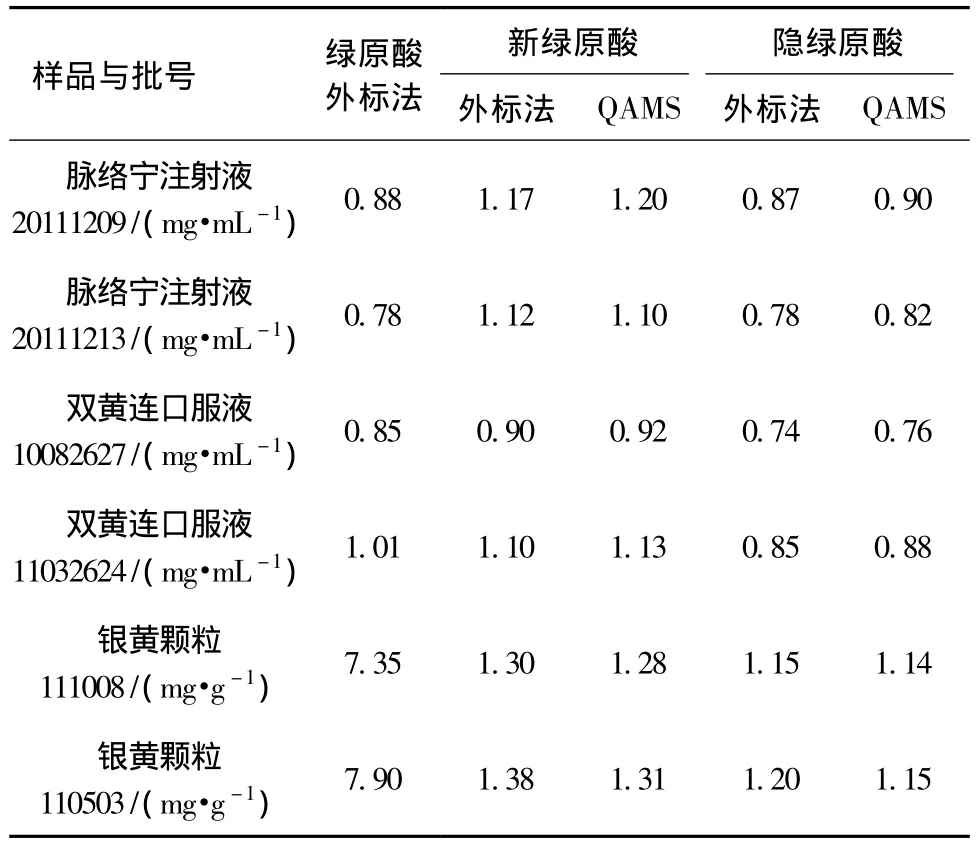
表6 外標(biāo)法和一測(cè)多評(píng)法測(cè)得復(fù)方金銀花制劑中新綠原酸、隱綠原酸含量Tab.6 Contents of components by external standard method and QAMS
3.2 金銀花藥材中,綠原酸的含有量較高,《中國(guó)藥典》規(guī)定綠原酸為其指標(biāo)性成分,而新綠原酸和隱綠原酸含有量較低[13-14]。而在金銀花的復(fù)方制劑脈絡(luò)寧注射液、雙黃連口服液和銀黃顆粒中新綠原酸、綠原酸和隱綠原酸量均較高,以此三種制劑為例,探討一測(cè)多評(píng)法在金銀花復(fù)方制劑質(zhì)量控制中的可行性和技術(shù)適應(yīng)性,證明了一測(cè)多評(píng)可用于多種金銀花復(fù)方制劑中,同時(shí)也避免了由于某一成分含有量較低而引起系統(tǒng)誤差,在建立的相對(duì)校正因子評(píng)價(jià)中,考察了Agilent1100 HPLC,Waters UPLC 2臺(tái)液相色譜系統(tǒng)和4根不同品牌、型號(hào)的色譜柱,對(duì)綠原酸與新綠原酸和隱綠原酸之間相對(duì)校正因子的重現(xiàn)性進(jìn)行考察,結(jié)果表明相對(duì)校正因子具有良好的重現(xiàn)性,一測(cè)多評(píng)法測(cè)定結(jié)果與傳統(tǒng)外標(biāo)法測(cè)定結(jié)果無顯著性差異,說明一測(cè)多評(píng)可以同時(shí)測(cè)定復(fù)方金銀花制劑脈絡(luò)寧注射液、雙黃連口服液和銀黃顆粒中新綠原酸、綠原酸和隱綠原酸的量。
3.3 《中國(guó)藥典》2010年版二部附錄XIXF藥品雜質(zhì)分析指導(dǎo)原則中規(guī)定,已知雜質(zhì)對(duì)主成分的相對(duì)校正因子在0.9~1.1范圍內(nèi),可以用主成分的自身對(duì)照法計(jì)算含有量,即用主成分作為對(duì)照品計(jì)算雜質(zhì)的量。在本實(shí)驗(yàn)中綠原酸對(duì)新綠原酸和隱綠原酸的平均校正因子分別為1.057和1.014,符合藥典要求,且黃連中小檗堿與巴馬汀、黃連堿、表小檗堿、藥根堿的相對(duì)校正因子在0.9~1.1之間[15],藥典中規(guī)定可以用小檗堿作為對(duì)照品計(jì)算其他4種生物堿的量[1]。酚酸是自然界中的一類重要化學(xué)成分,其中新綠原酸、綠原酸和隱綠原酸在很多中藥中同時(shí)存在,可以用綠原酸作為對(duì)照品計(jì)算新綠原酸和隱綠原酸的量,以節(jié)約成本。
3.4 在脈絡(luò)寧注射液和雙黃連口服液中,咖啡酸的含有量也較高,且其結(jié)構(gòu)與新綠原酸和隱綠原酸結(jié)構(gòu)相似。本實(shí)驗(yàn)前期研究中,以咖啡酸為內(nèi)參物時(shí),其對(duì)新綠原酸和隱綠原酸的相對(duì)校正因子4個(gè)柱子差別較大,推測(cè)可能是咖啡酸穩(wěn)定性較差,導(dǎo)致計(jì)算新綠原酸和隱綠原酸量與實(shí)測(cè)結(jié)果誤差大于5%。因此,本實(shí)驗(yàn)僅選擇綠原酸為內(nèi)參物,放棄以咖啡酸作為內(nèi)參物。
[1]國(guó)家藥典委員會(huì).中華人民共和國(guó)藥典:2010年版一部[S].北京:中國(guó)醫(yī)藥科技出版社,2010:285.
[2]馮偉紅,王智民,張啟偉,等.一測(cè)多評(píng)法測(cè)定秦皮藥材與飲片中香豆素類成分的含量[J].中國(guó)中藥雜志,2011,36(13):1782-1789.
[3]孔晶晶,朱晶晶,王智民,等.一測(cè)多評(píng)法測(cè)定連翹中多種不同類型成分的含量[J].中國(guó)藥學(xué)雜志,2010,45(17):1301-1304.
[4]王 瑞,黃山君,王崢濤.一測(cè)多評(píng)法測(cè)定赤芍中不同類型成分的含量[J].沈陽藥科大學(xué)學(xué)報(bào),2011,28(8):594-598.
[5]孔晶晶,朱晶晶,王智民,等.一測(cè)多評(píng)技術(shù)在中成藥香連制劑質(zhì)量評(píng)價(jià)中的應(yīng)用[J].中國(guó)中藥雜志,2011,36(11):1445-1448.
[6]單鳴秋,高 靜,丁安偉.超高效液相色譜法測(cè)定側(cè)柏炭中5個(gè)黃酮類成分[J].中草藥,2011,42(2)282-284.
[7]楊 柳,蘇芝軍,許舜軍,等.UPLC法同時(shí)測(cè)定蒼耳子中4種酚酸類成分的含量[J].藥學(xué)學(xué)報(bào),2010,45(12):1537-1540.
[8]王愛民,遲明艷,王永林,等.UPLC同時(shí)測(cè)定葒草藥材中8種指標(biāo)成分的含量[J].中國(guó)中藥雜志,2010,35(13):1723-1727.
[9]湯芳玲,蔡光明,袁 波,等.UPLC測(cè)定不同產(chǎn)地、不同部位小葉黑柴胡中黃酮含量[J].中國(guó)中藥雜志,2010,35(21):2874-2876.
[10]徐福平,林愛華,劉奕明,等.UPLC同時(shí)測(cè)定黃柏知母藥對(duì)中鹽酸小檗堿、新芒果苷、芒果苷的含量[J].中國(guó)藥學(xué)雜志,2010,45(24):1951-1953.
[11]何 迅,遲明艷,李勇軍,等.UPLC法測(cè)定蓮菊感冒膠囊中3種成分的含量[J].中國(guó)新藥雜志,2011,20(1):79-82.
[12]楊海英,曾 程,杜 剛.UPLC法測(cè)定旱蓮草中木犀草素和芹菜素的含量[J].中藥材,2010,33(18):1275-1276.
[13]陳永紅.金銀花指紋圖譜研究[D].吉林:吉林大學(xué),2007.
[14]張會(huì)敏.金銀花質(zhì)量控制關(guān)鍵技術(shù)與質(zhì)量評(píng)價(jià)體系的研究[D].濟(jì)南:山東中醫(yī)藥大學(xué),2008.
[15]匡艷輝,朱晶晶,王智民,等.一測(cè)多評(píng)法測(cè)定黃連中小檗堿、巴馬汀、黃連堿、表小檗堿、藥根堿含量[J].中國(guó)藥學(xué)雜志,2009,44(5):390-394.

