放射免疫治療中單克隆抗體藥物研究現狀
潘俊男, 程作用
(1.成都云克藥業有限責任公司,四川 成都 610041;2.成都放射性藥物工程技術研究中心,四川 成都 610041)
放射免疫治療(radioimmuntherapy,RIT)是將放射性核素與腫瘤特異或相關的單克隆抗體(McAb)相連接,形成抗腫瘤免疫耦聯物治療腫瘤的一種方法。目前對惡性腫瘤的治療仍以傳統的放射性療法和化學療法為主,但放療和化療并不能徹底治愈惡性腫瘤以及延長患者的有效生存時間和降低其死亡率,而基于單抗的靶向治療以及利用核素標記單抗的RIT卻顯示出巨大的潛力和應用前景。早在1991年,Magerstadt[1]就指出,作為腫瘤導向治療藥物,單抗耦聯核素是單抗免疫耦聯物中最有希望的一種。2003年,Press[2]再一次指出,當前低度非霍奇金淋巴瘤(non-Hodgkin’s lymphona,NHL)治療最有希望的藥物之一是核素標記的抗體[2]。
靶向治療用單抗主要有兩種作用方式。1)直接作用:通過抗體依賴性細胞毒(ADCC)和補體依賴性細胞毒(CDC)的細胞溶解效應殺傷腫瘤細胞。2)間接作用:單抗作為靶向載體,將化療藥物、毒素、核素等細胞毒藥物與單抗耦聯。RIT的作用機理主要是間接作用。利用針對腫瘤相關特異性抗體作為核素載體,標記核素后注入體內與腫瘤細胞相應抗原特異性結合,使腫瘤組織內濃聚大量的核素,通過射線的電離輻射作用破壞或干擾腫瘤細胞的結構及功能,起到抑制、殺傷或殺死腫瘤細胞的作用。
1 用于RIT的核素
用于RIT核素應具備的條件包括:1)適中的半衰期、能量和組織射程;2)標記方法簡單易行;3)標記后不影響McAb的免疫活性,且單位McAb 攜帶核素的量足夠大;4)價格便宜[3]。滿足這些條件的核素有多種,例如131I、188Re、90Y、177Lu、213Bi、211At、225Ac、125I和111In等,按發射射線種類不同可分為:1)發射β射線的核素;2)發射α射線的核素;3)發射俄歇電子(EC)的核素(表1)[4]。
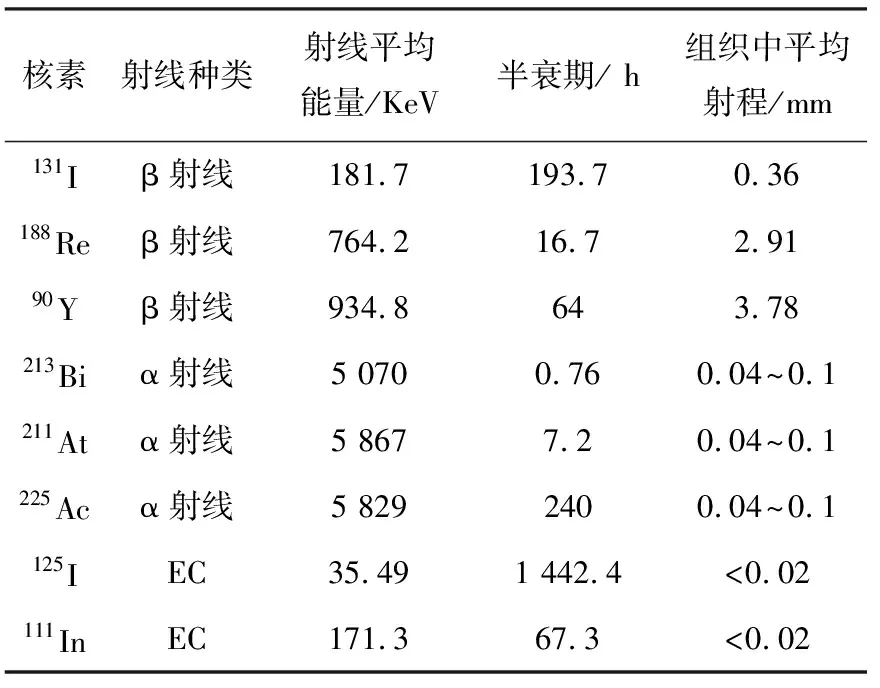
表1 用于RIT的核素性質
2 用于RIT的單抗
目前用于RIT的單抗都是用來治療腫瘤疾病的,根據靶點不同可以分為:抗CD20單抗、抗CD22單抗、抗CD33單抗、抗表皮生長因子受體2 (human epidermal growth factor receptor-2,HER2)單抗等,其中前三種主要用來治療血液循環系統惡性腫瘤,抗HER2單抗主要用于治療乳腺癌。
2.1 抗CD20單抗
CD20表達于除漿細胞外發育分化各階段的B細胞表面,通過調節跨膜鈣離子流動直接對B細胞的增殖和分化起調節作用[5]。Roche公司研發的以CD20為靶點的利妥昔單抗(Rituximab)是FDA批準的第一個治療淋巴癌的人鼠嵌合單抗,自1997年在美國獲準上市以來一直位列全球暢銷藥前列,其2010年的全球銷售額更是達62億美元。近十年來,抗CD20的單抗藥物開發方興未艾。GLaxoSmithKline與Genmab聯合開發的抗CD20單抗ofatumumab于2009年上市,臨床試驗數據顯示,對于復發性/難治性B細胞型慢性淋巴細胞性白血病患者,其臨床有效率達63%[6]。2010年8月,LFB Biotechnologies開發的重組抗CD20單抗(LFB-R603)被FDA授予罕用藥資格,用于治療慢性淋巴細胞性白血病[5]。另外,由Genentech、GlycArt 和Roche聯合開發的人源化抗CD20單抗RG7159(GA101)已進入III期臨床試驗,并有望用于治療與B細胞相關的癌癥,如非霍奇金淋巴瘤和慢性淋巴細胞性白血病等[5]。
2.2 抗CD22單抗
抗原CD22 是一種跨膜唾液酸糖蛋白,僅表達于分化成熟期B細胞表面,對B細胞的生長、存活和功能起重要作用。CD22在99%的NHL細胞中均有表達,而B細胞在自身免疫性疾病的發病機制中也發揮重要作用[7]。Epratuzumab ( IMMU-103,AMG-412,IMMUhLL2,LymphoC ideTM )是人源化抗CD22單抗,可通過與CD22結合而抑制B細胞產生抗自身蛋白抗體。它最初由Immunomedics公司開發用于治療SLE(進入III期臨床試驗) 以及Waldenstrem巨球蛋白血癥、Sjegren綜合征和CD22陽性小兒急性淋巴細胞白血病(進入I/II期臨床試驗),其用于NHL的II期臨床研究也已獲得陽性結果[7]。
2.3 抗CD33單抗
抗原CD33高度表達于90%急性骨髓系白血病(AML)患者的髓系白血病細胞表面,可能是AML特異性治療的理想靶點[8]。吉妥珠單抗(mylotarg,gemtuzumab)為人源化的CD33單抗與卡奇霉素的免疫連接物。2000年5月吉妥珠單抗被FDA批準作為治療年齡大于60歲、首次復發的AML患者。但臨床應用中未發現吉妥珠單抗在療效上有改善,而且使用吉妥珠單抗患者的死亡數要高于只接受化療的患者[9]。使用吉妥珠單抗的患者患肝小靜脈閉塞病的幾率要高于FDA批準該藥時的數據,這是一種嚴重的肝臟疾病,有致命危險[10],因此本產品已經于2010年退市。
2.4 抗HER2單抗
HER2為相對分子質量185 000的跨膜受體樣蛋白,具有酪氨酸激酶活性[11]。目前已有針對該基因過度表達的單抗藥物—赫賽汀(Herceptin)。赫賽汀是重組DNA人源化的單抗,其作用靶點是HER2基因調控的細胞表面P185糖蛋白,可與HER2受體細胞外近膜區結合,阻止細胞內酪氨酸激酶的活化。Viloria等[12]對過度表達HER2乳癌動物模型的研究表明,赫賽汀可通過調節促血管生成和抗血管生成因子誘導血管結構正常化和復原來抑制血管生成。2011年美國臨床腫瘤學會年會(ASCO)上,Chang等[13]報告了關于拉帕替尼聯合赫賽汀(不聯合化療)治療HER2 過度表達乳腺癌的Ⅱ期臨床試驗結果,在無化療藥物情況下,也可顯著改善患者病情。全組64例HER2 陽性乳腺癌患者總有效率為75%,完全緩解率和部分緩解率分別為31%和44% 。2012年ASCO會議上,美國杜克癌癥研究所的Kimberly L博士報告的抗體-藥物共軛新藥T-DM1III期隨機試驗結果表明,T-DM1用于進展期HER2陽性乳腺癌比標準治療更有效,毒性也更小[14]。其中T-DM1是赫賽汀和化療藥物DM1的抗體耦聯藥。2010年10月Roche制藥宣布,赫賽汀繼成功用于HER2陽性乳腺癌治療后,繼續在胃癌治療領域實現重大突破。2012年8月,赫賽汀聯合化療正式被中國食品藥品監督管理局(SFDA)批準用于HER2陽性轉移性胃癌的一線治療[15]。這意味著我國胃癌治療進入了分子靶向時代。
3 RIT藥物
目前RIT藥物主要用于血液循環系統惡性腫瘤治療,其次應用于乳腺癌、肺癌、肝癌、腦癌、甲狀腺癌及卵巢癌等其他實體惡性腫瘤的治療。
3.1 血液循環系統惡性腫瘤RIT藥物
惡性腫瘤細胞對放射線具有較高的敏感性,而血液循環系統惡性腫瘤靶癌細胞又主要位于血液、骨髓及淋巴結內,核素標記抗體容易到達這些位置,故療效好。Zevalin(90Y-ibritumomab)和Bexxer(131I-tositumomab)是分別由Spectrum Pharms和GSK公司開發的放射免疫耦聯物,分別于2002年和2003年上市。相比于利妥昔單抗(美羅華),Zevalin和Bexxer在治療低級別、形態改變的和侵襲性的NHL有更好的療效并用于化療或美羅華治療后復發和難治性低級別濾泡或轉化的B細胞NHL[16]。難治性患者或者抵抗化療和利妥昔單抗的患者,在Zevalin和Bexxer治療后獲得長期緩解。Zevalin的主要不良反應為可逆性的骨髓抑制。由于131I半衰期較長,Bexxar 的骨髓抑制更加明顯,同時因為131I還發射γ射線,接受Bexxar治療的患者必須隔離。此外,由Bayer Schering Pharma公司進行的Zevalin治療彌漫性大B細胞淋巴瘤已經進入III期臨床實驗(表2)[17]。Sharkey 等[18]研究了DOTA螯合的111In和90Y-epratuzumab在NHL患者體內的生物分布和腫瘤靶向性、藥物代謝動力學、劑量和抗抗體反應,結果表明,治療效果與血液中的放射性劑量和外顯影所見的腫瘤靶向性和尺寸無關。Linde等[19]研究了應用90Y-DOTA-epratuzmab進行逐步RIT,發現該療法一方面可以減少病人服用的藥物劑量、血液毒性,另一方面可以增加核素使用量,結果提示,90Y-DOTA-epratuzmab是一個非常有希望的NHL治療藥物。因CD33表達于80% ~ 90%血液細胞,而在造血干細胞和非造血細胞中不表達,所以是白血病治療的理想靶點。131I、90Y 和213Bi標記抗CD33單抗( HuM195)耦聯物均處于I、II期臨床試驗階段。90Y-HuM 195的I期臨床試驗結果表明,其可用于自體干細胞移植及非清髓性異基因干細胞移植預處理。Actinium Pharmaceuticals開發的225Ac-HuM195和213Bi-HuM195分別于2009年進入臨床I期和II期研究[17],由于213Bi產生α射線射程很短,殺滅的腫瘤細胞數量有限,213Bi-HuM195對難治復發的AML療效不明顯,更適合于低負荷AML 治療及殘留病灶的清除。Jurcie等[20]用213Bi-HuM195治療18例難治復發的AML及CML患者,雖然67.7%的患者獲得部分緩解(PR),但存在一定的安全性問題,已終止研究。目前在研的核素標記單抗藥物中,60%的適應癥是血液循環系統惡性腫瘤,均已進入II期臨床試驗(表2)[17],可以預見未來核素標記單抗藥物將在血液循環系統惡性腫瘤的治療中發揮重要作用。
3.2 乳腺癌RIT藥物
赫賽汀是RIT 良好的核素載體。采用Iodogen 法對Herceptin進行131I 標記的標記率高,所制備的131I-Herceptin 的放化純度能達到RIT 的要求(放化純度可達95%),比活度適中,既保證了足夠的放射性活度,又避免了過高的活度對單抗的輻射損傷。Herceptin經131I標記后,其細胞結合能力仍然很高,與HER2高表達的腫瘤細胞特異性結合能力強。楊志學[21]對荷人乳癌裸鼠模型的研究證實,131I-Herceptin對HER2高表達的乳癌組織具有很高的靶向性,能明顯抑制荷人乳癌裸鼠模型腫瘤的生長。188Re和90Y對Herceptin的標記較131I 復雜,可采用直接與間接兩種方法。間接連接又有多種耦聯劑可供選擇,其中最常用的為DTPA,尚無統一的最佳標記方式。在一些研究中[22-23]90Y-Herceptin和188Re-Herceptin的放化純度及標記后單抗的免疫活性也均達到了RIT的要求,90Y-Herceptin和188Re-Herceptin均可顯著抑制HER2過表達腫瘤的生長。體外或動物實驗已證實[24],一些發射α射線的核素,如225Ac、211At、213Bi 等標記的Herceptin具有抑制HER2 過表達乳癌生長作用。然而,由于其組織穿透力弱,細胞對單抗-核素耦聯物的內化及細胞核的大小對其RIT效果影響較大。標記時耦聯劑的選擇仍存在問題,而且發射α射線核素的來源不如發射β射線的方便,具有復雜的子核素等問題,使α核素的應用受到限制。
單抗-核素耦聯物在靶細胞是否內化直接影響核素保留時間,進而影響療效。2007年,Danny等[25]用111In標記核定位序列(NLS)修飾的Herceptin單抗,其中NLS為蛋白質的一個結構域,通常為短氨基酸序列,能與單抗相互作用,使單抗轉運進細胞核,從而實現單抗的細胞內化。Danny等的研究結果表明,111In-NLS-Herceptin的標記解離常數比111In-Herceptin的降低了3倍,證明其具有更好的標記穩定性。進一步的細胞實驗表明,111In-NLS-Herceptin的內化率是111In-Herceptin的8倍,其對腫瘤細胞的殺傷力提高了2~5倍。由此可見111In-NLS-Herceptin具有強的殺傷力和靶向性,為未來開發核素標記單抗提供了一種新思路。
3.3 其他實體惡性腫瘤的RIT藥物
唯美生(131I-chTNT)經SFDA批準用于放化療失敗的晚期肺癌治療。TNT抗體僅鎖定實體瘤的變性壞死組織,唯美生與腫瘤細胞核抗原結合,131I殺傷壞死區邊緣的腫瘤活細胞,造成新的壞死,接著唯美生擴展到新的壞死區,周而復始地使腫瘤壞死區不斷擴大,由內向外摧毀腫瘤,達到治療目的。臨床治療表明,唯美生的治療總有效率為35%,相比其他藥物治療的有效率10%有了大幅度提高[26]。
由華神生物和第四軍醫大學聯合研制的利卡汀(131I-美妥昔單抗注射液)用于靶向治療肝癌。美妥昔單抗HAb18可與分布在肝癌細胞膜蛋白中的HAb18G抗原結合,將其荷載的核素131I載帶到腫瘤部位,從而產生抗腫瘤作用。采用選擇性插管給藥或在靶血管中埋泵給藥也獲得了較滿意的結果,64.5%的患者有部分緩解,患者的生存質量和生存期都得到了明顯改善[27]。
腦膠質瘤的手術后容易復發,且惡性程度高。Zalutsky等[28]報道了用211At標記嵌合的81C6單抗,18名惡性腦腫瘤患者腔內注射劑量不等(74 MBq~370 MBq)的211At-chMab,平均96.7%ID/g停留在局部,血中的藥物劑量占注射劑量小于0.26%,未見毒性反應,18例病人平均生存期56.5周,優于傳統的治療方法(25~30周)。Paganelli等[29]報道了采用90Y-DOTA-生物素三步預定位法治療19例確診且腱生蛋白染色陽性的Ⅲ~Ⅳ級惡性神經膠質瘤的病例,使用的90Y劑量達1.48 GBq/m2~2.96 GBq/m2時未見急性毒副作用,腫瘤平均劑量為(1 520±870) cGy,肝、腎、腦和骨髓吸收劑量分別為(150±100) cGy。
采用131I 高效碘標記法標記自制的抗胃癌鼠單抗(MG7),標記率約90%,在胃鏡下局部多點注射給藥,靶與非靶放射性攝取比平均2.4~11.2,標記抗體在瘤內滯留8 d~17 d,而用同法注射游離131I 的靶與非靶放射性攝取比為1.3,僅在瘤內滯留2 d~5 d[30]。可見單抗可以明顯增加標記核素在靶器官的攝取比和滯留時間。
RP215單抗具有抗OC-3-VGH卵巢癌細胞的作用。Gregory等[31]進行了裸鼠實驗,發現經過注射未標記的RP215(劑量:10 mg/kg),15 d后裸鼠卵巢腫瘤(OC-3-VGH卵巢癌細胞)的大小與對照組相比減少了50%。而將RP215用131I標記后再進行同樣的實驗,發現在相同劑量(劑量:10 mg/kg;活度:12.5 μCi/mg)相同時間內,其腫瘤減小為對照組的約70%,可見用放射性核素標記能進一步增強單抗抑制腫瘤的作用。
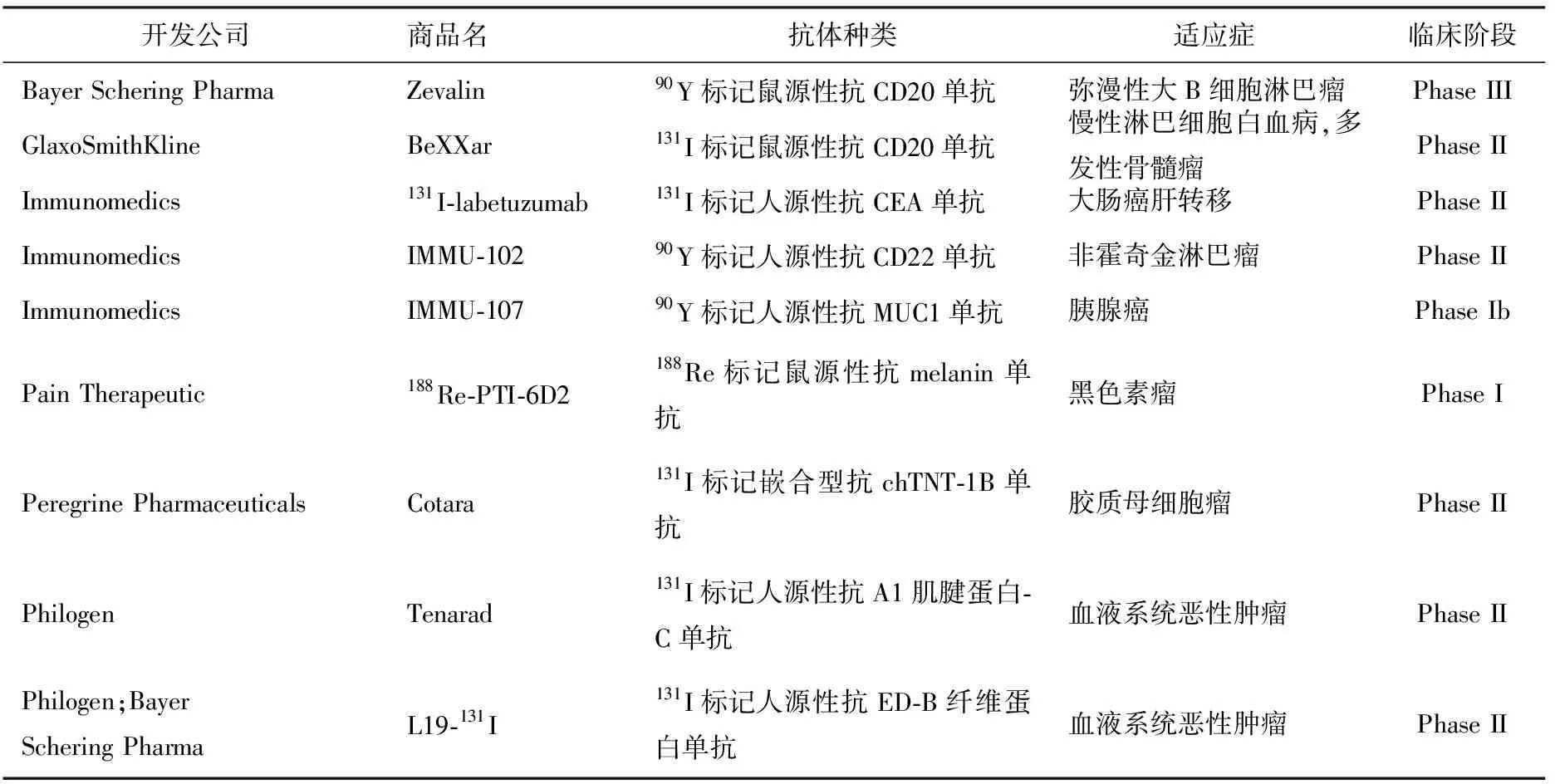
表2 國外在研的主要RIT藥物
4 結束語
綜上所述,目前RIT在腫瘤治療方面取得了顯著進展,但主要應用于血液循環系統腫瘤的治療,而對實體瘤的治療并未廣泛應用,主要原因是抗體對實體瘤的靶向性不強,往往腫瘤對抗體的實際攝取率低于0.05%。這使PIT應用于實體瘤治療時難度較大。科學家已經采取多項技術來達到增加抗體靶向性的目的,如抗體的細胞內化、靶抗原的上調、生物素-親和素預定位技術及增加腫瘤細胞血流和通透性等技術。另外,鼠源性抗體的應用會產生HAMA反應,因此RIT藥物開發的目標之一是制備出符合RIT治療用的人源性抗體,降低免疫原性,減少或消除HAMA反應。相信通過基因技術等進一步發展必將促進RIT進入更廣泛的臨床應用。
參考文獻:
[1]Magerstadt M. Antibody Conjugates and Malignant Disease[M].CRC Press: Boca Raton, 1991: 42-45.
[2]Press OW. Radioimmunotherapy for non-Hodgkin's lymphomas: A historical perspective[J].Seminars in Oncology, 2003, 30(2): 10-21.
[3]張迎,袁勝利. 曲妥珠單抗在乳癌放射免疫治療的研究進展[J]. 齊魯醫學雜志, 2011 , 26(4):372-376.
Zhang Ying, Yuan Shengli. Research progress of trastuzumab in breast cancer radioimmunotherapy[J]. Medical Journal of Qilu, 2011, 26(4):372-376(in Chinese).
[4]Andrew BC, Brechbiel MW. Development of rad-ioimmunotherapeutic and diagnostic antibodies:an inside-out view[J]. Nuclear Medicine and Biology, 2007, 34: 757-778.
[5]CD20:單抗藥物的“寵兒” [EB/OL][2011-06-17].http://www.51atgc.com/BioSpecial/Mantibody/2011-06-17/9810_2.html.
[6]Hagenbeek A, Plesner T, Johnson P, et al. Hu Max-CD20,a novelfully human anti-CD20 monoclonal antibody: Results of a phase I/II trial in relapsed or refractory follicular non-Hodgkin's lymphoma[J]. Blood, 2005, 106(4): 4 760.
[7]康銀花, 范鳴. 抗CD22單克隆抗體Epratuzumab[J]. 藥學進展, 2009, 33(3): 138-139.
Kang Yinhua , Fan Ming. Anti-CD22 monoclonal antibody Epratuzumab[J]. Progress in Pharmaceutical Sciences, 2009, 33(3): 138-139(in Chinese).
[8]Legrand O, Perrot JY, BaudardM, et al. The Immunophenotype of 177 Adluts with AcuteMyeloid Leukemia: Proposal of a Prognostic Score[J]. Blood, 2000, 96(3): 870-877.
[9]FDA: Pfizer Voluntarily Withdraws Cancer Treatment Mylotarg from US Market[EB/OL] (2010-06-22).http://www.fda.gov/NewsEvents/Newsroom/PressAnnouncements/ucm216448.htm.
[10]Mylotarg[EB/OL]. [2008-06-24].http://www.rxlist.com/mylotarg-drug.htm.
[11]Valabrega G, Aglietta M. Trastuzumab: mechanism of action, resistance and future perspectives in HER2-over expressin g breast cancer[J]. Annals of Oncology, 2007, 18(6): 977-984.
[12]Viloria PA, Crombet T. Acquired resistance to the antitum or effect of epidermal growth factor receptor-blocking antibodies in vivo: a role f or altered tumor angiogenesis[J]. Cancer Research, 2001, 61: 5 091-5 101.
[13]Chang JC,Mayer IA,Forero-Torres A, et al. TBCRC 006:a multicenter phase Ⅱ study of neoadjuvant lapatinib andtrastuzumab in patients with HER2-overexpressing breastcancer:2011 ASCO Annual Meeting, McCormick Place in Chicago: 2011[C]. Chincago: American Society of Clinical Oncology, 2011: 505.
[14]張冰.T-DM1治療進展期HER2陽性乳腺癌優于卡培他濱+拉帕替尼[EB/OL] (2012-06-06). http://www.chinapharm.com.cn/html/kyxx/1338948602156.html.
[15]陳靜.中國首個晚期胃癌靶向藥物上市[EB/OL] (2012-10-15). http://www.chinapharm.com.cn/html/kyxx/1350267351874.html.
[16]Kainski MS, Zelenetz AD, Press OW, et al. Pivotal study of iodine I131 tositumomab for chemotherapy refractory low-grade or transformed low-grade B-cell non-Hodgk in’s lymphomas [J]. American Society of Clinical Oncology, 2001, 19(19): 3 918-3 928.
[17]Mark C.Via. Monoclonal Antibodies:Pipeline Analysis and Competitive Assessment[M]. Cambridge Healthtech Institute, 2009: 96-98.
[18]Sharkey RM, Brenner A, Burton J, et al. Radioimmunotherapy of non-Hodgkin′s lymphoma with90Y-DOTA humanized anti-CD22 IgG (90Y-Epratuzumab): do tumor targeting and dosimetry predict therapeutic response? [J].Journal of Nuclear Medicine, 2003, 44: 2 000-2 018
[19]Linden O, Hindorf C, Cavallin-Stahl E, et al. Do-se-fractionated radioimmunotherapy in non-Hodgkin′s lymphoma using DOTA-conjugated,90Y-radiolabeled, humanized anti-CD22 monoclonal antibody, epratuzumab[J]. Clin Cancer Research, 2005, 11: 5 215-5 222.
[20]Jurcic JG, Larson SM, SgourosG, et al.Targeted alpha particle immunotherapy for myeloid leukemia[J]. Blood, 2002, 100: 1 233-1 239.
[21]楊志學,蔣國勤.131I-Hercentin在乳腺癌裸鼠模型中的體內分布[J]. 蘇州大學學報(醫學版), 2011, 31(6): 909-911.
Yang Zhixue, Jiang Guoqin. Biodistribution of131I-Hercentin in Breast Cancer Xenograft[J]. Suzhou University Journal of Medical, 2011, 31(6): 909-911(in Chinese).
[22]Zhang Xiao. Novel therapeutic approaches for ma-mmary cancer[J]. Dissertation Abstracts International, 2007, 68(6): 3 706.
[23]Griffths GL, Goldenberg DM, Knapp FF, et al. Direct radiolabeling of monoclonal antibodies with generator-produced rhenium-188 for radioimmunotherapy: labeling and animal biodistribution studies[J]. Cancer Research, 1991,51(17): 4 594-4 602.
[24]Allen BJ, Rizvi SLY. In vitro and preclinical tarteged alpha therapy for melanoma, breast , prostate and colorectal cancers[J]. Crit Rev Oncol Hematol, 2001, 39(1-2): 139-146.
[25]Danny L, Costantini CC.111In-Labeled Trastuzumab (Herceptin) Modified with Nuclear Localization Sequences (NLS): An Auger Electron-Emitting Radiotherapeutic Agent for HER2/neu-Amplified Breast Cancer[J]. Journal of Nuclear Medicine, 2007, 48:1 357-1 368.
[26]王禹冰. 關于全球首個肺癌放射免疫治療新藥——唯美生Vivatuxin[EB/OL] (2011-10-08). http://www.haodf.com/zhuanjiaguandian/wyb95117_528615866.htm.
[27]郭曉東, 孫婷, 李珊珊. 碘[131I]美妥昔單抗注射液聯合TACE治療原發性肝癌的效果分析[J]. 中國現代醫學雜志, 2011, 21(10): 1 206-1 208.
Guo Xiaodong, Sun Ting, Li Shanshan. The effect of iodine[131I] metuximab injection combined with TACE on primary liver cancer[J]. China Journal of Modern Medicine, 2011, 21(10): 1 206-1 208(in Chinese).
[28]Zalutsky MR, Reardon DA, Akabani G et al. Clinical Experience with Particle Emitting211At: Treatment of Recurrent Brain Tumor Patients with211At-Labeled Chimeric Antitenascin Monoclonal Antibody 81C6[J]. Journal of Nuclear Medicine, 2007, 49(1): 30-38.
[29]Paganelli G, Chinol M. Radioimmunotherapy: is avidin-biotinpret argeting the preferred choice among pretargeting methods?[J]. Journal of Nuclear Medicine, 2003, 30: 773.
[30]汪靜, 鄧敬蘭. RIT在腫瘤臨床治療中的應用[J]. 同位素, 2000, 13(4): 239-242.
Wang Jing, Deng Jinglian. Application of RIT in Clinical Therapy of Tumors[J]. Journal of Isotopes, 13(4): 239-242(in Chinese).
[31]Gregory Lee, Rui-Ai Chu, Hong Hoi Ting. Preclinical assessment of anti-cancer drugs by using RP215 monoclonal antibody[J]. Cancer Biology & Therapy, 2009, 8(2): 161-166.

