電子溫針對胰島素抵抗糖尿病周圍神經病模型大鼠神經保護作用機制的研究
李凌雁,王麗巖△,肖洪彬,侯 靜
(1.大慶醫學高等專科學校,黑龍江 大慶163312;2.黑龍江中醫藥大學,黑龍江哈爾濱150040)
糖尿病是繼心血管疾病及腫瘤之后第3位威脅人類健康和生命的非傳染性慢性病,其中90%以上為2型糖尿病。研究發現74%的2型糖尿病患者存在胰島素抵抗(IR)。糖尿病周圍神經病變(DPN)是胰島素抵抗性糖尿病最常見的慢性并發癥[1]。目前臨床主要采用藥物治療,效果不佳,毒副作用大。因此尋求安全有效的防治DPN的方法尤為迫切。電子溫針[2]是將溫針、電針與傳統針刺完美結合,與傳統溫針灸相比具有獨特的控溫功能,能確保銀針針體溫度恒定,并可根據治療需要設置具體參數,操作簡單,安全可靠。本研究擬從降糖及抗氧化應激的角度揭示電子溫針對DPN神經修復過程的干預機制,現將研究過程及結果概述如下。
1 材料
1.1 主要試劑
鏈脲佐菌素,上海科興實驗室設備有限公司生產;彌可保(甲鈷銨針)日本衛材珠式會社制造(500 ug/支);TOCA測定試劑盒等,南京建成生物工程研究所生產;胰島素試劑盒,北京北方生物技術研究所生產等。
1.2 主要儀器
血糖儀,德國羅氏公司;Medlab-u/4cs生物信號采集處理系統,南京美易科技有限公司;溫針電熱針綜合治療儀,北京中西泰安技術服務有限公司,型號:M150002。
2 研究方法
2.1 實驗動物分組及造模
選取重量(220±30)g,雄性wistar大鼠60只,適應性喂養1周后,隨機取10只大鼠作為空白組,其余大鼠造模后隨機分組。除空白組外,各組均高脂飼料(豬油12%、花生10%、糖15%、蛋黃粉10%、鹽5%、豬膽鹽0.03%、基礎飼料47%)喂養[3],第8周時將鏈脲佐菌素用檸檬酸-檸檬酸鈉緩沖液0.1 mol/L在避光條件下配成濃度為0.2%(PH值為4.2~4.5)的溶液,按劑量30 mg/kg腹腔單次注射,72 h后尾靜脈取血測試血糖(FBG)、空腹胰島素水平(FINS),計算胰島素敏感指數(ISI)。血糖>16.7 mmol/L為糖尿病大鼠。空白組注射相同體積的0.1 mol/L檸檬酸-檸檬酸鈉緩沖液(PH值為4.2)。
用以上造模方法獲得造模成功的糖尿病胰島素抵抗大鼠48只。所有大鼠飼養8周后進行坐骨神經傳導速度測定,其傳導速度與空白組相比顯著減慢即為糖尿病周圍神經病變造模成功,淘汰未成模者。如此獲得糖尿病周圍神經病變大鼠42只,造模成功后的大鼠隨機分為模型組(14只)、藥物組(14只)、電子溫針組(14只),各治療組均在成模后開始治療,共治療8周。
2.2 干預方法
電子溫針組大鼠穴位依據人體穴位及大鼠穴位圖譜,結合大鼠解剖結構定位,用自制大鼠固定器固定,使大鼠成俯臥位,取背部夾脊穴(T6~L3各椎骨棘突正中旁開約0.5寸,左右各取5穴)、雙側脾俞、腎俞、足三里、環跳,以溫熱電針施治,設定參數為疏密波,溫度37~45℃,時間35 min,隔日1次,共治療8周;藥物組60 μg/kg彌可保隔日注射于下肢肌肉治療8周;空白組和模型組隔日捆綁固定 1次,每次 30 min,共8周。
2.3 觀察指標及方法
2.3.1 血糖(FPG)、空腹胰島素水平(FINS)、胰島素敏感性指數(ISI) 血糖儀測定血糖;放免法檢測空腹胰島素水平;依據我國學者李光偉提出的ISI=1/(FPG×FINS)公式計算[4]。
2.3.2 血清和坐骨神經丙二醛(MDA)、超氧化物歧化酶(SOD)、總抗氧化能力(T-AOC)含量測定 在治療后8周,用濃度10%水合氯醛(350 mg/kg)腹腔注射麻醉大鼠,心臟穿刺取血后分離血清,在-20℃的條件下保存。取出坐骨神經立即冷凍下保存,準確進行組織稱重,按重量體積比加生理鹽水制成10%的勻漿,4000轉/分離心10 min,取上清液,用生理鹽水稀釋成1∶9的1%組織勻漿待測。應用化學比色檢測法測血清和坐骨神經中MDA、SOD和T-AOC含量。
2.3.3 坐骨神經傳導速度[5]將大鼠俯臥固定于檢測板上,剝離出雙側梨狀肌下緣坐骨神經,將坐骨神經約1 cm置于4%多聚甲醛中固定24~48 h。將暴露分離的坐骨神經放在生物信號采集處理系統的刺激器上,用4 mA、0.2 ms脈沖電流刺激后肢末,記錄感覺神經動作電位,計算出兩個動作電位的潛伏期差值(t2-t1),以及刺激點至記錄點距離長度,通過v=d/t2-t1算出感覺神經傳導速度。
2.4 統計方法
統計分析利用SPSS17.0軟件做統計學分析處理,計算各組間變化差異。
3 實驗結果
3.1 電子溫針對大鼠的FPG、FINS、ISI的影響
表1 電子溫針對大鼠FPG、FINS、ISI的影響(±s)
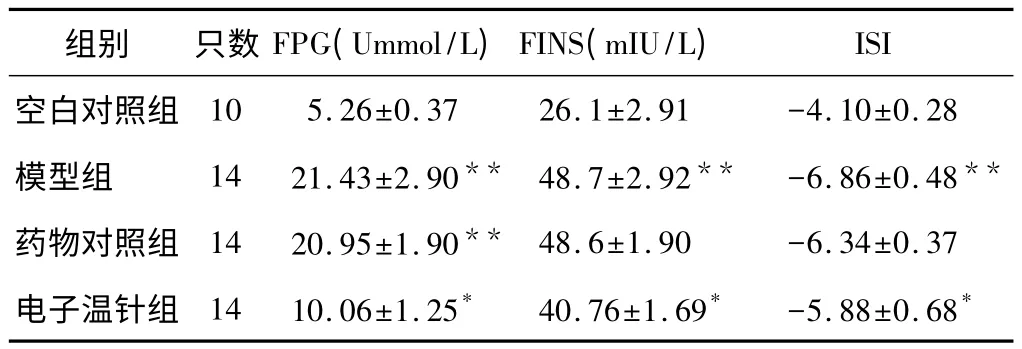
表1 電子溫針對大鼠FPG、FINS、ISI的影響(±s)
注:與空白對照組比較,**P<0.01;與模型組比較,*P<0.05。
組別 只數FPG(Ummol/L)FINS(mIU/L) ISI空白對照組 10 5.26±0.37 26.1±2.91 -4.10±0.28模型組 14 21.43±2.90** 48.7±2.92** -6.86±0.48**藥物對照組 14 20.95±1.90** 48.6±1.90 -6.34±0.37電子溫針組 14 10.06±1.25* 40.76±1.69* -5.88±0.68*
從表1可見,模型組大鼠血糖、血漿胰島素均較正常組顯著升高,胰島素敏感性指數明顯下降,差異具有非常顯著性意義(P<0.01),提示胰島素抵抗性糖尿病大鼠造模成功。電子溫針組治療8周后,大鼠空腹血糖、血漿胰島素均較模型組明顯降低,胰島素敏感性指數明顯上升,經統計學分析,治療前后兩組相比,具有顯著性差異(P<0.05)。但電子溫針組與空白組比較,各項指標具有顯著性差異(P<0.05),說明電子溫針組大鼠的血糖、血漿胰島素水平并未達到正常,可能與治療時間有關系。
3.2 電子溫針對大鼠坐骨神經傳導速度的影響
表2 大鼠坐骨神經傳導速度治療前后變化對比(±s)
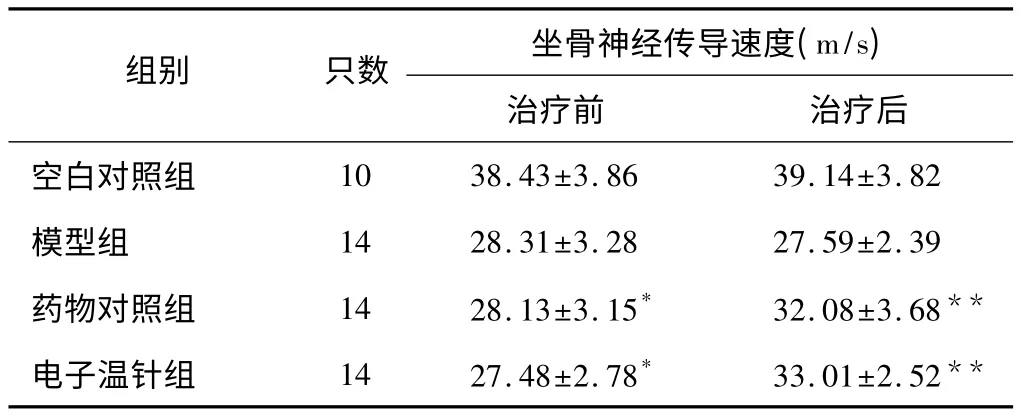
表2 大鼠坐骨神經傳導速度治療前后變化對比(±s)
注:與模型組比較,**P<0.01,*P>0.05。
組別 只數 坐骨神經傳導速度(m/s)治療前 治療后空白對照組 10 38.43±3.86 39.14±3.82模型組 14 28.31±3.28 27.59±2.39藥物對照組 14 28.13±3.15* 32.08±3.68**電子溫針組 14 27.48±2.78* 33.01±2.52**
從表2可見,治療前、后各組坐骨神經傳導速度與空白組相比均明顯下降(P<0.01),提示糖尿病周圍神經病變大鼠模型造模成功。治療前,治療組與模型組進行對比無顯著差異(P>0.05),能說明具有可比性。治療后,治療組與模型組進行對比坐骨神經傳導速度呈現顯著增高(P<0.01),其中,電子溫針組與藥物組進行對比未呈現明顯差異性(P>0.05),提示電子溫針與彌可保藥物治療均能有效提高糖尿病周圍神經病變大鼠的坐骨神經傳導速度,二者無統計學差異。
3.3 電子溫針對糖尿病周圍神經病變大鼠血清中MDA、SOD和T-AOC水平的影響
表3 大鼠血清中MDA、SOD和T-AOC水平的比較(nmol/ml,±s)
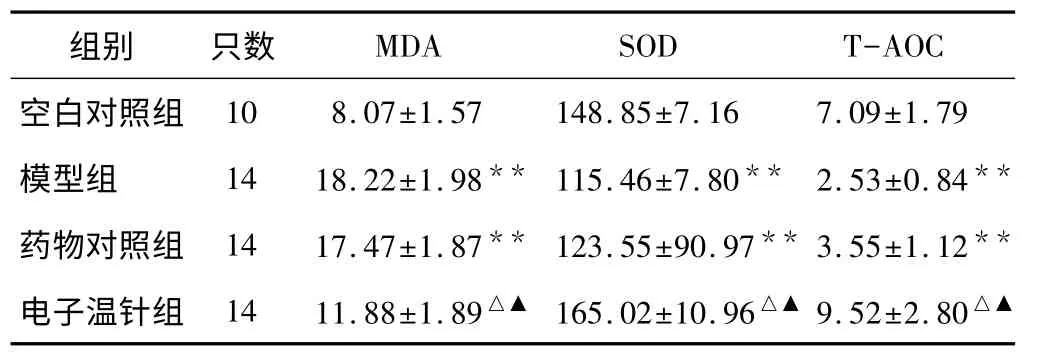
表3 大鼠血清中MDA、SOD和T-AOC水平的比較(nmol/ml,±s)
注:與空白對照組比較,**P<0.01;與模型組比較,△P<0.05;與藥物對照組比較,▲P<0.05。
組別 只數 MDA SOD T-AOC空白對照組 10 8.07±1.57 148.85±7.16 7.09±1.79模型組 14 18.22±1.98** 115.46±7.80** 2.53±0.84**藥物對照組 14 17.47±1.87** 123.55±90.97** 3.55±1.12**電子溫針組 14 11.88±1.89△▲ 165.02±10.96△▲ 9.52±2.80△▲
從表3結果可以看出,模型組大鼠血清中MDA水平明顯高于空白組(P<0.01),而 SOD、T-AOC水平則明顯低于空白組(P<0.05)。與模型組相比電子溫針能有效減低坐骨神經中MDA水平,提高SOD和TAOC水平(均P<0.05),電子溫針組與藥物組進行對比有顯著差異(P<0.05),說明其具有抗氧化應激和清除氧自由基的作用。
3.4 電子溫針對糖尿病周圍神經病變大鼠坐骨神經中MDA、SOD和T-AOC水平的影響
表4 大鼠坐骨神經中MDA、SOD和T-AOC的比較(nmol/ml,±s)
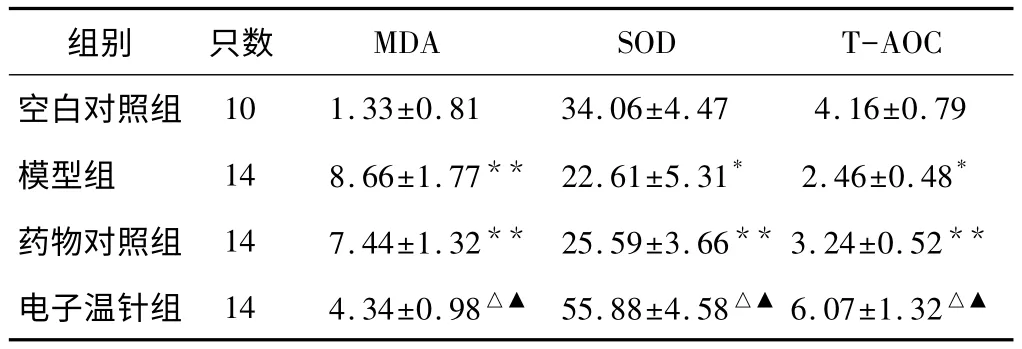
表4 大鼠坐骨神經中MDA、SOD和T-AOC的比較(nmol/ml,±s)
注:與空白對照組比較,**P<0.01,*P<0.05;與模型組比較,△P<0.05;與藥物對照組比較,▲P<0.05。
組別 只數 MDA SOD T-AOC空白對照組 10 1.33±0.81 34.06±4.47 4.16±0.79模型組 14 8.66±1.77** 22.61±5.31* 2.46±0.48*藥物對照組 14 7.44±1.32** 25.59±3.66** 3.24±0.52**電子溫針組 14 4.34±0.98△▲ 55.88±4.58△▲ 6.07±1.32△▲
從表4結果顯示模型大鼠坐骨神經MDA的水平明顯高于空白組(P<0.01),而SOD和 T-AOC水平則明顯低于空白組(P<0.05)。與模型組相比,電子溫針組能有效減低坐骨神經中MDA的水平,提高SOD和T-AOC水平(均 P<0.05),電子溫針組與藥物對照組相比有顯著性差異(P<0.05),說明其具有抗氧化應激和清除氧自由基的作用。
4 討論
電子溫針治療8周后,大鼠FBG、FINS較模型組明顯降低,ISI明顯升高,其與模型組比較有統計學意義。說明該治療有效干預了代謝紊亂、降低了血糖、改善了胰島素抵抗程度,這是電子溫針對胰島素抵抗性糖尿病大鼠周圍神經結構和功能的保護作用機制之一。
電子溫針可以減少糖尿病周圍神經病變大鼠坐骨神經纖維的功能損傷,具有神經保護作用,可以減低血清及坐骨神經中MDA水平、增高SOD和T-AOC水平,具有抗氧化應激和清除氧自由基作用,減少神經細胞受氧化應激的損傷,這可能是對周圍神經的結構和功能起到保護作用的又一機制。
[1]蔣雨平.臨床神經病學[M].上海:上海醫科大學出版社,1999:370-378
[2]李玉榕,陳建國,杜民,等.溫針傳熱研究與電子溫針的研制[J].燕山大學學報,2010,34(2):157-161
[3]葛鵬玲,李冀,盛波.西洋參對胰島素抵抗大鼠脂代謝的影響[J].中醫藥學報,2010,38(3):18-20
[4]張麗紅,向紅丁,李偉,等.不同糖耐量狀態孕婦的胰島素敏感性與胰島β細胞功能的研究[J].中國糖尿病雜志,2010,18(6):444-448
[5]王瑞輝,屈紅艷,劉飛虎,等.電針對家兔坐骨神經損傷后神經傳導速度的影響[J].陜西中醫學院學報,2007,30(3):56-57

