超聲引導下羅哌卡因連續股神經阻滯用于20例全膝關節置換術后康復鎮痛的療效分析*
單海華,朱常花,謝 紅,王 琛
(蘇州大學附屬第二醫院麻醉科,江蘇蘇州 215004)
全膝關節置換(total knee arthroplasty,TKA)術后應早期進行主動和被動功能訓練,以最大限度地改善假體關節的功能。但其術后60%的患者有劇烈疼痛,30%的患者有中度疼痛,顯著降低了康復訓練的效果[1]。近年來,連續股神經阻滯用于TKA術后康復鎮痛漸成新的熱點。在神經阻滯的實施中,穿刺置管的定位直接影響神經阻滯鎮痛的效果[2],盡管神經刺激器的使用大幅提高了神經阻滯鎮痛的成功率,但因其不能直接看到神經結構,故仍有可能導致神經損傷及鎮痛不完善。本文采用超聲引導技術進行股神經阻滯鎮痛,效果滿意,報道如下。
1 資料與方法
1.1 一般資料 選擇美國麻醉醫師協會(American Society of Anesthesiology,ASA)分級Ⅰ~Ⅱ級行單側TKA術患者40例,年齡55~87歲,體質量51~85kg。排除標準:穿刺部位感染、非首次手術、神經系統疾病、不能正確理解疼痛視覺模擬評分(visual analogue scale,VAS)的患者。隨機分為患者自控靜脈鎮痛(patient-controlled intravenous analgesia,PCIA)組和患者自控神經干鎮痛(patient-controlled nerve analgesia,PCNA)組各20例。兩組患者年齡、性別、體質量、手術時間比較差異無統計學意義(P>0.05)。
1.2 方法
1.2.1 麻醉及手術 兩組患者均于L3~4間隙行硬腰聯合麻醉,給予0.5%布比卡因重比重液2~3mL,置入硬膜外導管,麻醉平面控制在T10左右。在氣囊止血帶下,取膝關節前正中切口髕骨內側入路完成手術,術畢靜脈給予格拉司瓊6mg。
1.2.2 股神經穿刺置管 術后,患者取仰臥位,患肢外展且外旋15°,采用便攜式彩色二維超聲儀(MicroMAXX,索諾聲公司,美國),高頻線陣探頭(7~13MHz)。行股神經阻滯時,在腹股溝韌帶下方2cm處水平放置探頭,長軸與大腿縱軸垂直,待清晰顯示髂恥弓筋膜處由內向外排列的股靜脈、股動脈和股神經橫斷面超聲圖像,采用平面內技術,由大腿外側皮膚進針(16G靜脈注射套管針),穿刺針沿超聲束掃描平面向內側與皮膚成30°~45°進針,經縫匠肌至髂腰肌表面股神經處,回吸無血后注入少量生理鹽水,觀察擴散情況,若生理鹽水在髂筋膜深處股神經周圍擴散,即注入負荷量0.25%羅哌卡因15 mL,通過“水分離”技術擴大股神經周圍間隙,置入硬膜外導管,導管在股神經周圍留置1~2cm,再次通過導管注入少量生理鹽水觀察擴散情況,如仍在神經周圍擴散,即固定導管,否則調整導管直至擴散滿意后固定。
1.2.3 術后鎮痛 兩組患者均于術后接電子鎮痛泵(BCDBF,上海博創)行患者自控鎮痛(patient controlled analgesia,PCA)。PCIA組患者行靜脈芬太尼鎮痛,藥物配方:芬太尼1.0mg加生理鹽水至120mL,負荷量芬太尼0.05mg,背景劑量2mL/h,PCA每次1mL,鎖定時間30min。PCNA組行連續股神經阻滯鎮痛,藥物配方:0.25%羅哌卡因140mL,負荷量15mL(操作時已注入),背景劑量2mL/h,PCA每次3mL,鎖定時間30min。兩組患者均于功能鍛煉前15min行PCA 1次,持續鎮痛2d,任一時間點若患者的VAS評分大于4分,則加服塞來昔布200mg,緩解不佳者肌注哌替啶75mg。
1.3 觀察指標 (1)疼痛評分:隨訪并記錄患者術后4、8、12、24、48h靜息狀態 VAS 評分(rest visual analogue scale,RVAS)和術后48h持續被動運動時的VAS評分(passive visual analogue scale,PVAS),0分=無痛,10分=劇痛。(2)康復指數:觀測術后12、24、48h患肢主動關節屈曲角度。(3)肌力分級:記錄各時間點患肢股四頭肌肌力,0為完全癱瘓,1分為可收縮,2分為不能抗重力,3分為抗重力不抗阻力,4分為可抗弱阻力,5分為正常。(4)鎮靜程度采用Rameasay鎮靜評分:1分為不安靜、煩躁,2分為安靜合作,3分為嗜睡能聽從指令,4分為睡眠狀態、可喚醒,5分為不易喚醒,6分為深睡狀態、不可喚醒。1分為鎮靜不足,2~4分為鎮靜滿意,5~6分為鎮靜過度。(5)不良反應:包括尿潴留、低氧(定義為SpO2<90%)、惡心、嘔吐及加用鎮痛藥情況。(6)隨訪:鎮痛結束4周后,電話隨訪所有患者,詢問有無下肢感覺、運動障礙,置管部位有無感染等。
1.4 統計學處理 應用SAS8.2統計軟件進行數據分析,計量資料以±s表示,組間比較采用t檢驗,計數資料采用χ2檢驗,以P<0.05為差異有統計學意義。
2 結 果
硬膜外導管沿股神經橫向置入,且導管頭端緊貼其表面,局部麻醉藥液分布于股神經周圍(圖1)。鎮痛效果、康復指數見表1~2。PCNA組術后惡心、鎮靜過度和加用鎮痛藥例數少于PCIA組(P<0.05)。術后4周隨訪所有患者,未出現置管部位感染及患肢感覺運動障礙,見表3。
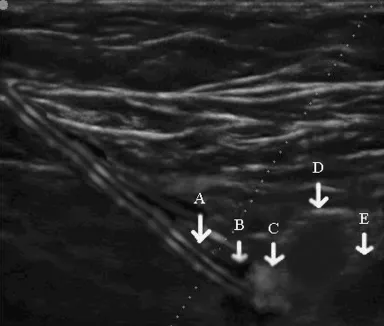
圖1 股神經旁置管的超聲圖像
表1 兩組患者VAS評分(±s,分,n=20)

表1 兩組患者VAS評分(±s,分,n=20)
*:P<0.05,與PCIA組比較。
組別RVAS 4h 8h 12h 24h 48h PVAS 48h PCIA組 0.4±0.3 2.3±0.7 3.9±1.0 1.7±0.6 1.3±0.7 4.6±1.0 PCNA組 0.4±0.2 0.6±0.3*1.8±0.4*1.2±0.5*0.8±0.6* 2.1±0.8*
表2 患肢主動關節屈曲角度(±s,°,n=20)
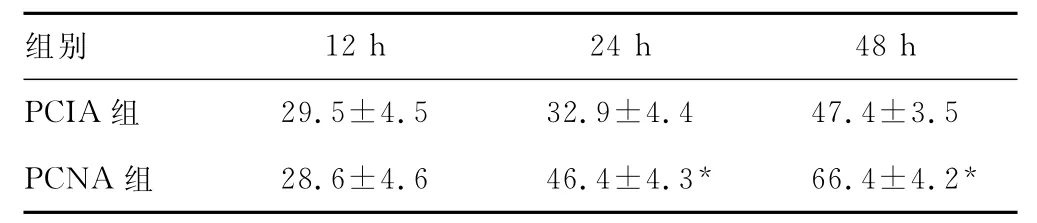
表2 患肢主動關節屈曲角度(±s,°,n=20)
*:P<0.05,與PCIA組比較。
組別12h 24h 48h PCIA組29.5±4.5 32.9±4.4 47.4±3.5 PCNA組 28.6±4.6 46.4±4.3* 66.4±4.2*
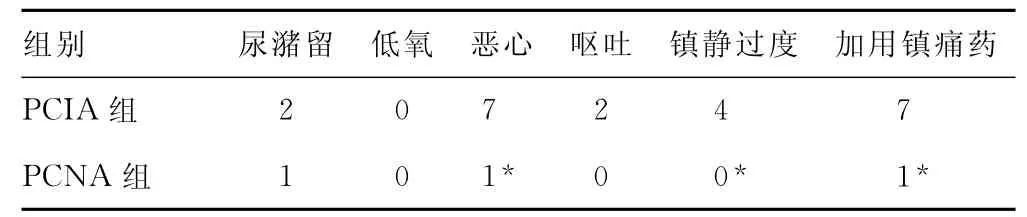
表3 術后不良反應情況(n,n=20)
3 討 論
TKA術后患者在完善鎮痛下早期行康復訓練可以使患側膝關節活動比較容易,對防止術后粘連、縮短術后恢復時間、減少因長期臥床而產生的心血管及肺部并發癥有積極意義[3]。靜脈鎮痛操作簡便、不影響肌力、適用范圍廣,但藥物作用于全身,不良反應較多。硬膜外鎮痛效果確切,全身不良反應較少,臨床上普遍采用,但此法有低血壓及尿潴留等不良反應,且膝關節置換老年患者居多,圍術期易出現下肢深靜脈血栓形成和肺栓塞[4],為預防該并發癥,患者在術后需應用抗凝藥物,有增加硬膜外血腫的可能性,限制了硬膜外鎮痛的臨床使用。
近年來,有連續股神經阻滯用于TKA術后鎮痛的報道,其阻滯鎮痛成功的關鍵是確保局部麻醉藥在神經周圍充分擴散。臨床上用于神經阻滯定位的方法有解剖定位、異感定位、神經刺激器定位及超聲定位等。只根據解剖標志和異感定位的盲探法不能觀察到局部麻醉藥的擴散,不能保證效果,且不可避免地損傷神經及周圍血管,即使神經刺激器也難以達到完善的效果,而且還可能直接損傷神經。超聲引導可以直接看到神經結構及穿刺針,并能準確地將導管前端放置在股神經表面,確保局部麻醉藥液分布于股神經周圍(圖1),明顯提高阻滯效果。國外已廣泛應用[5],但此方法國內報道較少。
TKA術后患者的疼痛特別是運動時的疼痛很大部分原因是由于股四頭肌的痙攣引起的[6],靜脈鎮痛并不能使痙攣的股四頭肌松弛。而TKA術后良好的神經阻滯,不僅能提供和硬膜外鎮痛同樣的效果,而且并發癥更低[6-7]。本研究表明,術后4h因蛛網膜下腔阻滯麻醉作用兩組患者VAS評分相似;PCNA組術后8、12、24、48h的RVAS和術后48h的PVAS評分明顯低于PCIA組,可能因為連續股神經阻滯時局部麻醉藥在髂筋膜深面向頭側彌散,可同時阻滯股神經、股外側皮神經和閉孔神經[8],故顯著緩解TKA術后患肢的靜息痛和運動痛,有利于患肢關節主動康復鍛煉。羅哌卡因連續股神經阻滯的常用濃度為0.2%,24h最大總量為800mg[9]。Scott等[10]研究發現,羅哌卡因的運動神經阻滯作用和濃度呈正相關,0.2%羅哌卡因可達到最佳鎮痛和最小的運動阻滯的平衡。本研究為了達到康復鍛煉時更完善的鎮痛,故采用更高濃度羅哌卡因(0.25%)。結果發現,兩組患者術后各時間點肌力無差異,除4h因蛛網膜下腔阻滯麻醉作用尚未消退外其余各時間點肌力均達到3級,表明0.25%羅哌卡因不影響患肢關節主動康復鍛煉。由于連續股神經阻滯能松弛痙攣的股四頭肌且肌力可達到3級,因此,其術后24、48h患肢主動關節屈曲角度明顯大于PCIA組,而術后12h患者膝部明顯滲血腫脹,影響患肢主動關節屈曲,故兩組屈曲角度無差別。PCIA組惡心、鎮靜過度的例數較多與阿片類藥物不良反應有關。PCIA組有7例患者術后12h左右自覺術側膝部脹痛難忍,加服塞來昔布或肌內注射哌替啶后好轉,而PCNA組僅1例患者加服塞來昔布,考慮可能與股神經導管移位有關。術后隨訪未見穿刺引起股神經功能障礙的并發癥,顯示了超聲引導可視化的特點。
綜上所述,與靜脈芬太尼鎮痛相比,超聲引導下0.25%羅哌卡因連續股神經阻滯用于TKA術后鎮痛,效果良好,對下肢肌力影響輕微,并發癥發生率低,是TKA術后較為理想的鎮痛方法。
[1] Salinas FV,Liu SS,Mulroy MF.The effect of single-injection femoral nerve block versus continuous femoral nerve block after total knee arthroplasty on hospital length of stay and long-term functional recovery within an established clinical pathway[J].Anesth Analg,2006,102(4):1234-1239.
[2] 石英,魯開智.股神經阻滯在全膝關節置換術鎮痛中的應用進展[J].重慶醫學,2009,38(17):222-224.
[3] Adrew TB,David WM.Analgesia following total knee arthroplasty[J].Current Opinion in Orthopaedics,2007,18(1):76-80.
[4] 關振鵬,呂厚山,吳淳,等.人工關節置換術后肺栓塞的早期診斷和處理[J].中華外科雜志,2003,41(1):37-40.
[5] Marhofer P,Greher P,Kapral S.Ultrasound guidance in regional anaesthesia[J].British J Anaesth,2005,94(1):7-17.
[6] Fowler SJ,Symons J,Sabato S,et al.Epidural analgesia compared with peripheral nerve blockade after major knee surgery:a systematic review and meta-analysis of randomized trials[J].Br J Anaesth,2008,100(2):154-164.
[7] Szczukowski MJ,Hines JA,Snell JA,et al.Femoral nerve block for total knee arthroplasty patients:a method to control postoper-ative pain[J].J Arthroplasty,2004,19(6):720-725.
[8] Winnie AP,Ramamuahy S,Dunaai Z.The inguinal paravascular technic of lumbar plexus anesthesia:the “3-in-1 block”[J].Anesth Analg,1973,52(6):989-996.
[9] 莊心良,曾因明,陳伯鑾.現代麻醉學[M].北京:人民衛生出版社,2006.
[10]Scott DA,Chamley DM,Mooney PH,et al.Epidural ropivacaine infusion for postoperative analgesia after mafor lower abdominal surgery a dose finding study[J].Anesth-Analg,1995,81(5):982-986.

