siRNA 沉默MIF基因抑制大細胞肺癌H460細胞增殖*
侯俊娜, 羅益鋒, 王杜娟, 楊惠玲, 郭禹標△
(中山大學 1附屬第一醫院呼吸內科, 2中山醫學院病理生理學教研室,廣東 廣州 510080)
siRNA 沉默MIF基因抑制大細胞肺癌H460細胞增殖*
侯俊娜1, 羅益鋒1, 王杜娟2, 楊惠玲2, 郭禹標1△
(中山大學1附屬第一醫院呼吸內科,2中山醫學院病理生理學教研室,廣東 廣州 510080)
目的: 研究小干擾RNA(siRNA)阻斷巨噬細胞抑制因子(MIF)基因表達對大細胞肺癌細胞株H460細胞增殖的抑制效應并探討其抑瘤機制。方法在體外培養的H460細胞中,采用免疫熒光法觀測siRNA轉染效率,Western blotting檢測MIF蛋白的表達,MTT法和平板克隆形成實驗檢測 MIF siRNA對H460細胞活性和增殖的抑制作用,Hoechst染色出現后熒光顯微鏡觀測轉染后細胞的形態學變化,流式細胞儀觀測細胞凋亡。結果與陰性對照組相比,siRNA能有效阻斷MIF蛋白的表達,顯著抑制H460細胞活性及增殖能力(Plt;0.05);Hoechst染色可見轉染MIF siRNA后的H460細胞出現典型的凋亡形態學改變;流式細胞術結果顯示轉染MIF siRNA1和MIF siRNA2后細胞凋亡較陰性對照組顯著增加[ (18.09±0.41)% 和(23.38±2.67)%vs(5.87±1.05)%,Plt;0.05]。結論MIF在大細胞肺癌的發生發展過程中發揮著重要作用,siRNA阻斷MIF蛋白表達,可抑制H460細胞增殖,提示其極有可能成為肺癌的新治療靶點。
巨噬細胞抑制因子; 小干擾RNA; 肺腫瘤
肺癌為當前世界各地最常見的惡性腫瘤之一,半個世紀以來世界各國肺癌的發病率和病死率都有明顯增高的趨勢。肺癌分為小細胞肺癌和非小細胞肺癌(non-small cell lung cancer,NSCLC),其中NSCLC占80%以上。NSCLC早期侵犯血管,易發生遠處轉移,且多數NSCLC對放化療并不敏感,尋找新的診療方法迫在眉睫[1,2]。在多數腫瘤可見負調控因子的表達或功能異常,設法拮抗異常的細胞信號轉導通路、提高負調控因子或沉默正調控因子,使其達到新的平衡,是治療肺癌的新策略[3]。目前認為,巨噬細胞移動抑制因子(macrophage migration inhibitory factor,MIF)是一種獨特的促進惡性腫瘤發生的細胞因子。MIF不僅作為重要的炎癥細胞因子參與機體的炎癥及免疫反應,而且和細胞增殖、細胞分化及腫瘤血管生成等關鍵環節密切相關[4-7]。還有研究證明,靶向沉默MIF基因后,肺腺癌A549細胞的侵襲與遷移能力下降90%,若MIF過表達,則可觀察到相反現象[7]。在NSCLC其它類型如大細胞肺癌中是否存在MIF表達及相關的作用,國內外尚未見報道。本研究采用小干擾RNA(small interfering RNA,siRNA)技術阻斷MIF蛋白的表達,觀察其對人大細胞肺癌H460細胞增殖的影響并探討其可能機制,為研發NSCLC的新治療靶點提供實驗依據。
材 料 和 方 法
1材料
H460細胞株由中山大學實驗動物中心提供。Lipofectamine 2000購自Invitrogen。MIF的siRNA序列由Invitrogen合成,MIF siRNA1: 正義鏈5′-AUAGUUGAUGUAGACCCUGUCCGGG-3′,反義鏈5′-CCCGGACAGGGUCUACAUCAACUAU-3′; MIF siRNA2:正義鏈5′- UUGGUGUUUACGAUGAACAUCGGCA-3′,反義鏈5′-UGCCGAUGUUCAUCGUAAACACCAA-3′; Opti-MEM培養基、BLOCK-iT Alexa Fluor Red Oligo和Stealth RNAi Negative Control Hi GC Kit均購自Invitrogen。MIF鼠抗人單克隆抗體購自Abcam,HRP標記的羊抗小鼠IgG(Ⅱ抗)購自Cell Signaling Technology。噻唑藍[3-(4,5-dimethylthiahiazol-2-y1)-3,5-diphenyltetrazoliumromide,MTT]、二甲基亞砜(dimethyl sulfoxide,DMSO)為Sigma產品,RPMI-1640培養基為Gibco產品;小牛血清為杭州四季青產品。Leica DMI4000B 智能型倒置熒光顯微鏡購自Leica。Annexin V-FITC 細胞凋亡檢測試劑盒購自凱基生物;ECL發光液購自北京普利萊基因技術有限公司;流式細胞儀購自BD。
2方法
2.1細胞培養 H460細胞株采用含10%小牛血清、無抗生素的RPMI-1640細胞培養基,置37 ℃、5%CO2、飽和濕度條件下培養。取對數生長期細胞進行實驗。轉染前24 h消化細胞,傳代于6孔板,第2 d按Lipofectamine 2000轉染試劑說明書操作。分別用Opti-MEM稀釋siRNA及脂質體,室溫靜置5 min后混和,室溫孵育20 min,轉染細胞。實驗分為陰性對照組(轉染negative control siRNA,NC siRNA)和實驗組(分別轉染MIF siRNA1和MIF siRNA2)。
2.2免疫熒光法觀測siRNA轉染效率 轉染前24 h 消化細胞,傳代于6孔板,第2 d按Lipofectamine 2000轉染試劑說明書操作,按照濃度梯度加入熒光標記的siRNA,熒光siRNA轉染H460細胞,6 h后PBS沖洗1次,倒置熒光顯微鏡下觀察并拍照。
2.3Western blotting法測定目的蛋白MIF的表達 轉染后48 h,收集全細胞蛋白標本,常規BCA方法蛋白定量。制備15%聚丙烯酰胺凝膠,進行SDS-PAGE電泳(2-3 h),轉移到PVDF膜(50 min),室溫5%BSA封閉1 h,加MIF Ⅰ 抗(1∶750)孵育PVDF膜4 ℃過夜,后TBST洗膜3次,加HRP偶聯的Ⅱ 抗(1∶2 000),孵育90 min,TBST洗膜3次,ECL發光液顯色曝光,Qantity One 軟件分析結果。
2.4MTT法測定細胞活性 胰酶消化對數生長期細胞,以每孔5×103細胞接種于96孔板,培養24 h后按Lipofectamine 2000轉染試劑說明書操作轉染siRNA,使液體終體積100 μL/well,每組設4個復孔,6 h后每孔加入含20%小牛血清、無抗生素RPMI-1640細胞培養基100 μL/well,孵育0、24、48、72 h后,棄去培養液,加入MTT溶液(20 μL/well)培養4 h,吸出孔內培養液后,加入DMSO液(150 μL/well),將培養板置于微孔板扳蕩器上振蕩10 min,使結晶物溶解,酶聯免疫檢測490 nm處測量其吸光度值(A值)。
2.5平板克隆實驗檢測細胞增殖能力 siRNA轉染細胞24 h后,胰酶消化細胞,以200 cells/well接種于6孔板,加全培養基2 mL/well繼續培養10 d,常規固定染色,顯微鏡下計數集落,以≥50個細胞作為一個集落,并計算克隆形成率。
克隆形成率=克隆數/接種細胞數×100%
2.6Hoechst染色法觀察細胞形態學變化 胰酶消化細胞,按1.5×105cells/well接種于6孔板,第2 d轉染,6 h后換液,48 h后棄上清,PBS洗滌2次,常規固定,Hoechst 33342染色(0.3 mL/well),染色10 min,PBS洗滌3次,熒光顯微鏡下觀察并拍照。
2.7流式細胞儀檢測細胞凋亡率 轉染48 h后棄上清,無EDTA胰酶消化收集細胞,用膜聯蛋白(Annexin V)/碘化丙啶(propidium iodide,PI)(Annexin V/PI)雙染法檢測細胞凋亡率。
3統計學處理
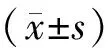
結 果
1免疫熒光法觀測轉染效率
免疫熒光結果表明,siRNA的成功轉染效率可達70%以上,但是在siRNA濃度≥50 nmol/L后,隨著siRNA濃度的增加,轉染效率沒有表現出相應的劑量依賴關系,因此我們選擇50 nmol/L的濃度做后續功能研究實驗,見圖1。
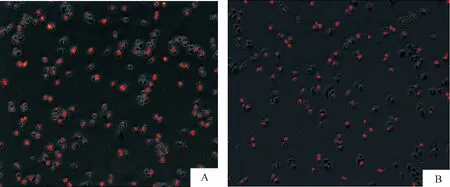
Figure 1.The transfection efficiency of siRNA directed against MIF was assessed by immunofluorescence technique.A: 50 nmol/L siRNA; B: 100 nmol/L siRNA.
2Westernblotting檢測靶向沉默MIF基因后,H460細胞中MIF蛋白的表達
與NC siRNA組相比,MIF siRNA1和MIF siRNA2均能有效阻斷MIF蛋白的表達,見圖2。
3靶向沉默MIF基因對H460細胞活性及增殖的影響
MTT結果表明,H460細胞轉染siRNA 48 h后,與NC siRNA組相比,MIF siRNA能顯著抑制H460細胞的活性,差異顯著(Plt;0.05),見表1。平板克隆實驗結果顯示,MIF siRNA1和MIF siRNA2組細胞克隆形成率分別為(32.00±4.44)%、(22.00±3.46)%,顯著低于NC組細胞克隆形成率(66.67±2.56)%,差異顯著(Plt;0.05),見圖3。
4MIFsiRNA對H460細胞凋亡的影響
4.1電鏡形態學觀察 Hoechest 33342染色結果顯示,轉染siRNA 48 h后,與NC組細胞相比,可見MIF siRNA1組和MIF siRNA2組細胞數減少,并且可見染色質濃縮、碎裂和邊集,出現凋亡的形態學改變,見圖4。
4.2細胞凋亡的流式檢測 流式細胞儀檢測轉染siRNA 48 h后H460細胞的凋亡情況。結果顯示,NC組凋亡率為5.87%,MIFsiRNA1和MIFsiRNA2組凋亡率分別為18.09%、23.38%。差異顯著(Plt;0.05),見圖5。
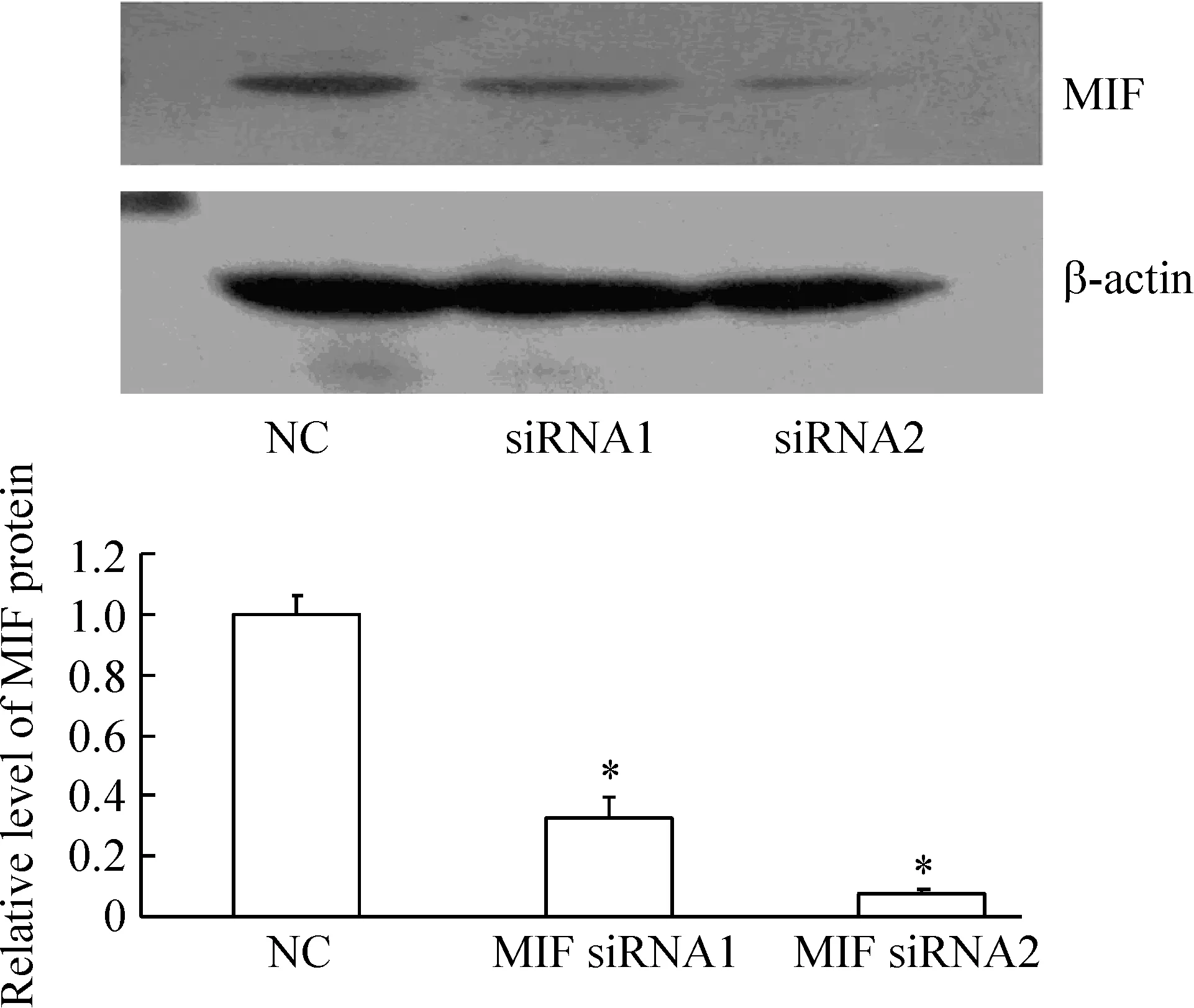
Figure 2.Expression of MIF protein detected by Western blotting in H460 cells after knockdown of MIF gene by siRNA.NC: negative control±s.n=3.*P lt;0.05 vs NC group.

表1 MTT法檢測MIF siRNA對H460細胞活性影響

Figure 3.The proliferation of H460 cell induced by MIF siRNA.A: negative control group; B: MIF siRNA1 group ;C: MIF siRNA2 group.
Figure 4.The morphological character of apoptosis in H460 cell induced by MIF-siRNA was detected by Hoechst 33342.A: negative control group;B: MIF siRNA1 group;C:MIF siRNA2 group.
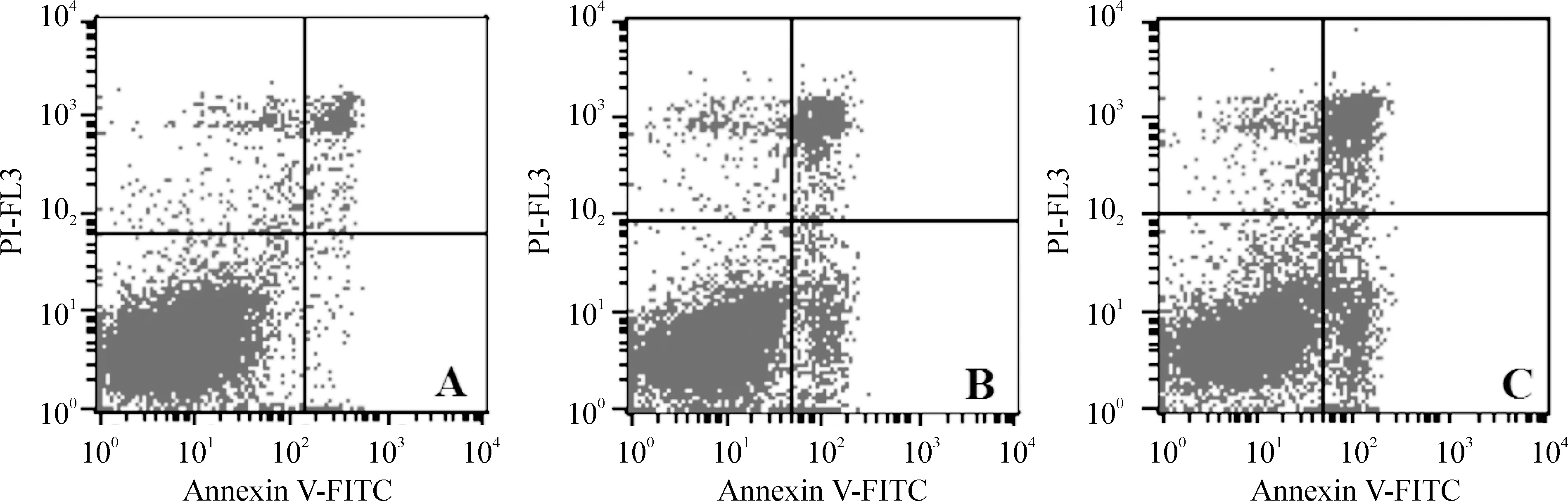
Figure 5.The apoptosis of H460 cell line after treatment with MIF siRNA for 48 h.±s.n=3.A: negative control group(5.87±1.05)%; B: MIF siRNA1 group(18.09±0.41)%*;C: MIF siRNA2 group(23.38±2.67)%*#.*Plt;0.05 vs negative control group;#Plt;0.05 vs MIF siRNA1 group.
討 論
MIF是一個相對分子量為12.5 kD的非糖基化蛋白,最初它作為激活的T淋巴細胞產生的一種可溶性淋巴因子被發現,認為其有抑制巨噬細胞遷移作用。后來進一步研究表明,它在炎癥及腫瘤的發生發展中發揮著重要作用。目前認為,巨噬細胞移動抑制因子是一種獨特的促進惡性腫瘤發生的細胞因子。MIF在多種腫瘤如肝癌﹑結腸癌、肺腺癌﹑乳腺癌﹑膀胱癌、前列腺癌、神經母細胞瘤及慢性粒細胞白血病等腫瘤細胞過度表達[4-11]。
已有多項研究發現,MIF參與了肺癌特別是NSCLC的發生和發展,Khan等[11]研究發現,NSCLC病人的血清MIF和血清淀粉樣蛋白-A(SAA)水平明顯增高,提示MIF可作為腫瘤生物標志物檢測早期肺癌;Kamimura等[12]通過免疫組化/原位雜交發現非小細胞肺癌病人的肺組織MIF過度表達且與預后明確相關;White 等[13]研究表明:NSCLC肺癌組織標本高表達MIF與血中血管內皮生長因子(vascular endothelial growth factor,VEGF)和肺癌組織CXC趨化因子(CXC chemokine)表達升高呈正相關,特別是與腫瘤組織微血管密度(mierovascular density,MVD)呈顯著正相關。McClelland等[14]進一步發現,NSCLC組織標本中特異的MIF受體-CD74表達同樣顯著增高且誘導體內外促血管新生的CXC趨化因子表達升高;MIF這種誘導血管新生效應可被CD74抗體所拮抗。上述結果均提示MIF與NSCLC血管生成和腫瘤細胞轉移有密切關系。至于肺癌細胞自分泌或旁分泌MIF究竟如何參與控制腫瘤細胞增殖、遷移以及促進血管生成,其信號通道與分子機制目前尚不清楚,我們在國內首次用siRNA阻斷或減少MIF蛋白表達,探討研究其抑瘤作用,對尋求治療肺癌的新途徑和新治療靶點具有重要意義。
大量研究表明,MIF通過抑制抑癌基因p53的功能、持續激活胞外信號調節激酶(extracellular signal-regulated kinase,ERK)/ 絲裂原活化蛋白激酶(mitogen-activated protein kinase,MAPK)信號轉導通路、誘導環氧化酶(cyclooxygenase,COX)/前列腺素E2(prostaglandin E2,PGE2)激活、促進血管內皮細胞的增殖及分化等獨特的生物學作用多層次促進腫瘤的生長、增殖及侵襲[15];并且在低分化腫瘤中,MIF表達與預后相關[16],提示MIF與腫瘤的發生、發展及預后關系密切,但具體的分子機制尚未完全闡明。Jung 等[9]研究表明,MIF阻止P53從胞漿轉移至胞核,并且可抑制P53的活性,抑制細胞增殖、促進凋亡。Binsky等[10]在慢性淋巴細胞白血病的研究中發現,MIF表達明顯升高,通過激活IL-8,繼而Bcl-2表達增加,抑制腫瘤細胞凋亡,促進細胞增殖。Arenberg 等[17]發現,在C57BL/6小鼠肺損傷急性期,MIF表達增加,抑制在急性期注入小鼠體內的Louis癌細胞的凋亡,促進其增殖,而在敲除MIF基因的小鼠中則無此現象。
我們的研究結果表明:大細胞肺癌H460細胞株高表達MIF蛋白,體外應用siRNA靶向沉默MIF基因后,H460細胞的活性、增殖能力下降;繼而用Annexin V - FITC/ PI 雙染色凋亡檢測發現,轉染MIF siRNA部分阻斷MIF表達后,H460細胞凋亡率顯著增加,與之前Jung等[9]的研究結果相似,為MIF在人類惡性腫瘤特別是NSCLC中發揮著重要作用提供了更豐富的證據。
我們的研究首次證實在大細胞肺癌的生長、進展過程中,MIF可能通過促進細胞凋亡抑制腫瘤細胞的增殖,這也為研發大細胞肺癌新的治療靶點提供了重要的實驗依據,并且研究過程中所用的MIF siRNA也可能成為有效的抗癌藥物。但是,目前關于MIF siRNA 促進細胞凋亡、抑制細胞增殖的具體信號通道與分子生物學機制尚不明了,基于之前國內外學者的大量研究,我們審慎地推測:MIF作為一種促炎、促癌的細胞因子,廣泛參與非小細胞肺癌的各種細胞生物學行為,介導不同信號轉導通路之間的交互對話(crosstalk),從而協同促進非小細胞肺癌的發生發展,當然這尚需要更完善的體內外實驗來驗證。通過特異的MIF siRNA阻斷MIF表達,檢測凋亡和增殖相關的上、下游信號轉導分子,進一步探討其可能的體內外抑癌機制,本課題組正在進行深入研究。
[1]閻春紅,范小航,楊惠玲.等.2-甲氧雌二醇對人肺癌細胞的放射增敏作用[J].中國病理生理雜志,2010,26(1):137-141.
[2]張淑香,謝燦茂,高橋和久.毒蕈堿膽堿能受體3在小細胞肺癌增殖和遷移中的調節作用[J].中國病理生理雜志,2010,26(9):1679-1683.
[3]Lee MH,Yang HY.Regulators of G1 cyclin-dependent kinases and cancers[J].Cancer Metastasis Rev,2003,22(4): 435-449.
[4]Takahashi N,Nishihira J,Sato Y,et al.Involvement of macrophage migration inhibitory factor(MIF) in the mechanism of tumor cell growth[J].Mol Med,1998,4(11):707-714.
[5]Hira E,Ono T,Dhar DK,et al.Overexpression of macrophage migration inhibitory factor induces angiogenesis and deteriorates prognosis after radical resection for hepatocellular carcinoma[J].Cancer,2005,103(3): 588-598.
[6]Meyer-Siegler KL,Bellino MA,Tannenbaum M.macrophage migration inhibitory factor evaluation compared with prostate specific antigen as a biomarker in patients with prostate carcinoma[J].Cancer,2002,94(5): 1449-1456.
[7]Rendon BE,Roger T,Teneng I,et al.Regulation of human lung adenocarcinoma cell migration and invasion by macrophage migration inhibitory factor[J].J Biol Chem,2007,282(41): 29910-29918.
[8]Ren Y,Chan HM,Li Z,et al.Upregulation of macrophage migration inhibitory factor contribute to induced N-Myc expression by the activation of ERK signaling pathway and increased expression of interleukin-8 and VEGF in neuroblastoma[J].Oncogene,2004,23(23): 4146-4154.
[9]Jung H,Seong HA,Ha H.Critical role of cysteine residue 81 of macrophage migration inhibitory factor(MIF) in MIF-induced inhibition of p53 activity[J].J Biol Chem,2008,283(29):20383-20396.
[10]Binsky I,Haran M,Starlets D,et al.IL-8 secreted in a macrophage migration-inhibitory factor- and CD74-dependent manner regulates B cell chronic lymphocytic leukemia survival[J].Proc Natl Acad Sci USA,2007,104(33):13408-13413.
[11]Khan N,Cromer CJ,Campa M,et al.Clinical utility of serum amyloid A and macrophage migration inhibitory factor as serum biomarkers for the detection of nonsmall cell lung carcinoma[J].Cancer,2004,101(2):379-384.
[12]Kamimura A,Kamachi M,Nishihira J,et al.Intracellular distribution of macrophage migration inhibitory factor predicts the prognosis of patients with adenocarcinoma of the lung[J].Cancer,2000,89(2):334-341.
[13]White ES,Flaherty KR,Carskadon S,et al.Macrophage migration inhibitory factor and CXC chemokine expression in non-small cell lung cancer: role in angiogenesis and prognosis[J].Clin Cancer Res,2003,9(2): 853-860.
[14]McClelland M,Zhao L,Carskadon S,et al.Expression of CD74,the receptor for macrophage migration inhibitory factor,in non-small cell lung cancer[J].Am J Pathol,2009,174(2):638-646.
[15]Conroy H,Mawhinney L,Donnelly SC.Inflammation and cancer: macrophage migration inhibitory factor(MIF)-the potential missing link[J].QJM,2010,103(11):831-836.
[16]Tomiyasu M,Yoshino I,Suemitsu R,et al.Quantification of macrophage migration inhibitory factor mRNA expression in non-small cell lung cancer tissues and its clinical significance[J].Clin Cancer Res,2002,8(12):3755-3760.
[17]Arenberg D,Luckhardt TR,Carskadon S,et al.Macrophage migration inhibitory factor promotes tumor growth in the context of lung injury and repair[J].Am J Respir Crit Care Med,2010,182(8):1030-1037.
血管鈣化轉化醫學研究進展研討會第一輪通知
血管鈣化是動脈粥樣硬化、糖尿病、慢性腎衰的常見并發癥,與上述疾病的心血管事件發生率和死亡率密切相關。為促進國內血管鈣化領域臨床工作者和基礎科研人員的深入交流與廣泛合作,提升我國在血管鈣化領域的國際學術影響力,凝練血管鈣化的轉化醫學研究隊伍,由教育部分子心血管重點實驗室、北京大學醫學部生理與病理生理系、附屬北醫三院和人民醫院、《生理科學進展》雜志、中日友好醫院聯合主辦,茲定于2011年8月27日在北京大學醫學部召開首屆血管鈣化轉化醫學研究進展研討會,就血管鈣化的臨床流行病學、發病機制、診治及預后等熱點問題進行為期一天的探討與交流。會議邀請了國內該領域知名專家與會作專題報告,歡迎從事臨床、基礎、預防和藥學工作對血管鈣化感興趣的學者踴躍參會。
會議無需注冊費。26號下午和27號早8點前報到,報名者請于6月1日之前將回執發至kongfanwei2000@gmail.com,由大會主席批準后確認參會名單。會議征集500字論文摘要,內容涉及血管鈣化相關臨床流行病學、診斷、發病機制、治療等方面,請于7月15日之前提交至kongfanwei2000@gmail.com。
會 議 主 席: 唐朝樞 教授,王 憲 教授
會議籌備組: 王 悅 教授,王 梅 教授,齊永芬 教授,孔 煒 教授
會議聯系人: 孔 煒 教授
電 話: 010-82805594
InhibitionofhumanlungcarcinomaH460cellproliferationbysiRNA-mediatedMIFknockdown
HOU Jun-na1,LUO Yi-feng1,WANG Du-juan2,YANG Hui-ling2,GUO Yu-biao1
(1DepartmentofPulmonaryandCriticalCareMedicine,TheFirstAffiliatedHospital,2DepartmentofPathophysiology,ZhongshanSchoolofMedicine,SunYat-senUniversity,Guangzhou510080,China.E-mail:guoyubiao@hotmail.com)
AIM: To investigate the inhibitory effect of siRNA-mediated MIF knockdown on the proliferation of human lung carcinoma H460 cells and to elucidate the molecular mechanism of anti-tumor effect of the siRNA.METHODSThe transfection efficiency was assessed by immunofluorescence technique.The expression of MIF after the gene knockdown was determined by Western blotting.The viability and proliferation of H460 cancer cells were detected by MTT assay and colony formation assay,respectively.The cell apoptosis and morphological changes were examined by flow cytometry and electron microscopy,respectively.RESULTSMIF siRNA significantly inhibited MIF expression in H460 cells,and decreased the proliferation of the cells(Plt;0.05).The morphological changes were detected in the nuclei of H460 cells induced by MIF siRNA.The apoptotic rates were much higher in the groups of MIF siRNA1 and MIF siRNA2 than that in negative control group[(18.09±0.41)% and(23.38±2.67)%vs(5.87±1.05)%,Plt;0.05].CONCLUSIONMIF might play an important role in the pathogenesis and progression of large cell lung cancer.siRNA-mediated knockdown of MIF results in the inhibition of H460 cell proliferation,indicating that MIF might be used as a potential therapeutic target in lung cancer.
Macrophage migration inhibitory factor; Small interference RNA; Lung neoplasms
1000-4718(2011)05-0853-06
R734.2
A
10.3969/j.issn.1000-4718.2011.05.005
2010-12-20
2011-03-07
廣東省自然科學基金資助項目(No.10151008901000242);2010年廣東省科技計劃資助項目(No.2010B080701010)
△通訊作者 Tel: 020-87755766-8132; E-mail: guoyubiao@hotmail.com

